黃色金針菇菌株提純復壯技術研究
劉昆昂 張根偉 馬 宏 李書生 劉振國 付艷菊
(河北省科學院生物研究所,石家莊050081)
金針菇(Flammulina velutipes)又名構菌、冬菇、毛柄金錢菌等[1],按子實體顏色的深淺可將金針菇分為黃色品系、白色品系、淡黃色品系[2]。黃色金針菇是我國傳統金針菇生產品種,相對于白色金針菇,具有產量高、口感好、抗性強等特點。金針菇菌種作為金針菇栽培的基礎生產資料,對產量和質量起著關鍵性作用。然而黃色金針菇主要是散戶栽培,由于科研投入不足、管理不善,金針菇菌種在保藏及傳代過程中出現生產周期延長、產量下降、容易感染等退化現象。
菌種退化分為可逆和不可逆兩種類型,可逆的退化現象可通過提純復壯恢復其優良特性[3]。生產上常用的菌種提純復壯方法有,(1)“斷橋法”和菌絲尖端分離提純復壯,其特點是僅可篩選出生長速度快的菌株,而生長速度快往往并非高產優質食用菌菌株[4];(2)原生質體再生法:需要產生大量原生質體,并對產生的大量原生質體進行分離、篩選和出菇驗證,技術難度較大[5]。
研究以黃色金針菇蘇金6 號為樣本,通過在含有不同濃度結晶紫的PDA 培養基培養后,采用菌絲尖端分離和原生質體再生相結合的方法進行提純復壯。此方法較常規金針菇提純復壯方法更簡便、更高效。
1 材料與方法
1.1 供試菌株黃色金針菇品種蘇金6 號,引自河北省創新食用菌研究所,生產中主要表現為污染率高、生產周期延長、產量下降、畸形菇增多等。
1.2 培養基①PDA 培養基(g/L):馬鈴薯200,葡萄糖20,磷酸二氫鉀3,硫酸鎂1.5,蛋白胨2,瓊脂12;②再生培養基:PDA 培養基+ 0.6 mol/L 的甘露醇;③栽培培養料:棉籽皮83%,麩皮15%,石灰1%,石膏1%;料水質量比1∶1.3;④木質素酶顯色培養基:1%梨木屑煮汁+0.02%愈創木酚+1.2%瓊脂;⑤纖維素酶顯色培養基:0.2%微晶纖維素+0.02%剛果紅+1.2%瓊脂。
1.3 提純復壯培養取供試菌株試管種不同部位菌塊,分別接入含有0~40 mg/L 結晶紫的PDA 培養基中,26℃培養,待菌絲將要長滿皿,挑取菌絲尖端,轉入PDA培養基中,26℃培養,比較生長情況。
1.4 鎖狀聯合觀察計數菌株接入鋪有玻璃紙的PDA培養基中,26℃培養,待菌絲長到玻璃紙上,400倍顯微鏡下觀察視野中鎖狀聯合數量。
1.5 酶解液1%蝸牛酶(Snailase)+1%溶壁酶(Sig?ma),用0.6 mol/L MgSO4配制,經4000 r/min 離心20 min 后,上清液無菌條件下用0.45 μm 微孔濾膜過濾除菌后,分裝于10 mL 試管中,4℃冰箱保存備用。
1.6 原生質體再生對提純復壯處理的菌株進行原生質體再生,取金針菇斜面菌絲碎片,接入盛有30 mL 液體PDA 培養基的100 mL 三角瓶中,25℃左右靜置培養7 d。過濾收集菌絲體,分別用無菌水和0.6 mol/L 的MgSO4各洗滌1 次。按菌絲重∶酶液量為150 mg∶1 mL 的比例將菌絲置于酶解管中,30℃酶解3 h,每隔1 h 振蕩并鏡檢原生質體釋放情況。酶解完畢后,用6 層擦鏡紙過濾,以除去殘留菌絲。濾液經1000 r/min離心后棄上清液收集沉淀,用0.6 mol/L 的MgSO4洗滌2 次,得到純化的原生質體。取0.1 mL 原生質體懸液梯度稀釋,涂布于再生培養基平板,25℃下恒溫培養,4~6 d即見再生菌落[6]。
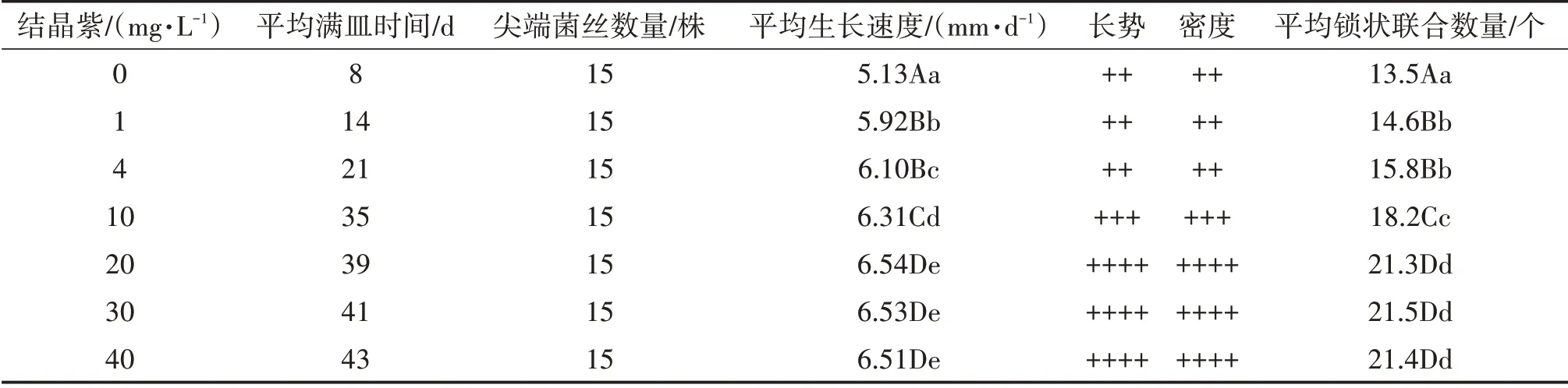
表1 不同質量濃度結晶紫培養基培養對蘇金6號的提純復壯作用
1.7 再生菌株的篩選挑取再生菌株到PDA 培養基中,26℃培養,挑選生長快、長勢好、菌絲粗壯、鎖狀聯合多而整齊;同法接入栽培料中,測定生長速度,重復3次[7]。
1.8 再生菌株的酶活測定變色圈法測定木質素和纖維素酶活性。菌塊接入PDA 培養基平皿中部,滿皿后用打孔器在菌落邊緣取直徑50 mm 的菌餅,接入顯色培養基中,分別在5、10、15、20、25℃和30℃培養3 d,測定變色圈直徑[8]。
1.9 栽培試驗用聚丙烯塑料袋(17.5 cm×40 cm×0.005 cm)裝料,每袋約裝干料400 g,以套環封口。高壓滅菌(121~126℃)維持2 h,待料溫降至25℃以下,按無菌操作規范接種,各接30袋。置于20~28℃培養室內發菌,菌絲滿袋后按再生法進行催蕾—開袋—抑制—再生菇培養等工藝進行出菇管理[9]。當子實體長至16 cm 左右,菌蓋直徑小于1 cm 及時采收。復壯效果。
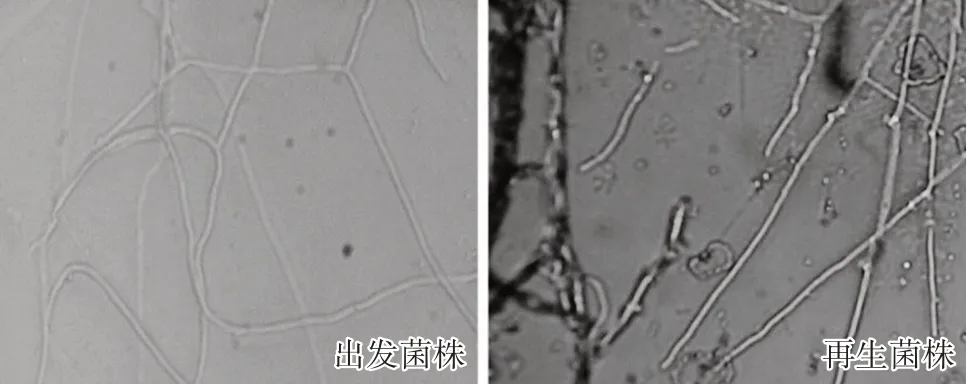
圖1 出發菌株及再生菌株的菌絲形態觀察
2.2 原生質體再生菌株篩選
2.2.1 提純復壯培養對原生質體再生的影響 對20 mg/L 結晶紫提純復壯培養的菌株進行原生質體再生,并設出發菌株對照。挑取再生菌株各100株,初篩各得到60株長勢較強、生長快的菌株,經傳代3次后在PDA 培養基上進行比較。處理組篩選得到的菌絲生長速度≥7 mm/d 的菌株為45 個,達到75.0%,而對照僅14個,占13.3%;處理組400倍顯微鏡下,視野中平均鎖狀聯合數量為28.6 個,而對照組平均鎖狀聯合數量為22.4 個。可見,含有結晶紫PDA 培養基提純復壯培養,可以顯著提高金針菇原生質體再生的篩選效率。
2 結果與分析
2.1 提純復壯培養結果一定質量濃度的結晶紫可抑制金針菇菌絲生長,尤其對細胞壁不完整的退化菌絲產生更大的殺傷作用;而抗性強的菌絲,可以觀察到:菌絲生長停頓1~2周后,部分萌發點成扇形向外生長。由表1可知,在含有1~40 mg/L結晶紫的PDA 培養基中培養,隨著濃度增加,滿皿時間逐步延后;20~40 mg/L 處理時,提純復壯的菌株,平均生長速度、長勢和菌絲密度達到最大;如圖1 所示,400 倍顯微鏡下觀察可見菌絲生長整齊、粗壯,鎖狀聯合數量最多,而且組間差異不顯著。因此,含有20 mg/L 結晶紫的PDA 培養基即可以達到最佳提純
2.2.2 原生質體再生菌株篩選 篩選生長快、長勢強、菌絲密度大、鎖狀聯合數量多的菌株。如表2所示,5 株菌在PDA 培養基和棉籽皮基質上菌絲長速都快于出發菌株,而且長勢強、菌絲密度大、鎖狀聯合規則而且多;但兩種基質上的生長速度并不成正比,例如,在PDA 培養基以13D10 生長最快,達到9.25 mm/d,但在棉籽皮基質上菌絲生長速度排第二位,為4.90 mm/d;而棉籽皮基質上生長速度最快的13B7,達到5.01 mm/d,PDA 培養基上生長速度排第三位,為8.93 mm/d。
2.2.3 木質素、纖維素酶活性比較 對篩選的再生菌株進行木質素和纖維素酶活測定。結果如表3、表4 所示,再生菌株木質素和纖維素酶活性均高于對照。20~30℃條件下,木質素酶活性由高到低依次為:13B7>13C9>13C10>13D10>13A2>CK;纖維素酶活性由高到低依次為:13B7>13C9>13D10>13A2=13C10>CK。5~15℃條件下,木質素酶活性由高到低依次為:13D10>13B7>13C9>13A2>13C10>CK;纖維素酶活性由高到低依次為:13C9>13B7>13D10>13A2=13C10>CK。其中,13B7在中高溫具有最高的酶活性,低溫酶活性排在第二位;13A2 在各溫度點酶活均相對低。
2.3 出菇試驗結果選取13B7、13D10、13C9 和13C10四株生長速度快、酶活高的再生菌株進行出菇試驗。結果如表5 所示,再生菌株可縮短滿袋時間5~6 d,提高產量11.2%~15.5%,均為優于親本的高產菌株。以13B7產量最高,達到381 g/袋,增產15.5%,生物學效率為95.3%。同時發現,生長速度慢于13D10 和13C9 的13B7 出菇最早,而且產量最高,可見菌株的長速與產量之間并不一定存在正相關性,提示我們菌株篩選要從多方面考慮,以免漏篩。

表2 在PDA培養基和栽培料(棉子殼)上原生質體再生菌株的菌絲生長情況
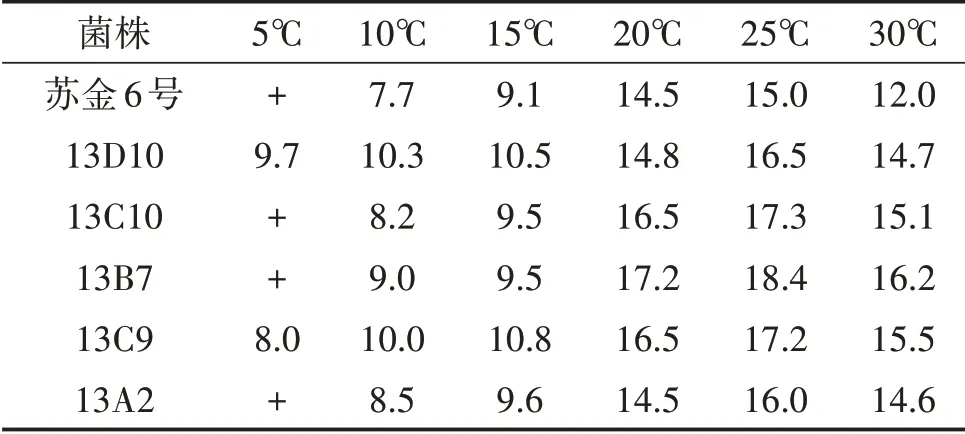
表3 在不同溫度下再生菌株的木質素酶活(變色圈直徑)/mm
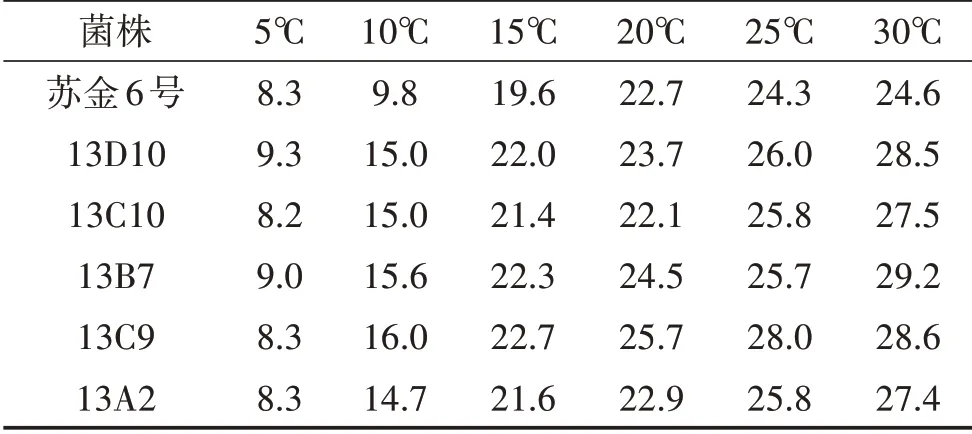
表4 在不同溫度下再生菌株的纖維素酶活性(變色圈直徑)/mm
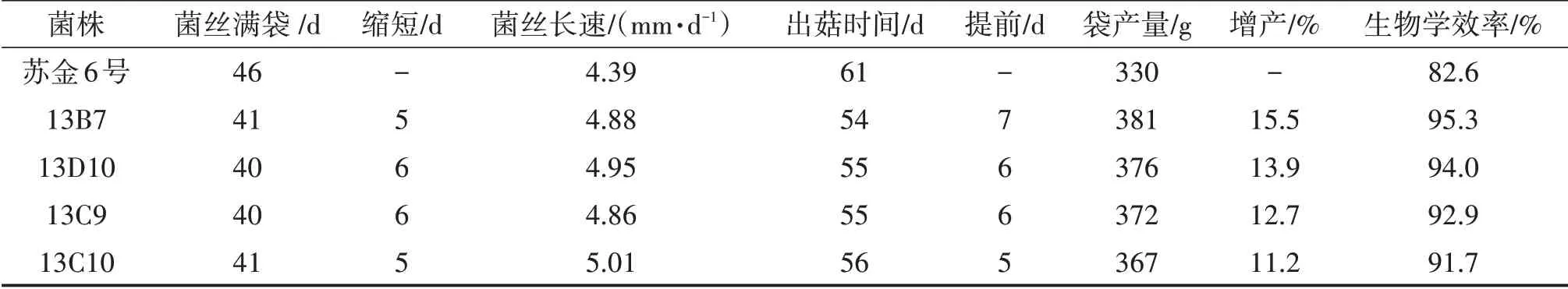
表5 復篩(再生)菌株與出發菌株的出菇試驗
3 小結與討論
在食用菌菌株的脫毒復壯中,采用的方法主要有菌絲尖端脫毒法、原基組織脫毒法、原生質體再生法等。相比原生質體再生法,菌絲尖端分離不容易得到純的提純復壯的菌株,但以退化的菌株直接進行原生質體再生,無疑增加了篩選的工作量,也很難達到滿意的效果。研究提供的提純復壯方法,不但使退化菌株在生長速度、木質素和纖維素酶活和產量均有提高,而且在形態上也有差異,退化的菌株細胞壁破損、穿孔,菌絲生長不整齊,而再生菌株生長快,鎖狀聯合多而且規則。另外,當培養溫度在20~30℃時,在生長速度相近的情況下,產量與木質素酶活、纖維素酶活成正相關。這可能和試驗中中溫發菌培養有關。試驗結果表明,在優良菌株提純復壯篩選過程中,可以從不同溫度下酶活、形態特征角度進一步篩選。此外,筆者還對黃色金針菇雜19進行了提純復壯,從菌絲形態角度判斷雜19菌株退化較輕,提純復壯菌株增產幅度低于蘇金6號。初步判斷,此方法更適合于退化的金針菇菌株的提純復壯。

