流溪河入侵魚類豹紋脂身鯰繁殖生物學研究
劉 飛,韋 慧,顧黨恩,牟希東,羅 渡,徐 猛,胡隱昌
(1.農業部休閑漁業重點實驗室,中國水產科學研究院珠江水產研究所,廣州,510380;2.上海海洋大學水產與生命技術學院,上海 201306)
流溪河入侵魚類豹紋脂身鯰繁殖生物學研究
劉 飛1,2,韋 慧1,顧黨恩1,牟希東1,羅 渡1,徐 猛1,胡隱昌1
(1.農業部休閑漁業重點實驗室,中國水產科學研究院珠江水產研究所,廣州,510380;2.上海海洋大學水產與生命技術學院,上海 201306)
2015年12月-2016年10月,在廣州市流溪河采集入侵魚類豹紋脂身鯰(Pterygoplichthyspardalis)283尾用于繁殖生物學研究。結果顯示:流溪河豹紋脂身鯰在3-9月性成熟系數較高。雄性最小性成熟個體體長204 mm,體重154.88 g;雌性最小性成熟個體體長201 mm,體重183.01 g;最早性成熟年齡均為1齡。其平均成熟卵徑為1.87 mm,絕對繁殖力為636-6 148粒,平均絕對繁殖力為2 524.49粒,平均相對繁殖力為10.43粒/g。絕對繁殖力與體長和體重呈顯著的正相關。繁殖群體性比為(♀∶♂)為 1∶1.15,符合1∶1比例。卵徑分布為單峰型。研究表明豹紋脂身鯰具有性成熟早、繁殖力高等特征,有利于其在分布區域迅速建群擴張,并對河流生態系統形成危害。
豹紋脂身鯰(Pterygoplichthyspardalis);性腺發育;周年變化;懷卵量
魚類入侵從中世紀的歐洲開始顯現,伴隨著殖民移民和世界貿易的發展,漸漸席卷全球,對水域生態系統造成嚴重危害[1]。我國生物多樣性資源極為豐富[2],但是外來魚類入侵已經成為破壞水生生物多樣性的主要威脅[3],且在我國愈演愈烈[4]。以云南省為例,由于近年來盲目而頻繁的進行魚類引種,洱海和滇池等高原湖泊原有的魚類很多已經瀕臨滅絕[5]。廣東省地處我國改革開放的第一線,國際貿易相對我國其他地區較發達,同時氣候溫暖,適宜生長的物種相對寒冷地區較多,因而成為我國遭受外來魚類入侵最嚴重的地區之一[6],外來魚類如尼羅羅非魚(Oreochromisniloticus)、莫桑比克羅非魚(Oreochromismossambica)、奧利亞羅非魚(Oreochromisaureus)、豹紋脂身鯰(Pterygoplichthyspardalis)、革胡子鯰(Clariasleather)、食蚊魚(Cambusiaaffinis)、麥瑞加拉鯪(Cirrhinamrigala)、露斯塔野鯪(Labeorohita)、斑點叉尾鮰(Lctaluruspunctatus)和大口黑鱸(Micropterussalmoides)等已成為廣東省主要水系漁獲物常見種類[7]。但我國對外來魚類入侵的入侵機制、入侵效應、風險評估及管理對策等相關領域的研究進展還很有限,因而我國應對外來魚類入侵問題提高重視,加大研究力度,以便降低魚類入侵對我國生物多樣性、入侵地生態系統及生態環境的破壞,并依據這些研究制定相應的生態系統恢復策略[8]。
豹紋脂身鯰,別名清道夫,吸盤魚、琵琶魚、琵琶鼠魚,屬于鯰形目(Siluriformes)骨甲鯰科(Loricariidae)翼甲鯰屬(Pterygoplichthys)魚類。原產于南美洲亞馬遜河流域,目前已在美國、墨西哥、南非、東南亞、日本、臺灣等國家和地區形成入侵[9-12]。據報道,豹紋脂身鯰能夠與本地魚類競爭食物和生境,排擠本地魚類[13];破壞網具,影響漁民漁業生產活動[14];其掘洞產卵行為能夠造成河堤水土流失[15];改變河流養分循環[16]。豹紋脂身鯰最早于1990年作為觀賞魚類引進中國廣東省[17],隨著觀賞漁業貿易傳播至全國各省。并于2014年被列入國家環保部和中國科學院發布的入侵物種名單。但對豹紋脂身鯰在野外的建群狀況及生態影響尚不清楚。
廣州地處亞熱帶沿海,屬海洋性亞熱帶季風氣候,年平均氣溫21.9 ℃,最低溫-2.6 ℃,最高溫39.1℃,年降雨量1720.5 mm,平均相對濕度77%。流溪河,珠江水系二級支流,位于廣州西北部(113°46' 52" E,23°45' 22" N),主流全長156 km,流域面積2 300 km2,中上游建有國家級光倒刺鲃水產種質資源保護區和從化市級唐魚自然保護區,是廣州市淡水魚類物種多樣性最豐富的區域之一。在2007-2008年廣州市漁業資源調查中發現流溪河中有豹紋脂身鯰的分布,但后續并未見關于豹紋脂身鯰入侵生物學相關報道,對其生態影響也不清楚[18]。是否能夠在野外繁殖并產生可持續種群是評價外來物種建群成功和生態影響的重要指標。本研究以流溪河人和段為研究區域,按月份采樣,探索豹紋脂身鯰繁殖生物學的時間節律,闡明豹紋脂身鯰在流溪河的建群狀況,旨在為外來魚類的管理和防控提供理論依據。
1 材料與方法
1.1 樣本采集
用蝦籠、刺網和拋網等工具在流溪河人和段采集豹紋脂身鯰樣本,采樣時間為2015年12月~2016年10月,共計418尾,其中可鑒定出性別的樣本共計283尾。
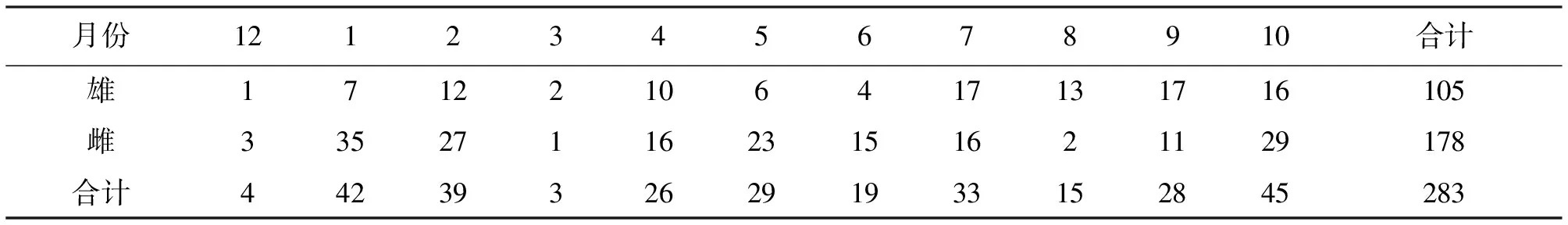
表1 雌雄豹紋脂身鯰樣本采集情況表
1.2 樣本處理
樣品采集后于新鮮狀態下測量全長、體長、體重、性腺重、肝胰臟重、脂肪重和去內臟體重。使用電子天平進行質量的測量(精確到0.01 g),使用量程為60 cm的直尺進行形態數據的測量(精確到0.1 cm)。并通過對性腺發育狀況,對所有樣本的性別進行鑒定,根據性腺形態及色澤特征判別雌性、雄性、未成熟及靜息期幼魚。卵巢淡黃色、黃色,卵粒沉積卵黃的為雌性,精巢淡玫瑰紅色或乳白色的為雄性,性腺透明細線狀或扁平帶狀肉眼難以辨別雌雄為未成熟及靜息期幼魚[19]。根據性腺在不同發育期表現出的不同形態特征,分別對應6個性腺發育期,用羅馬數字I~ VI表示[18]。采用重量估算法測量絕對繁殖力[20],以成熟期(IV 、V期)卵巢為研究材料,取半個卵巢,稱重,用5%的福爾馬林溶液固定保存,用計數器計數所有沉淀和可以分離的卵粒,用以計算其絕對繁殖力和相對繁殖力。取IV期卵巢作為卵徑測量材料,從卵巢上、中、下、前、后五個部位隨機抽取100粒卵,使用數顯游標卡尺進行卵徑測量,精確至0.01 mm。
1.3 數據處理
成熟系數、肥滿度、絕對繁殖力和相對繁殖力分別采用以下公式進行計算[19,21]:成熟系數(Gonado-somatic index)=(性腺重/去內臟體重)×100%,肥滿度=(去內臟體重/體長3)×100,絕對繁殖力=(樣品卵粒數/樣品重)×卵巢重,相對繁殖力=絕對繁殖力/去內臟體重,單位為(粒/g)。IBM SPSS Statistics 22.0軟件對測量數據進行數據分析,使用SigmaPlot 10.0和Photoshop CS 6 進行圖片處理。
2 結果與分析
2.1 成熟系數與性腺發育期的周年變化
統計283尾(雄:105尾;雌:178尾)個體的月平均成熟系數。12月雌魚的成熟系數為(0.39±0.14)%,處于周年最低值;12月至2月越冬期間雌魚卵巢發育96%位于Ⅱ期,越冬后Ⅱ期卵巢開始向Ⅲ期卵巢慢慢發育;4月成熟系數開始顯著上升,Ⅲ期卵巢出現比例劇增,并出現少量IV期、V期雌魚;6-8月份為繁殖旺季,卵巢主要為Ⅳ期、Ⅴ期,7月份雌魚成熟系數達到峰值(9.74±2.18)%,之后持續緩慢下降,并且隨著部分親魚繁殖活動的結束,Ⅵ期卵巢出現比例不斷提高,雌魚成熟系數在12月降到谷值(圖1A)。周年內雄魚成熟系數明顯低于雌魚,但成熟系數及性腺發育期周年變化趨勢與雌魚基本保持一致。雄魚的成熟系數在2月份最低,3月成熟系數上升較慢;4月、5月和6月成熟系數也呈現一路穩定上升的趨勢,至7月達到峰值(0.21±0.05)%;8月后繁殖系數開始降低,9月份又出現一個小的峰值(0.17±0.07)%,之后逐步降低(圖1B)。
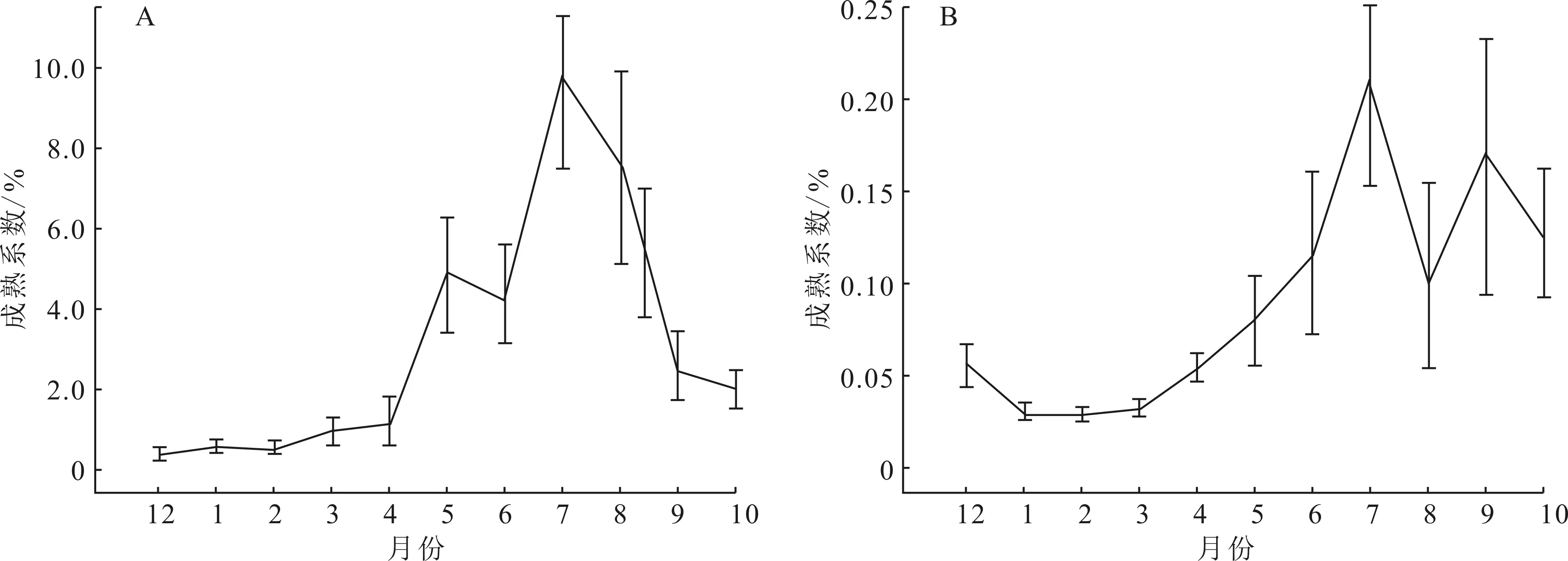
圖1 豹紋脂身鯰雌(A)、雄魚(B)成熟系數周年變化Fig.1 Annual change of gonado-somatic index in female (A) and male (B) of P.pardalis
2.2 卵徑分布
從283尾樣本中采集到性腺發育IV期雌魚56尾。卵巢從4月開始發育,卵粒數在6-7月達到最高。卵徑均值(1.87±0.96) mm,6-8月,平均卵徑2.05 mm,占絕對優勢。卵徑分布曲線為單峰形(圖2),推測豹紋脂身鯰屬于同步產卵類型。
2.3 肥滿度
雌魚肥滿度在12月份出現一個峰值(1.69±0.08),之后從2月份開始上升,在5月份出現最高值(1.87±0.13),在8月份出現谷值 (圖3A)。雄魚肥滿度在12月份出現一個峰值(1.74±0.08),之后從1月份開始慢慢上升,2月份開始迅速攀升,在3月份出現周年最高峰值(1.77±0.09),之后下降;在6月份出現谷值后又慢慢回升(圖3B)。
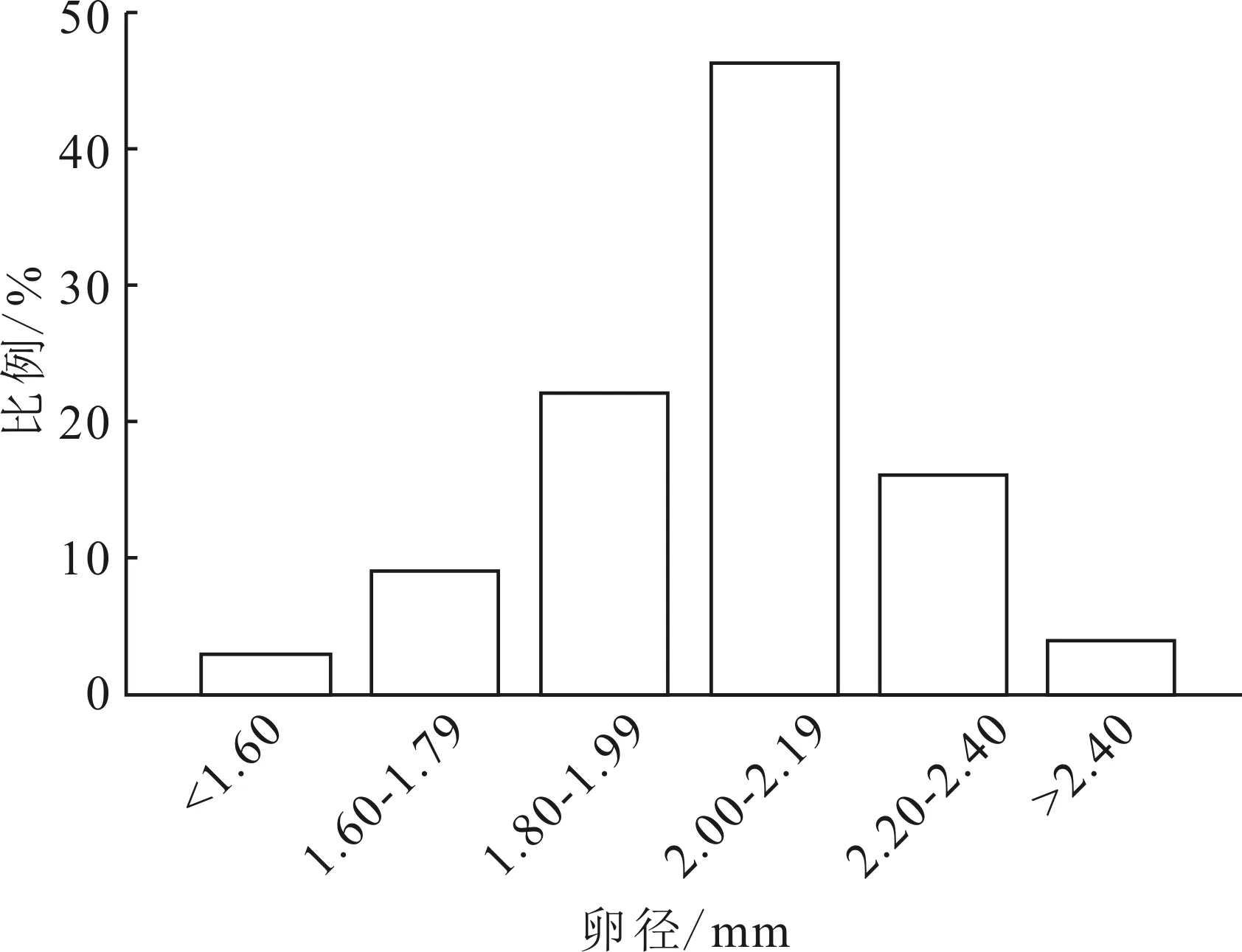
圖2 56尾Ⅳ期豹紋脂身鯰卵巢中卵徑的分布Fig.2 Oocyte diameter distribution in 56 P.pardalis orary at stage Ⅳ
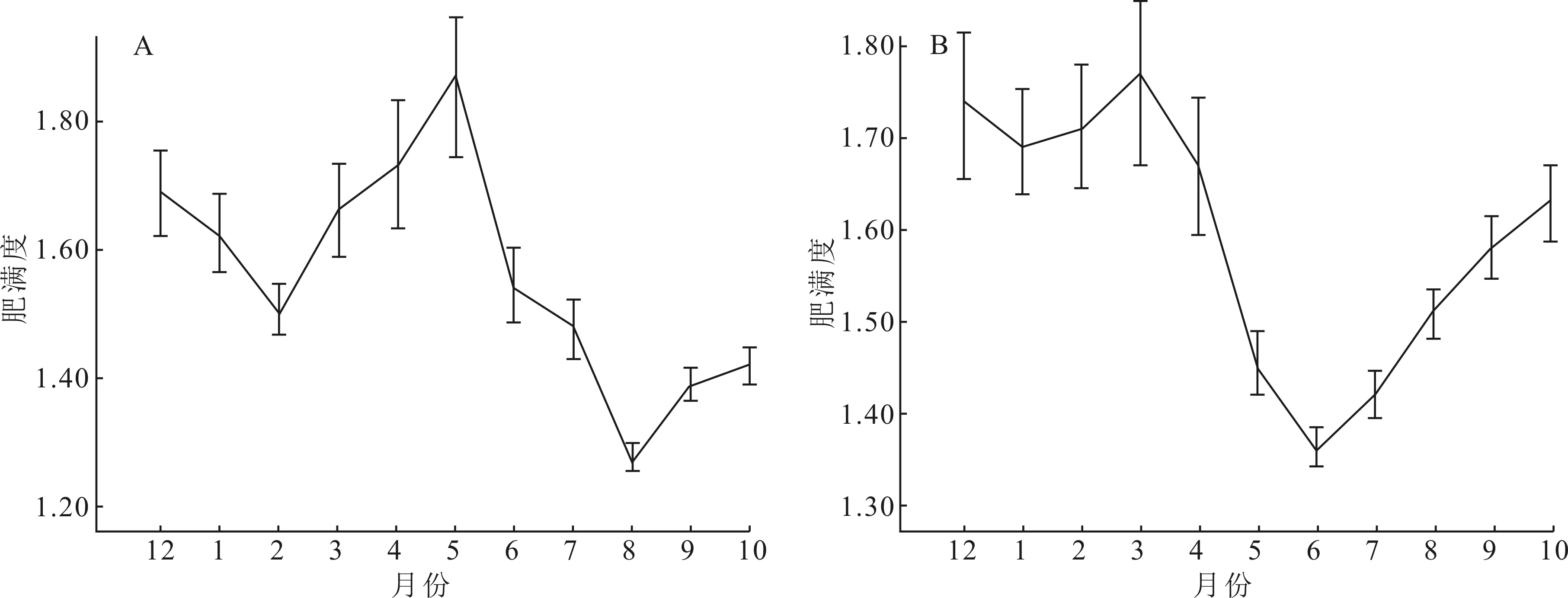
圖3 豹紋脂身鯰雌(A)、雄魚(B)肥滿度周年變化Fig.3 Annual change of fullness in female (A) and male (B) of P.pardalis
2.4 繁殖力
統計56尾雌魚的絕對繁殖力和相對繁殖力(表2)。56尾性成熟個體,體長范圍201~341 mm,體重范圍183.01~642.43 g。絕對繁殖力為636~6 148粒,均值(2 231±1 643)粒;相對繁殖力范圍5~39粒/g,均值為(10±4)粒/g。
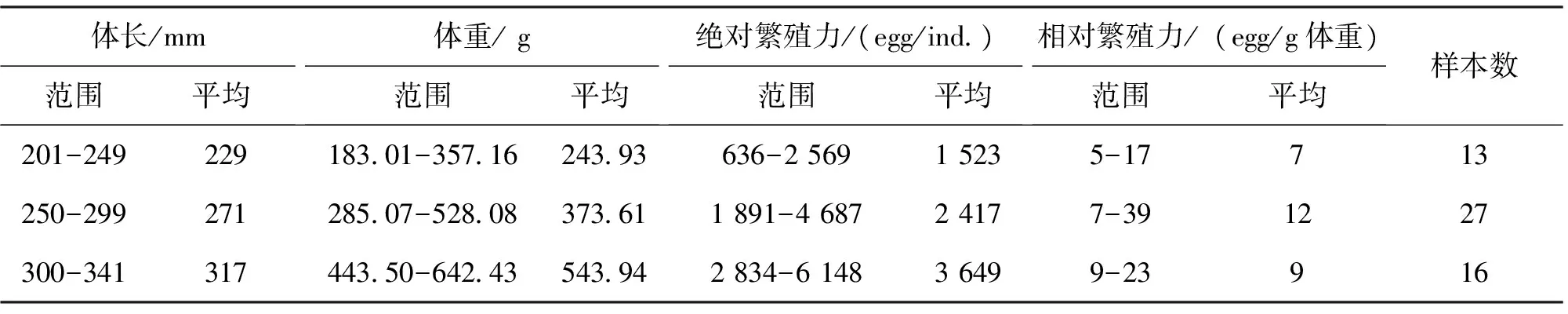
表2 豹紋脂身鯰的繁殖力
分別用直線方程和冪函數方程擬合絕對繁殖力(F)與體長(L)和體重(W)的關系,獲得絕對繁殖力與體長、體重的關系式。絕對繁殖力與體長關系式:F=32.947L-6129.558(n=56,R2=0.530,P<0.01),F=3.484×10-6L(R2=0.544,P<0.01)(圖4A)。絕對繁殖力與體重關系式:F=8.531W-412.671(n=56,R2=0.516,P<0.01),F=1.243×W1.619(R2=0.529,P<0.01)(圖4B)。絕對繁殖力與體長、體重冪函數方程和直線方程的相關系數相差不大,表明豹紋脂身鯰絕對繁殖力隨體長、體重的增加而增加。
相對繁殖力與體長、體重的相關性不顯著。在體長小于299 mm時,相對繁殖力的均值隨著體長的增加而增加至(10±3)粒/g;體長在300~341mm之間,相對繁殖力略有下降且保持在9粒/g(圖5A)。體重小于400.0 g時,相對繁殖力的均值隨體重的增加而增至(12±3)粒/g;體重在400~600 g之間時,相對繁殖力呈現下降趨勢;體重大于600.0 g時,相對繁殖力保持在9粒/g(圖5B)。
2.5 繁殖群體結構組成
在能夠鑒定出性別的283尾樣本中,雌魚178條,雄魚105條,雌∶雄=1.70∶1(x2=12.449,P<0.05);在性腺為III期的129尾樣本中,雌魚96尾,雄魚33尾,雌∶雄=1∶0.35(x2=30.767,P<0.05);在性腺為IV-Ⅴ期的114尾樣本中,雌魚59尾,雄魚68尾,雌∶雄=1∶1.15(x2=0.561,P>0.05),符合1∶1比例。
雄性最小性成熟個體體長204 mm,體重154.88 g,成熟系數為0.13%。雌性最小性成熟個體體長201 mm,體重183.01g;成熟系數為3.03%,最早性成熟年齡均為1齡。
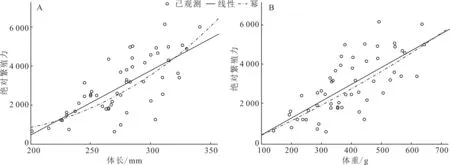
圖4 豹紋脂身鯰絕對繁殖力與體長(A)、體重(B)的關系曲線Fig.4 Correlation curve between body length (A),total weight (B) and absolute fecundity of P.pardalis
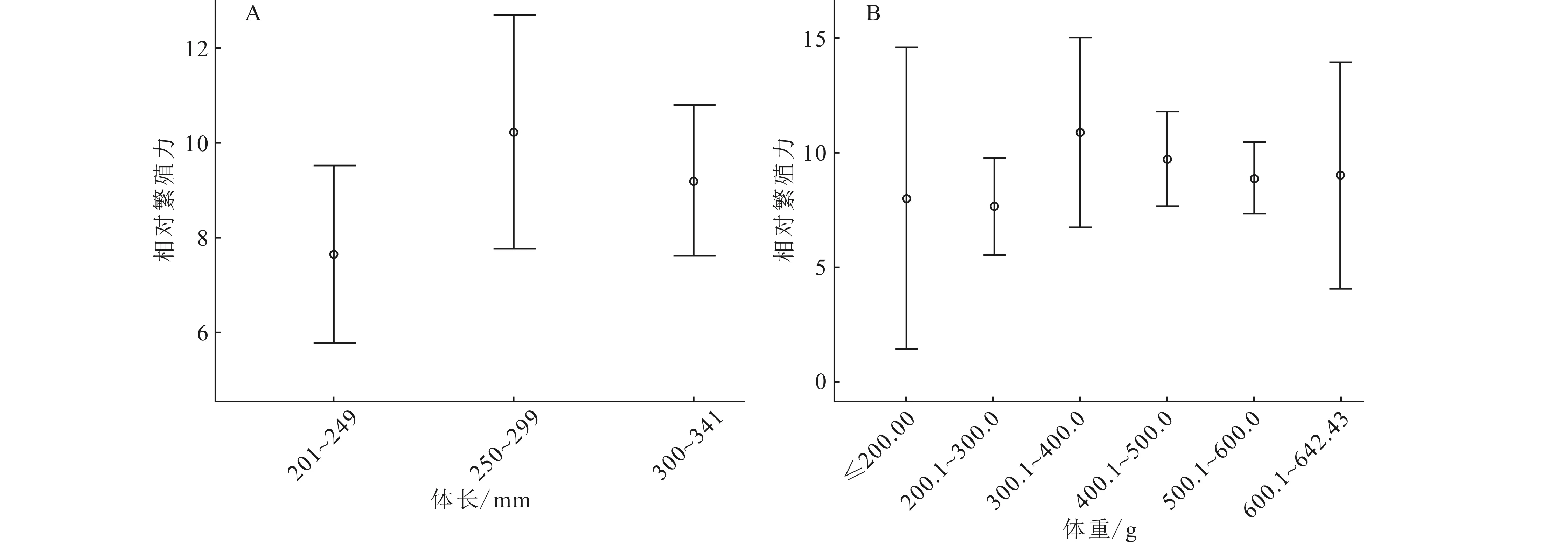
圖5 豹紋脂身鯰相對繁殖力隨體長(A)、體重(B)增加變化特征(均值±標準差)Fig.5 Variation of relative fecundity along with the increase of body length (A),total weight (B) of P.pardalis (Mean±SD)
3 討論
在魚類生活史過程中,繁殖群體的數量和繁殖持續的時間可以用成熟系數的波動直觀表現;種群整體的繁殖潛力一般和成熟系數成正比[22]。同時魚類的性腺發育與產卵繁殖在其整個生活史過程中不僅受到諸如性激素等內在生理因子的調控,而且還會受到來自外界環境因子的影響,例如光照、水流、水溫以及營養因子等都會對其性腺的發育和產卵繁殖造成一定影響[23-26]。豹紋脂身鯰的成熟系數呈現出明顯的周期年變化,3月份廣州天氣開始回暖,成熟系數也隨之逐漸升高,并發現少量IV期及V期性腺。本研究中雌、雄魚的成熟系數均在7月達到峰值,6-8月份卵巢主要為Ⅳ期、Ⅴ期,之后成熟系數開始逐漸下降,但9月份仍出現少量IV期、V期卵巢,因此結合成熟期和繁殖期卵巢出現時間及持續時間以及成熟系數的周年變化規律等理化指標特征的監測和分析可以推測豹紋脂身鯰的繁殖季節為3-9月,繁殖旺季為6-8月。與豹紋脂身鯰在臺灣和美國佛羅里達洲的繁殖節律一致[27-28]。但在原產地,豹紋脂身鯰主要在雨季開始繁殖(5-10月)[29]。其原產地亞馬遜河流域巴西境內,雨季平均水位46.3 m,旱季水位較雨季降低12~15 m,最低水位只有4.4 m,水位波動幅度大。流溪河人和段全年最低水位14.93 m,洪峰水位17.3 m,水位變化較穩定。說明入侵地穩定的水位條件可能是豹紋脂身鯰延長繁殖時間的重要原因。不同地區不同生境的豹紋脂身鯰繁殖習性上略有差異,反映了魚類繁殖行為對生境的高度適應能力,這有利于仔魚保持較高的出膜和成活率,從而保證有足夠種群補充[23]。跟雌魚略有不同的是,9月份雄魚的成熟系數又出現一個較小的波動,這種現象可能跟錯過繁殖時間導致成熟精子退化被吸收有關。同時在一次性產卵魚類瓦氏黃顙魚的研究中該現象也曾出現[21,30]。對此,楊家云[30]認為雄魚為了減少越冬時期的能量消耗,在越冬前有排精現象。
判斷魚類產卵類型的依據通常采用成熟系數周年變化和卵徑分布等[21,31-33]。豹紋脂身鯰在繁殖季節產卵結束后,成熟系數會出現急劇變化,呈現降低的趨勢。樣本解剖及測量結果表明,卵徑1.80-2.10 mm范圍內的個體占統計量的64.41%,卵徑分布呈現明顯的單峰型特征,進一步證實了豹紋脂身鯰具有同步產卵的繁殖習性。
肥滿度的季節變化明顯,和性成熟系數的周年變化存在相反的趨勢,可以用來衡量魚體的營養狀況、豐滿程度和環境條件等[19,21]。12月到2月期間處于水溫低下的越冬期,自然水域餌料豐沛程度較低,豹紋脂身鯰攝食量減少,肥滿度呈現一個較低的水平;2月后,天氣變暖,豹紋脂身鯰生長加速,營養物質在體內迅速累積,雌、雄魚的肥滿度上升顯著,繁殖活動會大量消耗體內能量,故而體內儲存的大量物質和脂肪被消耗,肥滿度出現較小值;在繁殖旺季6-8月份,肥滿度處于周年最小值,而成熟系數處于周年最大值;繁殖活動結束后,越冬前的10-12月份,為度過食物緊缺的寒冬時節,魚體開始大量存儲營養物質和脂肪,肥滿度呈現快速上升趨勢。
繁殖力是評估種群數量變動的重要指標,體現了物種或種群對環境變動的適應特征[19]。豹紋脂身鯰卵徑均值為1.87 mm,較常見鯰形目魚類偏大,瓦氏黃顙魚(Pelteobaggrusvachelli)為1.5 mm[23],光澤黃顙魚(Pelteobaggrusnitidus)為1.56 mm[34],革胡子鯰(Clariidaegariepinus)為1.05 mm[35]。說明豹紋脂身鯰的單位體重繁殖投入、仔魚出膜和成活率可能會較其他鯰形目魚類高。從而可以保證當繁殖群體數量較少時仍可維持一定的種群數量[32]。
豹紋脂身鯰卵徑大,意味著卵含有更多的營養物質供孵化后的仔魚利用,從而增加每個卵發育成為成體的機會,故而出膜率和成活率高[19]。全年都具有一定比例的性成熟個體,說明豹紋脂身鯰已經在其分布區域建立可持續種群。樣本采集期間,通過走訪漁民,調查漁獲物組成與比例,我們發現豹紋脂身鯰的入侵已經給流溪河漁民帶來很大困擾,豹紋脂身鯰的大量繁殖減少了其他經濟魚類的捕獲量,并且破壞網具,嚴重影響了漁民的生產活動,造成了經濟損失。因此,豹紋脂身鯰做為一種常見的觀賞魚,在養殖和交易過程中,要避免逃逸并加強對自然種群的監測,以掌握其種群狀態及生態危害。同時我們應加強對豹紋脂身鯰的生物學和生態學研究,制定合適的管理和防治策略,在一定范圍內對入侵災害嚴重區域的豹紋脂身鯰進行集中清理。
[1] Sala O E, Chapin F S Ⅲ, Gardner R H, et al. Global Change, Biodiversity and Ecological Complexity[M]. Cambridge: Cambridge University Press, 1999: 304-328.
[2] 秦 偉, 賈文方, 杭雪花. 魚類多樣性保護與漁業的可持續發展[J]. 淡水漁業, 1999, 29(9):10-13.
[3] 湯嬌雯, 張 富, 陳兆波. 我國生物多樣性保護策略[J]. 淡水漁業, 2009, 39(4):77-81.
[4] 萬方浩, 郭建英, 王德輝, 等. 中國外來入侵生物的危害與管理對策[J]. 生物多樣性, 2002, 10(1):119-125.
[5] 周 偉. 云南濕地生態系統魚類物種瀕危機制初探[J]. 生物多樣性, 2000, 8(2):163-168.
[6] Radhakrishnan K V, Lan Z J, Zhao J. Invasion of the African sharp-tooth catfishClariasgariepinus( Burchell, 1822) in South China[J]. Biol Invas, 2011, 13:1723 -1727.
[7] 顧黨恩, 牟希東, 胡隱昌, 等. 廣東省主要水系外來水生動物初步調查[J]. 生物安全學報, 2012, 21(4):272-276.
[8] 潘 勇, 曹文宣, 徐立蒲, 等. 魚類入侵的生態效應及管理策略[J]. 淡水漁業, 2005, 35(6):61-64.
[9] Fuller P L, Nico L G, Williams J D. Nonindigenous fishes introduced to inland waters of the United States [M]. Bethesda, Maryland:American Fisheries Society, 1999:613.
[10] Jones R W, Weyl O L, Swartz E R, et al. Using a unified invasion framework to characterize Africa’s first loricariid catfish invasion [J]. Biol Invas, 2013, 15:2139-2145.
[11] Ishikawa T, Tachihara K. Introduction history of non-native freshwater fish in Okinawa-jima Island: ornamental aquarium fish pose the greatest risk for future invasions [J]. Ichthyol Res, 2014, 61:17-26.
[12] Jumawa J C, Herrera A A. Ovary morphology and reproductive features of the female suckermouth sailfin catfish,Pterygoplichthysdisjunctivus(Weber 1991) from Marikina River, Philippines [J].Asian Fish Sci, 2014, 27:75-89.
[13] Pound K L, Nowlin W H, Huffman D G, et al. Trophic ecology of a nonnative population of suckermouth catfish (Hypostomusplecostomus) in a central Texas spring-fed stream [J]. Environ Biol Fish, 2011, 90:277-285.
[14] Chavez J M, Manohar S K, Pagulayan R C, et al. New Philippine record of South American sailfin catfishes (Pisces: Loricariidae) [J]. Zootaxa, 2006, 1109:57-68.
[15] Nico L G, Jelks H L, Tuten T. Non-native suckermouth armored catfishes in Florida: Description of nest burrows and burrow colonies with assessment of shoreline conditions [J]. Aquat Nuis Spec Res Prog (ANSRP) Bull, 2009, 9(1):1-30.
[16] Capps K A, Flecker A S. Invasive aquarium fish transform ecosystem nutrient dynamics [J]. Proceed Royal Soc B-Biol Sci, 2013, 280:1520.
[17] 李家樂, 董志國, 李應森, 等. 中國外來水生動植物[M].上海:上海科學技術出版社, 2007: 57.
[18] 趙 俊, 易祖盛, 周先葉, 等. 廣州市水生動植物本底資源[M]. 北京:科學出版社, 2010:185-210.
[19] 殷名稱. 魚類生態學[M]. 北京:中國農業出版社, 1995.
[20] 凌建忠, 嚴利平, 林龍山, 等. 東海帶魚繁殖力及其資源的合理利用[J]. 中國水產科學, 2005, 12(6):726-730.
[21] 段中華, 孫建貽. 瓦氏黃顙魚的繁殖生物學研究[J]. 水生生物學報, 1999, 23(6):610-616.
[22] Alabsawy M A E. The reproductive biology and the histological and ultrastructural characteristics in ovaries of the female gadidae fishMerlucciusmerlucciusfrom the Egyptian Mediterranean water [J]. Afric J Biotech, 2010, 9(17):2544-2559.
[23] Wootton R J. Ecology of Teleost Fishes. Fish and Fisheries Series [M]. University of Michigan, Chapman and Hall, 1990:1-370.
[24] 何長才. 兩種海拔最高的魚類及其分布[J]. 四川動物, 1996, 15(3):116-117.
[25] 何德奎, 陳詠霞, 陳毅峰. 高原鰍屬TriPlophysa魚類的分子系統發育和生物地理學研究[J]. 自然科學進展, 2006, 16(11):1395-1404.
[26] Lashari P K, Narejo N T, Laghari M Y, et al. Studies on the gonado somatic index and fecundity of a carp Cirrhinusreba (Hamilton) from fishponds of district Jacobabad, Sindh, Pakistan [J]. Pakistan J Zool, 2007, 39(2):95-98.
[27] Liang S, Wu H, Shieh B. Size structure, reproductive phenology, and sex ratio of an exotic armored catfish (Liposarcusmultiradiatus) in the Kaoping River of southern Taiwan [J]. Zool Stud, 2005, 44:252-259.
[28] Gibbs M A, Shields J H, Lock D W, et al. Reproduction in an invasive exotic catfishPterygoplichthysdisjunctivusin Volusia Blue Spring, Florida, U.S.A [J]. J Fish Biol, 2008, 73:1562-1572.
[29] Moroni F T, Ortega A C, Moroni R B, et al. Limitations in decision context for selection of Amazonian armoured catfish acari-bod (Pterygoplichthyspardalis) as candidate species for aquaculture [J]. Int J Fish Aquacult, 2015, 7:142-150.
[30] 楊家云. 嘉陵江瓦氏黃顙魚的繁殖生物學[J]. 西南師范大學學報(自然科學版), 1994, 19(6):639-645.
[31] 劉 筠, 劉素嫻, 壽孝鍾, 等. 草魚性腺發育研究[J]. 湖南師范學院學報, 1962,(4):63-96.
[32] 曹克駒, 李明云. 鳧溪香魚繁殖生物學的研究[J]. 水產學報, 1982, 6(4):107-118.
[33] 劉明典, 黃福江, 朱佳志, 等. 大鱗裂峽鲃繁殖生物學特征[J]. 動物學雜志, 2015, 50(3):405-414.
[34] 諶海虎. 贛江南昌段光澤黃顙魚的年齡、生長和繁殖特征的初步研究[D]. 武漢:華中農業大學, 2010.
[35] 朱赟杰. 外來魚類革胡子鯰在華南地區的分布和種群生物學研究[D]. 上海:上海海洋大學, 2016.
(責任編輯:張紅林)
Reproductive biology ofPterygoplichthyspardalisin the Liuxi River
LIU fei1,2, WEI Hui1, GU Dang-en1, MU Xi-dong1, LUO Du1,XU Meng1, HU Yin-chang1
( 1.KeyLaboratoryofRecreationalFisheriesResearch,MinistryofAgriculture/PearlRiverFisheriesResearchInstitute,ChineseAcademyofFisherySciences,Guangzhou510380,China;2.CollegeofFisheriesandLifeScience,ShanghaiOceanUniversity,Shanghai201306,China)
To study reproductive biology of an invasive fish species,Pterygoplichthyspardalis, 283 specimens were collected from December 2015 to September 2016 in the Liuxi River, Guangzhou city. Sexual maturity coefficient ofP.pardaliswas relative high from March to September. The minimum size of mature male was 204 mm, and the minimum body weight was 154.88 g. The minimum size and weight of mature female were 201 mm and 183.01 g, respectively. The minimum age at maturity was age 1 for male and female. The mean mature oocyte diameter was 1.87 mm, and the absolute fecundity was 636-6 148 eggs. The mean absolute fecundity was 2 524.49 eggs and the mean relative fecundity was 10.43 eggs /g. Absolute fecundity positively correlated with body length and body weight. Sex ratio (♀∶♂) of mature individuals was 1∶1.15, which accorded with the 1∶1 ratio. These results suggested thatP.pardalismatured at small size and age, with high fecundity in the Liuxi River, which may contribute to population establishment and spread, resulting in adverse impact on the freshwater ecosystem.
Pterygoplichthyspardalis; gonad development; year cycle; fecundity
2016-11-08;
2017-01-18
農業部外來入侵生物防治項目(2130108)
劉 飛(1991- ),男,碩士研究生,專業方向為魚類生態學。E-mail:liufei636@163.com 通訊作者:胡隱昌,E-mail:huyc22@163.com
S931
A
1000-6907-(2017)02-0042-07

