血管緊張素轉化酶2減少胰島細胞的氧化應激及凋亡
史婷婷 楊芳遠,2 曹 曦,2 盧 晶,2 謝榮榮,2 袁明霞 楊金奎,2*
(1.首都醫科大學附屬北京同仁醫院內分泌科,北京 100730; 2.糖尿病防治研究北京市重點實驗室,北京 100730)
·內分泌與代謝病專題 ·
血管緊張素轉化酶2減少胰島細胞的氧化應激及凋亡
史婷婷1楊芳遠1,2曹 曦1,2盧 晶1,2謝榮榮1,2袁明霞1楊金奎1,2*
(1.首都醫科大學附屬北京同仁醫院內分泌科,北京 100730; 2.糖尿病防治研究北京市重點實驗室,北京 100730)
目的 探討血管緊張素轉化酶2(angiotensin converting enzyme 2,ACE2) 在胰島素分泌中的作用及可能的機制。方法提取C57BL/6小鼠的胰島,用棕櫚酸誘導氧化應激及凋亡。用ACE2及對照GFP的腺病毒對胰島進行感染。ELISA方法檢測胰島素分泌功能。DHE探針檢測活性氧(reactive oxygen species,ROS)濃度。蛋白質印記(Western blotting)方法檢測糖代謝及凋亡水平。結果 1)ACE2腺病毒感染后,胰島素分泌增加。2)ACE2腺病毒感染降低了氧化應激水平。3)ACE2 腺病毒感染減低胰島凋亡。結論 ACE2改善胰島素分泌功能,其機制可能與ACE2對氧化應激和凋亡的保護作用有關。
腎素血管緊張素系統; 血管緊張素轉化酶2; 胰島素; 氧化應激; 凋亡
腎素-血管緊張素系統(renin-angiotensin system, RAS)是人體內重要的體液調節系統。近年來研究[1-2]表明,RAS 系統參與糖尿病的發展。經典的血管緊張素轉化酶-血管緊張素Ⅱ途徑增加氧化應激及凋亡,從而造成胰島功能障礙及糖耐量受損[3-5]。血管緊張素轉化酶2(angiotensin-converting enzyme 2,ACE2)-血管緊張素(1-7)[Ang-(1-7)]-Mas軸作為RAS 系統新的調解軸,可能對2型糖尿病的發展起到一定的保護作用[6-8]。筆者的前期研究[9]表明,ACE2敲除的小鼠表現為糖耐量受損及胰島素分泌功能障礙。本文將通過體外胰島培養的方式研究ACE2對胰島及氧化應激的影響。
1 材料與方法
1.1 動物分組
成年雄性C57BL/6小鼠,體質量18~24 g,購自北京維通利華實驗動物公司[實驗動物許可證號:SCXK(京)2008-0001]。實驗所使用的所有動物均經過首都醫科大學附屬北京同仁醫院動物委員會批準。SPF級別動物房飼養。
1.2 胰島分離及培養
C57BL/6小鼠處死,打開腹腔,將十二指腸乳頭夾閉,在膽總管與膽囊管匯合處勻速注入膠原酶P, 注射過程中觀察胰腺膨脹程度,剪下充盈的胰腺放入盛有膠原酶的離心管中。37 ℃ 水浴消化10 min,使胰腺成泥沙狀。迅速取出,終止液終止消化,Ficoll 梯度離心,挑取胰島。將胰島移入RMPI 1640的培養基[10%(體積分數)胎牛血清,1%(體積分數)谷氨酰胺及1%(體積分數)青霉素鏈霉素]的培養皿,于37 ℃,5%(體積分數) CO2培養箱中孵育,過夜培養[10]。
1.3 藥物處理
用0.1 mol/L 的NaOH 溶液在70 ℃水浴中溶解一定量的棕櫚酸(palmitate, PA), 振蕩混勻10 min, 然后過濾,配成100 mmol/L的PA 儲存液。在55 ℃水浴中用去離子水配制50 g/L的牛血清白蛋白(bovine serum albumin,BSA)溶液, 過濾。然后將上述的PA溶液和BSA 溶液按1∶19的體積比混合配成5 mmol/L PA+50 g/L BSA 復合液。復合液在水浴中振蕩10 s后繼續水浴10 min, 取出后冷卻至室溫, 過濾。然后在培養液中稀釋至終濃度(0.4 mmol/L)[11]。
1.4 病毒感染
胰島原代細胞在ACE2腺病毒(5×108pfu/mL)或對照GFP病毒(5×108pfu/mL)孵育24 h,24 h后熒光顯微鏡觀察病毒感染效率。
1.5 實驗分組
用棕櫚酸處理胰島原代細胞24 h后,進行ACE2腺病毒(5×108pfu/mL)或對照GFP病毒(5×108pfu/mL)感染24 h。收集胰島,進行下一步功能實驗及蛋白水平檢測。
我們不去統計國家對文化事業投入的各項數據,但我們通過在基層的采訪和調研,所看到聽到的一些現象和聲音,應該是最生動的說明。
1.6 葡萄糖刺激的胰島素分泌試驗(glucose stimulated insulin secretion, GSIS)
將每孔15個胰島種于12孔板,用KRBB緩沖液 [129 mmol/L NaCl, 4.8 mmol/L KCL, 1.2 mmol/L MgSO4, 1.2 mmol/L KH2PO4, 2.5 mmol/L CaCL2, 5 mmol/L NaHCO3, 0.1% (質量分數) BSA, 10 mmol/L HEPES, pH 7.4]洗滌2遍并37 ℃孵箱平衡30 min,分別用2.8 mmol/L葡萄糖的KRBB孵育和含16.7 mmol/L葡萄糖的KRBB在37 ℃孵箱中處理1 h,收集上清,ELISA試劑盒(Millipore, Billerica, MA, 美國)測定胰島素[12]。
1.7 活性氧(reactive oxygen species, ROS)檢測
胰島細胞用棕櫚酸刺激,之后用ACE2腺病毒或GFP病毒處理24 h。二氫乙錠(dihydroethidium,DHE)檢測:培養的胰島用5 μmol/L DHE(Sigma公司,美國)在37 ℃孵箱中孵育40 min,磷酸緩沖鹽溶液(phosphate buffered saline, PBS)洗滌2次,讀取熒光強度[13]。
1.8 Western blotting
在4 ℃條件下,加入裂解液提取胰島蛋白。用BCA Protein Assay Kit 測定樣品蛋白濃度。每個樣本用30~60 μg蛋白進行SDS聚丙烯酰胺凝膠電泳并轉至PVDF上,用含5%(質量分數)脫脂奶粉的TBST溶液封閉4 h,加入一抗于4 ℃孵育過夜。TBST漂洗2次,每次5 min,加入1∶5 000辣根過氧化酶標記的二抗,室溫孵育1 h,TBST漂洗6次,每次5 min,肌動蛋白(beta actin)為內參,將膜用化學發光試劑孵育 1 min,于X線膠片上曝光,常規顯影、定影。抗體均購自美國Santa Cruz公司。
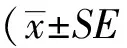
2 結果
2.1 ACE2過表達改善了胰島的GSIS功能
在高糖(16.7 mmol/L)刺激下, PA孵育胰島后胰島素分泌水平顯著下降,但感染ACE2腺病毒后,葡萄糖刺激的胰島素分泌水平較對照GFP病毒組升高(圖1)。該結果提示ACE2可以部分恢復高脂肪酸造成的胰島素分泌障礙。
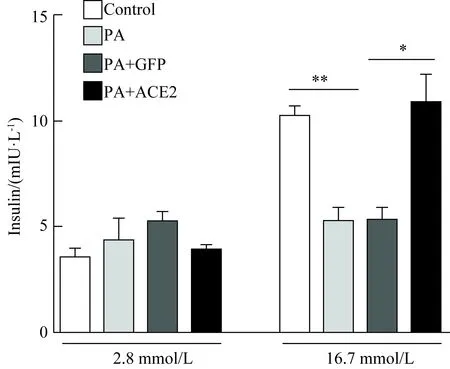
圖1 ACE2對胰島GSIS 功能的影響
*P<0.05;**P<0.01; ACE2: angiotensin converting enzyme 2; GSIS:glucose stimulated insulin secretion;PA:palmitate;GFP: green fluorescent protein;n=5, Data are shown as means ±SE.
2.2 ACE2過表達降低胰島中活性氧簇(ROS)的產生
用PA干預后胰島的活性氧簇(ROS)較未干預組明顯增高,但ACE2病毒感染后ROS較對照GFP組顯著降低(圖2)。結果提示,ACE2可以抑制胰島細胞內ROS的產生及氧化應激。
2.3 ACE2過表達降低了胰島的凋亡
與對照GFP病毒組相比,ACE2腺病毒感染后降低了caspase 9 及caspase 3 表達(圖3),因此提示ACE2抑制了caspase 3凋亡途徑。
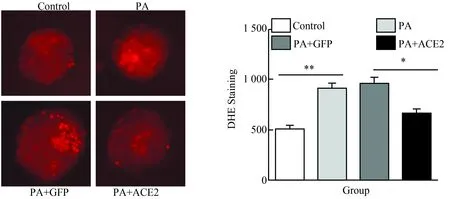
圖2 ACE2對胰島內ROS濃度的影響
*P<0.05;**P<0.01; Data are shown as means ±SE. ACE2: angiotensin converting enzyme 2; ROS: reactive oxygen species; PA:palmiate; GFP: green fluorescent protein; DHE: dihydroethidium.
圖3 ACE2 對胰島中凋亡通路的影響
*P<0.05;**P<0.01;n=3. Data are shown as means ±SE. ACE2: angiotensin converting enzyme 2; PA:palmiate; GFP: green fluorescent protein.
3 討論
腎素-血管緊張素系統是人體內重要的體液調節系統。RAS既存在于循環系統中,也存在于胰腺、血管壁、心臟、中樞、腎臟和腎上腺等組織中,共同參與對靶器官的調節。在正常情況下,它對心血管系統的正常發育、心血管功能穩態、電解質和體液平衡的維持以及血壓的調節均有重要作用。目前已經有研究[14]表明該系統參與調解糖代謝,阻斷RAS可以減少新發糖尿病,對卡托普利預防計劃(CAPPP)、心臟轉歸預防評估(HOPE)等研究的薈萃分析顯示,ACEI可以減少27%的新發糖尿病。其確切機制尚不清楚,部分歸因于胰島素抵抗的改善,但隨著胰島局部RAS系統的確立,RAS抑制劑對胰島細胞的保護作用逐漸受到關注[15]。胰島局部的AngⅡ可以調節胰島血流、氧分壓、胰島素合成和氧化應激[16-17]。ACE2是RAS系統中的關鍵酶,它將血管緊張素Ⅱ分解為血管緊張素1-7,血管緊張素1-7通過與其mas受體結合發揮著拮抗血管緊張素Ⅱ 的作用。筆者前期的研究[9]表明,ACE2敲除的小鼠表現為糖耐量受損及胰島素分泌功能障礙。腺病毒轉染ACE2基因到糖尿病db/db小鼠,檢測到胰島的凋亡減少及胰島素分泌增加[18]。研究[19]表明,ACE2可以提高胰島微血管內皮功能從而保護胰島功能。筆者的研究表明,ACE2腺病毒感染胰島后可以提高胰島素分泌能力,該現象可能與減少了胰島的氧化應激及凋亡有關。
棕櫚酸可以誘導細胞中ROS的產生以及細胞氧化應激及凋亡[20]。在正常情況下,機體內ROS的產生和ROS清除系統處于動態平衡狀態。由于種種原因,導致ROS產生增多或/和機體清除ROS能力的下降,機體就會出現氧化應激。當機體處于氧化應激狀態時,體內組織細胞ROS量相對升高,超過機體的清除能力,可導致機體組織脂質過氧化水平升高,引起細胞凋亡。在細胞凋亡早期ROS濃度升高和線粒體膜電位下降,隨后出現caspase-3的激活和DNA斷裂產生凋亡。在本研究中,筆者通過在體外棕櫚酸孵育,誘導胰島細胞出現分泌功能障礙及氧化應激。caspase-3 通路是經典的凋亡途徑,這個通路的表達上調提示細胞凋亡水平的增加[21-22]。有研究[23]表明血管緊張素Ⅱ 增加caspase-3的表達從而增加凋亡,本研究表明ACE2可以抑制氧化應激的水平及caspase-3的表達從而抑制凋亡的發生,更加明確了ACE2在胰島中起到的保護作用。
本研究存在以下不足:1)目前的實驗結果為體外實驗,下一步筆者計劃在高脂喂養的小鼠模型上進一步觀察ACE2-Ang1-7-MAS軸對胰島氧化應激和胰島功能的影響。2)目前,ACE2對氧化應激的影響得到一定的證實,但其具體機制需要進一步探討,筆者將在線粒體線內質網方面進行進一步的研究。
綜上所述,本研究結果表明,ACE2上調可以對胰島素分泌起到保護作用。這一過程可能是通過減少氧化應激水平來實現的。本研究結果進一步明確了ACE2在糖代謝中的調節作用,并為糖尿病的治療提供了新的線索。
[1] Hayden M R, Sowers J R. Pancreatic renin-angiotensin-aldosterone system in the cardiometabolic syndrome and type 2 diabetes mellitus[J]. J Cardiometab Syndr, 2008,3(3):129-131.
[2] Bindom S M, Lazartigues E. The sweeter side of ACE2: physiological evidence for a role in diabetes[J]. Mol Cell Endocrinol, 2009,302(2):193-202.
[3] Takayanagi T, Kawai T, Forrester S J, et al. Role of epidermal growth factor receptor and endoplasmic reticulum stress in vascular remodeling induced by angiotensin Ⅱ[J]. Hypertension, 2015,65(6):1349-1355.
[4] Ha T S, Park H Y, Seong S B, et al. Angiotensin Ⅱ induces endoplasmic reticulum stress in podocyte, which would be further augmented by PI3-kinase inhibition[J].Clin Hypertens,2015,21:13.
[5] Wang J, Wen Y, Lv L L. Involvement of endoplasmic reticulum stress in angiotensin Ⅱ-induced NLRP3 inflammasome activation in human renal proximal tubular cells in vitro[J]. Acta Pharmacol Sin,2015, 36(7):821-830.
[6] Murugan D, Lau Y S, Lau C W, et al. Angiotensin 1-7 protects against angiotensin Ⅱ-Induced endoplasmic reticulum stress and endothelialdDysfunction via mas receptor[J]. PLoS One, 2015,10(12):e0145413.
[7] Uhal B D, Nguyen H, Dang M. Abrogation of ER stress-induced apoptosis of alveolar epithelial cells by angiotensin 1-7[J]. Am J Physiol Lung Cell Mol Physiol, 2013,305(1):L33-41.
[8] Singh T, Singh K, Sharma P L. Ameliorative potential of angiotensin1-7/Mas receptor axis in streptozotocin-induced diabetic nephropathy in rats[J]. Methods Find Exp Clin Pharmacol, 2010,32(1):19-25.
[9] Niu M J, Yang J K, Lin S S, et al. Loss of angiotensin-converting enzyme 2 leads to impaired glucose homeostasis in mice[J]. Endocrine, 2008,34(1-3):56-61.
[10]Carter J D, Dula S B, Corbin K L,et al. A practical guide to rodent islet isolation and assessment[J]. Biol Proced Online,2009, 11:3-31.
[11]Cnop M, Abdulkarim B, Bottu G, et al. RNA sequencing identifies dysregulation of the human pancreatic islet transcriptome by the saturated fatty acid palmitate[J]. Diabetes, 2015, 63(6):1978-1993.
[12]McCommis K S, Hodges W T, Bricker D K, et al. An ancestral role for the mitochondrial pyruvate carrier in glucose-stimulated insulin secretion[J]. Mol Metab, 2016, 5(8):602-614.
[13]Zhang F, Liu C, Wang L, et al. Antioxidant effect of angiotensin (17) in the protection of pancreatic β cell function[J]. Mol Med Rep, 2016,14(3):1963-1969.
[14]Liang D L, Li X Y, Wang L, et al. Current status and influence factors of ACEⅡ/ARB application in elderly coronary heart disease outpatients complicated with diabetes mellitus in China[J]. Zhonghua Yi Xue Za Zhi, 2016, 96 (36):2917-2922.
[15]Prentki M, Nolan C J. Islet beta cell failure in type 2 diabetes[J]. J Clin Invest, 2006, 116(7):1802-1812.
[16]Favre G A, Esnault V L, Van Obberghen E. Modulation of glucose metabolism by the renin-angiotensin-aldosterone system[J]. Am J Physiol Endocrinol Metab, 2015,308(6):E435-E449.
[17]Lau Y S, Tian X Y, Mustafa M R, et al. Boldine improves endothelial function in diabetic db/db mice through inhibition of angiotensin Ⅱ-mediated BMP4-oxidative stress cascade[J]. Br J Pharmacol, 2013,170(6):1190-1198.
[18]Bindom S M, Hans C P, Xia H, et al. Angiotensin I-converting enzyme type 2 (ACE2) gene therapy improves glycemic control in diabetic mice[J]. Diabetes, 2010,59(10):2540-2548.
[19]Lu C L, Wang Y, Yuan L, et al. The angiotensin-converting enzyme 2/angiotensin (1-7)/Mas axis protects the function of pancreaticβ cells by improving the function of islet microvascular endothelial cells[J]. Int J Mol Med, 2014,34(5):1293-1300.
[20]Cnop M, Abdulkarim B, Bottu G, et al. RNA sequencing identifies dysregulation of the human pancreatic islet transcriptome by the saturated fatty acid palmitate[J]. Diabetes, 2014,63(6):1978-1993.
[21]Zhu B, Zhang L, Zhang Y Y, et al. DNase I aggravates islet β-cell apoptosis in type 2 diabetes[J]. Mol Med Rep, 2016,13(6):4577-4584.
[22]Yu C, Cui S, Zong C, et al. The orphan nuclear receptor NR4A1 protects pancreatic β-Cells from endoplasmic reticulum (ER) stress-mediated apoptosis[J]. J Biol Chem, 2015,290(34):20687-20699.
[23]李偉,羅振華,付凌云,等. 銀杏提取物對血管緊張素Ⅱ 誘導的新生大鼠心肌細胞凋亡的影響[J]. 貴陽醫學院學報,2015,40(9):910-918.
編輯 陳瑞芳
Angiotensin converting enzyme 2 improves insulin secretion in islets
Shi Tingting1, Yang Fangyuan1,2, Cao Xi1,2, Lu Jing1,2, Xie Rongrong1,2, Yuan Mingxia1,2, Yang Jinkui1,2*
(1.DepartmentofEndocrinology,BeijingTongrenHospital,CapitalMedicalUniversity,Beijing100730,China; 2.BeijingKeyLaboratoryofDiabetesResearchandCare,Beijing100730,China)
Objective The aim of the study was to identify the roles of angiotensin-converting enzyme 2 (ACE2) in insulin secretion in islets and to characterize the related mechanisms. Methods Islets from C57BL/6 mice were treated with palmitate acid and infected with adenovirus combined ACE2 or GFP. Glucose stimulated insulin secretion was assayed by ELISA kit. Reactive oxygen species (ROS) was measured by dihydroethidium (DHE). The expression of glucose metabolism gene expression and caspase was assayed by Western blotting. Results ①ACE2 over-expression increased insulin secretion. ②ACE2 over-expression down-regulated ROS content in islets. ③ACE2 over-expression down-regulated apoptosis in islets. ConclusionACE2 could be involved in improving insulin secretion via anti-oxidative and anti-apoptotic effects.
rennin-angiotensin system; angiotensin-converting enzyme 2; insulin; oxidative stress; apoptosis
國家自然科學基金(81370946, 81400824, 81300726),北京市自然科學基金(7131005),首都醫科大學附屬北京同仁醫院科研基金(2015-YJJ-ZZL-006 )。This study was supported by National Natural Science Foundation of China (81370946, 81400824, 81300726),Natural Science Foundation of Beijing (7131005), Foundation of Beijing Tongren Hospital, Capital Medical University (2015-YJJ-ZZL-006 )
時間:2017-04-13 19∶30
http://kns.cnki.net/kcms/detail/11.3662.R.20170413.1930.002.html
10.3969/j.issn.1006-7795.2017.02.002]
R587.1
2017-01-20)
*Corresponding author, E-mail:jinkui.yang@gmail.com

