辛二酰苯胺異羥肟酸誘導大鼠原代肝星狀細胞凋亡*
劉 幸, 田 甜, 余 蕾, 詹 瑋, 韓 冰, 謝汝佳, 楊 婷, 羅新華, 楊 勤
(貴州醫科大學病理生理學教研室, 貴州 貴陽 550000)
辛二酰苯胺異羥肟酸誘導大鼠原代肝星狀細胞凋亡*
劉 幸, 田 甜, 余 蕾, 詹 瑋, 韓 冰, 謝汝佳, 楊 婷, 羅新華, 楊 勤△
(貴州醫科大學病理生理學教研室, 貴州 貴陽 550000)
目的: 通過研究辛二酰苯胺異羥肟酸(SAHA)對大鼠原代肝星狀細胞(HSCs)凋亡及相關蛋白表達的影響,探討SAHA誘導HSCs凋亡的作用機制。方法: 采用OptiPrep梯度離心法分離大鼠原代HSCs;通過實時細胞分析技術檢測SAHA對HSCs增殖的影響;倒置顯微鏡觀察不同濃度SAHA處理HSCs后的形態變化;熒光顯微鏡及流式細胞術Annexin V-FITC/PI法檢測細胞凋亡率;Western blotting法檢測α-平滑肌肌動蛋白(α-SMA)、Ⅰ型膠原、金屬蛋白酶組織抑制物1(TIMP1)、葡萄糖調節蛋白78(GRP78)和組蛋白去乙酰化酶6(HDAC6)的蛋白表達;免疫共沉淀法檢測GRP78蛋白與HDAC6蛋白是否形成復合物。結果: 成功分離的HSCs連續培養14 d,HSCs逐漸由靜止狀態變為激活狀態。 SAHA可顯著抑制HSCs增殖,且呈劑量時間依賴性(P<0.05); SAHA對HSCs的促凋亡作用具有時間依賴性(P<0.05)。SAHA處理HSCs后, α-SMA、Ⅰ型膠原、HDAC6和TIMP1的蛋白表達水平明顯降低(P<0.05),GRP78的蛋白表達水平明顯升高(P<0.05)。與激活型的HSCs相比,SAHA處理后的HSCs中免疫共沉淀下的蛋白復合物中GRP78與總的乙酰化賴氨酸蛋白顯著增多,而HDAC6蛋白顯著降低,同時證明GRP78與HDAC6形成復合物。結論: SAHA抗肝纖維化的機制可能是,SAHA下調HDAC6蛋白表達水平,上調乙酰化GRP78蛋白表達水平,誘導HSCs內質網應激,促進肝星狀細胞凋亡,從而起到抗肝纖維化的作用。
肝星狀細胞; 辛二酰苯胺異羥肟酸; 肝纖維化; 細胞凋亡
各種慢性肝損傷因素如病毒、酒精、脂肪以及免疫因子導致肝細胞受損,壞死而產生并釋放大量炎性物質,直接或間接地損害臨近的肝臟細胞,并引起肝Kupffer細胞、肝竇內皮細胞、肝星狀細胞等合成分泌更多細胞因子及炎性物質,作用于靜息狀態下的肝星狀細胞(hepatic stellate cells,HSCs),使其活化增殖向肌成纖維樣細胞方向分化轉變為激活型HSCs。激活型HSCs合成并分泌以Ⅰ型和Ⅲ型膠原為主的細胞外基質(extracellular matrix,ECM),同時分泌大量的金屬蛋白酶組織抑制物(tissue inhibitor of metalloproteinases,TIMPs),抑制組織基質金屬蛋白酶(tissue metalloproteinases,TMPs)對ECM的降解,使得過多的ECM在肝內沉積[1-2],從而導致肝纖維化的發生發展。
近來的研究表明,辛二酰苯胺異羥肟酸(suberoylanilide hydroxamic acid,SAHA)對血液系統疾病、骨髓瘤及肺纖維化有良好的治療作用,SAHA主要通過抑制組蛋白去乙酰化酶(histone deacetylase,HDAC)活性,干擾HDAC的募集功能,調控凋亡相關基因,抑制癌細胞增殖及誘導癌細胞周期阻滯、分化和凋亡,從而達到抗腫瘤目的[3-4]。有研究報道,SAHA可通過調節p53和bax基因影響人肝癌SMMC-7721細胞的增殖和凋亡[5]。本實驗擬通過觀察SAHA對HSCs增殖及凋亡的影響,探討SAHA有無促肝星狀細胞凋亡的作用及其可能的機制。
材 料 和 方 法
1 實驗動物
清潔級雄性Wistar大鼠,體重350~500 g,由貴州省實驗動物中心提供,合格證編號為(黔)2003-01。
2 主要試劑
DMEM培養基購自HyClone;胎牛血清購自Gibco;蛋白Marker購自Solarbio;二甲基亞砜購自北京鼎國公司;細胞裂解液、Annexin V-FITC/PI細胞凋亡檢測試劑盒和噻唑藍均購自上海碧云天生物技術有限公司;BCA蛋白定量試劑盒購自康為世紀有限公司;山羊抗兔IgG以及抗β-actin、α-平滑肌肌動蛋白(α-smooth muscle actin,α-SMA)、TIMP1、I型膠原和HDAC6抗體均購自武漢博士德有限公司;兔抗葡萄糖調節蛋白78(glucose-regulated protein 78,GRP78)購自Abcam;免疫共沉淀試劑盒購自Thermo Scientific;SAHA購自上海瀚香生物科技公司。
3 主要方法
3.1 大鼠原代肝星狀細胞分離與培養 參考戴春蕾等[6]的實驗方法,分離大鼠HSCs,用1 mL含20%胎牛血清的DMEM重懸細胞,臺盼藍染色計算細胞存活率。用血球計數板進行細胞計數,調整細胞濃度為(1~2)×1010/L,接種于10 cm無包被塑料培養皿中,倒置顯微鏡下連續觀察細胞形態學變化情況,并置于5% CO2、37 ℃培養箱中培養。培養24 h后換液,以后根據細胞生長狀況,2~3 d換液1次。
3.2 實時細胞分析技術檢測SAHA對HSCs細胞增殖的影響 取E-plate16細胞增殖檢測板,每孔加入培養液50 μL,放入RTCA DP設備中檢測背景值,然后將細胞消化懸浮于含有血清的培養液中,吹打均勻調整細胞密度為1×108/L,接種E-plate 16細胞增殖檢測板,置于37 ℃、5 % CO2及飽和濕度條件下細胞培養箱中穩定30 min后,對照組為不含SAHA的全培養基,實驗組SAHA終濃度為分別為1、5和10 μmol/L進行動態檢測72 h,觀察細胞增殖曲線。
3.3 倒置顯微鏡觀察HSCs細胞形態變化 靜止型的HSCs連續培養12 d以上,HSCs由靜止狀態變為激活型的HSCs,待細胞融合成片,分為對照組(DMEM培養基)和實驗組(5 μmol/L SAHA)。觀察SAHA處理HSCs 48 h后的形態變化。
3.4 凋亡原位熒光及流式細胞術檢測經5 μmol/L SAHA處理后HSCs 細胞的凋亡 HSCs由靜止狀態變為激活型的HSCs,待細胞融合成片進行操作。實驗分對照組以及5 μmol/L SAHA處理HSCs 24 h、48 h和72 h組;培養結束后,按Annexin V-FITC/PI細胞凋亡檢測試劑盒說明書進行操作,用倒置熒光顯微鏡進行觀察拍照、流式細胞儀檢測細胞凋亡率。
3.5 Western blotting法檢測α-SMA、TIMP1、I型膠原、GRP78和HDAC6蛋白的表達 收集各實驗組細胞,提取蛋白。聚丙烯酰胺凝膠電泳,轉膜,脫脂奶粉封閉,加入對應抗體,4 ℃過夜。次日,TBST洗膜后加入對應 II 抗,室溫孵育90 min,ECL發光成像,用ImageLab圖像分析軟件對每個條帶灰度值進行定量分析。
3.6 免疫共沉淀法檢測GRP78與HDAC6是否形成復合物 免疫共沉淀試劑盒說明書操作,單個IP,取10 μL GRP78單克隆抗體與50 μL AminoLink偶聯樹脂進行交聯固定,陰性對照組為正常兔IgG,按照10 μL兔IgG與50 μL AminoLink偶聯樹脂進行交聯固定,將固定好的AminoLink-GRP78和AminoLink-IgG復合物置于4 ℃冰箱保存備用。接下來將預冷的IP裂解液按照試劑盒要求每10 cm培養皿中加入500 μL IP裂解液,冰上孵育5 min,收集細胞裂解液于離心管中,13 000×g離心10 min,棄沉淀,收集上清于新的離心管中,然后用對照瓊脂糖樹脂預處理各實驗組細胞裂解液,以去除免疫共沉淀過程中非特異性結合的蛋白,每個實驗組取10 μL上清液留作input。接下來進行免疫共沉淀,向交聯好的單個IP的抗體復合物AminoLink-GRP78和AminoLink-IgG 中分別加入對應實驗組細胞裂解液200 μL,4 ℃搖床過夜。洗脫與AminoLink-GRP78和AminoLink-IgG結合的目的蛋白復合物,收集洗脫液于新的離心管中,制備蛋白樣品,向樣品中加入試劑盒配備的上樣緩沖液,置于金屬水浴鍋中100 ℃、5 min,冷卻至室溫,進行電泳。
4 統計學處理
用SPSS 19.0統計軟件進行分析。數據均采用均數±標準差(mean±SD)表示,多組間比較采用單因素方差分析,各組均數間兩兩比較采用最小顯著性差異法(LSD法);兩組樣本均數比較采用兩個獨立樣本的t檢驗,以P<0.05為差異有統計學意義。
結 果
1 大鼠原代HSCs提取及培養
普通光學顯微鏡下觀察分離出的HSCs,經血球計數板計數,細胞得率為每只4×107個。0.4%臺盼藍染色計算細胞活率為97%。光學顯微鏡下觀察分離的HSCs為折光性強的圓球形小體,隨著培養時間增加,細胞逐漸貼壁,形態發生明顯改變,由圓球形變為橢圓型、梭型、T型、不規則三角形,連續培養14 d,HSCs 融合成片,完全活化,見圖1。

Figure 1.The morphological changes during the culture of hepa-tic stellate cells isolated from the rats (×200). A: the ratinsituperfusion; B: the gradient centrifugation; C: 0 h after isolation; D: 14 d after isolation.
圖1 大鼠原代HSCs提取及體外培養過程中大鼠原代HSCs的形態學變化
2 RTCA 檢測SAHA對HSCs增殖的影響
與對照組相比,SAHA能夠顯著抑制HSCs增殖,并呈現時間劑量依賴性。1、5和10 μmol/L的SAHA培養HSCs 24 h、48 h和72 h后均能顯著抑制HSCs增殖(P<0.05),見圖2、表1。

Figure 2.The time-effect curves of HSCs treated with SAHA.n=5.
圖2 SAHA對HSCs增殖的時-效曲線
3 不同濃度的SAHA對HSCs細胞形態的影響
不同濃度SAHA處理HSCs 48 h后,形態發生顯著改變;1 μmol/LSAHA處理HSCs 48 h后,少數細胞體積縮小,上清液中可見少許漂浮細胞;以5及10 μmol/L的SAHA處理HSCs后,細胞增殖明顯被抑制,活細胞數目減少、發生貼壁不良、折光率差等形態變化,見圖3。
表1 SAHA對HSCs增殖的影響
Table 1.The effects of SAHA on the proliferation of HSCs (Mean±SD.n=3)
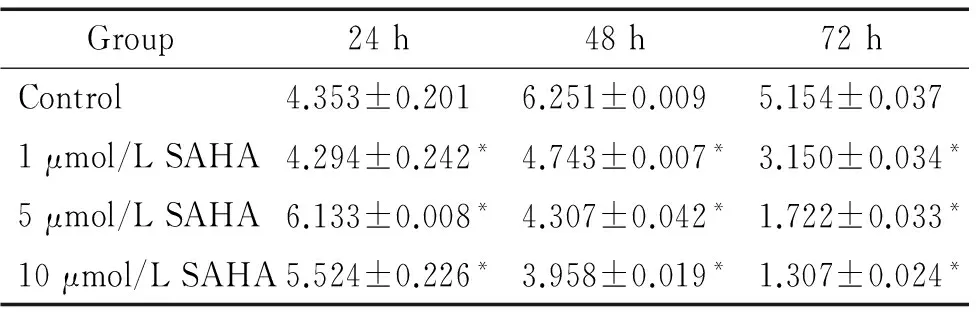
Group24h48h72hControl4.353±0.2016.251±0.0095.154±0.0371μmol/LSAHA4.294±0.242*4.743±0.007*3.150±0.034*5μmol/LSAHA6.133±0.008*4.307±0.042*1.722±0.033*10μmol/LSAHA5.524±0.226*3.958±0.019*1.307±0.024*
*P<0.05vscontrol group.
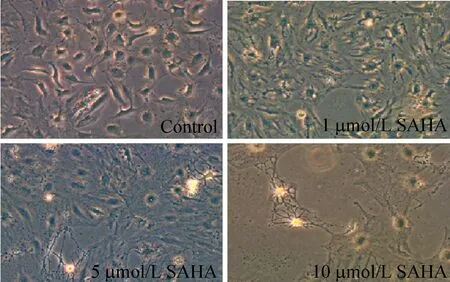
Figure 3.The effect of SAHA on the morphological changes of HSCs observed under inverted microscope (×200).
圖3 SAHA處理HSCs 48 h對細胞形態學變化的影響
4 5 μmol/L SAHA對HSCs凋亡的影響
5 μmol/L SAHA處理HSCs 24 h可見少許早期凋亡細胞,細胞膜被染成綠色,細胞核被染成紅色;48 h可見較多細胞膜被染色,72 h,大部分細胞膜不完整,細胞核被PI染成紅色。隨著SAHA處理時間延長,HSCs的早期凋亡率和晚期凋亡率逐漸上升,24 h、48 h和72 h早期凋亡率為分別為(7.99±0.03)%、(9.59±0.23)%和(16.31±0.83)%,均高于對照組(P<0.05),見圖4、5和表2。
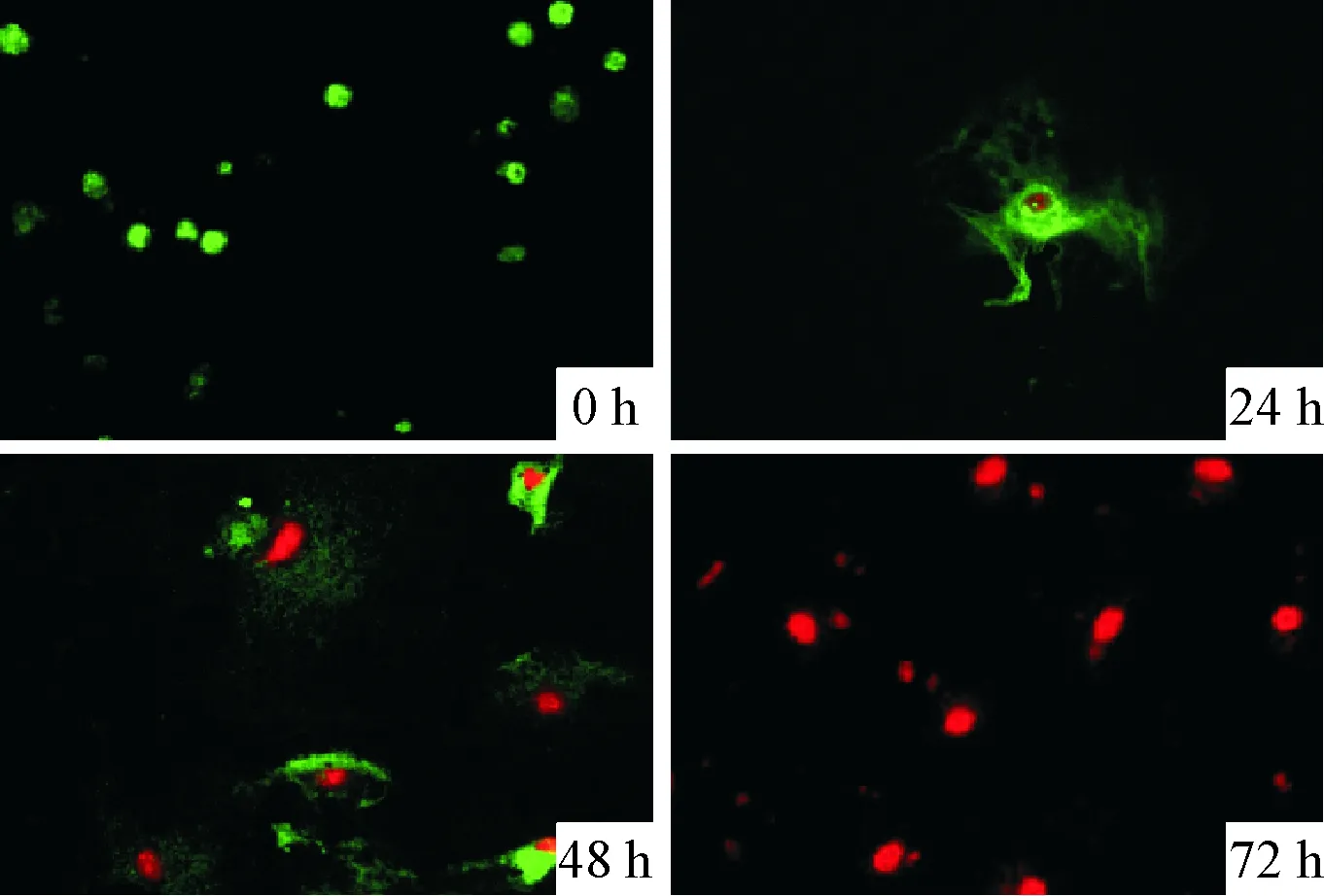
Figure 4.The apoptosis of HSCs treated with 5 μmol/L SAHA at different time points (×200).
圖4 5 μmol/L SAHA處理HSCs不同時間對細胞凋亡的影響

Figure 5.The apoptosis of HSCs cells treated with 5 μmol/L SAHA at different time points.
圖5 SAHA 對HSCs凋亡的影響
表2 5 μmol/L SAHA對 HSCs凋亡率的影響
Table 2.The effects of SAHA at 5 μmol/L on the apoptotic rate of HSCs cells (%. Mean±SD.n=3)
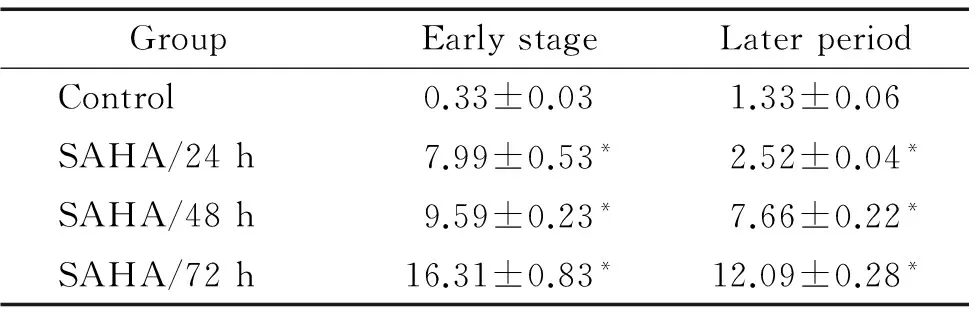
GroupEarlystageLaterperiodControl0.33±0.031.33±0.06SAHA/24h7.99±0.53*2.52±0.04*SAHA/48h9.59±0.23*7.66±0.22*SAHA/72h16.31±0.83*12.09±0.28*
*P<0.05vscontrol group.
5 5 μmol/L SAHA處理HSCs 48 h 對α-SMA、TIMP1、I型膠原、GRP78和HDAC6表達的影響
5 μmol/L SAHA處理HSCs細胞48 h后,HSCs細胞中α-SMA、TIMP1、HDAC6及Ⅰ型膠原蛋白表達水平明顯降低(P<0.05);而GRP78蛋白表達水平較對照組顯著升高(P<0.05),見圖6、7。
6 GRP78和HDAC6在HSCs中形成復合物
在激活型HSCs中和經SAHA處理后的HSCs中均檢測到GRP78與HDAC6形成復合物,見圖8。
討 論
HSCs的凋亡與肝纖維化的發生發展有密切的關系,HSCs由靜止狀態變為激活狀態是肝纖維化的關鍵環節,激活型的HSCs合成大量的細胞外基質,
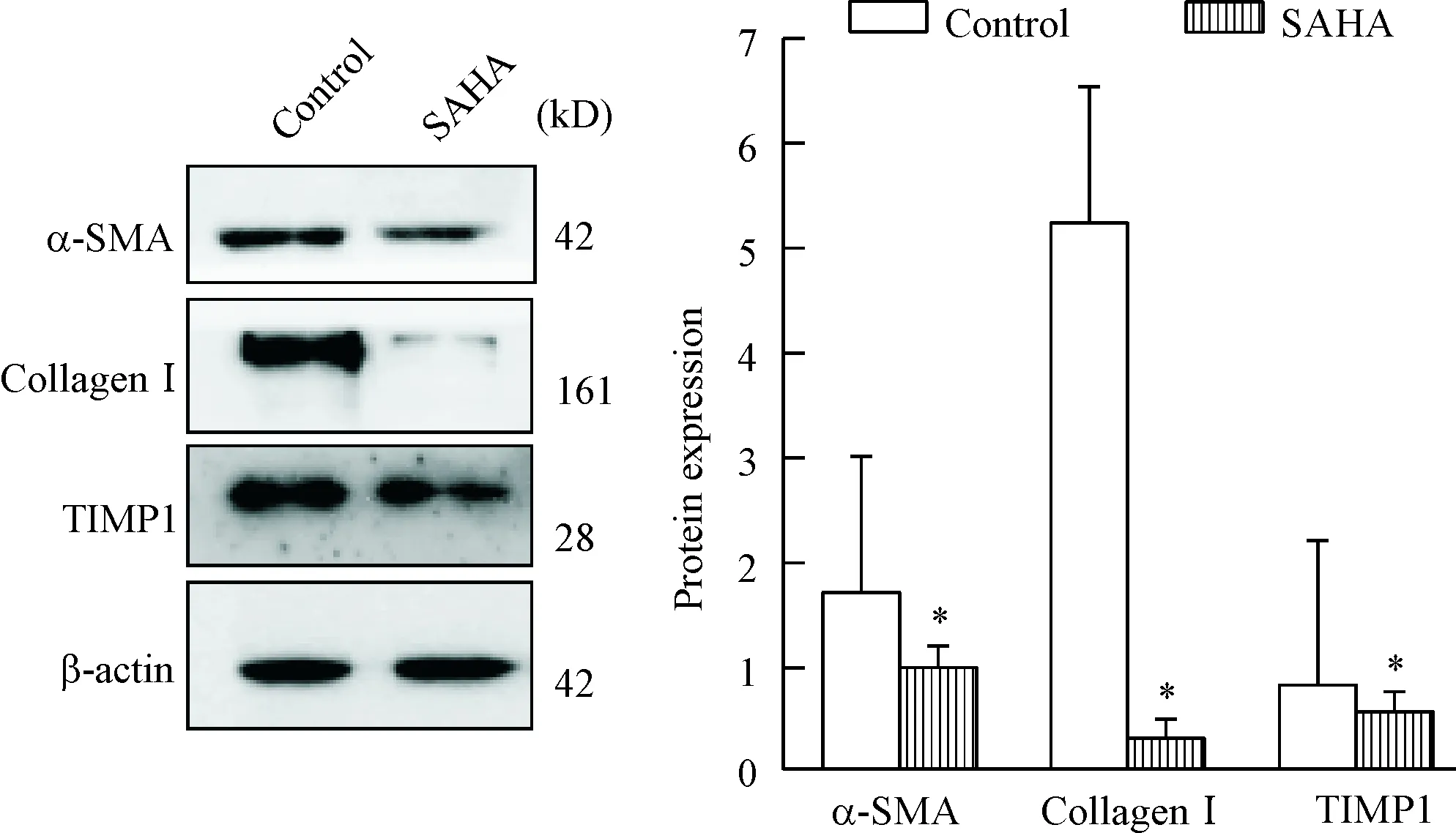
Figure 6.The protein expression of α-SMA, TIMP1 and collagen I in active HSCs treated with or without SAHA. Mean±SD.n=5.*P<0.05vscontrol group.
圖6 經SAHA處理后的激活型HSCs中α-SMA、 I型膠原和TIMP1蛋白表達的變化
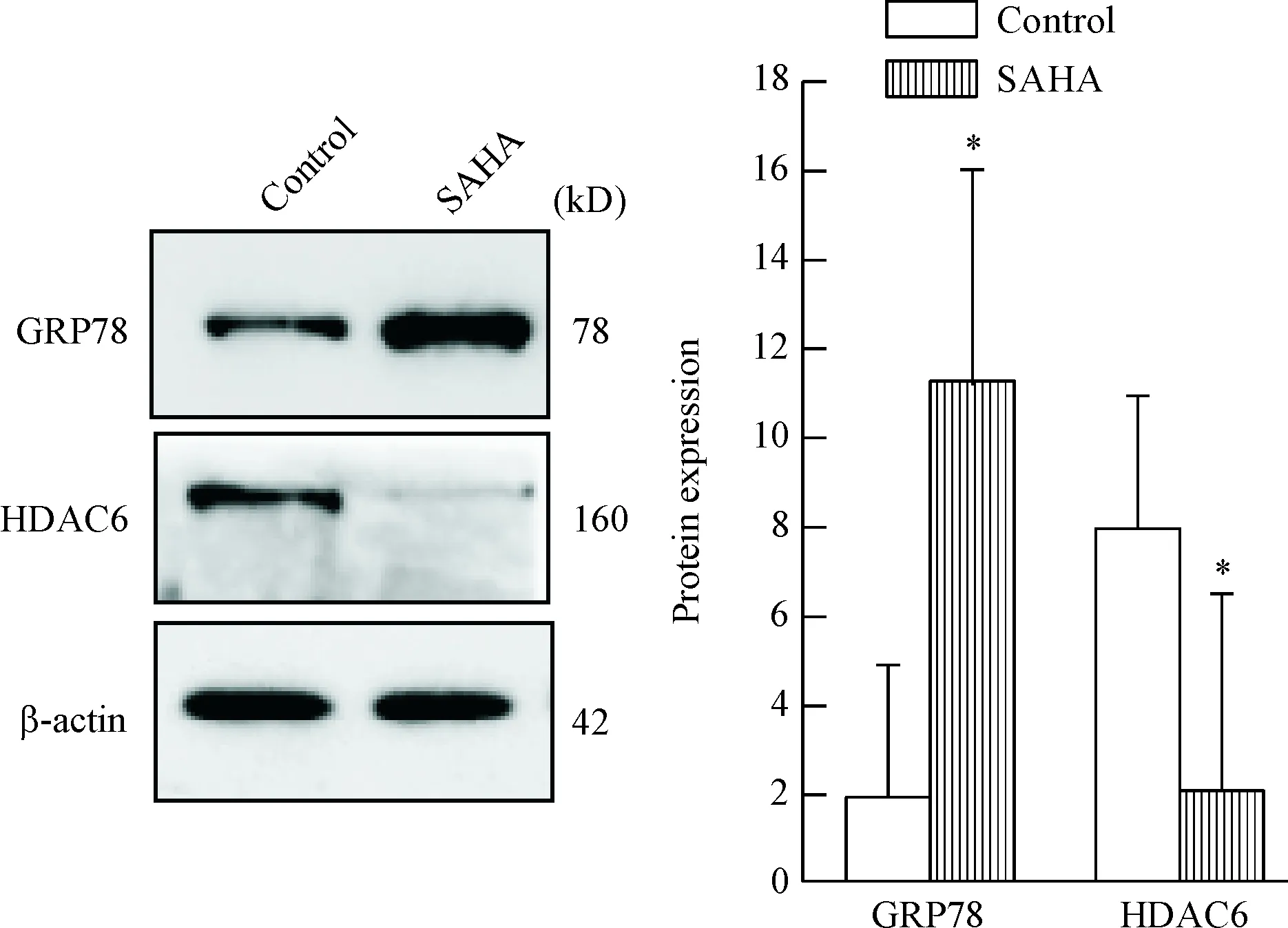
Figure 7.The protein expression of HDAC6 and GRP78 in active HSCs treated with or without SAHA. Mean±SD.n=5.*P<0.05vscontrol group.
圖7 經SAHA處理后的激活型HSCs中HDAC6和GRP78蛋白表達

Figure 8.Identification of GRP78, HDAC6 and ac-lysine by Co-IP and Western blotting.
圖8 Western blotting檢測Co-IP 分離HSCs的GRP78、HDAC6和乙酰化lysine蛋白水平
沉積在細胞間隙,導致肝纖維化[7]。因此,尋求有效誘導HSCs凋亡的藥物是防治肝纖維化的關鍵。
SAHA中文名伏立諾他,是美國食品藥品管理局批準的第一個可以用于臨床的制劑。有體外研究表明,SAHA在納摩爾級濃度即可抑制HDAC1、HDAC2、HDAC3和HDAC6的活性,且可特異性誘導腫瘤細胞凋亡,對正常細胞毒副作用小[8]。
本實驗用實時細胞分析技術的檢測結果提示,不同濃度SAHA隨著作用時間的延長,與對照組相比HSCs增殖明顯下降。倒置顯微鏡下可見HSCs形態發生顯著變化,部分HSCs發生貼壁不良,折光性差等改變。正常HSCs不會被Annexin-V FITC/PI染色,在細胞凋亡發生的早期,細胞膜電位和線粒體膜電位下降,膜流動性降低,細胞膜結構發生了重排,一些在細胞膜內部的生物大分子如磷脂酰絲氨酸(phosphatidylserine,PS)基團從細胞膜內側暴露到細胞膜外側,Annexin-V FITC可以特異性標記磷脂酰絲氨酸基團,進而識別發生早期凋亡的細胞;在細胞凋亡晚期,細胞膜的完整性幾乎全部遭到破壞,PI直接與DNA結合,發出紅色熒光;通過流式細胞術觀察到5 μmol/L SAHA能有效誘導HSCs凋亡,具有潛在的抗肝纖維化作用。
有文獻報道,SAHA可以明顯降低TGF-β1誘導的大鼠肺成纖維化細胞ILF細胞株α-SMA和Ⅰ型膠原表達水平,起到抗肺纖維化的作用[9]。α-SMA是HSCs由靜止狀態變為活化狀態的重要標志物。活化的HSCs合成和分泌大量的細胞外基質,Ⅰ型膠原蛋白是細胞外基質的主要成分之一。有文獻報道靜止狀態的HSCs主要表達MMP-1,不表達TIMP-1,活化的HSCs 中TIMP-1表達明顯升高,TIMP-1表達增高一定程度上反映了HSCs活化的狀態及細胞外基質堆積情況[10]。本實驗結果表明SAHA明顯降低激活型HSCs中α-SMA、Ⅰ型膠原蛋白及TIMP-1表達水平,提示SAHA有一定的抗肝纖維化作用。
近來研究發現,內質網應激與GRP78蛋白乙酰化有著密切的聯系,有文獻報道:去乙酰化酶抑制劑帕比司他誘導乳腺癌細胞的凋亡與GRP78乙酰化水平增高有關,主要是通過帕比司他抑制HDAC6蛋白的表達,激活乳腺癌細胞中未折疊蛋白反應,發生內質網應激,最終導致癌細胞凋亡[11]。另外還有文獻報道,帕比司他在硼替佐米的協同作用下誘導內質網應激,抑制了腎癌細胞增殖和蛋白泛素化堆積[12]。帕比司他是新型羥肟酸類去乙酰化酶抑制劑,對HDAC6有較強的選擇性,SAHA是一種廣泛的羥肟酸類去乙酰化酶抑制劑,對HDAC1、HDAC2、HDAC3和HDAC6都有抑制作用。本研究發現SAHA可降低HDAC6蛋白表達水平,升高GRP78蛋白表達水平;進一步采用免疫共沉淀的方法發現GRP78與HDAC6形成復合物,由此說明GRP78與HDAC6存在相互作用。另外,SAHA處理組HSCs中GRP78蛋白復合物中乙酰化lysine水平顯著升高,更進一步說明SAHA處理組HSCs中GRP78乙酰化水平升高。GRP78是內質網應激的標志蛋白[13],GRP78持續增高會誘導未折疊蛋白反應,觸發內質網應激,促進HSCs凋亡。綜上所述,SAHA抗肝纖維化的機制可能通過SAHA下調HDAC6蛋白表達水平,上調乙酰化GRP78蛋白表達水平,誘導HSCs內質網應激,促進肝星狀細胞凋亡,起到抗肝纖維化的作用。
[1] 戴 晴, 李 欣, 鄭 磊, 等. 丹參素對肝星狀細胞TGF-β信號轉導的影響[J]. 中國病理生理雜志,2009, 25(10):1988-1994.
[2] 張錦生. 蛋白質乙酰化與肝纖維化[J]. 世界華人消化雜志,2012,20(36):3621-3624.
[3] Shi ZJ, Ouyang DY, Zhu JS, et al. Histone deacetylase inhibitor suberoylanilide hydroxamic acid exhibits anti-inflammatory activities through induction of mitochondrial damage and apoptosis in activated lymphocytes[J]. Int Immunopharmacol, 2012, 12(4):580-587.
[4] 于 濤, 張 鵬, 鹿全意, 等. 組蛋白去乙酰化酶抑制劑SAHA誘導骨髓瘤細胞的凋亡[J]. 中國組織工程研究, 2012, 16(6):1062-1066.
[5] 王迎春, 邢蘭花, 楊 旭, 等. 辛二酰苯胺異羥肟酸對人肝癌SMMC-7721細胞增殖和凋亡的影響[J]. 實用肝臟雜志, 2013, 16(6):532-535.
[6] 戴春蕾, 陳少隆, 陳黎黎, 等. Optiprep 梯度離心法提取大鼠肝星狀細胞的研究[J]. 醫學研究雜志, 2013, 42(1):142-144.
[7] 田 甜, 張金娟, 羅新華, 等. 大鼠原代肝星狀細胞活化后組蛋白修飾水平觀察[J]. 中國病理生理雜志, 2015, 31(10):871-876.
[8] 張 玥, 蘇明波, 周宇波. 組蛋白去乙酰化酶6(HDAC6)抑制劑分子水平高通量篩選模型的建立[J]. 生物技術通報, 2012(8):181-188.
[9] Sanders YY, Hagood JS, Liu H, et al. Histone deacetylase inhibition promotes fibroblast apoptosis and ameliorates pulmonary fibrosis in mice[J]. Eur Respir J, 2014, 43(5):1448-1458.
[10]杜 超, 程雙平. 基質金屬蛋白-1與肝纖維化的研究進展[J]. 醫學綜述, 2015, 21(13):2321-2323.
[11]Rao R, Nalluri S, Kolhe R, et al. Treatment with panobinostat induces glucose-regulated protein 78 acetylation and endoplasmic reticulum stress in breast cancer cells[J]. Mol Cancer Ther, 2010, 9(4):942-952.
[12]Sato A, Asano T, Isono M, et al. Panobinostat synergizes with bortezomib to induce endoplasmic reticulum stress and ubiquitinated protein accumulation in renal cancer cells[J]. BMC Urol, 2014, 14:71.
[13]Zhang XQ, Xu CF, Yu CH, et al. Role of endoplasmic reticulum stress in the pathogenesis of nonalcoholic fatty liver disease[J]. World J Gastroenterol, 2014, 20(7):210-215.
(責任編輯: 林白霜, 羅 森)
Suberoylanilide hydroxamic acid induces apoptosis of rat hepatic stellate cellsinvitro
LIU Xing, TIAN Tian, YU Lei, ZHAN Wei, HAN Bing, XIE Ru-jia, YANG Ting, LUO Xin-hua, YANG Qin
(DepartmentofPathophysiology,GuizhouMedicalUniversity,Guiyang550000,China.E-mail: qinyang@gmc.edu.cn)
AIM: To study the effects of suberoylanilide hydroxamic acid (SAHA) on the apoptosis of hepatic stellate cells (HSCs) and expression of associated proteins, and to investigate the mechanisms of SAHA to induce apoptosis. METHODS: The rat HSCs were isolated by OptiPrep gradient centrifugation method. The effect of SAHA on HSC proliferation was detected by real-time cell analyzer. The morphological changes of HSCs treated with SAHA at different concentrations were observed under inverted microscope. The apoptotic rates of HSCs were analyzed by flow cytometry with Annexin V-FITC/PI staining and fluorescence microscopy. The protein expression of α-smooth muscle actin (α-SMA), collagen I, tissue inhibitor of metalloproteinase 1 (TIMP1), glucose-regulated protein 78 (GRP78) and histone deacetylase 6 (HDAC6) was detected by Western blotting. The interaction of GRP78 with HDAC6 in the HSCs was determined by co-immunoprecipitation.RESULTS: HSCs were successfully isolated and cultured for 14 d, during which the HSCs changed gradually from rest state to active state. SAHA significantly inhibited the proliferation of HSCs in a time- and dose- dependent manner (P<0.05). The results of Western blotting showed that the protein expression levels of α-SMA, TIMP1, collagen-I and HDAC6 were significantly decreased (P<0.05), while GRP78 was significantly increased (P<0.05). Compared with activated HSCs, GRP78 and total acetyl-lysine protein were significantly increased in the co-immunoprecipitated HSCs treated with SAHA, while HDAC6 protein was significantly decreased, indicting that GRP78 formed a complex with HDAC6. CONCLUSION: The anti-hepatic fibrosis effect of SAHA may be related to down-regulation of HDAC6 and up-regulation of acetylated GRP78, thus inducing endoplasmic reticulum stress of HSCs and promoting the apoptosis of HSCs.
Hepatic stellate cells; Suberoylanilide hydroxamic acid; Hepatic fibrosis; Apoptosis
1000- 4718(2017)05- 0913- 06
2016- 11- 30
2017- 03- 02
國家自然科學基金資助項目(No. 81160064);省衛計委基金資助項目(No. gzwjkj2015-1-037)
R575.2+9; R363
A
10.3969/j.issn.1000- 4718.2017.05.024
雜志網址: http://www.cjpp.net
△通訊作者 Tel: 0851-86908489; E-mail: qinyang@gmc.edu.cn

