三七粉對四氯化碳(C Cl4)誘導的大鼠慢性肝損傷的保護作用
董婧婧,劉艷菊,陳祥勝,付偉,李鑫
[湖北中醫藥大學藥學院(湖北省中藥炮制工程技術研究中心),湖北武漢430065]
三七粉對四氯化碳(C Cl4)誘導的大鼠慢性肝損傷的保護作用
董婧婧,劉艷菊,陳祥勝,付偉,李鑫
[湖北中醫藥大學藥學院(湖北省中藥炮制工程技術研究中心),湖北武漢430065]
目的探討三七粉對四氯化碳(CCl4)誘導的慢性肝臟損傷和肝纖維化的保護作用。方法采用SD大鼠皮下注射10%CCl4花生油溶液,建立慢性肝損傷和肝纖維化模型,分別對給藥后模型大鼠血清中的丙氨酸氨基轉移酶(ALT)、天冬氨酸氨基轉移酶(AST)、炎癥因子(IL-1、IL-6及IL-8)和腫瘤壞死因子(TNF-α),以及肝勻漿中的丙二醛(MDA)、超氧化物歧化酶(SOD)、谷胱甘肽(GSH)、谷胱甘肽過氧化物酶(GSH-Px)和肝藥酶(Cyt.P450、Cyt.b5)等生化指標進行測定,并通過蘇木精-伊紅染色法(HE)染色后,顯微觀察三七粉對模型大鼠肝臟病理變化的影響。結果三七粉降低CCl4模型大鼠ALT和AST水平,促進Cyt.P450和Cyt.b5酶的活力,增強肝臟SOD和GSH-Px水平,降低肝臟MDA的水平,并且對IL-1、IL-6、IL-8和TNF-α水平具有抑制作用。結論三七粉具有抗CCl4誘導的肝損傷和肝纖維化作用。
三七粉;四氯化碳;肝纖維化;肝損傷;保護作用
三七為五加科植物三七[panax notoginseng(Burkill)F.H.Chen ex C.H]的干燥根和根莖。藥性甘、微苦、溫、歸肝經和胃經,主要功效為止血化瘀、消腫定痛。在《中國藥典》(2015年版)中收載有三七粉飲片[1],也是在中醫臨床中常用的組方藥物。近代研究發現,三七還有抗腫瘤、降血糖等作用[2-9]。本文通過皮下注射四氯化碳溶液建立大鼠肝損傷和肝纖維化模型,評價三七粉整體對慢性肝損傷和肝纖維化的保護作用,為拓展三七粉的臨床應用范圍提供理論基礎。
1 材料與方法
1.1 試驗動物
SD大鼠,雄性,體重180~200g,清潔級[由安徽醫科大學實驗動物中心提供,許可證號:SCXK(皖)2011-002;溫度19~23℃,濕度45%~55%,空調控制]。
1.2 試驗藥物
聯苯雙酯片(上海信誼天平藥業有限公司),三七粉[購于云南省文山州(20頭、3年生),三七原料經粉碎、過篩后制備得三七粉]。
1.3 試驗試劑
細胞色素P450(cytochrome P450,Cyt.P450)(上海源葉生物技術有限公司,批號:E30118),細胞色素b5(cytochrome b5,Cyt.b5)(上海源葉生物技術有限公司,批號:E20089),谷胱甘肽(Glutathione,GSH)(上海源葉生物技術有限公司,批號:E31034),谷胱甘肽過氧化物酶(glutathione peroxidase,GSH-Px)(上海源葉生物技術有限公司,批號:E31036),丙氨酸氨基轉移酶(alanine aminotransferase,ALT)測定試劑盒、天冬氨酸氨基轉移酶(aspartate aminotransferase,AST)測定試劑盒、丙二醛(malondiadehyde,MDA)試劑盒和超氧化物歧化酶(superoxide dismutase,SOD)試劑盒(均購于江蘇省南京建成生物工程研究所)。
1.4 試驗儀器
RT-6000酶標儀(美國雷杜公司),JW3021HR離心機(安徽省合肥嘉文儀器裝備有限公司),GL-88B漩渦混合器(江蘇省海門其林貝爾儀器制造公司),移液器(德國eppendorf公司),DNP-9052BS-Ⅲ電熱恒溫箱(上海三發科學儀器有限公司),灌胃針頭,注射器,天平。
1.5 方法
1.5.1 動物分組及給藥將SD雄性大鼠,隨機分成6組,每組10只,正常對照組和損傷對照組灌胃生理鹽水5mg/kg,陽性對照組聯苯雙酯灌胃100mg/kg;受試樣品分高、中、低3個劑量組,分別給予受試藥按以相當2倍臨床常用量、臨床常用量、0.5倍臨床常用量。設立高、中、低三組;每日1次,灌胃給藥。另外除正常對照組外,其他各組每周2次皮下注射10%四氯化碳(carbon tetrachloride,CCl4)花生油溶液5 mg/kg,以誘導慢性肝損傷和肝纖維化,給予正常飲食。連續給予CCl4和三七粉以及聯苯雙酯12周。
1.5.2 對肝藥酶誘導的影響取部分肝組織勻漿后,按試劑盒說明書測定Cyt.P450和Cyt.b5的含量。
1.5.3 抗氧化作用肝臟勻漿后,按試劑盒說明書測定肝組織中SOD、MDA、GSH和GSH-Px的含量。
1.5.4 對肝功能的影響末次給藥后,麻醉,腹主動脈取血,按試劑盒說明書測定AST和ALT的水平。
1.5.5 對炎癥因子的影響末次給藥后,麻醉,腹主動脈取血,用ELISA試劑盒檢測大鼠血清中白細胞介素(interleukin-1,IL-1)、白細胞介素6(interleukin-6,IL-6)、白細胞介素8(interleukin-8,IL-8)和腫瘤壞死因子α(tumor necrosis factor-α,TNF-α)的含量。
1.5.6 對肝臟組織的病理學觀察切取SD大鼠肝臟右葉0.5 cm×0.5 cm×1.0 cm的組織塊,進行蘇木精-伊紅染色法(hematoxylin-eosin staining,HE)染色,并置于顯微鏡下觀察結果。
1.6 統計學方法
數據分析采用SPSS 17.0統計軟件,計量資料以均數±標準差(±s)表示,采用one-way-AVOVA進行方差分析,方差不齊,采用Dunnettt檢驗;采用LSD-t檢驗,組間兩兩比較用t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 三七粉灌胃后C C l4模型大鼠肝藥酶水平
大鼠連續灌胃12周后,三七粉對CCl4模型大鼠肝藥酶的影響水平測試結果見表1。各實驗組對大鼠肝臟Cyt.b5水平的比較,經方差分析,差異有統計學意義(F=15.375,P=0.003),兩兩比較經LSD-t檢驗,模型組大鼠肝臟Cyt.b5水平低于正常組(t= 6.675,P=0.000),陽性對照組大鼠肝臟Cyt.b5水平高于模型組(t=4.354,P=0.001),三七粉中劑量組大鼠肝臟Cyt.b5水平高于模型組(t=3.200,P=0.005)。各實驗組對大鼠肝臟Cyt.P450水平的比較,經方差分析,差異有統計學意義(F=12.438,P=0.004),兩兩比較經LSD-t檢驗,模型組大鼠肝臟Cyt.P450水平低于正常組(t=7.363,P=0.000),陽性對照組大鼠肝臟Cyt.P450水平高于模型組(t=2.106,P=0.032),三七粉高、中、低劑量組大鼠肝臟Cyt.P450水平高于模型組(t三七粉高劑量組=4.184,P=0.001;t三七粉中劑量組= 5.491,P=0.000;t三七粉低劑量組=3.110,P=0.006)。
2.2 三七粉灌胃后C C l4模型大鼠肝功能狀況
三七對CCl4模型大鼠肝功能的影響結果見表2,各實驗組對大鼠肝臟丙氨酸轉氨酶含量的比較,經方差分析,差異有統計學意義(F=11.530,P=0.004),兩兩比較經LSD-t檢驗,模型組大鼠丙氨酸轉氨酶含量高于正常組(t=8.628,P=0.000),陽性對照組大鼠丙氨酸轉氨酶含量低于模型組(t=5.873,P=0.002),三七粉高劑量組大鼠丙氨酸轉氨酶含量低于模型組(t=7.965,P=0.000)。各實驗組對大鼠肝臟丙氨酸轉氨酶含量的比較,經方差分析,差異有統計學意義(F= 9.532,P=0.006),兩兩比較經LSD-t檢驗,模型組大鼠天冬氨酸轉氨酶含量高于正常組(t=7.831,P= 0.000),陽性對照組大鼠天冬氨酸轉氨酶含量低于模型組(t=4.846,P=0.005),三七粉中、高劑量組大鼠天冬氨酸轉氨酶含量低于模型組(t三七粉中劑量組= 2.712,P=0.014;t三七粉高劑量組=4.211,P=0.001)。
2.3 三七粉灌胃后大鼠肝臟氧化酶水平
三七粉對大鼠肝臟谷胱甘肽和谷胱甘肽過氧化物酶的影響水平結果見表3,各實驗組對大鼠肝臟谷胱甘肽水平的比較,經方差分析,差異有統計學意義(F=11.800,P=0.004),兩兩比較經LSD-t檢驗,模型組大鼠肝臟谷胱甘肽的水平低于正常組(t=9.832,P= 0.000),陽性對照組大鼠肝臟谷胱甘肽的水平高于模型組(t=6.547,P=0.001),三七粉中、高劑量組大鼠肝臟谷胱甘肽的水平均高于模型組(t三七粉中劑量組= 4.432,P=0.000;t三七粉高劑量組=13.408,P=0.000),各實驗組對大鼠肝臟谷胱甘肽過氧化物酶水平的比較,經方差分析,差異有統計學意義(F=18.406,P=0.002),兩兩比較經LSD-t檢驗,模型組大鼠肝臟谷胱甘肽過氧化物酶的水平低于正常組(t=8.566,P=0.000),陽性對照組大鼠肝臟谷胱甘肽過氧化物酶的水平高于模型組(t=5.837,P=0.002),三七粉高、中、低劑量組大鼠肝臟谷胱甘肽過氧化物酶的水平均高于模型組(t三七粉高劑量組=3.378,P=0.003;t三七粉中劑量組=4.699,P= 0.000;t三七粉低劑量組=6.637,P=0.000)。
三七粉對大鼠血漿MDA和SOD的含量檢測如表4所示,各實驗組對大鼠血漿MDA含量的比較,經方差分析,差異有統計學意義(F=24.640,P=0.000),兩兩比較經LSD-t檢驗,模型組大鼠血漿MDA含量高于正常組(t=15.865,P=0.001),陽性對照組大鼠血漿MDA含量低于模型組(t=23.910,P=0.000),三七粉高、中、低劑量組大鼠血漿MDA含量均低于模型組(t三七粉高劑量組=13.534,P=0.000;t三七粉中劑量組=8.724,P=0.000;t三七粉低劑量組=4.023,P=0.001)。各實驗組對大鼠血漿SOD含量的比較,經方差分析,差異有統計學意義(F=25.540,P=0.000),兩兩比較經LSD-t檢驗,模型組大鼠SOD含量低于正常組(t=29.454,P=0.000),陽性對照組大鼠SOD含量高于正常組(t= 7.618,P=0.021),三七粉高、中、低劑量組大鼠血漿SOD含量高于模型組(t三七粉高劑量組=27.356,P=0.000;t三七粉中劑量組=11.832,P=0.000;t三七粉低劑量組=8.189,P= 0.000)。
表1 各組大鼠肝臟C yt.b5和C yt.P450水平(n=6±s)
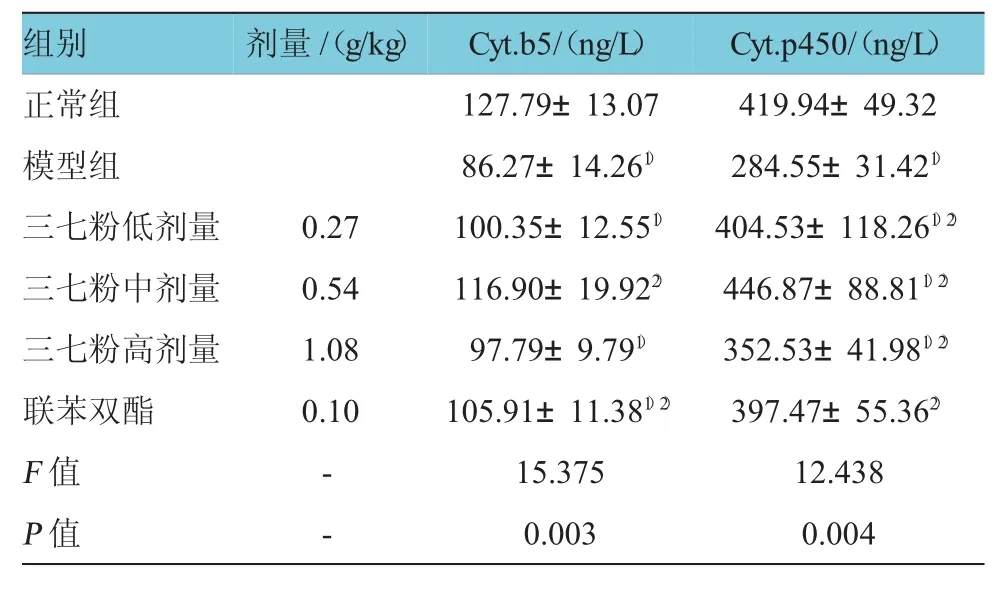
表1 各組大鼠肝臟C yt.b5和C yt.P450水平(n=6±s)
注:1)與正常組比較,P<0.05;2)與模型組比較,P<0.05
C y t . p 4 5 0 /(n g / L)正常組4 1 9 . 9 4 ± 4 9 . 3 2模型組2 8 4 . 5 5 ± 3 1 . 4 21)三七粉低劑量4 0 4 . 5 3 ± 1 1 8 . 2 61)2)三七粉中劑量4 4 6 . 8 7 ± 8 8 . 8 11)2)三七粉高劑量3 5 2 . 5 3 ± 4 1 . 9 81)2)聯苯雙酯3 9 7 . 4 7 ± 5 5 . 3 62)F值1 2 . 4 3 8P值0 . 0 0 4組別劑量/(g / k g)C y t . b 5 /(n g / L)1 2 7 . 7 9 ± 1 3 . 0 78 6 . 2 7 ± 1 4 . 2 61)0 . 2 7 1 0 0 . 3 5 ± 1 2 . 5 51)0 . 5 4 1 1 6 . 9 0 ± 1 9 . 9 22)1 . 0 8 9 7 . 7 9 ± 9 . 7 91)0 . 1 0 1 0 5 . 9 1 ± 1 1 . 3 81)2)-1 5 . 3 7 5 -0 . 0 0 3
表2 各組大鼠肝臟谷丙轉氨酶和谷草轉氨酶含量測定(n=6,±s)
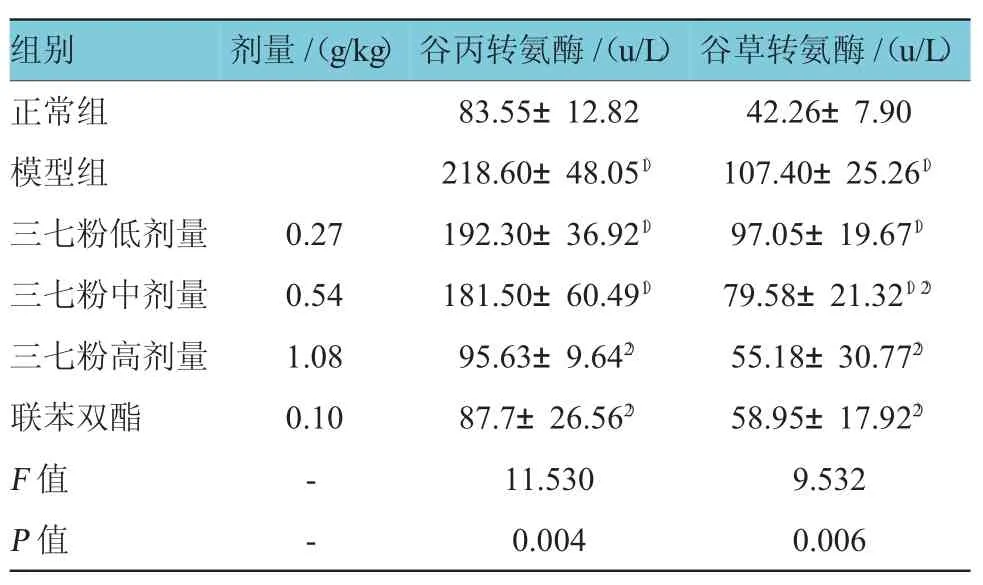
表2 各組大鼠肝臟谷丙轉氨酶和谷草轉氨酶含量測定(n=6,±s)
注:1)與空白對照組比較,P<0.05;2)與模型組比較,P<0.05
?
表3 各組大鼠肝臟谷胱甘肽和谷胱甘肽過氧化物酶的水平(n=6±s)
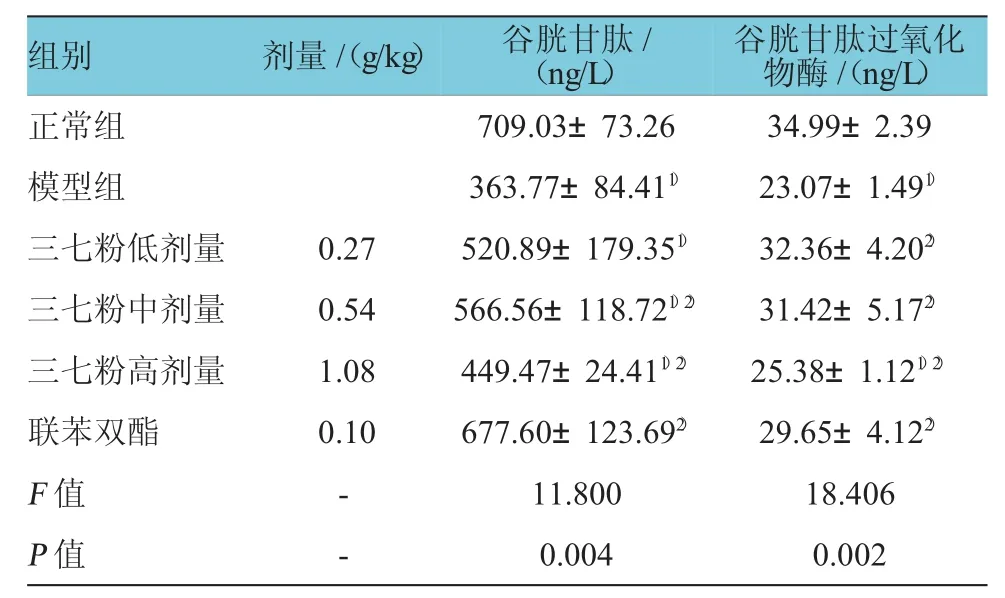
表3 各組大鼠肝臟谷胱甘肽和谷胱甘肽過氧化物酶的水平(n=6±s)
注:1)與空白對照組比較,P<0.05;2)與模型組比較,P<0.05
谷胱甘肽過氧化物酶/(n g / L)正常組3 4 . 9 9 ± 2 . 3 9模型組2 3 . 0 7 ± 1 . 4 91)三七粉低劑量3 2 . 3 6 ± 4 . 2 02)三七粉中劑量3 1 . 4 2 ± 5 . 1 72)三七粉高劑量2 5 . 3 8 ± 1 . 1 21)2)聯苯雙酯2 9 . 6 5 ± 4 . 1 22)F值1 8 . 4 0 6P值0 . 0 0 2組別劑量/(g / k g)谷胱甘肽/(n g / L)7 0 9 . 0 3 ± 7 3 . 2 6 3 6 3 . 7 7 ± 8 4 . 4 11)0 . 2 7 5 2 0 . 8 9 ± 1 7 9 . 3 51)0 . 5 4 5 6 6 . 5 6 ± 1 1 8 . 7 21)2)1 . 0 8 4 4 9 . 4 7 ± 2 4 . 4 11)2)0 . 1 0 6 7 7 . 6 0 ± 1 2 3 . 6 92)-1 1 . 8 0 0 -0 . 0 0 4
2.4 三七粉灌胃后C C l4模型大鼠炎癥相關因子水平
由表5、6可知,各實驗組對大鼠血漿IL-1含量的比較,經方差分析,差異有統計學意義(F=19.843,P=0.002),兩兩比較經LSD-t檢驗,模型組IL-1含量高于正常組(t=25.089,P=0.000),陽性對照組IL-1含量低于模型組(t=18.762,P=0.000),三七粉高、中、低劑量組IL-1含量低于模型組(t三七粉高劑量組=16.209,P=0.000;t三七粉中劑量組=10.485,P=0.000;t三七粉低劑量組= 7.047,P=0.001)。各實驗組對大鼠血漿IL-6含量的比較,經方差分析,差異有統計學意義(F=16.809,P= 0.003),兩兩比較經LSD-t檢驗,模型組IL-6含量高于正常組(t=16.667,P=0.000),陽性對照組IL-6含量低于模型組(t=9.786,P=0.000),三七粉高、中、低劑量組IL-6含量低于模型組(t三七粉高劑量組=16.812,P=0.000;t三七粉中劑量組=10.304,P=0.000;t三七粉低劑量組=3.982,P=0.001)。各實驗組對大鼠血漿IL-8含量的比較,經方差分析,差異有統計學意義(F=22.500,P=0.000),兩兩比較經LSD-t檢驗,模型組IL-8含量高于正常組(t=47.173,P=0.000),陽性對照組IL-8含量低于模型組(t=20.331,P=0.000),三七粉高、中、低劑量組IL-8含量低于模型組(t三七粉高劑量組=35.531,P=0.000;t三七粉中劑量組=32.527,P=0.000;t三七粉低劑量組= 16.404,P=0.000)。各實驗組對大鼠血漿TNF-α含量的比較,經方差分析,差異有統計學意義(F=13.432,P=0.004),兩兩比較經LSD-t檢驗,模型組TNF-α含量高于正常組(t=17.454,P=0.000),陽性對照組TNF-α含量低于模型組(t=18.587,P=0.000),三七粉高、中、低劑量組TNF-α含量均低于模型組(t三七粉高劑量組=6.526,P=0.000;t三七粉中劑量組=12.663,P=0.000;t三七粉低劑量組=8.533,P=0.001)。
表4 各組大鼠血漿M D A和SO D的含量檢測(n=6±s)
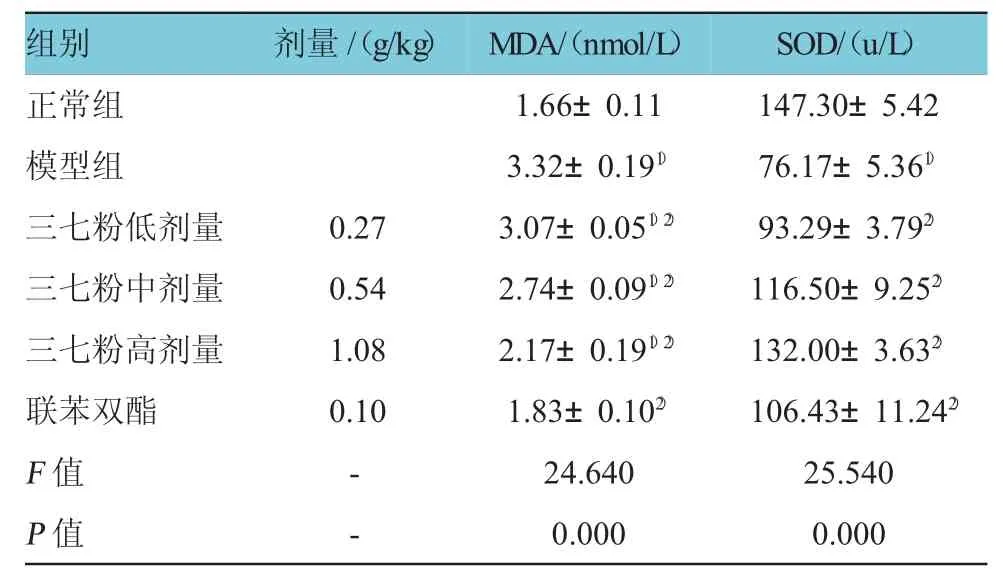
表4 各組大鼠血漿M D A和SO D的含量檢測(n=6±s)
注:1)與空白對照組比較,P<0.05;2)與模型組比較,P<0.05
S O D /(u / L)正常組1 4 7 . 3 0 ± 5 . 4 2模型組7 6 . 1 7 ± 5 . 3 61)三七粉低劑量9 3 . 2 9 ± 3 . 7 92)三七粉中劑量1 1 6 . 5 0 ± 9 . 2 52)三七粉高劑量1 3 2 . 0 0 ± 3 . 6 32)聯苯雙酯1 0 6 . 4 3 ± 1 1 . 2 42)F值2 5 . 5 4 0P值0 . 0 0 0組別劑量/(g / k g)M D A /(n m o l / L)1 . 6 6 ± 0 . 1 1 3 . 3 2 ± 0 . 1 91)0 . 2 7 3 . 0 7 ± 0 . 0 51)2)0 . 5 4 2 . 7 4 ± 0 . 0 91)2)1 . 0 8 2 . 1 7 ± 0 . 1 91)2)0 . 1 0 1 . 8 3 ± 0 . 1 02)-2 4 . 6 4 0 -0 . 0 0 0
2.5 三七粉灌胃后C C l4模型大鼠肝組織病理學改變
肝臟病理學檢測結果(見附圖)。正常組大鼠肝小葉結構正常,肝細胞無變性、壞死;而CCl4模型大鼠肝小葉結構破壞,肝細胞明顯腫脹,胞漿內可見彌漫性、大小不等的脂肪空泡,可見點狀、灶狀壞死,大量炎性細胞浸潤,大量纖維組織增生。聯苯雙酯陽性對照組及三七粉治療組以上病理改變較模型組均有改善,尤以三七粉高劑量組、中劑量組改變最明顯。
表5 各組大鼠血漿I L-1和I L-6含量(n=6±s)
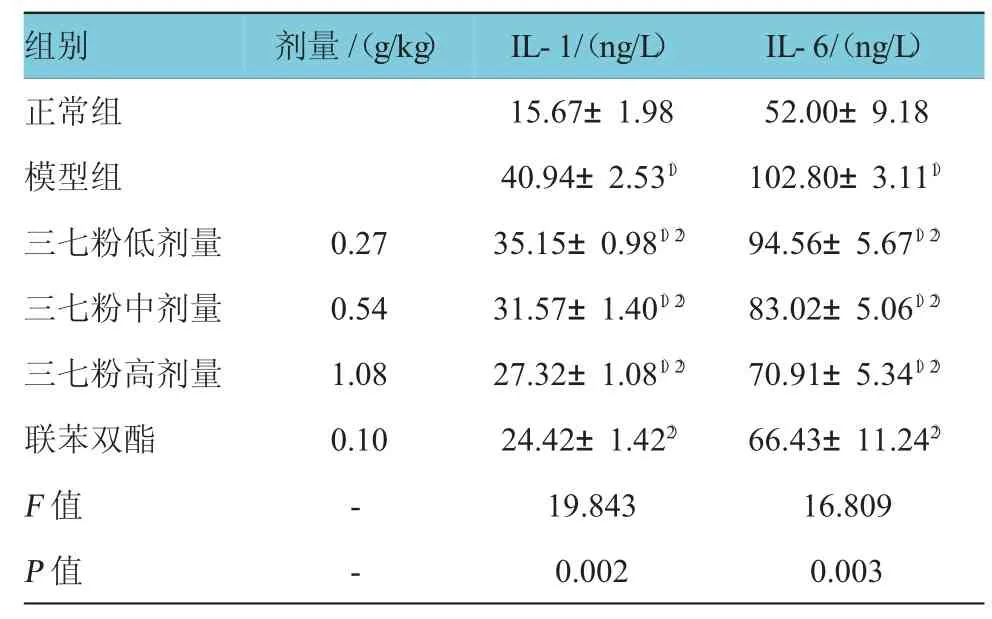
表5 各組大鼠血漿I L-1和I L-6含量(n=6±s)
注:1)與空白對照組比較,P<0.05;2)與模型組比較,P<0.05
I L -6 /(n g / L)正常組5 2 . 0 0 ± 9 . 1 8模型組1 0 2 . 8 0 ± 3 . 1 11)三七粉低劑量9 4 . 5 6 ± 5 . 6 71)2)三七粉中劑量8 3 . 0 2 ± 5 . 0 61)2)三七粉高劑量7 0 . 9 1 ± 5 . 3 41)2)聯苯雙酯6 6 . 4 3 ± 1 1 . 2 42)F值1 6 . 8 0 9P值0 . 0 0 3組別劑量/(g / k g)I L -1 /(n g / L)1 5 . 6 7 ± 1 . 9 8 4 0 . 9 4 ± 2 . 5 31)0 . 2 7 3 5 . 1 5 ± 0 . 9 81)2)0 . 5 4 3 1 . 5 7 ± 1 . 4 01)2)1 . 0 8 2 7 . 3 2 ± 1 . 0 81)2)0 . 1 0 2 4 . 4 2 ± 1 . 4 22)-1 9 . 8 4 3 -0 . 0 0 2
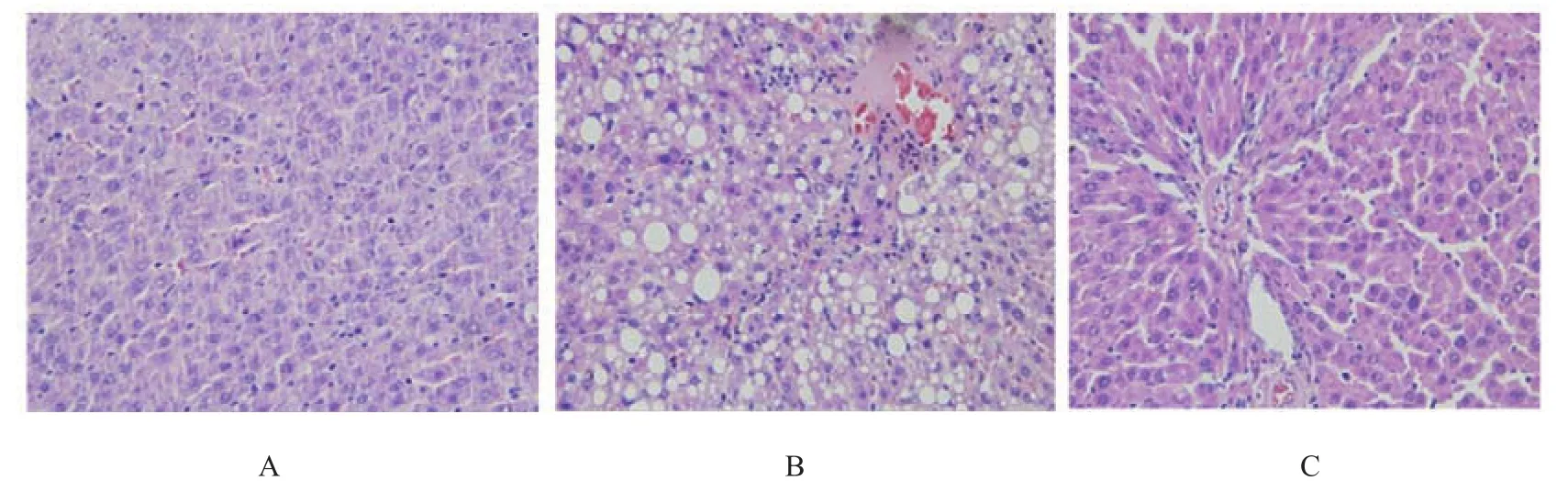
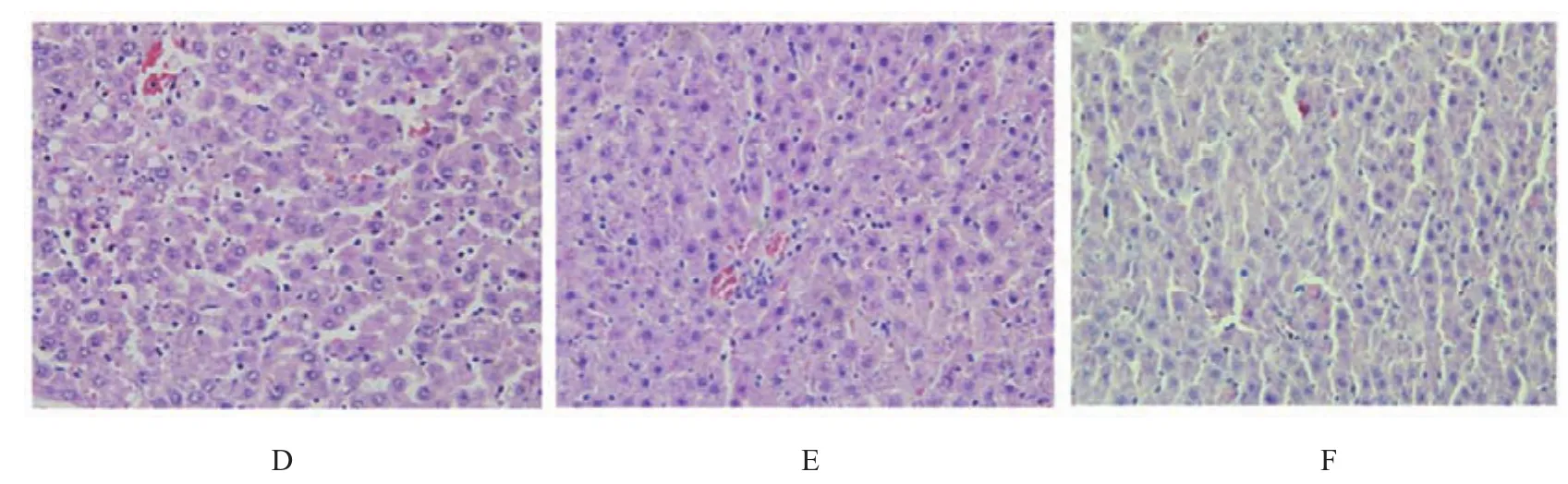
附圖各組大鼠肝臟病理學變化(HE染色×200)
表6 各組大鼠血漿I L-8和TN F-α含量(n=6±s)
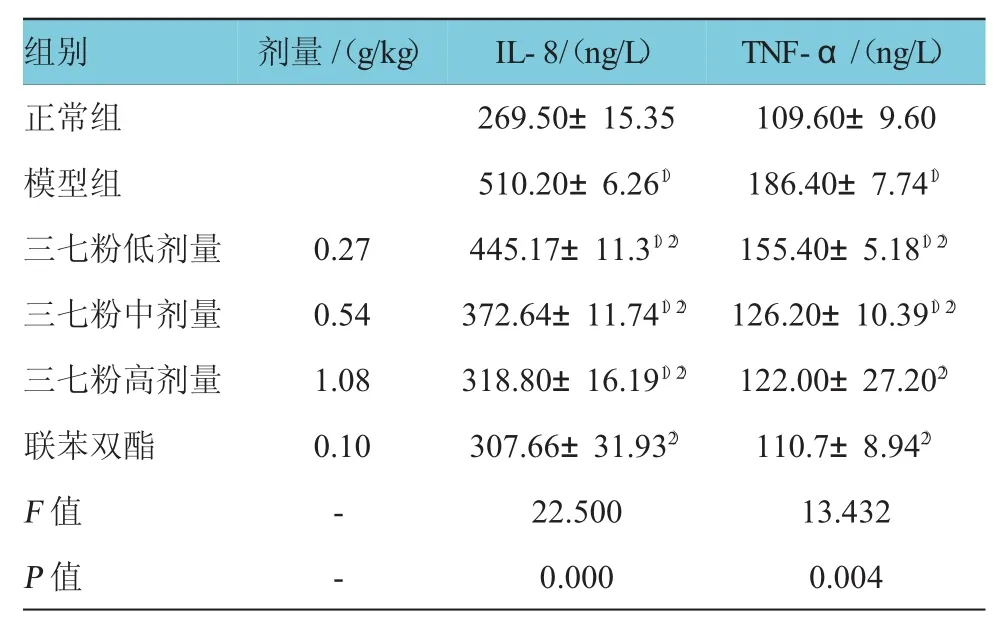
表6 各組大鼠血漿I L-8和TN F-α含量(n=6±s)
注:1)與空白對照組比較,P<0.05;2)與模型組比較,P<0.05
T N F -α /(n g / L)正常組1 0 9 . 6 0 ± 9 . 6 0模型組1 8 6 . 4 0 ± 7 . 7 41)三七粉低劑量1 5 5 . 4 0 ± 5 . 1 81)2)三七粉中劑量1 2 6 . 2 0 ± 1 0 . 3 91)2)三七粉高劑量1 2 2 . 0 0 ± 2 7 . 2 02)聯苯雙酯1 1 0 . 7 ± 8 . 9 42)F值1 3 . 4 3 2P值0 . 0 0 4組別劑量/(g / k g)I L -8 /(n g / L)2 6 9 . 5 0 ± 1 5 . 3 55 1 0 . 2 0 ± 6 . 2 61)0 . 2 7 4 4 5 . 1 7 ± 1 1 . 31)2)0 . 5 4 3 7 2 . 6 4 ± 1 1 . 7 41)2)1 . 0 8 3 1 8 . 8 0 ± 1 6 . 1 91)2)0 . 1 0 3 0 7 . 6 6 ± 3 1 . 9 32)-2 2 . 5 0 0 -0 . 0 0 0
3 討論
CCl4造成肝損傷是因其進入肝細胞后,由于脂質過氧化使肝細胞膜脂質溶解,致使肝細胞變性壞死,肝細胞膜在受損傷的同時可產生大量新的活性氧基團,促發脂質過氧化的鏈式反應,由此產生的脂質過氧化物可以損傷肝臟中的各種細胞,因此肝細胞膜的脂質過氧化是肝細胞損傷時的主要作用機制之一,也是在中藥肝損傷的保護作用研究中得到較為廣泛認可的因素之一[10-13]。SOD作為細胞內主要的防御性抗氧化酶,能夠清除自由基和抑制其脂質過氧化反應,由GSH-Px轉變為水而清楚自由基,達到保護細胞免受損傷的作用;MDA作為一種脂質過氧化物,導致肝細胞破壞,其含量的高低可間接反映機體細胞受自由基攻擊的嚴重程度[14-17]。因而本研究通過測定MDA的含量評價三七粉對CCl4大鼠體內脂質過氧化的程度的影響,檢測GSH、GSH-Px和SOD的水平來衡量三七對CCl4大鼠的抗氧化水平。結果表明,三七粉能提高四氯化碳模型大鼠肝臟還原型谷胱甘肽的含量,誘導谷胱甘肽還原酶活性,能增強解毒功能。并降低四氯化碳模型大鼠體內的過氧化脂質水平而起到抗氧化損傷作用。
肝細胞的平滑內質網脂質中的微粒體酶是藥物代謝最重要的酶系統,稱為肝藥酶,肝藥酶是動物體內一種重要的代謝酶,進入血液循環的藥物基本上是經肝藥酶代謝的,所以對肝藥酶有影響的藥物,也會影響到藥物(毒物)的代謝[18-20]。因而,本研究還檢測了細胞色素b5和細胞色素P450酶的活力,結果表明三七粉能誘導細胞色素b5和細胞色素P450酶活性的增強,進而加速機體內毒物在肝臟的代謝速度。
細胞因子IL-1、IL-6、IL-8和TNF-α是炎癥反應性介質,當肝組織存在活動性炎癥時,可促進細胞分泌IL-1、IL-6、IL-8和TNF-α,從而加強細胞毒性作用,可以間接反映肝損傷的嚴重程度[21-23]。因此,本研究進一步檢測IL-1、IL-6、IL-8和TNF-α的水平,結果表明三七粉具有一定抑制肝臟疾病細胞因子表達的作用。
綜上所述,三七粉可通過改善谷丙轉氨酶和谷草轉氨酶水平,促進細胞色素b5和細胞色素P-450酶的活力,增強肝臟SOD和GSH-PX水平,降低肝臟MDA的水平,并對IL-1、IL-6、IL-8等多種炎癥因子和腫瘤壞死因子TNF-α產生抑制作用,進而對CCl4誘導的大鼠慢性肝損傷起到保護作用。
[1]國家藥典委員會.《中華人民共和國藥典》(2015年版)[M].北京:中國醫藥科技出版社,2015.
[2]武雙,崔秀明,郭從亮,等.三七“生打熟補”物質基礎及藥理作用研究進展[J].安徽農業科學,2015,43(8):50-53.
[3]CHAN P,THOMAS G N,TOMLINSON B.Protective effects of trilinolein extracted from panax notoginseng against cardiovascular disease[J].Acta Pharmacologica Sinica,2002,23(12):1157-1162.
[4]LIU L,ZHU L,ZOU Y,et al.Panax notoginseng saponins promotes stroke recovery by influencing expression of Nogo-A,NgR and p75NGF,in vitro and in vivo.Biol[J].Biological&Pharmaceutical Bulletin,2014,37(4):560-568.
[5]UZAYISENGA R,AYEKA PA,WANG Y.Anti-diabetic potential of panax notoginseng saponins(PNS):a review[J].Phytotherapy Research,2014,28(4):510-516.
[6]YUAN H F,PAN J F,LI S,et al.Protective effects of total saponinsofpanaxnotoginsengonsteroid-inducedavascular necrosis of the femoral head in vivo and in vitro[J].Evid Based-Complement Alternat Med,2015,2015(12):65679.
[7]DEFOUR A,DESSALLE K,CASTRO P A,et al.Sirtuin 1 regulates SREBP-1c expression in a LXR dependent manner in skeletal muscle[J].PLOs One,2012,7(9):e43490.
[8]WANG P,CUI J,DU X,et al.Panax notoginseng saponins (PNS)inhibits breast cancer metastasis[J].Ethnopharmacol,2014, 154(3):663-671.
[9]DING R B,TIAN K,CAO Y W,et al.Protective effect of panax notoginseng saponins on acute ethanol-induced liver injury is associated with ameliorating hepatic lipid accumulation and reducing ethanol-mediated oxidative stress[J].Journal of Agricultural& Food Chemistry,2015,63(9):2413-2422.
[10]AKIHARA R,HOMMA T,LEE J,et al.Ablation of aldehyde reductase aggravates carbon tetrachloride-induced acute hepatic injuryinvolvingoxidativestressandendoplasmicreticulum stress[J].Biochemical&Biophysical Research Communications, 2016,16(3):1277-1283.
[11]羅文基,張坤水,陳逸生,等.左旋蝦青素對四氯化碳致大鼠慢性肝損傷保護作用的研究[J].時珍國醫國藥,2012,23(8):2057.
[12]覃洪含,夏星,王勤,等.三葉香茶菜對大鼠慢性肝損傷的保護作用[J].時珍國醫國藥,2013,24(6):1372-1373.
[13]羅亦靈,石磊,王穎鈺,等.復方龍葵顆粒對四氯化碳致大鼠慢性肝損傷的保護作用[J].中藥藥理與臨床,2014,30(1):105-108.
[14]沈洪,薛潔,朱路佳,等.生姜油不同部位對肝損傷模型大鼠肝細胞保護作用的比較[J].時珍國醫國藥,2009,20(1):90.
[15]尚新濤,張琳,祖元剛,等.京尼平苷對CCl4誘導的大鼠慢性肝損傷保護作用研究[J].中藥藥理與臨床,2012,28(4):29-31.
[16]馬加慶,云宇,后文俊,等.三七總皂苷對藥物性肝損傷小鼠的保護作用[J].中國實驗方劑學雜志,2013,19(23):246-248.
[17]張萌.醋制南五味子降酶保肝作用機理研究[D].咸陽:陜西中醫學院,2013.
[18]孫長海,王瑜,徐明亮,等.中藥莪術對四氯化碳所致急性肝損傷的保護作用[J].時珍國醫國藥,2010,21(10):2460.
[19]胡穎,蘇健.穿心蓮內酯對小鼠肝細胞色素P450的影響[J].大眾科技,2015(5):96-98.
[20]黃苗,劉欣,董蕾,等.太白楤木對CCl4誘導肝纖維化大鼠的干預作用[J].中國中藥雜志,2015,40(21):4251-4255.
[21]李剛,陳金春,付榮權,等.前列腺,素E1治療肝硬化對IL-1β、IL-6、IL-8、TNF-α的影響[J].海峽藥學,2012,24(6):74.
[22]尹連紅,于浩,彭金詠.四氯化碳誘導肝損傷的分子機制及中藥干預的研究進展[J].中國現代應用藥學,2015,32(9):1147-1155.
[23]馮曉亮.三氯乙烯致敏豚鼠肝組織中細胞因子TNF-α、IL-1、IL-6、IL-8水平研究[D].合肥:安徽醫科大學,2010.
Protective effect ofpanax notoginsengpowder on CCl4-induced chronic liver injury in rats*
Jing-jing Dong,Yan-ju Liu,Xiang-sheng Chen,Wei Fu,Xin Li
[Pharmacy School(Hubei Research Center of Chinese Materia Medica Processing Engineering and Technology),Hubei University of Chinese Medicine,Wuhan,Hubei 430065,China]
ObjectiveTo investigate the protective effects ofpanax notoginsengpowder on chronic liver injury and liver fibrosis induced by CCl4.MethodsThe model of CCl4-induced chronic liver injury and fibrosis in SD rats was established by hypodermic injection of 10%CCl4in peanut oil.Biochemical criteria were measured respectively,including ALT,AST,IL-1,IL-6,IL-8 and TNF-α in serum,and MDA,SOD,GSH, GSH-PX,Cyt.P450 and Cyt.b5 in liver homogenate.And HE dyeing,histopathological changes in liver were observed on the effects ofpanax notoginsengpowder through the microscope.ResultsThe levers of ALT,AST were decreased,and the activity of Cyt.P450 and Cyt.b5 enzyme was promoted.The levels of SOD,GSH and GSH-Px were enhanced,and the level of MDA were reduced,and the activity of IL-1,IL-6,IL-8 and TNF-α was inhibited observably in liver.ConclusionsPanax notoginsengpowder has been proved to possess significant effects on the liver fibrosis and injury induced by CCl4.
panax notoginsengpowder;CCl4;liver fibrosis;liver injury;protective effect
R282.71;R575
A
10.3969/j.issn.1005-8982.2017.08.007
1005-8982(2017)08-0032-06
2016-11-01
國家中醫藥管理局2015年中醫藥部門公共衛生專項資金(中藥科技類)
劉艷菊,E-mail:1416@hbtcm.edu.cn,Tel:027-68890231

