利用微滴式數字PCR技術分析轉基因玉米抗除草劑標記基因EPSP拷貝數
王 犇,張 春,李向龍,張中保,鄒華文,吳忠義
(1.長江大學 農學院,主要糧食作物產業化湖北省協同創新中心,湖北 荊州 434023;2.北京市農林科學院 北京農業生物技術研究中心,北京市農業基因資源和生物技術重點實驗室,北京 100097)
利用微滴式數字PCR技術分析轉基因玉米抗除草劑標記基因EPSP拷貝數
王 犇1,2,張 春2,李向龍2,張中保2,鄒華文1,吳忠義2
(1.長江大學 農學院,主要糧食作物產業化湖北省協同創新中心,湖北 荊州 434023;2.北京市農林科學院 北京農業生物技術研究中心,北京市農業基因資源和生物技術重點實驗室,北京 100097)
基于微滴式數字PCR(Droplet digital PCR,ddPCR)平臺,以轉基因玉米為例,建立了轉基因作物(Genetically modified crops,GM crops)外源基因拷貝數分析方法,對待測樣品進行了快速鑒定,并從T0轉基因玉米株系中鑒定出多個單拷貝單株。對該方法與實時熒光定量PCR(Quantitative real-time PCR,qRT-PCR)方法在分析結果的準確性方面進行了比較,從試驗數據可以看出,2種檢測方法的結果比較一致,單拷貝檢測結果高度一致;但是ddPCR試驗操作更加簡便,試驗結果可重復性強,試驗數據更加準確可靠。研究表明,ddPCR方法是一種更加便捷、快速和準確的外源基因拷貝數分析新方法,基于其在準確性和靈敏度方面的顯著優勢,將會在轉基因作物的外源基因拷貝數分析中得到廣泛的應用。
微滴式數字PCR;轉基因玉米;外源基因;拷貝數;絕對定量
隨著轉基因技術的廣泛應用,轉基因產品檢測技術研究的一個關鍵點在于精準地鑒定轉基因植物外源基因拷貝數[1]。外源基因的表達情況與其整合到受體基因組中的拷貝數有密切關系,一般以低拷貝(1~2個)整合時可高效表達,而多拷貝數的整合往往會造成外源基因不穩定表達甚至基因沉默[2]。目前,實時熒光定量PCR(Quantitative real-time PCR,qRT-PCR)、Southern 印跡雜交(Southern Blot)等經典方法已經成熟的應用于轉基因生物外源基因拷貝數的分析中。
qRT-PCR技術是一種經典的DNA定量方法,最常用的方法主要有非特異性SYBR Green I染料法和特異性TaqMan探針法2種,其中TaqMan探針法是在定性PCR的基礎上添加一條特異性的寡核苷酸熒光探針,其5′端標記一個報告熒光集團,3′端標記一個淬滅熒光集團,兩者之間構成能量傳遞結構。在探針完整時,報告集團發射的熒光信號被淬滅集團吸收,檢測系統檢測不到熒光信號。PCR擴增時,Taq酶的5′-3′外切酶活性將與底物結合的探針酶切降解,使熒光集團和淬滅集團分離,熒光檢測系統可以檢測到熒光信號,即每擴增一條DNA鏈就有一個熒光分子形成,實現了熒光信號的累積與PCR產物形成完全同步,從而實現了定量。TaqMan探針法的成功在于以下2個方面:一是Taq聚合酶所具有的雙鏈特異性的5′-3′外切酶活性;二是利用熒光能量傳遞技術構建的雙標記寡核苷酸探針(TaqMan探針)。實時熒光定量PCR一般使用Ct值(每個反應熒光信號達到設定閾值所需的循環數)定量,Ct值與模板初始拷貝數的對數呈線性關系,利用已知起始拷貝數的標準品可制作標準曲線,只要獲得未知樣品的Ct值,即可代入方程計算出該樣品的起始拷貝數[3]。qRT-PCR方法在分析中需要構建標準曲線,由于利用標準曲線進行定量本身就是一種并不十分精確的相對定量方法,而且建立標準曲線的過程中需要在體系的摸索和優化上投入大量的時間和精力,致使試驗周期比較長[4],所以qRT-PCR不是理想的外源基因拷貝數分析方法[5]。傳統的Southern Blot方法在分析時存在操作步驟繁瑣、樣本量大、工作量大、周期長和準確性較差等缺點,并且使用放射性同位素標記會對人體和環境造成較大安全隱患;特別是玉米的基因組較大,雜交信號弱,因此該方法在鑒定T0轉基因玉米拷貝數方面難度非常大。
近年來,在核酸定量分析技術領域中,數字PCR(Digital PCR,dPCR)是一種發展迅速的突破性技術。1992年Sykes等[6]嘗試在復雜背景下檢測低豐度的IgH重鏈突變基因時,對樣品進行有限稀釋,使每個反應孔中只存在單個模板分子,通過收集PCR擴增后的信號確定起始分子數,并且確定了以“終點信號的有或無”作為定量標準的數字PCR檢測的原則,這也正是數字PCR的雛形。1999年Vogelstein等[7]提出了數字PCR的概念, 將反應體系均勻分配到大量反應單元中,每個反應單元中不包含或包含1個到少數幾個目的核酸分子,在每個反應單元中獨立地進行PCR擴增,然后逐一檢測其熒光信號,再根據泊松分布和熒光信號呈陽性的反應單元數占所有反應單元數的比例來計算目的核酸序列的拷貝數。數字PCR技術具有極高的靈敏度、特異性和精確性,因此被迅速應用于生命科學研究的多個領域,如拷貝數變異分析[8-10]、基因表達分析[11-13]、轉基因成分檢測[14-16]、基因突變檢測[17-20]、微生物檢測[21-24]、測序文庫質控[25-26]、測序結果驗證[27-31]、無創產前診斷[32-34]等。
微滴式數字PCR(Droplet digital PCR,ddPCR)是一種基于泊松分布原理的對待檢核酸靶分子實現其濃度或拷貝數鑒定的絕對定量技術,目前在檢測核酸分子的絕對計數或定量方面發揮著越來越重要的作用。2015年,中國檢驗檢疫科學研究院朱水芳老師實驗室聯合國內多家實驗室完成了ddPCR用于轉基因生物(Genetically modified organisms,GMOs)檢測的研究[35]。根據形成反應單元的方式不同,數字PCR主要分為微反應室(孔板)、微流控芯片和微滴等3個系統[36]。ddPCR作為數字PCR技術的一種,包含兩部分核心內容:微滴化和微滴分析。微滴化是將配好的包含模板、引物或探針、Mix等成分的20 μL ddPCR預混液制備成20 000個均一的微滴,每個微滴約為1 nL,微滴中或者含有一個至數個待檢核酸靶分子,或者不含有靶分子,而且每個微滴均被微滴生成油所包裹并作為一個獨立的PCR反應器。區別于qRT-PCR的實時檢測,ddPCR是在擴增結束后,在微滴分析儀中逐一對每個微滴的熒光信號進行采集,有熒光信號的說明含有目標靶分子記為陽性微滴(判讀為1),沒有熒光信號的說明沒有目標靶分子則記為陰性微滴(判讀為0),最終分析軟件統計陽性微滴數占總微滴數的比例,結合泊松分布原理計算出目標靶分子的絕對濃度或拷貝數(拷貝/μL)。由此看出ddPCR的優點是:不依賴于擴增曲線的循環閾值,以分子計數的方式直接獲得樣本的拷貝數濃度,這樣的絕對定量結果便于直接進行橫向或縱向比較;更高的精確度,對同一個樣本的技術重復的檢測能獲得一致的結果,變異系數小;更好的重復性,即在不同的實驗室之間,或同一實驗室不同的檢測批次間,能對同一個樣本獲得一致的定量結果;更高的靈敏度,能更靈敏地檢測出其他技術無法檢出的或超低豐度的靶標序列;更高的準確度,更準確測定樣本中靶標序列的真實含量,真正實現絕對定量分析。
ddPCR作為一種全新的核酸分子定量技術,相較于傳統PCR和qRT-PCR,其結果具有更高的準確性、精確度和靈敏度,已被廣泛應用于生命科學研究的多個領域,如絕對定量、稀有突變檢測和拷貝數變異分析等[36]。本研究采用ddPCR技術開展T0轉基因玉米株系中抗除草劑篩選基因EPSP的拷貝數分析。
1 材料和方法
1.1 試驗材料
冬季在海南三亞崖城轉基因玉米試驗基地通過花粉管通道法轉化獲得玉米種子[37-40],玉米種子播種出苗后長到三葉期噴灑200 mg/L的草甘膦除草劑,經篩選獲得的具有除草劑抗性的轉基因株系視為T0,以后對轉基因株系進行自交擴繁并依次獲得T1、T2、T3、T4轉基因株系。在實際用于測定的T2和T4樣品由不同T0純化而來。
1.2 ddPCR引物設計
試驗內參基因選用玉米醇溶蛋白Zein,經過引物篩選和比較,采用以下具有高度專一性和特異性的引物對進行擴增(表1)。
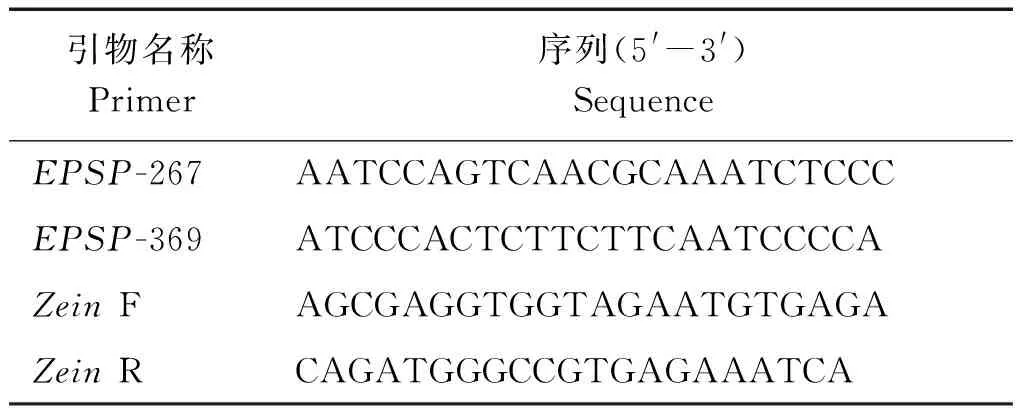
表1 ddPCR引物對序列
1.3 葉片DNA提取
轉基因株系葉片基因組DNA的提取采用CTAB法[40-41],濃度測定采用NanoDrop 2000分光光度計檢測。為了保證相鄰近的2個外源基因插入位點能夠被監測到,需要對葉片基因組DNA進行核酸酶的前處理,試驗中采用TaKaRa的Hind Ⅲ進行基因組的酶切反應,每微克DNA加入1個單位Hind Ⅲ,在37 ℃條件下水浴處理4 h,65 ℃條件下處理30 min,使酶失活。
1.4 PCR擴增
將模板DNA稀釋為20 ng/μL,使用北京農業生物技術研究中心Bio-Rad公司產品QX200ddPCR系統進行ddPCR試驗。PCR采用以DNA為模板的EvaGreen染料法,采用20 μL反應體系:2×ddPCR EvaGreen SuperMix 10 μL,上、下游引物各0.4 μL,ddH2O 6.2 μL,DNA 模板 3 μL(20 ng/μL)。PCR反應條件:95 ℃預變性5 min;95 ℃變性30 s,58 ℃退火30 s,72 ℃延伸30 s,共40個循環;4 ℃ 5 min,90 ℃固化5 min(Ramp rate=2.0 ℃/s),立即用于檢測(4 ℃保存,不超過2 h)。試驗重復1次。
1.5 ddPCR試驗操作流程
第1步:微滴生成。將配置好的20 μL樣品反應體系加到微滴發生卡(DG8 cartridge)中間一排的8個孔內,注意需緩慢打出液體以避免引入氣泡;在微滴發生卡最底下一排8個孔中各加入70 μL微滴生成油(DG oil);蓋上膠墊(Gasket),注意兩邊的小孔都要鉤牢;放入微滴生成儀中,一般需2 min即可完成微滴生成;微滴生成于微滴發生卡最上面一排孔內,體積為40 μL,轉移至96孔板相應位置孔內,用預熱好的PX1熱封儀進行封膜。第2步:微滴PCR。在PCR儀上進行PCR擴增,注意升降溫速度需低于2.5 ℃/s。第3步:微滴分析。將96孔板放入微滴分析儀中,逐個分析讀取微滴熒光信號,判斷微滴陽性或陰性。第4步:結果分析。分析軟件計算出每個樣品中目的序列的拷貝數(拷貝/μL),然后根據內參基因的拷貝數計算得出待檢測目的基因的拷貝數。
1.6 qRT-PCR檢測轉基因株系外源基因拷貝數
該內容委托大北農生物技術公司進行測定,均采用TaqMan探針法。試驗重復1次。
2 結果與分析
試驗中ddPCR反應進展順利,所檢測每個樣品的微滴數均在12 000個以上,而且所有微滴能夠分成明顯的上下兩簇,閾值線以上的點表示能夠擴增出目的基因的陽性微滴,閾值線以下的點則代表陰性微滴(圖1)。試驗利用ddPCR檢測T2轉基因玉米EPSP基因的絕對拷貝數,先后進行2次獨立試驗,結果表明,重復性較好,測得數值試驗誤差為0.43%~4.39%,但不同樣品之間內參基因的拷貝數相差較大,如樣品108-5測得內參基因為784拷貝,而在108-4樣品中測得內參基因絕對拷貝數為1 353(表2)。
由表3可知,ddPCR與TaqMan方法檢測T4轉基因玉米外源基因拷貝數的結果達到高度一致,表明這2種方法在檢測外源基因拷貝數方面的可行性和結果一致性。一般方法對T0轉基因植株外源基因拷貝數檢測難度較大,而ddPCR技術通過檢測到的抗除草劑篩選基因EPSP拷貝數與玉米內參基因Zein拷貝數的比值,可以得出轉基因玉米中外源EPSP基因的實際拷貝數。從表4可以看出,ddPCR測定的12個T0轉基因玉米植株中有6個EPSP基因拷貝數低于1,其他植株均大于1拷貝,最多達到11拷貝,說明ddPCR方法在對T0轉基因植株外源基因拷貝數檢測方面有一定的優勢。


名稱WellE試驗Experiment樣品SampleT試驗Assay類型Status濃度ConcentrationA06AABS572-2UZein手動96.3H06AABSH2OUZein手動0A07AABS572-2UEPSP手動111H07AABSH2OUEPSP手動0.0792

A06和A07.572-2樣品;H06和H07.水對照。
3 結論與討論
生物學的基礎研究和分子技術的發展伴隨著更精確和更靈敏的測量技術的發展。在目前的轉基因研究中,能夠準確、快速地鑒定轉基因生物中外源基因的拷貝數,已經成為轉基因產品檢測的一個關鍵內容[42]。除了外源基因的整合拷貝數多少對其是否正常表達至關重要之外,外源基因的整合方式(包括拷貝數、插入位置和側翼序列等) 也會影響目的基因和蛋白的表達,而且對外源基因在受體中的遺傳穩定性具有很大的影響[43]。經典的外源基因拷貝數檢測方法主要有qRT-PCR和Southern Blot 2種。其中qRT-PCR 分析方法的步驟較為繁瑣,首先需要準備標準DNA樣品,然后利用此樣品構建標準曲線,而標準曲線的建立又涉及體系的摸索與優化,需要耗費大量的時間和精力,所需試驗周期比較長;另外,借助標準曲線進行定量本身就是一種相對定量方法,所以試驗結果并不準確。而傳統的Southern Blot方法不但對DNA需求量大、試驗操作步驟復雜,而且對人員操作的技術要求比較高:轉膜必須要充分以保證DNA轉到膜上,雜交條件及漂洗要嚴格控制以保證陽性結果與背景反差對比明顯,洗膜要充分但不能過度等;另外,若要用同位素法,對人體健康和環境安全存在嚴重威脅。此法在分析時的最大問題在于試驗工作量大、周期長、結果準確性較差。
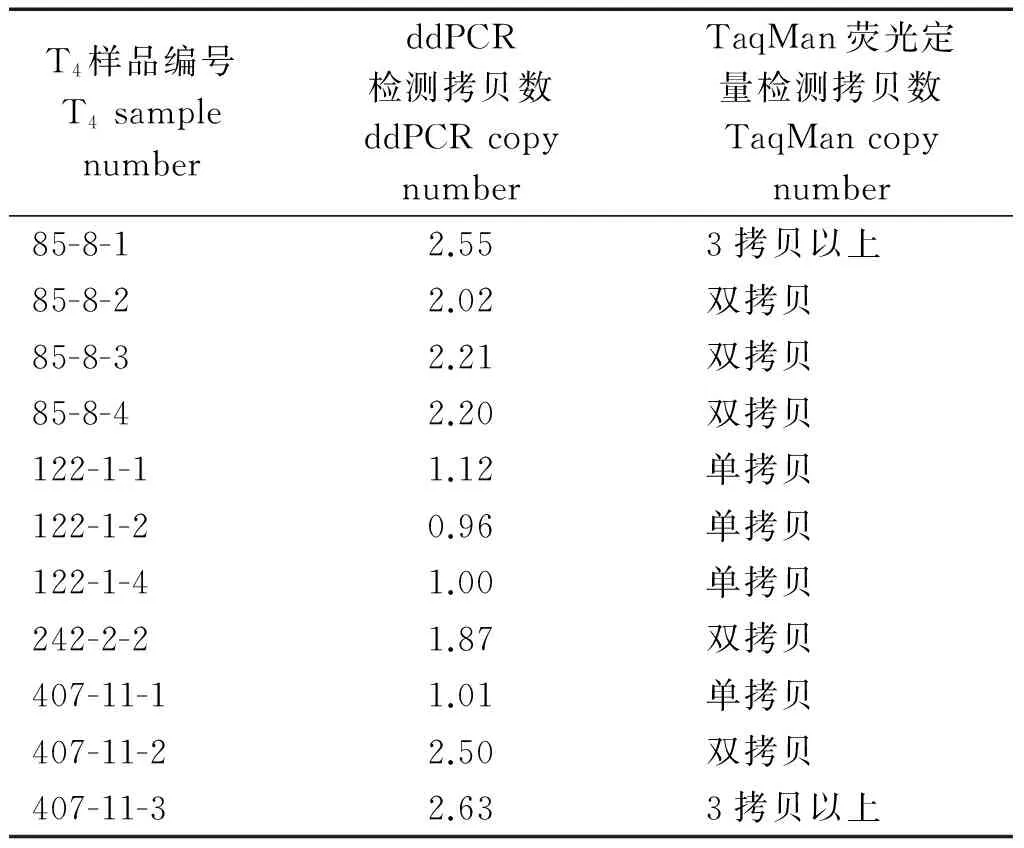
表3 ddPCR與TaqMan檢測T4轉基因玉米EPSP基因拷貝數結果比較

表4 ddPCR測定T0轉基因玉米EPSP基因拷貝數
研究通過試驗探究了ddPCR方法在分析轉基因作物外源基因拷貝數方面的應用。ddPCR作為一種新興的、準確的絕對定量技術,已經被越來越多的應用于生命科學研究的多個領域,比如核酸絕對定量、稀有突變檢測和拷貝數變異等。但目前用ddPCR分析轉基因生物的外源基因拷貝數的研究還較少。與傳統方法相比較,ddPCR的優勢非常明顯,主要體現在操作流程更加簡單,不需要構建標準曲線,并且是對待檢核酸分子直接進行絕對定量,試驗結果更加準確可靠。另外,ddPCR在線性范圍、檢測極限和定量極限等方面都更勝于qRT-PCR[13]。這些優點已得到了其他研究人員的認可[44]。
本研究建立并優化了ddPCR檢測試驗體系,分析了整合到轉基因玉米中的外源基因(EPSP)的拷貝數。結果表明,采用qRT-PCR檢測外源基因拷貝數,與ddPCR的檢測結果相一致,特別是在對單拷貝轉化單株的檢測結果上兩者高度一致。對比發現,ddPCR檢測方法簡便,操作簡單,不需構建標準曲線,節約時間。結果表明,不同樣品之間檢測到的內參基因拷貝數相差較大,由于上樣DNA總濃度(以NanoDrop光度法計算)是一樣的,這可能是因為在濃度測定中無法排除其中雜質的干擾,由此得知,在測定每個試驗樣品時都需設置內參基因以保證不同樣品之間結果的可比性。ddPCR檢測T0轉基因玉米EPSP基因拷貝數時,存在拷貝數低于0.5的檢測單株,可能是目的基因在T0轉基因玉米植株中以嵌合體形式存在;其中拷貝數大于1的單株居多,說明通過花粉管通道轉化法獲得的轉基因玉米株系中以多拷貝整合的幾率較大;通過該方法能獲得一些以理想的拷貝數(單拷貝或雙拷貝)整合的轉基因玉米株系,以提供試驗所需的材料。試驗初步建立了T0轉基因玉米植株的外源基因拷貝數鑒定方法,能夠快速、規模化地鑒定轉基因玉米外源基因的拷貝數。
ddPCR方法在試驗中充分體現了它的優點:操作簡便、節約時間和檢測結果準確可重復等,但也存在以下缺點,一是對于檢測結果的數值進行拷貝數界定依據不夠明確,以雙拷貝為例,可以將檢測數值為1.80~2.20的單株鑒定為雙拷貝,但是對于數值為1.50~1.80或2.20~2.50的單株的鑒定依據并不明確,試驗中,編號407-11-2和85-8-1單株的ddPCR檢測結果分別為2.50和2.55,而熒光定量檢測結果也是分別簡單定性為雙拷貝和三拷貝及以上,2個樣品的ddPCR檢測結果很相近,但在熒光定量的檢測結果上卻相差很大;二是該試驗所需試劑和耗材只能使用該儀器生產商匹配的,并且全部依靠進口,因此,存在訂貨周期長、試劑耗材費用高等不利因素。三是測定的絕對拷貝數是針對引物之間的擴增片段而言,并不代表全長的外源DNA所有信息,要想知道全長的信息,有必要針對DNA不同部位開展ddPCR分析。
利用ddPCR進行拷貝數檢測時,待檢測樣品在反應室中隨機、獨立分布是單分子成功擴增和準確定量核酸靶分子拷貝數的關鍵因素,所以研究在設計試驗時選用了內切酶Hind Ⅲ對基因組DNA處理。研究是以轉基因玉米單株中的篩選標記基因為檢測對象,在一定程度上也可以作為目的基因的拷貝數參考;另外可嘗試在目的基因的不同位置設計引物進行檢測,以保證目的基因拷貝數檢測結果的準確性。由于該方法可以對經過除草劑篩選獲得的T0單株進行拷貝數鑒定,這是本試驗所提到的其他2種方法無法實現的,所以能夠最大程度的減少其通過多代自交達到純合所需的時間,提高選擇效率。通過試驗發現:ddPCR能夠有效節省試驗試劑和樣品量、對核酸純度要求不高,試驗操作簡便省時,具有更高的檢測靈敏度和結果準確度,是一種快速、靈敏、精確的轉基因作物外源基因拷貝數鑒定新方法。
[1] Heyries K A,Tropini C,Vaninsberghe M,et al.Megapixel digital PCR[J].Nature Methods,2011,8(8):649-651.
[2] 萬 艷,李麗玲,陳小佳.應用實時熒光定量PCR檢測外源基因拷貝數的新方法[J].暨南大學學報:自然科學與醫學版,2009,30(3):310-313.
[3] 王愛民.實時熒光定量PCR(TaqMan)法測定外源基因的拷貝數[J].廣西植物,2009,29(3):408-412.
[4] Whale A S,Huggett J F,Cowen S,et al.Comparison of microfluidic digital PCR and conventional quantitative PCR for measuring copy number variation[J].Nucleic Acids Research,2012,40(11):e82.
[5] 姜 羽,胡佳瑩,楊立桃.利用微滴數字PCR分析轉基因生物外源基因拷貝數[J].農業生物技術學報,2014,22(10):1298-1305.
[6] Sykes P J,Neoh S H,Brisco M J,et al.Quantitation of targets for PCR by use of limiting dilution[J].Bio Techniques,1992,13(3):444-449.
[7] Vogelstein B,Kinzler K W.Digital PCR[J].Proceedings of the National Academy of Sciences of the United States of America,1999,96(16):9236-9241.
[8] Abyzov A,Mariani J,Palejev D,et al.Somatic copy number mosaicism in human skin revealed by induced pluripotent stem cells[J].Nature,2012,492(7429):438-442.
[9] Boettger L M,Handsaker R E,Zody M C,et al.Structural haplotypes and recent evolution of the human 17q21.31 region[J].Nature Genetics,2012,44(8):881-885.
[10] Hindson B J,Ness K D,Masquelier D A,et al.High-throughput droplet digital PCR system for absolute quantitation of DNA copy number[J].Analytical Chemistry,2011,83(22):8604-8610.
[11] Nair V D,Ge Yongchao,Balasubramaniyan N,et al.Involvement of histone demethylase LSD1 in short-time-scale gene expression changes during cell cycle progression in embryonic stem cells[J].Molecular and Cellular Biology,2012,32(23):4861-4876.
[12] Gorbachev A Y,Fisunov G Y,Izraelson M,et al.DNA repair inMycoplasmagallisepticum[J].BMC Genomics,2013,14(1):726.
[13] Jiang Ke,Ren Chunyan,Nair V D.MicroRNA-137 represses Klf4 and Tbx3 during differentiation of mouse embryonic stem cells[J].Stem Cell Research,2013,11(3):1299-1313.
[14] Morisset D,tebih D,Milavec M,et al.Quantitative analysis of food and feed samples with droplet digital PCR[J].PLoS One,2013,8(5):e62583.
[15] Corbisier P,Bhat S,Partis L,et al.Absolute quantification of genetically modified MON810 maize (ZeamaysL.) by digital polymerase chain reaction[J].Analytical and Bioanalytical Chemistry,2010,396(6):2143-2150.
[16] Burns M J,Burrell A M,Foy C A.The applicability of digital PCR for the assessment of detection limits in GMO analysis[J].European Food Research and Technology,2010,231(3):353-362.
[17] Shlush L I,Zandi S,Mitchell A,et al.Identification of pre-leukaemic haematopoietic stem cells in acute leukaemia[J].Nature,2014,506(7488):328.
[18] Johnson B E,Mazor T,Hong Chibo,et al.Mutational analysis reveals the origin and therapy-driven evolution of recurrent glioma[J].Science,2014,343(6167):189-193.
[19] Miyaoka Y,Chan A H,Judge L M,et al.Isolation of single-base genome-edited human iPS cells without antibiotic selection[J].Nature Methods,2014,11(3):291-293.
[20] Abdel-wahab O,Klimek V M,Gaskell A A,et al.Efficacy of intermittent combined RAF and MEK inhibition in a patient with concurrent BRAF- and NRAS-mutant malignancies[J].Cancer Discovery,2014,4(5):538-545.
[22] Rothrock M J,Hiett K L,Kiepper B H,et al.Quantification of zoonotic bacterial pathogens within commercial poultry pro-cessing water samples using droplet digital PCR[J].Advances in Applied Microbiology,2013,3(5):403-411.
[23] Zhao Hui,Wilkins K,Damon I K,et al.Specific qPCR assays for the detection ofOrfvirus,PseudocowpoxvirusandBovinepapularstomatitisvirus[J].Journal of Virological Methods,2013,194(1/2):229-234.
[24] Kelley K,Cosman A,Belgrader P,et al.Detection of methicillin-resistantStaphylococcusaureusby a duplex droplet digital PCR assay[J].Journal of Clinical Microbiology,2013,51(7):2033-2039.
[25] Laurie M T,Bertout J A,Taylor S D,et al.Simultaneous digital quantification and fluorescence-based size characterization of massively parallel sequencing libraries[J].BioTechniques,2013,55(2):61-67.
[26] White R A,Grassa C J,Suttle C A.Draft genome sequence of exiguobacterium pavilionensis strain RW-2,with wide thermal,salinity,and pH tolerance,isolated from modern freshwater microbialites[J].Genome Announcements,2013,1(4):e00513-e00597.
[27] Cangi M G,Biavasco R,Cavalli G,et al.BRAFV600E-mutation is invariably present and associated to oncogene-induced senescence in Erdheim-Chester disease[J].Annals of the Rheumatic Diseases,2015,74(8):1596-1602.
[28] Chong I Y,Cunningham D,Barber L J,et al.The genomic landscape of oesophagogastric junctional adenocarcinoma[J].The Journal of Pathology,2013,231(3):301-310.
[29] Frésard L,Leroux S,Servin B,et al.Transcriptome-wide investigation of genomic imprinting in chicken[J].Nucleic Acids Research,2014,42(6):3768-3782.
[30] Wang I X,Core L J,Kwak H,et al.RNA-DNA differences are generated in human cells within seconds after RNA exits polymerase Ⅱ[J].Cell Reports,2014,6(5):906-915.
[31] Chen Rui,Mias G I,Li-pook-than J,et al.Personal omics profiling reveals dynamic molecular and medical phenotypes[J].Cell,2012,148(6):1293-1307.
[32] Holmberg R C,Gindlesperger A,Stokes T,et al.Akonni TruTip(?) and qiagen(?) methods for extraction of fetal circulating DNA-evaluation by real-time and digital PCR[J].PLoS One,2013,8(8):e73068.
[33] Gu Wei,Koh W,Blumenfeld Y J,et al.Noninvasive prenatal diagnosis in a fetus at risk for methylmalonic acidemia[J].Genetics in Medicine,2014,16(7):564-567.
[34] Pornprasert S,Prasing W.Detection of alpha(0)-thalassemia South-East Asian-type deletion by droplet digital PCR[J].European Journal of Haematology,2014,92(3):244-248.
[35] Fu Wei,Zhu Pengyu,Wang C,et al.A highly sensitive and specific method for the screening detection of genetically modified organisms based on digital PCR without pretreatment[J].Scientific Reports,2015,5(1):12715.
[36] Sedlak R H,Jerome K R.Viral diagnostics in the era of digital polymerase chain reaction[J].Diagnostic Microbiology and Infectious Disease,2013,75(1):1-4.
[37] 李志亮,吳忠義,楊 清,等.花粉管通道法在玉米基因工程改良中的應用[J].玉米科學,2010,18(4):71-73,76.
[38] 王艷杰,申家恒.花粉管通道法轉基因技術的細胞胚胎學機理探討[J].西北植物學報,2006,26(3):628-634.
[39] 王秀君,郎志宏,陸 偉,等.利用花粉管通道法將耐草甘膦基因mG2-epsps導入玉米自交系的研究初報[J].中國農業科技導報,2008,10(4):56-62.
[40] 王永鋒,欒雨時,高曉蓉.花粉管通道法在植物轉基因中的研究與應用[J].東北農業大學學報,2004,35(6):764-768.
[41] 陳向明.用CTAB法提取植物DNA的技術改進[J].合肥教育學院學報,2000(4):14-16.
[42] Zhang Dabing,Guo Jinchao.The development and standardization of testing methods for genetically modified organisms and their derived products[J].Journal of Integrative Plant Biology,2011,53(7):539-551.
[43] Vaucheret H,Béclin C,Elmayan T,et al.Transgene-induced gene silencing in plants[J].The Plant Journal,1998,16(6):651-659.
[44] Hayden R T,Gu Z,Ingersoll J,et al.Comparison of droplet digital PCR to Real-time PCR for quantitative detection of cytomegalovirus[J].Journal of Clinical Microbiology,2013,51(2):540-546.
Analysis of the Copy Number of Herbicide Resistant Marker GeneEPSPin Transgenic Maize by Droplet Digital PCR
WANG Ben1,2,ZHANG Chun2,LI Xianglong2,ZHANG Zhongbao2,ZOU Huawen1,WU Zhongyi2
(1.College of Agriculture,Yangtze University,Hubei Collaborative Innovation Center for Grain Industry,Jingzhou 434023,China;2.Beijing Agro-Biotechnology Research Center,Beijing Academy of Agriculture and Forestry Sciences,Beijing Key Laboratory of Agricultural Gene Resources and Biotechnology,Beijing 100097,China)
The droplet digital PCR (ddPCR) method to evaluate the exogenous gene copy number in genetically modified crops (GM crops) as the example from genetically modified maize was developed,and some T0transgenic maize plants with single copy ofEPSPgene were selected from all the samples to be detected.The results were also compared with those from quantitative real-time PCR (qRT- PCR),as could be seen from the experimental datas,the results from qRT-PCR(TaqMan) and ddPCR forEPSPwere consistent,especially the single copy detection results of both in a high degree of consistency.And the ddPCR method was easy to operate,the result was repeatable and accurate.Therefore,the ddPCR would be well developed as a novel method for estimating transgenic copy number with high accuracy,which might be widely used in the exogenous genes copy number analysis in GM crops in the near future.
Droplet digital PCR; Genetically modified maize; Exogenous gene; Copy number; Absolute quantification
2017-03-10
國家轉基因重大專項重點課題(2014ZX0800303B);北京市農林科學院科研能力創新項目;北京市科委項目(Z171100001517001)
王 犇(1988-),男,安徽宿州人,在讀碩士,主要從事玉米抗旱分子生物學研究。王犇、張春為同等貢獻作者。
鄒華文(1973-),男,江蘇邳州人,教授,博士,碩士生導師,主要從事植物抗逆分子生物學研究。 吳忠義(1969-),男,福建德化人,研究員,博士,碩士生導師,主要從事植物抗逆分子生物學研究。
S513.03
A
1000-7091(2017)03-0070-07
10.7668/hbnxb.2017.03.011

