小鼠11β-1基因真核表達載體的構建及應用
辛婧,葉磊,楊可,沈亞非,鄧飛
[1.河南省漯河市中心醫院(漯河市醫學高等專科學校第一附屬醫院)內分泌科,河南 漯河 462000;2.河南省漯河市召陵區人民醫院神經內科,河南 漯河 462000]
辛婧1,葉磊2,楊可1,沈亞非1,鄧飛1
[1.河南省漯河市中心醫院(漯河市醫學高等專科學校第一附屬醫院)內分泌科,河南 漯河 462000;2.河南省漯河市召陵區人民醫院神經內科,河南 漯河 462000]
目的構建小鼠11β-羥類固醇脫氫酶基因的慢病毒真核表達載體PLJM1-11β-HSD1-GFP,建立小鼠前體脂肪細胞(3T3-L1)高表達基因的穩定感染細胞株,為基因的功能研究奠定基礎。方法利用逆轉錄聚合酶鏈反應(RT-PCR)從小鼠肝臟cDNA中擴增11β-HSD1開放閱讀框ORF,構建針對基因的真核表達載體,轉化感受態DH5α菌株,抽提質粒并進行測序鑒定。用測序成功的質粒和慢病毒包裝質粒共同轉染293T細胞,產生慢病毒并轉染3T3-L1細胞。根據綠色熒光效率挑取單克隆細胞團篩選出穩定細胞株,通過Western blot鑒定PLJM1-11β-HSD1-GFP轉染成功。結果經酶切、PCR及測序驗證,PLJM1-11β-HSD1-GFP真核表達載體構建成功,并包裝慢病毒,綠色熒光效率90%以上,并利用其慢病毒懸液成功感染3T3-L1細胞,篩選出的穩定感染細胞株的3T3-L1細胞成功高表達11β-HSD1蛋白。結論成功構建了基因的真核表達載體,并建立高表達的穩定感染細胞株PLJM1-11β-HSD1-GFP-3T3-L1,為進一步研究基因的功能,特別是在肥胖中的研究奠定了基礎。
基因;真核表達載體;前體脂肪細胞;肥胖
11β-羥類固醇脫氫酶(11beta-hydroxysteriod dehydrogenase,11β-HSD1)在體內廣泛分布,表達于脂肪、肝臟、肌肉、性腺及中樞神經系統等,以脂肪組織和肝臟中的含量最高[1]。它是糖皮質激素的代謝酶,有重要的生物學活性,有還原酶與氧化酶的雙重作用,但以還原酶作用為主,需要煙酰胺腺嘌呤二核苷磷酸(NADP+)參與,有活化糖皮質激素的作用,可以使人體無活性的可的松(動物的皮質酮)轉化為有活性的氫化可的松(皮質醇)[2]。資料顯示,11β-HSD1的轉基因小鼠顯示內臟脂肪組織肥厚;在代謝綜合征患者脂肪庫中細胞內11β-HSD1的活性是普遍增加的[3]。這可能與糖皮質激素能增加脂肪細胞內合成代謝有關,而11β-HSD1主要使糖皮質激素活化,提示其可能與向心性肥胖、胰島素抵抗及糖尿病有關[4]。本研究擬構建基因的真核表達載體,并建立高表達該基因的穩定感染細胞株,以進一步研究該基因與肥胖、胰島素抵抗及糖脂代謝相關性。
1 材料與方法
1.1 材料
PolyATtract_Series9600TMmRNA Isolation System試劑盒、末端轉移酶(TdT)、逆轉錄酶(AMV)及Taq DNA聚合酶均購自美國Promega公司,焦碳酸二乙酯(DEPC)及ExpandTMTemplate PCR System購自日本TaKaRa公司,DH5α菌株及PLJM1-NRG1-GFP載體由南京醫科大學分子遺傳研究室李建民教授饋贈,Lipofectamine 2000細胞轉染試劑盒購自美國Invitrogen公司,3T3-L1前體脂肪細胞株、293T細胞購自上海細胞生物研究所,DMEM培養液、10%胎牛血清購自南京生興公司,3-異丁基-1-甲基磺嘌呤(MIX)、胰島素及地塞米松購自美國Sigma公司,11β-HSD1兔源抗體購自美國Research Genetics公司,二抗羊抗兔IgG-辣根過氧化物酶及β-actin抗體購自武漢生物有限公司。
1.2 方法
1.2.1 引物設計根據GenBank登錄號NM_008288 mRNA序列設計引物,由上海華大基因科技有限公司合成。正向引物:GGGGCTAGCGGATCCGCCACC ATGGCAGTTATGAAAAATTACC;反向引物:GGGG AATTCCTCGAGCCTAGTTACTTACAAACATGTCC。正向引物酶切位點為,反向引物酶切位點為擴增目的片段大小881 bp。
1.2.2 小鼠肝臟總RNA的抽提用PolyAT-tract_Series9600TMmRNA Isolation System試劑盒提取BABL/C 8周的小鼠肝臟組織總RNA,提取2μl經瓊脂糖凝膠電泳觀察總RNA完整性,并用紫外分光光度計分別測定260 nm、280 nm波長下的光密度(OD)值,并檢測總RNA的純度,其余RNA于-70℃冰箱冷凍保存。
1.2.3 逆轉錄聚合酶鏈反應(RT-PCR)擴增目的基因取2μg mRNA加入PrimeSriptTMRT reagent Kit逆轉錄反應體系中,42℃孵育90 min,逆轉錄合成cDNA,結束后加入RNAase H內切酶,37℃孵育30 min,降解RNA。以上述小鼠的cDNA為模板擴增目的片段。PCR的反應條件為:94℃預變性5 min,94℃30 s,54℃30 s,72℃延伸1 min,35個循環,72℃10 min,4℃2 min,獲取小鼠基因全長開放閱讀框ORF。
1.2.4 真核表達質粒PLJM-11β-HSD1-GFP制備以上述小鼠3T3-L1細胞的cDNA為模板,相應引物擴增11β-HSD1全長ORF,用TaKaRa DNA Fragment Purification Kit純化靶DNA片段。將純化后的PCR產物行雙酶切。對酶切后產物用1%瓊脂糖凝膠行電泳檢測。并在切膠儀上切下目的片段。用Ultra-Sep Gel Extraction Kit(OMEGA)純化切膠產物。將酶切純化后的目的片段11β-HSD1連接至PLJM1-NRG1(NheI/EcoRI)載體(10μl體系:目的片段2μl,載體1μl,2×Ligase buffer 5μl,T4連接酶1μl,ddH2O 1μl;條件22℃1 h)。用連接產物轉化大腸桿菌DH5α菌株,在氨芐青霉素(Ampicillin,Amp)抗性的LB固體平板上生長過夜(37°孵箱16~18 h)。在過夜后的固體平板上挑取5個單克隆,分別加至Amp抗性的5 ml LB培養基里搖菌過夜并做好標記,次日以菌液為模板,以11β-HSD1-F/R為引物作PCR并行1%瓊脂糖凝膠電泳鑒定。對獲取的陽性克隆進行保種,同時經堿裂解法提取質粒DNA,以CMV-F和11β-HSD1-R為測序引物并送上海華大基因科技有限公司進行測序。
1.2.5 序列分析應用NCBI網站BLAST分析軟件,對上述測序結果進行序列比對,鑒定PLJM1-11β-HSD1-GFP載體多克隆位點區表達序列的可靠性和準確性。
1.2.6 PLJM1-11β-HSD1-GFP-3T3-L1慢病毒細胞株的構建用中抽試劑盒抽取質粒PLJM1-11β-HSD1-GFP及空載對照質粒PLJM.1,保證OD值1.8~1.9,濃度在1 000μg/ml以上。轉染前24 h將處于對數生長期的293T細胞鋪6 cm培養皿,2×106~4×106個/皿。轉染體系如下:質粒PLJM1-11β-HSD1-GFP(或空載對照質粒PLJM.1)4μg,包裝質粒PVSVG 2μg,delta 8.91 3μg,與Lipofectamine 2000 20μl混合共同孵育形成復合物,然后轉染293T細胞。轉染后24 h換液3 ml,并用熒光顯微鏡觀察拍照。轉染后48和72 h收集包裝產生的病毒上清,經0.45μm濾膜過濾后加入polybrene(Millipore),使終濃度為10μg/ml。感染前24 h將3T3-L1細胞接種至6 cm培養皿,使感染前細胞密度為10%~20%。24 h后棄去培養液,用上述病毒上清3 ml感染靶細胞,37℃培養6 h后換液加入3 ml完全培養液DMEM。感染48 h后觀察熒光表達情況。根據熒光效率挑單克隆篩選穩定轉染株,并進行冷凍保存。
1.2.7 Western blot檢測分別提取正常3T3-L1細胞、高表達11β-HSD1的3T3-L1及轉入空載質粒的3T3-L1細胞的總蛋白質,用考馬斯亮藍法測定蛋白質濃度,制備14.7%分離膠和5%濃縮膠,60 V穩壓電泳;半干轉膜,封閉,按Western blot檢測試劑盒說明書進行操作。一抗為11β-HSD1多克隆抗體(抗體濃度為1∶200),二抗為羊抗兔IgG-辣根過氧化物酶,(抗體濃度為1∶800),用免疫印跡增強化學發光法分別檢測3組細胞株的11β-HSD1蛋白表達水平。實驗所得的Western blot條帶經Photoshop軟件處理,在Bandscan分析軟件中測得各自總度值,采用自身β-actin灰度值校正并進行定量分析。實驗數據輸入Excel數據庫用Excel軟件進行作圖。
1.3 統計學方法
采用SPSS 14.0統計學軟件對本研究中的數據進行分析和處理,計量資料應用均數±標準差(±s)表示,采用配對檢驗,<0.05為差異有統計學意義。
2 結果
2.1 小鼠11β-HSD1 ORF片段擴增及載體克隆
以小鼠肝臟cDNA為模板,用正向引物和反向引物進行PCR擴增,得到小鼠11β-HSD1 ORF片段,目的片段為881 bp(見圖1)。
2.2 PLJM1-11β-HSD1-GFP重組載體的鑒定
以正向引物與反向引物進行PCR擴增,用Promega PCR純化試劑盒進行純化,酶切產物(見圖2)行切膠純化,將純化后產物連接至PLJM1-NRG1-GFP載體。隨機選取5個陽性克隆,行PCR鑒定(見圖3),獲取的陽性克隆經堿裂解法提取質粒DNA測序(見圖4),測序結果經序列比對分析確認無任何突變、插入等異常,慢病毒載體PLJM1-11β-HSD1-GFP構建成功(見圖5)。
2.3 慢病毒載體轉染293T細胞

圖1 小鼠11β-1基因ORF擴增片段
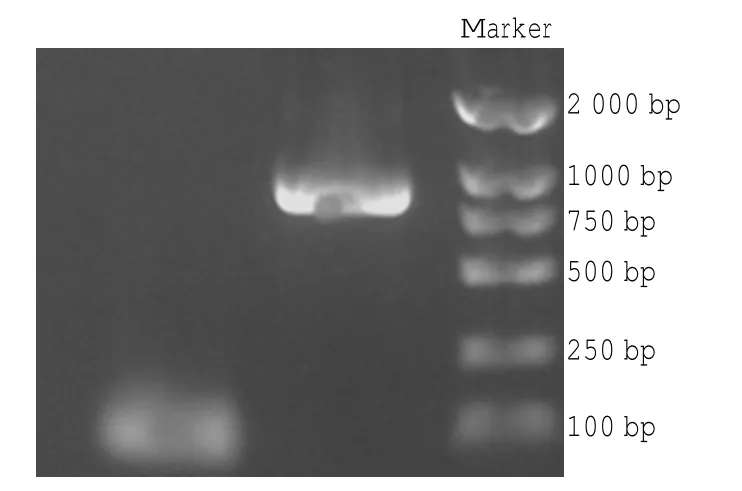
圖2 小鼠11β-1基因PCR酶切產物

圖3 小鼠11β-基因ORF片段單克隆PCR結果
慢病毒載體PLJM1-11β-HSD1-GFP轉染293T細胞24 h后熒光顯微鏡拍照見圖6,綠色熒光效率90%以上。
2.4 收取病毒上清感染3T3-L1細胞
收取293T細胞病毒上清感染3T3-L1細胞,48 h后熒光顯微鏡拍照結果見圖7。
2.53 T3-L1單克隆細胞株綠色熒光蛋白的表達
根據熒光情況挑單克隆并篩選穩定感染細胞株,3T3-L1單克隆細胞株綠色熒光蛋白的表達見圖8。

圖4 PLJM1-11β-HSD1-GFP質粒測序圖

圖5 PLJM1-11β-HSD1-GFP質粒序列比對圖

圖6 重組質粒轉染293T細胞后綠色熒光蛋白的表達(熒光顯微鏡×100)

圖7 重組質粒轉染3T3-L1細胞后綠色熒光蛋白的表達(熒光顯微鏡×100)
2.6PLJM1-11β-HSD1-GFP質粒轉染3T3-L1細胞蛋白水平驗證
分別提取3T3-L1、PLJM1-3T3-L1及PLJM1-11β HSD1-GFP-3T3-L1細胞組蛋白進行Western blot檢測,結果提示PLJM1-11βHSD1-GFP質粒轉染成功,PLJM1-11β-HSD1-GFP-3T3-L1組11β-HSD1蛋白表達水平明顯升高,見圖9。
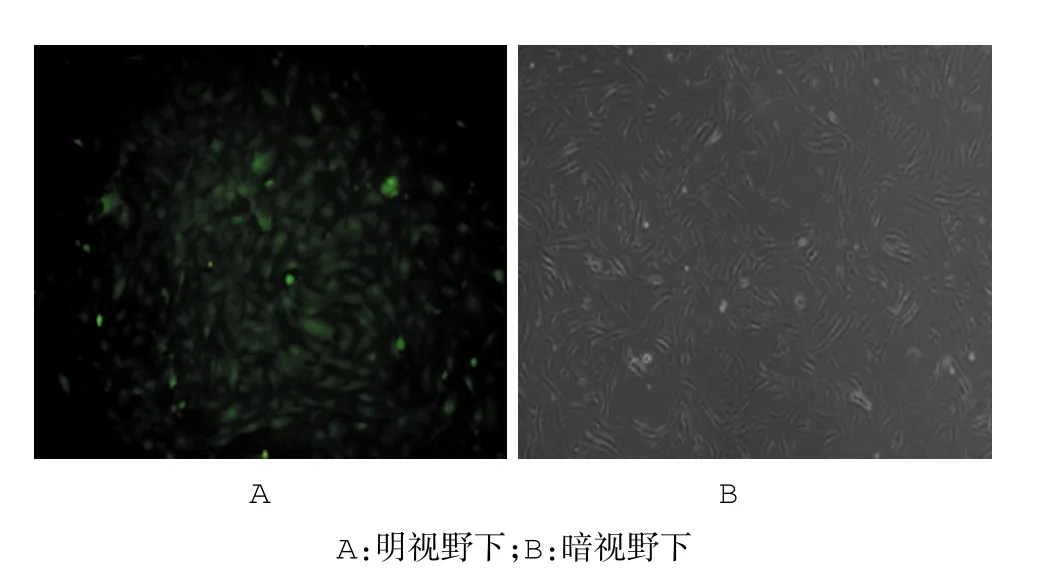
圖83 T3-L1單克隆細胞株綠色熒光蛋白的表達(熒光顯微鏡×100)

圖9 各組細胞11β-HSD1蛋白表達情況
3 討論
11β-HSD1作為一種微線粒體酶,主要負責有活性與無活性的糖皮質激素之間的互相轉化,通過控制底物即糖皮質激素的利用率,從而調控組織特異性糖皮質激素受體的活性[5-6]。11β-HSD有2種同工酶。其中11β-HSD2是輔酶Ⅰ(NAD)依賴性脫氫酶,主要使活性的可的松變為無活性的氫化可的松。主要作用于鹽皮質激素敏感的靶組織如腎臟,結腸,唾液腺,胎盤等[7]。11β-HSD1直到最近才被發現并認為是重要的生物酶,是還原型輔酶Ⅱ(NADPH)依賴性的還原酶,與11β-HSD2作用相反,主要負責將無活性的氫化可的松轉化為有活性的可的松[8]。它廣泛分布于各組織,主要分布于肝臟、脂肪、性腺、腦、脈管系統等,這些組織則以糖皮質激素受體占優勢。研究表明,11β-HSD1調節糖皮質激素受體與配體的結合,參與了庫欣綜合征相似的疾病的發生發展,如向心性肥胖、糖尿病、多囊卵巢綜合征以及癡呆[9-10]。
慢病毒(Lentivirus)載體是以人類免疫缺陷病毒-1(HIV-1)為基礎發展起來的基因治療載體[11]。攜帶有目的基因的慢病毒載體在慢病毒包裝質粒及細胞系的輔助下,經過病毒包裝成為有感染力的病毒顆粒,通過感染細胞或組織,實現目的基因在宿主細胞中得到長期而穩定的表達[12]。經過改建后的慢病毒載體能夠容納約10 kb左右的外源基因,因此大多數的cDNA都能夠被克隆入慢病毒載體。293T細胞由293細胞派生,屬人腎上皮細胞系,作為包裝細胞,在包裝后產生了高滴度的病毒顆粒,同時表達目的基因。
本文利用慢病毒載體技術成功構建了帶有GFP目的基因HSD1的慢病毒載體PLJM1-HSD1-GFP,同時建立了3T3-L1穩定感染細胞株PLJM1-HSD1-GFP-3T3-L1,為進一步研究HSD1的生物學功能奠定了必要的基礎。
[1]CHAPMAN K E,COUTINHO A E,ZHANG Z,et al.Changing glucocorticoid action:11β-hydroxysteroid dehydrogenase type 1 in acute and chronic inflammation[J].J Steroid Biochem Mol Biol,2013,137(100):82-92.
[2]LIU J,KONG X,WANG L,et al.Essential roles of 11β-HSD1 in regulating brown adipocyte function[J].J Mol Endocrinol,2013,50(1):103-113.
[3]HONGSP,NAMKY,SHINYJ,etal.Discoveryof 11β-hydroxysteroid dehydrogenase type 1 inhibitor[J].Biboorg Med Chem Lett,2015,25(17):3501-3506.
[4]MORGAN S A,GATHERCOLE L L,SIMONET C,et al.Regulation of lipid metabolism by glucocorticoids and 11β-HSD1 in skeletal muscle[J].Endocrinology,2013,154(7):2374-2384.
[5]DUBE S,SLAMA M Q,BASU A,et al.Glucocorticoid excessincreases hepatic 11β-HSD-1 activity in humans:implications in steroid-induced diabetes[J].Journal of Clinical Endocrinology Metabolism,2015,100(11):4155-4162.
[6]PAUL P,FREDIRK R,DAVID E,et al.Saturated fatty acids in humanvisceraladiposetissueareassociatedwithincreased 11β-hydroxysteroid dehydrogenase type 1 expression[J].Lipids in health Disease,2015,14(1):1-5.
[7]KOH E H,KIM A R,KIM H,et al.11β-HSD1 reduces metabolicefficacyandadiponectinsynthesisinhypertrophic adipocytes[J].J Endocrinol,2015,225(3):147-158.
[8]WOODS C,TOMLINSON J W.The dehydrogenase hypothesis[J].Advances inExperimentalMedicineandBiology,2015,872:353-380.
[9]LAVERY G G,ZIELINSKA A E,GATHERCOLE L L,et al.Lack of significant metabolic abnormalities in mice with liver-specific disruption of 11β-hydroxysteroid dehydrogenase type 1[J].Endocrinology,2012,153(7):3236-3248.
[10]ABRAHAMS L,SEMJONOUS N M,GUEST P,et al.Biomarkers of hypothalamic-pituitary-adrenal axis activity in mice lacking 11β-HSD1 and H6PDH[J].J Endocrinol,2012,214(3):367-372.
[11]WANG N,RAJASEKARAN N,HOU T,et al.Comparison of transductionefficiencyamongvariouslentivirusescontaining GFP reporter in bone marrow hematopoietic stem cell transplantation[J].Experimental Hematology,2013,41(11):934-943.
[12]GENG X,DOITSH G,YANG Z,et al.Efficient delivery of lentiviral vectors into resting human CD4 T cells[J].Gene Therapy,2014,21(4):444-449.
(張蕾編輯)
Construction and role of mouse PLJM1-11β-HSD1-GFP plasmid
Jing Xin1,Lei Ye2,Ke Yang1,Ya-fei Shen1,Fei Deng1
(1.Department of Endocrinology,Luohe Central Hospital,Luohe,Henan 462000,China;2.Department of Neurology,the People's Hospital of Shaoling District,Luohe,Henan 462000,China)
ObjectiveTo construct a lentiviral vector of PLJM1-11β-HSD1-GFP and establish a stable cell line of 3T3-L1 with high expression of mousegene,and lay the foundation for the research ofgene.MethodsOpen reading frame(ORF)fragment of mouse tissues by RT-PCR,then inserted into the PLJM1-NRG1-GFP vector and transformed into competent DH5α strain ofThe plasmid was extracted and used for sequencing.The successfully-sequenced plasmid PLJM1-11β-HSD1-GFP and the packaging plasmid were transfected to 293T cell line to produce recombinant lentivirus.3T3-L1 cell line was transfected by recombinant virus and the stable cell line was isolated by selecting the single clone with GFP,and high expression of 11β-HSD1 was identified by Western blot.ResultsThe eukaryotic expression vector of PLJM1-11β-HSD1-GFP was constructed and confirmed by DNA sequencing.The lentivirus vector ofnamed PLJM1-11β-HSD1-GFP was successfully constructed and the virus was packaged in 293T cells.3T3-L1 cells were transfected by recombinant virus and the stable cell line was selected by green fluorescence efficiency,which showed that the lentivirus vector transfection rate was over 90%.A dramatically elevated protein level of 11β-HSDl was expressed in the positive clones of 3T3-L1 cells compared with the control group.Conclusions Mouse PLJM1-11β-HSD1-GFP plasmid has been successfully constructed.The 3T3-L1 cellsgene was amplified from mouse livertransfected by PLJM1-11β-HSD1-GFP could effectively elevate the expression ofgene,and can be used in the functional researches of mousegene,especially those related to obesity.
gene;eukaryotic expression vector;3T3-L1 cell;obesity
10.3969/j.issn.1005-8982.2017.16.003
1005-8982(2017)16-0012-06
Q782
A
2016-11-28

