LRIG1在卵巢漿液性囊腺癌細胞對依托泊苷敏感性中的作用研究*
陽華,葉元,肖勝軍,雷小妹,羅小紅
(1.桂林醫學院第二附屬醫院 婦科,廣西 桂林 541199;2.桂林醫學院附屬醫院 婦科,廣西 桂林 541001;3.桂林醫學院第二附屬醫院 病理科,廣西 桂林 541199;4.桂林醫學院附屬醫院 統計室,廣西 桂林 541001)
基礎研究·論著
LRIG1在卵巢漿液性囊腺癌細胞對依托泊苷敏感性中的作用研究*
陽華1,葉元2,肖勝軍3,雷小妹1,羅小紅4
(1.桂林醫學院第二附屬醫院 婦科,廣西 桂林 541199;2.桂林醫學院附屬醫院 婦科,廣西 桂林 541001;3.桂林醫學院第二附屬醫院 病理科,廣西 桂林 541199;4.桂林醫學院附屬醫院 統計室,廣西 桂林 541001)
目的 探討亮氨酸重復序列免疫球蛋白樣結構域基因-1(LRIG1)在卵巢漿液性囊腺癌(SKOV3)細胞株中對依托泊苷敏感性的可能機制。方法 噻唑藍比色法(MMT)檢測不同濃度VP16干預下48 h的SKOV3細胞組、siRNA LRIG1轉染SKOV3細胞組、SKOV3/VP16細胞組和siRNA LRIG1轉染SKOV3/VP16細胞組的增殖。平板克隆檢測細胞增殖,流式檢測細胞凋亡情況,實時熒光定量聚合酶鏈反應(qRT-PCR)檢測LRIG1 mRNA表達。結果 半抑制濃度(IC50)分別為62.90、115.49、156.50和195.42μg/L,siRNALRIG1轉染SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16的耐藥指數分別為1.8、2.5和3.1。SKOV3、siRNA LRIG1轉染SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞組的克隆率(F=39.338,P=0.000),細胞的LRIG1 mRNA(F=63.095,P=0.000)和凋亡細胞(F=230.046,P=0.000)明顯不同,與 SKOV3 比較,siRNA LRIG1轉染SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞的克隆率增加(t=0.026、0.0710和0.125,P=0.042、0.000和 0.000),細胞的 LRIG1 mRNA 降低(t=0.130、0.525和 0.825,均 P=0.000),凋亡細胞減少(t=12.350、35.506和 44.412,均 P=0.000),與 siRNA LRIG1轉染 SKOV3比較,SKOV3/VP16和 siRNA LRIG1轉染SKOV3/VP16細胞的克隆率增加(t=0.044和0.099,P=0.001和0.000),LRIG1 mRNA降低(t=0.395和0.695,均 P=0.000),凋亡細胞減少(t=23.156 和 32063,均 P<0.05),與 SKOV3/VP16 比較,siRNA LRIG1 轉染SKOV3/VP16細胞的克隆率增加(t=0.055,P=0.000),細胞的 LRIG1 mRNA降低(t=0.300,P=0.000),凋亡細胞減少(t=8.906,P=0.000)。結論 LRIG1 mRNA影響SKOV3細胞對藥物的敏感性,沉默LRIG1的耐藥細胞可抑制SKOV3細胞凋亡。
卵巢癌;耐藥;亮氨酸重復序列免疫球蛋白樣結構域基因-1
當今,卵巢癌的發生率已經呈現出不斷上升的趨勢,成為危害女性的重要殺手,發病率僅次于子宮頸癌和子宮體癌而列居第3位,卵巢腫瘤中的卵巢上皮癌的死亡為女性各種腫瘤死亡之首,可見卵巢腫瘤已嚴重危害女性生命健康。隨著化療藥物使用的增加,卵巢癌細胞的耐藥性也逐漸受到了人們的關注。富含亮氨酸重復序列免疫球蛋白樣結構域基因 -1(leucine-rich repeats and immunoglobulinlike domains-1,LRIG-1)及其家族分子LRIG-2和LRIG-3是一類新興的腫瘤抑制分子,在多種惡性腫瘤如乳腺癌[1-2]、子宮頸癌[3-5]、頭部和頸部癌[6-8]、膠質瘤[9-10]、前列腺癌[11]與皮膚鱗狀細胞癌等[12]均有異常表達,與腫瘤的形成及多藥耐藥密切相關。近年來,RNAi技術的出現,給人類治療癌癥帶來巨大福音,可用來研究與癌癥相關基因的變化機制,成為可代替臨床治療,改變多藥耐藥機制的一種新方法。雙鏈核糖核酸(ribonucleic acid,RNA)經酶切后會形成很多小片段,稱為小干擾核糖核酸(small interfering ribonucleic acid,siRNA)。siRNA 與信使核糖核酸(messenger ribonucleic acid,mRNA)中的同源序列發生互補結合,導致mRNA失去功能,不能翻譯產生蛋白質,使基因“沉默”。本研究中LRIG-1是治療卵巢腫瘤的新靶點,在多種癌癥中的siRNA沉默LRIG-1將為一種新的高選擇性LRIGs開發提供可靠的科學依據。本研究在既往研究基礎上,進一步探討LRIG-1分子在卵巢癌及其耐藥細胞株中的作用。
1 材料與方法
1.1 材料和試劑
卵巢漿液性囊腺癌(SKOV3)細胞株(北京大學人民醫院),依托泊苷(VP16)(江蘇省連云港市恒瑞醫藥股份有限公司),SKOV3/VP16(選取SKOV3以濃度為300μg/ml的VP16反復大劑量沖擊用藥,培養8個月建立VP16耐藥細胞株,反復傳代>3個月),胎牛血清(fetal bovine serum,FBS)(美國 Thermo Fisher Scientific公司,No:10099-141),高糖培養基(dulbecco's modified eagle medium,DMEM)(美國Hyclone公司,No:SH30022.01B),青鏈霉素、磷酸鹽緩沖溶液(phosphate buffer saline,PBS)及CCK-8試劑盒 (cell counting Kit-8)(日本 Dojindo,No:CK04),LipofectamineTM2000(美國 Thermo Fisher Scientific 公司,No:52887),Annexin V/PI apoptosis kit(浙江省杭州市聯科生物公司,AP101),結晶紫染色液(自配),Trizol(日本TaKaRa株式會社),焦碳酸二乙酯(diethy pyrocarbonate,DEPC)(美國 Sigma公司),聚合酶鏈反應儀(丹麥DBI公司),逆轉錄試劑盒(DBI公司),RNasin(美國 Promega公司)。
1.2 實驗儀器
紫外分光光度計(日本Shimodzu公司),SCR20B型冷凍離心機(日本Hitachi公司),低溫高速離心機(德國Hermle公司),凝膠掃描系統(德國UVP公司),Stratagene Mx 3000P Quantitative RealTime PCR設備(美國Agilent公司),ABI9700PCR擴增儀(美國ABI公司),超凈工作臺(江蘇省蘇州凈化設備公司),Anke/飛鴿TDL-80-2B低速離心機(上海安亭科學儀器廠),倒置顯微鏡(德國Motic公司),INC108型二氧化碳CO2細胞培養箱(德國Memmert公司),流式細胞儀和酶聯免疫檢測儀(美國BD,FACS Calibur Thermo Fisher Scientific公司)。
1.3 SKOV3和SKOV3/VP16細胞培養與計數
將SKOV3和SKOV3/VP16細胞株按常規方法培養于含10%的FBS及青霉素、鏈霉素的MEM(minimum essential medium)培養基中,在 37℃、5%CO2、恒溫、飽和濕度條件下培養,將處于對數生長期的細胞用0.25%胰酶消化,制成單細胞懸液,取出40 μl單細胞懸液,40 μl臺盼藍試劑吹打均勻,放置5 min,取20 μl計數,細胞計數板一共16個小格,合成4個大格,活細胞清晰可現,其中SKOV3呈梭型,SKOV3/VP16呈不規則多邊形,算出4大格內的總細胞數。
1.4 siRNA LRIG1轉染SKOV3和SKOV3/VP16細胞
①轉染前1天,分別將100μl含有1×104個的SKOV3和SKOV3/VP16細胞加入培養基6孔內,令轉染過程中細胞密度達到至少50%;②在25 μl的DMEM無血清無抗生素培養基中加入siRNA LRIG1/sh LRIG1,混勻;③在 25 μl的 DMEM 無血清無抗生素培養基中加入LipofectamineTM2000,混勻,室溫放置5 min;④將稀釋好的siRNA LRIG1/sh LRIG1和LipofectamineTM2000試劑混合,室溫放置20 min,將50μl混合液放入內含50μl培養基和細胞的培養孔內,搖晃培養板;⑤把細胞培養板放在CO2培養箱內,孵育4 h,除去復合物,更換培養基,放入培養箱中;⑥轉染0、24、48和72 h后,吸去培養液,按每1ml完全培養基加入100μl CCK-8混合,每孔加入100μl CCK-8混合液,將培養板放到培養箱內孵育1 h。
1.5 噻唑藍比色法測定SKOV3細胞存活率
用96孔板接種細胞,24 h后進行轉染,轉染后再等待 6 h,加入 VP16,噻唑藍比色法[3-(4,5)-dimethylthiahiazo(-z-y1)-3,5-di-phenytetrazoliumromide,MTT]法檢測 SKOV3細胞、siRNA LRIG1轉染SKOV3細胞、SKOV3/VP16細胞和siRNA LRIG1轉染SKOV3/VP16細胞在VP16濃度梯度下的存活率,檢測各細胞在490 nm處的吸光值并計算其各自的半抑制濃度(50%inhibitory concentration,IC50)。
1.6 平板克隆形成
將SKOV3細胞、siRNA LRIG1轉染SKOV3細胞、SKOV3/VP16細胞和siRNA LRIG1轉染SKOV3/VP16細胞每孔200個/2 ml接種于6孔板中,置于培養箱中培養10d,棄培養基,加入PBS洗滌細胞2次,每個孔內加入無水甲醇,室溫靜置并固定15 min,棄去固定液,加入1%結晶紫染液1ml,室溫染色15min,計算克隆形成率,克隆形成率=克隆數面積/接種面積(100%)。
1.7 實時熒光定量聚合酶鏈反應檢測SKOV3細胞、siRNA LRIG1轉染SKOV3細胞、SKOV3/VP16細胞和siRNA LRIG1轉染SKOV3/VP16細胞的LRIG1 mRNA的表達
1.7.1 RNA提取 ①收集適量細胞,加入1ml Trizol,震蕩混勻室溫放置5 min;②加入0.2 ml氯仿,劇烈震蕩15s,靜置 3min;③4℃、12000r/min 離心 10min,取上清轉移到新EP管;④加入等體積異丙醇,混勻,靜置20min;4℃、12000r/min離心10min,棄去上清液;⑤用1 ml 75%DEPC酒精洗滌;⑥4℃、12 000 r/min離心5 min,棄去液體;⑦室溫晾干后,加入30μl DEPC處理過的雙蒸水(distillation-distillation H2O,ddH2O),溶解RNA,置入-80℃冰箱冷凍保存備用。
1.7.2 逆轉錄 以1 μg總RNA視為模板,依照使用說明書內容,對逆轉錄反應體系加以配置,體系的總含量為20μl。將其合成為DNA第一鏈,依照下述內容,全面配置反應液:Primer Mix 1.0,RNA 1.0 μg,DEPC 10.0μl,水 1.0μl,共 11 μl。后將其放置到35℃環境中共計300 s,急速冷凍。依照以下體系配置出反應液:5 RT Buffer 4.0 μl;RT Enzyme Mix 1.0 μl,DEPC 11.0 μl,水 4.0μl,共 20 μl。分別在98℃預變性10 min和37℃變性60 min,合成互補脫氧核糖核酸(complementary deoxyribonucleic acid,cDNA)第一鏈,再經Sephacryl s2300離心柱離心2 min除去引物等雜質,可獲得純凈cDNA分子。
1.7.3 實時熒光定量聚合酶反應(quantitative real time polymerase chain reaction,qRT-PCR)檢測 qRTPCR 反應條件:94℃預變性 2 min,94℃變性 20 s,58℃退火 20 s,72℃延伸 20 s,40 個循環,以 GAPDH為內參,通過2-△△CT方法進行相對定量分析LRIG1 mRNA的相對表達。GAPDH,正向引物:5'-TGTTCG TCATGGGTGTGAA-3',反向引物:5'-ATGGCATGGA CTGTGGTCAT-3'。LRIG1 正向引物:5'-GACCCTTTCTGACCGACAA-3',反向引物:5'-CGCTTTCCACGGC TCTTT-3'。
1.8 流式細胞術檢測SKOV3細胞、siRNA LRIG1轉染SKOV3細胞、SKOV3/VP16細胞和 siRNA LRIG1轉染SKOV3/VP16細胞凋亡
①轉染前1天將容量為2.5×105的細胞接種在2 ml 6孔培養基,確保密度達到50%~70%;②在250μl的DMEM無血清無抗生素培養基中加入質粒或siRNA,柔和混勻;③在250μl的DMEM無血清無抗生素培養基中加入LipofectamineTM2000,柔和混勻,室溫放置5 min;④將稀釋好的siRNA和LipofectamineTM2000混合,室溫放置20 min,把siRNA/Lipofectamin混合物放到內含有細胞以及培養基的小孔內,混合;⑤把細胞培養板放在CO2培養箱內,孵育4 h,更換完全培養基并放入培養箱;⑥轉染后48h,收集細胞進行后續檢測;⑦用ddH2O將5×結合緩沖液(Binding Buffer)稀釋為 1×Binding Buffer,每0.5 ml 1×Binding Buffer加入5μl Annexin V和10μl PI,配制Annexin V/PI染色工作液;⑧吸去培養板中的培養基,每孔用2 ml PBS輕輕潤洗培養板內細胞,吸去PBS,每孔加0.5 ml 0.25%胰酶,孵育,鏡下觀察,當胞質回縮,細胞之間不再連接成片,吸去胰酶,加入2 ml PBS,制成單細胞懸液,移至流式管,1000r/min離心5min,棄上清液;⑨加入200μl Annexin V/PI染色工作液,重懸細胞;⑩避光孵育15 mim,上機檢測。
1.9 統計學方法
數據分析采用SPSS 19.0統計軟件,計量資料以均數±標準差(±s)表示,組間比較用單因素方差分析,兩兩比較用LSD-t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 不同濃度VP16干預SKOV3細胞的存活情況
VP16干預 SKOV3、siRNA LRIG1轉染 SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞的存活率及 IC50,0、5、10、20、40、80、100、120、180和 200μg/L的 VP16處理 SKOV3、siRNA LRIG1轉 染 SKOV3、SKOV3/VP16和 siRNA LRIG1轉染SKOV3/VP16細胞48 h的吸光值逐漸降低,呈劑量依 賴 關 系 ,IC50 分 別 為 62.90、115.49、156.50 和195.42 μg/L,siRNA LRIG1 轉染 SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞的耐藥指數分別為1.8、2.5和3.1。見附表。
2.2 SKOV3、siRNA LRIG1 轉染 SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞增殖情況
SKOV3、siRNALRIG1 轉染 SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞進行平板克隆實驗,克隆率分別為(0.03±0.02)%、(0.05±0.01)%、(0.10±0.03)%和(0.15±0.04)%,4 組細胞增殖差異有統計學意義(F=39.338,P=0.000),與SKOV3比較,siRNA LRIG1轉染 SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞的克隆率增高(t=0.026,0.070和 0.125,P=0.042、0.000 和0.000),與 siRNA LRIG1轉染 SKOV3 比較,SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞的克隆率增高(t=0.044和 0.099,P=0.001和 0.000),與SKOV3/VP16比較,siRNA LRIG1轉染SKOV3/VP16細胞的克隆率增加(t=0.055,P=0.000)。見圖1。
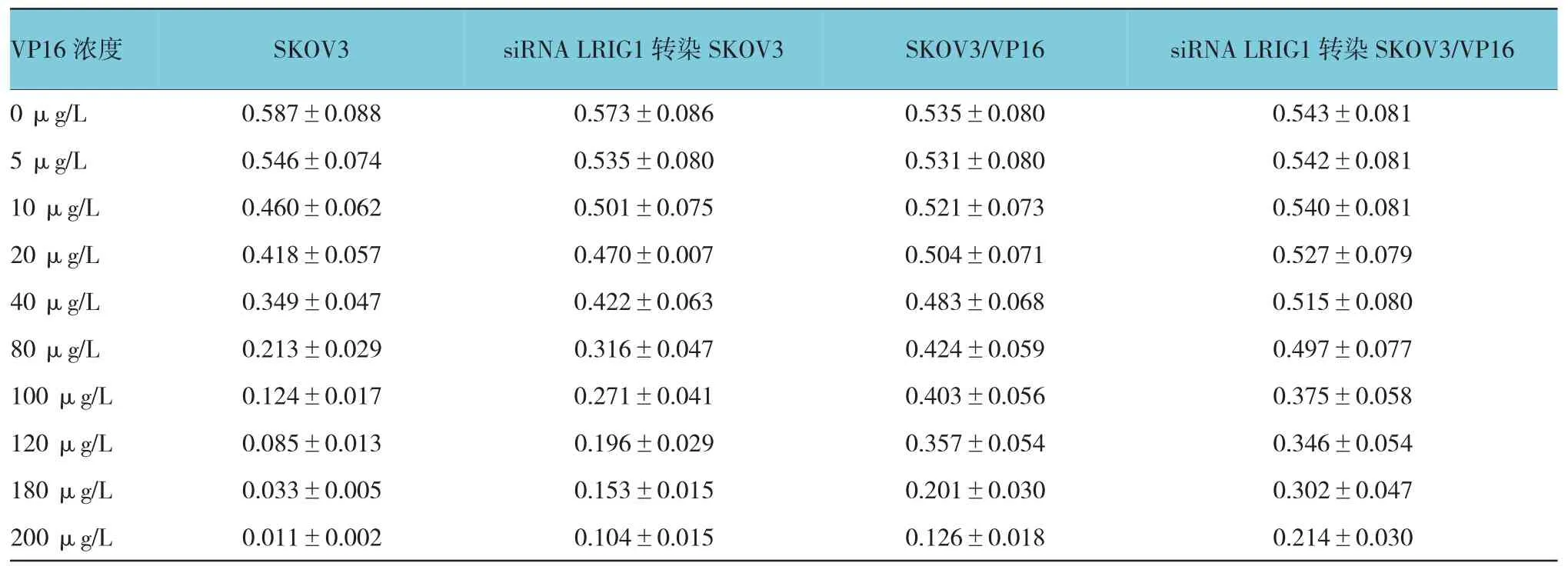
附表 VP16干預SKOV3、siRNA LRIG1轉染SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞的吸光值 (n=3)

圖1 4組SKOV3/VP16細胞增殖情況
2.3 SKOV3、siRNA LRIG1 轉染 SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞中LRIG1 mRNA的表達
SKOV3、siRNALRIG1 轉染 SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞的LRIG1 mRNA 分別為 1.05±0.15、0.93±0.16、0.53±0.09 和0.23±0.04,4組的LRIG1 mRNA表達有差異(F=63.095,P=0.000),與 SKOV3 比較,siRNA LRIG1 轉染 SKOV3、SKOV3/VP16 和 siRNA LRIG1 轉 染SKOV3/VP16細胞的LRIG1 mRNA降低(t=0.130、0.525 和 0.825,均 P=0.000),與 siRNA LRIG1 轉染SKOV3比較,SKOV3/VP16和 siRNA LRIG1轉染SKOV3/VP16細胞的LRIG1 mRNA降低(t=0.395和 0.695,均 P=0.000),與 SKOV3/VP16 比較,siRNA LRIG1轉染SKOV3/VP16細胞的LRIG1 mRNA降低(t=0.300,P=0.000)。見圖 2。
2.4 SKOV3、siRNA LRIG1 轉染 SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞凋亡情況
4組的凋亡細胞比較,差異有統計學意義(F=230.046,P=0.000),與 siRNA LRIG1 轉染 SKOV3 比較,SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16的凋亡細胞減少(t=12.350、35.506和44.412,均P=0.000),與 SKOV3/VP16 比較,siRNA LRIG1 轉染SKOV3/VP16凋亡細胞減少(t=23.156和32.063,均P=0.000),與 SKOV3/VP16比較,siRNA LRIG1轉染SKOV3/VP16 凋亡細胞減少(t=8.906,P=0.000)。見圖3。
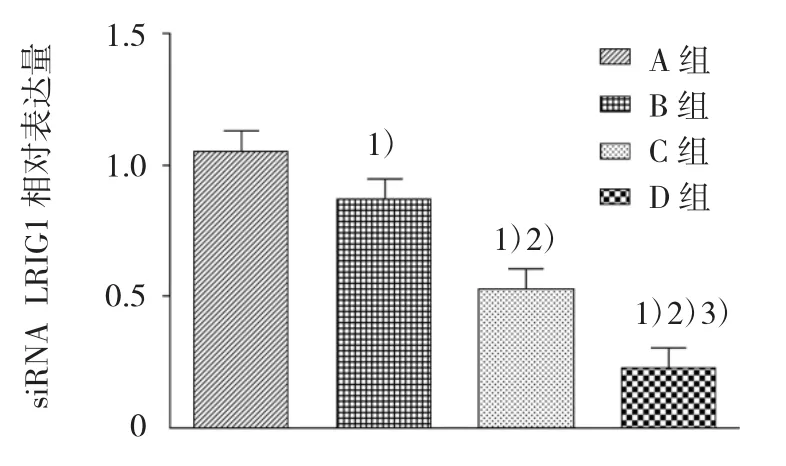
圖2 SKOV3、siRNA LRIG1轉染SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞LRIG1 mRNA表達
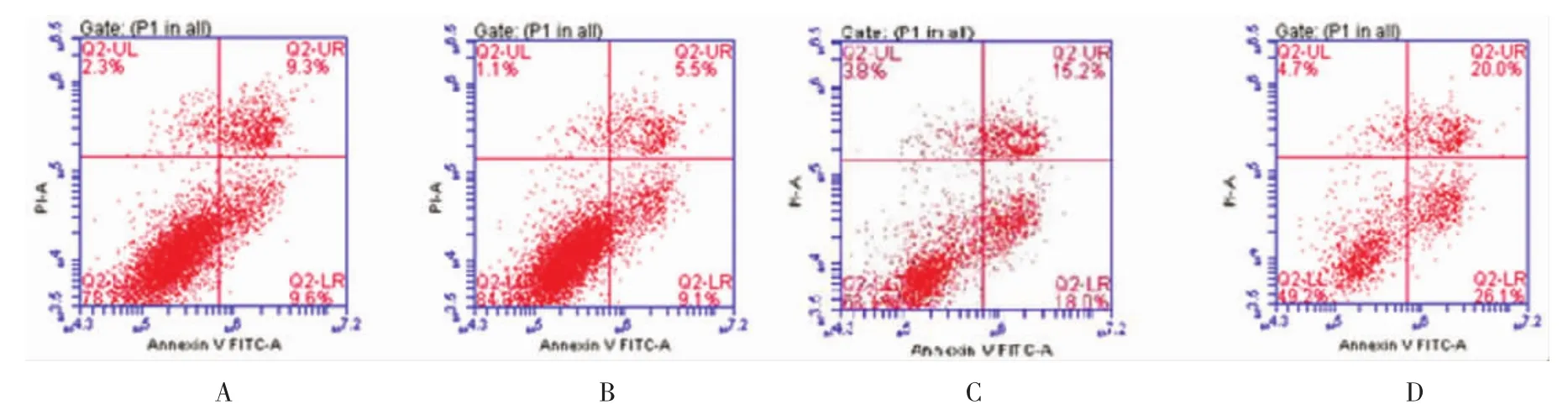
圖3 SKOV3、siRNA LRIG1轉染SKOV3、SKOV3/VP16和siRNA LRIG1轉染SKOV3/VP16細胞凋亡比較
3 討論
LRIG1發現于10多年前,科學家們開始假設其是一個腫瘤抑制基因[12]。一系列實驗和臨床數據都支持這一最初假設。此后,越來越多的證據證明,LRIG1可以抑制細胞的正常增殖和分化。LRIG1的增殖抑制作用在包括人胚胎腎細胞[14]、前列腺癌細胞[14]、小鼠成纖維細胞角質形成細胞[15-16]、膀胱癌細胞[17]、乳腺癌細胞[1,18-19]、星形細胞瘤、膠質母細胞瘤細胞[20-21]、非洲綠猴腎細胞[21]、鼻咽癌細胞[7]與肺癌細胞[22]在內一系列組織細胞。在分子水平上,LRIG1可以負性調節由致癌受體酪氨酸激酶介導的生長因子信號:LRIG1可誘導表皮生長因子受體(EGFR)家族成員EGFR、ERBB2、ErbB3 和 ErbB4 的泛素化[14-15],從而破壞MET受體[18],作用于RET受體并抑制RET和下游信號的磷酸化[23-24]。另一方面,在ErbB2陽性的腫瘤細胞系中,過表達ErbB2可以下調雌激素受體,從而抑制雌激素誘導的LRIG1轉錄[1,19]。
筆者研究發現,LRIG1 mRNA在SKOV3/VP16耐藥細胞株中的表達低于野生型SKOV3細胞株,使用siRNA沉默的SKOV3和SKOV3/VP16細胞中的LRIG1 mRNA進一步降低,差異有統計學意義,與之相對的,給予不同濃度的VP16,siRNA LRIG1轉染SKOV3細胞、SKOV3/VP16和 siRNA LRIG1轉染SKOV3/VP16細胞的IC50依次增高,克隆集落刺激增加和凋亡降低。本結果表明,LRIG1可以抑制卵巢癌細胞的增殖,將其沉默后,細胞增殖能力減弱而凋亡增加。該結論與既往研究基本吻合,該結果提示在卵巢癌的治療中,可以通過增強LRIG1蛋白的表達而促進腫瘤細胞凋亡,提高卵巢癌細胞放化療的敏感性。如臨床應用天然化合物藤黃酸可用于抗癌,機制在于藤黃酸可以通過AMP激酶的活化而上調LRIG1在膠質瘤細胞中的表達,從而抑制該細胞的增殖[25]。
結合本研究結果,筆者認為,LRIG1影響SKOV3細胞對藥物的敏感性,呈劑量相關特點,沉默細胞中的LRIG1后,可以抑制SKOV3細胞凋亡,增強卵巢癌細胞中LRIG1表達以提高卵巢癌細胞放化療敏感性。
[1]KRIG S R,FRIETZE S,SIMION C,et al.LRIG1 is an estrogen-regulated growth suppressor and correlates with longer relapse-free survival in ER alpha-positive breast cancer[J].Molecular Cancer Research,2011,9(10):1406-1417.
[2]THOMPSON P A,LJUSLINDER I,TSAVACHIDIS S,et al.Loss of LRIG1 locus increases risk of early and late relapse of stageⅠ/Ⅱ breast cancer[J].Cancer Research,2014,74(11):2928-2935.
[3]LINDSTROM A K,EKMAN K,STENDAHL U,et al.LRIG1 and squamous epithelial uterine cervical cancer:Correlation to prognosis,other tumor markers,sex steroid hormones,and smoking[J].International Journal of Gynecological Cancer,2008,18(2):312-317.
[4]HEDMAN H,LINDSTROM A K,TOT T,et al.LRIG2 in contrast to LRIG1 predicts poor survival in early-stage squamous cell carcinoma of the uterine cervix[J].Acta Oncologica,2010,49(4):812-815.
[5]MULLER S,LINDQUIST D,KANTER L,et al.Expression of LRIG1 and LRIG3 correlates with human papillomavirus status and patient survival in cervical adenocarcinoma[J].International Journal of Oncology,2013,42(1):247-252.
[6]SHEU J J,LEE C H,KO J Y,et al.Chromosome 3p12.3-p14.2 and 3q26.2-q26.32 are genomic markers for prognosis of advanced nasopharyngeal carcinoma[J].Cancer Epidemiology Biomarkers&Prevention,2009,18(10):2709-2716.
[7]SHEU J J,LEE C C,HUA C H,et al.LRIG1 modulates aggressiveness of head and neck cancers by regulating EGFR-MAPKSPHK1 signaling and extracellular matrix remodeling[J].Oncogene,2014,33(11):1375-1384.
[8]LINDQUIST D.Expression of LRIG1 is associated with good prognosis and human papillomavirus status in oropharyngeal cancer[J].British Journal of Cancer,2014,110(7):1793-1800.
[9]GUO D,NILSSON J,HAAPASALO H,etal.Perinuclear leucine-rich repeatsand immunoglobulin-like domain proteins(LRIG1-3)as prognostic indicators in astrocytic tumors[J].Acta Neuropathologica,2006,111(3):238-246.
[10]HOLMLUND C,HAAPASALO H,YI W,et al.Cytoplasmic LRIG2 expression is associated with poor oligodendroglioma patient survival[J].Neuropathology,2009,29(3):242-247.
[11]THOMASSON M,WANG B,HAMMARSTEN P,et al.LRIG1 and the liar paradox in prostate cancer:A study of the expression and clinical significance of LRIG1 in prostate cancer[J].International Journal of Cancer,2011,128(12):2843-2852.
[12]TANEMURA A,NAGASAWA T,INUI S,et al.LRIG-1 provides a novel prognostic predictor in squamous cell carcinoma of the skin:Immunohistochemical analysis for 38 cases[J].Dermatologic Surgery,2005,31(4):423-430.
[13]HEDMAN H,NILSSON J,GUO D,et al.Is LRIG1 a tumour suppressorgeneatchromosome3p14.3[J].ActaOncologica,2002,41(4):352-354.
[14]GUR G,RUBIN C,KATZ M,et al.LRIG1 restricts growth factor signaling by enhancing receptor ubiquitylation and degradation[J].Embo Journal.2004,23(16):3270-3281.
[15]LAEDERICH M B,FUNES-DURAN M,YEN L,et al.The leucine-rich repeat protein LRIG1 is a negative regulator of ErbB family receptor tyrosine kinases[J].Journal of Biological Chemistry,2004,279(45):47050-47056.
[16]JENSEN K B,WATT F M.Single-cell expression profiling of human epidermal stem and transit-amplifying cells:Lrig1 is a regulator of stem cell quiescence[J].Proceedings of the NationalAcademy of Sciences of the United States of America,2006,103(32):11958-11963.
[17]YANG W M,YAN Z J,YE Z Q,et al.LRIG1,a candidate tumour-suppressor gene in human bladder cancer cell line BIU87[J].BJU International,2006,98(4):898-902.
[18]SHATTUCK D L,MILLER J K,LAEDERICH M,et al.LRIG1 is a novel negative regulator of the Met receptor and opposes Met and Her2 synergy[J].Molecular&Cellular Biology,2007,27(5):1934-1946.
[19]MILLER J K,SHATTUCK D L,INGALLA E Q,et al.Suppression ofthe negativeregulatorLRIG1 contributesto ErbB2 overexpression in breast cancer[J].Cancer Research,2008,68(20):8286-8294.
[20]NILSSON J,VALLBO C,GUO D,et al.Cloning,characterization,and expression of human LIG1[J].Biochemical&Biophysical Research Communications,2001,284(5):1155-1161.
[21]HOLMLUND C,NILSSON J,GUO D,et al.Characterization and tissue-specific expression of human LRIG2[J].Gene,2004,332(4):35-43.
[22]GUO D,HOLMLUND C,HENRIKSSON R,et al.The LRIG gene family has three vertebrate paralogs widely expressed in human and mouse tissues and a homolog in Ascidiacea[J].Genomics,2004,84(1):157-165.
[23]NILSSON J,STAREFELDT A,HENRIKSSON R,et al.LRIG1 protein in human cells and tissues[J].Cell and Tissue Research,2003,312(1):65-71.
[24]LEDDA F,BIERAUGEL O,FARD S S,et al.LRIG1 is an endogenous inhibitor of Ret receptor tyrosine kinase activation,downstream signaling,and biological responses to GDNF[J].The Journal of Neuroscience,2008,28(1):39-49.
[25]ZHAO B,SHEN H,ZHANG L,et al.Gambogic acid activates AMP-activated protein kinase in mammalian cells[J].Biochem Biophys Res Commun,2012,424(1):100-104.
Role and mechanism of LRIG1 in SKOV3,siRNALRIG1 KOV3,KOV3/VP16 and siRNALRIG1 KOV3/VP16*
Hua Yang1,Yuan Ye2,Sheng-jun Xiao3,Xiao-mei Lei1,Xiao-hong Luo4
(1.Department of Gynaecology,the Second Affiliated Hospital of Guilin Medical University,Guilin,Guangxi 541199,China;2.Department of Gynaecology,Affiliated Hospital of Guilin Medical University,Guilin,Guangxi 541001,China;3.Department of Pathology,the Second Affiliated Hospital of Guilin Medical University,Guilin,Guangxi 541199,China;4.Department of Medical Records,Affiliated Hospital of Guilin Medical University,Guilin,Guangxi 541001,China)
ovarian cancer;drug resistance;leucine-rich repeats and immunoglobulin-like domains-1
Q344.14
A
10.3969/j.issn.1005-8982.2017.11.001
1005-8982(2017)11-0001-07
2016-12-15
桂林市科學研究與技術開發計劃項目(No:20130120-3)
葉元,Tel:13517738776
Abstract:ObjectiveTo investigate the role and possible mechanism of LRIG1 in SKOV3,siRNALRIG1 KOV3,KOV3/VP16 and siRNALRIG1 KOV3/VP16.MethodsThe cell proliferation of SKOV3,siRNALRIG1 KOV3,KOV3/VP16 and siRNALRIG1 KOV3/VP16 were detected by MMT at different concentrations of VP16,which had been con-cultured for 48 hours.Cell proliferation was detected by plate cloning.Cell apoptosis was detected by flow cytometry.LRIG1 gene expression was detected by quantitative real-time PCR.ResultsIC50 of SKOV3,siRNALRIG1 KOV3,KOV3/VP16 and siRNALRIG1 KOV3/VP1 were 62.90 μg/L,115.49 μg/L,156.50 μg/L and 195.42 μg/L,respectively,with the drug resistance index of 1.8,2.5 and 3.1 respectively.Compared with SKOV3,the cloning rates had increased (the mean differences were 8.000,37.692 and 72.000,P<0.05),the LRIG1 mRNA (the mean differences were 2.994,88.366 and 279.004,P<0.05)and apoptotic cells(the mean difference were 48.942,63.485 83.659,P<0.05)had decreased significantly in siRNALRIG1 KOV3,SKOV3/VP16 and siRNALRIG1 KOV3/VP16 cells.Compared with siRNALRIG1 KOV3,the cloning rates had increased(the mean differences were 25.000 and 58.824,P<0.05),the LRIG1 mRNA(the mean differences were 47.478 and 180.147,P<0.05)and apoptotic cells (the mean differences were 53.678 and 42.687,P<0.05)had decreased in SKOV3/VP16 and siRNALRIG1 KOV3/VP16 cells (P<0.05).Compared with SKOV3/VP16,the cloning rates had increased (the mean difference was 10.000,P<0.05),the LRIG1 mRNA (the mean difference was 92.784,P<0.05)and apoptotic cells (the mean difference was 37.625,P<0.05)had decreased in siRNA LRIG1 KOV3/VP16 cells(P<0.05).Conclusions The LRIG1 gene can affect drug sensitivity of SKOV3 for lower LRIG1 could decrease the apoptosis of cells.

