強制性運動療法對腦卒中大鼠神經功能的影響
王淑玲 劉 佳 鄧景貴 宋 濤 方翠霓 劉楚娟 陶 希
(湖南省人民醫院老年醫學研究所,湖南 長沙 410016)
強制性運動療法對腦卒中大鼠神經功能的影響
王淑玲 劉 佳1鄧景貴 宋 濤 方翠霓 劉楚娟 陶 希
(湖南省人民醫院老年醫學研究所,湖南 長沙 410016)
目的制作腦卒中大鼠模型,給予強制性運動療法(CMIT)干預,觀察干預后大鼠相關神經功能的變化。方法選取SD大鼠,隨機分為假手術組、模型組和CMIT訓練組,觀察各組大鼠行為障礙、組織病理學改變、天冬氨酸特異性半胱氨酸蛋白酶(Caspase)-3及程序化死亡基因(PDCD)-5表達情況、超氧化物歧化酶(SOD)及丙二醛(MDA)含量變化及神經元特異性烯醇化酶(NSE)及S-100β表達情況。結果與假手術組相比,模型組及CMIT訓練組神經功能評分顯著升高(P<0.05);與模型組相比,CMIT訓練組的神經功能評分顯著降低(P<0.05)。假手術組大鼠腦組織細胞結構完整,細胞核、核膜及核仁結構完整;模型組細胞排列紊亂,水腫嚴重,核膜界線不清晰,血管充血嚴重;相比于模型組,CMIT訓練組腦組織結構較完整,且壞死較模型組顯著降低,間質水腫較大緩解。假手術組基本未見Caspase-3及PDCD-5陽性細胞;模型組隨處可見大量Caspase-3及PDCD-5陽性細胞;但相對于模型組,CMIT訓練組Caspase-3及PDCD-5陽性細胞含量明顯降低。與假手術組相比,模型組及CMIT訓練組Caspase-3及PDCD-5 mRNA表達量顯著升高(P<0.05);與模型組大鼠相比,CMIT訓練組大鼠的Caspase-3及PDCD-5 mRNA表達量顯著降低(P<0.05)。相比于假手術組,模型組及CMIT訓練組SOD含量表達顯著降低MDA含量表達顯著升高(P<0.05);相比于模型組,CMIT訓練組SOD含量表達顯著升高MDA含量表達顯著降低(P<0.05);CMIT訓練組(P<0.05)。相比于假手術組,模型組及CMIT訓練組NSE、S-100β含量表達顯著升高;相比于模型組,CMIT訓練組NSE、S-100β含量表達顯著降低(P<0.05)。結論CMIT療法可以通過抑制Caspase-3及PDCD-5凋亡因子,升高SOD,減少MDA、NSE及S-100β含量,從而達到改善腦卒中后神經功能障礙。
強制性運動療法(CMIT);腦卒中;Caspase-3;PDCD-5;SOD;MDA;NSE;S-100β
腦卒中后常因神經功能損傷而造成較高的致殘率,給家庭和社會造成嚴重的負擔。臨床上多運用藥物、手術、康復治療等干預手段緩解腦卒中病情,改善神經功能恢復〔1〕。強制性運動療法(CMIT)通過限制健側上肢、強化訓練患肢,達到強制使用和強化訓練患肢的目的,多用于腦卒中后恢復期的上肢功能訓練〔2〕。然而,有關其對神經功能改善的基礎研究暫時缺如。本研究擬觀察CMIT干預改善大鼠神經功能的作用。
1 對象與方法
1.1動物及分組 從北京華阜康生物公司購置Wistar大鼠120只,隨機分為假手術組、模型組和CMIT訓練組,每組40只。模型組和CMIT訓練組均構建腦卒中大鼠模型,CMIT訓練組給予強制性運動康復。
1.2動物模型構建 參考相關文獻〔3〕建立腦卒中模型。7.2%水合氯醛腹腔注射麻醉大鼠,剪開鼠頭部皮膚,頸正中切口,分離頸外動脈(ECA)、右側頸總動脈(CCA)及頸內動脈(ICA)。結扎ECA及CCA近心端。在CCA近分叉處插入備用魚線,將栓線送至大腦中動脈分叉處,平均進線(18.5±0.5)mm(ECA與ICA分叉處為起點),栓線尾端留于皮膚外,栓塞90 min后抽線實現再灌注。以動物清醒后爬行時右轉圈,提尾時右前肢內收屈曲為入選標準。假手術組操作同上,僅暴露各組血管,而不進行線栓插入。
1.3CMIT訓練 參照相關文獻〔4〕,CMIT訓練組大鼠于造模后第7天行強制性訓練。大鼠給予7.2%水合氯醛腹腔注射麻醉,將健肢置于自然屈曲的位置,然后用石膏纏繞固定該肢體,限制該肢體活動,同時應用改良托盤試驗的訓練,每天訓練時間上下午各15 min。此項訓練可強迫大鼠進行患側肢體的運動。30 d后訓練停止,取腦組織及血清進行后續實驗。訓練過程無死亡率,存活率為100%。
1.4行為障礙評分 造模后30 d,對大鼠進行行為障礙評分,評分標準參照相關文獻〔3〕,采用4分制。0分,未見相關障礙;1分,左側前爪無力;2分,推手術側肩部,可發覺對側的移動阻力降低;3分,大鼠出現旋轉、轉圈及行動歪倒;4分,無肢體活動。分值越高說明行為障礙越重。
1.5腦組織病理形態檢測 造模后30 d,水合氯醛腹腔注射麻醉大鼠處死,斷頭取大鼠腦組織,4%多聚甲醛固定24 h,梯度乙醇脫水,包埋,切片后進行蘇木素-伊紅(HE)染色,光鏡下觀察腦組織形態。
1.6免疫組化檢測天冬氨酸特異性半胱氨酸蛋白酶(Caspase)-3及程序化死亡基因(PDCD)-5的表達 將石蠟切片脫蠟,二甲苯透明,梯度酒精脫水,磷酸鹽緩沖液(PBS)清洗,抗原修復,添加Caspase-3及PDCD-5一抗(購于CST公司)過夜孵育,第2天二抗孵育,室溫靜置2 h,PBS清洗,DAB及蘇木精染色,清洗后封片顯微鏡觀察。
1.7RT-PCR檢測Caspase-3及PDCD-5 mRNA表達 造模后30 d,水合氯醛腹腔注射麻醉大鼠并處死,斷頭取大鼠腦組織。實驗所需器械均經高壓去RNA酶處理,并經0.1%焦碳酸二乙酯(DEPC)水處理,且實驗均在冰塊上操作,降低溫度對結果的影響。取組織塊,加入1 ml TRIZOL,應用勻漿機裂解5 min,然后依次加入三氯甲烷、異丙醇及75%乙醇進行獲取RNA,10 μl DEPC水溶解RNA沉淀,紫外分光光度儀測定濃度及純度。應用逆轉錄試劑盒(購于Takara公司),嚴格按照說明書,將提取的RNA逆轉錄為cDNA,并嚴格按照擴增試劑反應要求進行PCR體系的擴增及反應。引物序列:Caspase-3上游引物5′-ATGGAAGTGTCTCTATTAA-3′,下游引物5′-AGAACGGATTGGGTATGCC-3′;β-actin上游引物5′-CCATAAGCATTTAAACCCTC-3′,下游引物5′-AGTGGGTCATTTCAATACG-3′;PDCD-5上游引物5′-TTGAATGTCTGACTGAAAA-3′,下游引物5′-CAGCCTTTTGTGTTAGACC-3′。
1.8神經元特異性烯醇化酶(NSE)及S-100β蛋白含量檢測 造模后30 d,對大鼠進行眼球取血,靜置2 h后高速離心取血清置于深凍冰箱備用。應用酶聯免疫吸附(ELISA)測定NSE及S-100β含量,取冷凍血清,4℃解凍,應用NSE試劑盒及S-100β試劑盒(均購于R&D公司)。操作嚴格按照試劑盒說明書,預包被孔板,將稀釋后的標準品加入標準品孔,將樣品血清加入樣品孔,加檢測抗體,加生物素標記抗體,室溫孵育,洗板,加入抗生物素蛋白鏈菌素-辣根過氧化物酶,室溫孵育,洗板,顯色液加入,室溫避光孵育15 min,加入終止液,酶標儀讀數,檢測血清中兩種蛋白含量。
1.9超氧化物歧化酶(SOD)檢測 血清制備同1.8。應用SOD試劑盒(碧云天試劑公司),嚴格按照說明書及文獻配置多種試劑及顯色劑及操作〔3〕,并應用儀器檢測吸光度。SOD(U/ml)=(對照管吸光度-測定管吸光度)/對照管吸光度×50%×稀釋倍數。
1.10丙二醛(MDA)檢測 血清制備同1.8。應用MDA試劑盒(碧云天試劑公司),采用熒光檢測法,嚴格參照說明書及相關文獻配置試劑及標準品〔3〕,試劑混勻后95℃水浴40 min,再流水一旁沖洗,3 500 r/min離心10 min,取上清后測定吸光度。MDA(nmol/ml)=(測定管吸光度-測定空白管吸光度)/(標準吸光度-標準空白管吸光度)×標準品濃度×稀釋倍數。
1.11統計學方法 應用SPSS17.0軟件行t檢驗。
2 結 果
2.1行為障礙評分 與假手術組(0分)大鼠相比,模型組〔(3.53±0.76)分〕及CMIT訓練組〔(2.51±0.69)分〕各大鼠的神經功能評分顯著升高(P<0.05);與模型組大鼠相比,CMIT訓練組大鼠的神經功能評分顯著降低(P<0.05)。
2.2腦組織病理學改變 假手術組大鼠腦組織細胞結構完整,細胞核、核膜及核仁結構完整;模型組細胞排列紊亂,水腫嚴重,核膜界線不清晰,血管充血嚴重;相比于模型組,CMIT訓練組腦組織結構較完整,且壞死較模型組顯著降低,間質水腫較大緩解,見圖1。
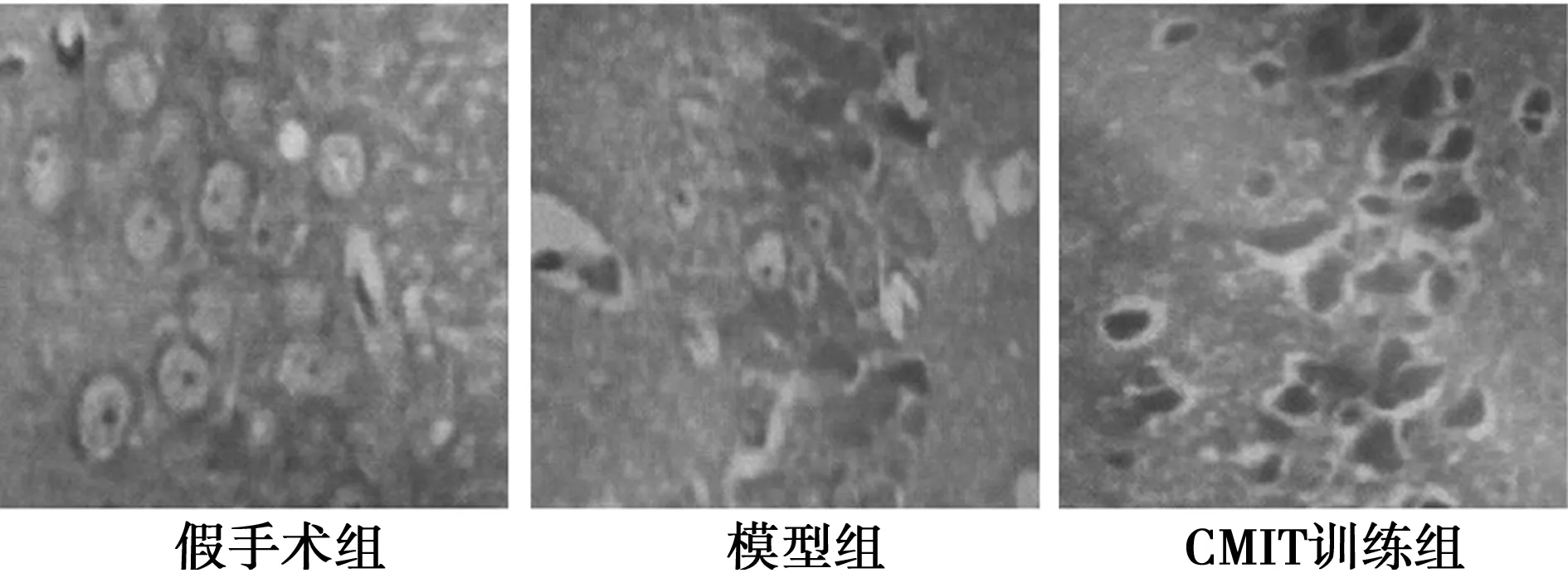
圖1 各組大鼠HE染色(×400)
2.3Caspase-3及PDCD-5表達變化 光鏡下,Caspase-3陽性細胞呈現棕黃色或黃褐色。假手術組基本未見Caspase-3陽性細胞;模型組隨處可見大量Caspase-3陽性細胞;相比于假手術組,CMIT訓練組及模型組Caspase-3陽性細胞含量明顯增加;相對于模型組,CMIT訓練組Caspase-3陽性細胞含量明顯降低,見圖2。光鏡下,PDCD-5陽性細胞呈現棕黃色或黃褐色。假手術組基本未見PDCD-5陽性細胞;模型組隨處可見大量PDCD-5陽性細胞;相比于假手術組,CMIT訓練組及模型組PDCD-5陽性細胞含量明顯增加;但相對于模型組,CMIT訓練組PDCD-5陽性細胞含量明顯降低,見圖3。與假手術組大鼠相比,模型組及CMIT訓練組大鼠的Caspase-3及PDCD-5 mRNA表達量顯著升高(P<0.05);與模型組大鼠相比,CMIT訓練組大鼠的Caspase-3及PDCD-5 mRNA表達量顯著降低(P<0.05),見圖4。
2.4SOD及MDA含量比較 相比于假手術組,模型組及CMIT訓練組SOD含量顯著降低、MDA含量顯著升高(P<0.05);相比于模型組,CMIT訓練組SOD含量表達顯著升高(P<0.05)。見表1。

圖2 各組腦組織Caspase-3表達(DAB,×400)

圖3 各組腦組織PDCD-5表達(DAB,×400)

圖4 Caspase-3及PDCD-5 mRNA含量表達

組別SODMDA假手術組379.44±7.122.23±1.43模型組142.75±7.881)15.32±1.211)CMIT訓練組192.16±8.191)2)7.37±1.091)2)
與假手術組比較:1)P<0.05;與模型組比較:2)P<0.05;下表同
2.5NSE及S-100β含量比較 相比于假手術組,模型組及CMIT訓練組NSE、S-100β含量表達顯著升高(P<0.05);相比于模型組,CMIT訓練組NSE、S-100β含量表達顯著降低(P<0.05)。見表2。
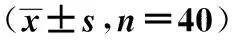
表2 各組大鼠NSE及S-100β含量比較
3 討 論
腦卒中后,腦組織缺血缺氧導致細胞凋亡以及氧自由基增高,促使多種腦組織損傷特異性蛋白,如NSE、S-100β分泌增多,并隨之誘導腦組織神經功能損傷。NSE是多由神經元細胞分泌的,是CNS特異性蛋白,正常情況下血清中無法被檢測到,但當顱內缺血缺氧時,胞質內的NSE即被釋放入血,可作為顱內損傷的標志物〔5〕;S-100β限制性表達于多種腦內膠質細胞,可調節細胞的生長代謝多種功能,參與顱內缺血缺氧的多種病理過程,被認為是腦損傷的特異性標記蛋白〔6〕。
作為腦卒中發病的重要因素之一,細胞凋亡是一種有序性的細胞死亡,是受多種基因調控的細胞正常死亡。已有研究表明,主要有3條信號通路可以干預凋亡:線粒體凋亡通路、內質網凋亡途徑和死亡受體通路,這三種通路最終都通過激活下游Caspase-3、PDCD-5等凋亡蛋白,從而誘發了細胞的程序性死亡〔7〕。Caspase-3處于凋亡系統的中心環節,多種因子及通道均可激活Caspase-3分子,從而啟動細胞凋亡〔8〕。PDCD-5是新近發現的凋亡因子,在凋亡過程中起著早期及始動性的功能,可誘發線粒體凋亡通路〔9〕。與此同時,機體在正常情況下可以清楚體內多余的自由基,然而在顱內缺血缺氧的情況下,機體內會出現較多的氧自由基的積聚,從而加重腦組織的損害。SOD是主要的抗氧化酶,能有效地清除體內自由基〔10〕;而MDA與線粒體膜的穩定性呈負相關〔11〕,因此通過測定兩者情況可以評估顱內氧自由基水平。
多種干預措施可促進腦卒中后的神經功能恢復,其中CMIT療法已被較廣泛地應用于腦卒中患者康復領域,可有效改善患者神經功能障礙〔12〕。然而CMIT通過何種機制干預腦卒中恢復仍然不清楚。本研究可以看出,CMIT療法可以形態學方面顯著改善大鼠腦卒中神經功能障礙,免疫組化染色發現CMIT療法可以改善大鼠顱內細胞凋亡程度,CMIT療法還可以顯著減輕腦卒中大鼠氧自由基的分泌。CMIT療法可以降低腦特異損傷蛋白的分泌,參與腦卒中的修復。以往研究顯示,CMIT療法可誘發大腦皮層發生使用-依賴性神經功能重組的可塑性變化,可使腦卒中恢復期患者大腦皮層發生功能重組變化,使患側上肢運動功能得到恢復〔13,14〕。本研究可以看出,CMIT療法可以通過減輕顱內凋亡程度,氧自由基分泌狀況及腦損傷蛋白的合成來改善腦卒中大鼠的神經功能障礙,然而有關其深入機制的研究仍需后續實驗。
1中華預防醫學會卒中預防與控制專業委員會介入學組,急性缺血性腦卒中血管內治療中國專家共識組.急性缺血性腦卒中血管內治療中國專家共識〔J〕.中國腦血管病雜志,2014;(10):556-60.
2張 璇,張林亭,張 霞,等.強制性使用運動療法對大鼠腦缺血后神經可塑性的影響〔J〕.中國康復醫學雜志,2014;29(7):615-8,623.
3李 紅,張 爽,紀影實,等.山楂葉總黃酮對大鼠局灶性腦缺血再灌注損傷的保護作用〔J〕.中草藥,2010;41(5):794-8.
4何 嬙.強制性運動訓練促進腦缺血大鼠功能恢復的作用機制研究〔D〕.上海:復旦大學,2013.
5Li ZM,Xiao YL,Zhu JX,etal.Recombinant human erythropoietin improves functional recovery in patients with severe traumatic brain injury:A randomized,double blind and controlled clinical trial〔J〕.Clin Neurol Neurosurg,2016;150:80-3.
6Gao J,Zheng Z.Development of prognostic models for patients with traumatic brain injury:a systematic review〔J〕.Int J Clin Exp Med,2015;8(11):19881-5.
7Brazier SP,Telezhkin V,Kemp PJ.Functional interactions between BKCaα-subunit and annexin A5:implications in apoptosis〔J〕.Oxid Med Cell Longev,2016;2016:1607092.
8Cui J,Chen B,Wang H,atal.Glucosidase Ⅱ β-subunit,a novel substrate for caspase-3-like activity in rice,plays as a molecular switch between autophagy and programmed cell death〔J〕.Sci Rep,2016;6:31764.
9張曉璇,李佳佳.丁苯酞對腦缺血再灌注大鼠凋亡情況的影響〔J〕.中國實用神經疾病雜志,2014;17(14):44-6.
10Choudhary R,Bodakhe SH.Magnesium taurate prevents cataractogenesis via restoration of lenticular oxidative damage and ATPase function in cadmium chloride-induced hypertensive experimental animals〔J〕.Biomed Pharmacother,2016;84:836-44.
11Hedayati Kashka R,Zavareh S,Lashkarbolouki T.Augmenting effect of vitrification on lipid peroxidation in mouse preantral follicle during cultivation:modulation by coenzyme Q10〔J〕.Syst Biol Reprod Med,2016;62(6):404-14.
12李瑩瑩,張 備,李 策,等.強制性運動對腦缺血再灌注大鼠前肢運動功能及情緒相關腦區葡萄糖代謝的影響〔J〕.中華物理醫學與康復雜志,2015;37(7):481-6.
13李 賀.強制性使用運動療法對亞急性期腦卒中患者上肢運動功能的康復〔D〕.長春:吉林大學,2013.
14樊留博,韓文勝,章 霞,等.電針聯合強制性運動對腦缺血大鼠神經功能及GFAP表達的影響〔J〕.中華全科醫學,2014;12(12):1891-3,封3.
〔2016-11-14修回〕
(編輯 徐 杰)
R743
A
1005-9202(2017)18-4440-04;doi:10.3969/j.issn.1005-9202.2017.18.005
湖南省自然科學基金(12JJ9029);湖南省科技廳項目(2013FJ3117)
1 湖南省人民醫院康復科
劉 佳(1963-),女,主治醫師,主要從事神經康復研究。
王淑珍(1984-),女,碩士,助理研究員,主要從事神經康復研究。

