Cyclin D1 siRNA轉染人肝癌細胞的增殖、凋亡變化及其機制
張弘英,胡利琳,元文峰,丁浩
(1南昌大學第二附屬醫院,南昌330006;2南昌大學醫學院;3江西省樂安縣人民醫院344300)
Cyclin D1 siRNA轉染人肝癌細胞的增殖、凋亡變化及其機制
張弘英1,胡利琳2,元文峰3,丁浩1
(1南昌大學第二附屬醫院,南昌330006;2南昌大學醫學院;3江西省樂安縣人民醫院344300)
目的觀察Cyclin D1 siRNA轉染的人肝癌細胞增殖、凋亡變化,并探討其機制。方法培養人肝癌細胞株Hep3B,將細胞分為空白對照組、陰性對照組和實驗組。陰性對照組和實驗組分別通過脂質體轉染NC siRNA和Cyclin D1 siRNA,轉染48 h后收獲細胞。采用MTT法檢測細胞增殖能力;流式細胞儀觀察凋亡細胞并計算細胞凋亡率;免疫組化法檢測各組細胞中的Caspase-3蛋白;采用RT-PCR法檢測各組細胞中的乙型肝炎病毒x蛋白(HBx)、著色性干皮病基因蛋白D(XPD)、Bcl-2、Bax mRNA;Western blotting法檢測各組細胞中的HBx、XPD、Bcl-2、Bax蛋白。結果與空白對照組和陰性對照組相比,實驗組細胞增殖能力減弱、凋亡率升高、Caspase-3相對表達量增高(P均<0.01)。與空白對照組和陰性對照組相比,實驗組HBx、Bcl-2 mRNA及蛋白表達下調,XPD、Bax mRNA及蛋白表達上調(P均<0.01)。結論Cyclin D1 siRNA轉染的人肝癌細胞增殖受到抑制、凋亡增多,其機制可能與HBx、Bcl-2表達下調及XPD、Bax表達上調有關。
細胞周期蛋白D1;肝細胞癌;細胞增殖;細胞凋亡;人剪切修復基因
Abstract:ObjectiveTo observe the changes of proliferation and apoptosis of human hepatocellular cells transfected with Cyclin D1 siRNA, and to explore the mechanism.MethodsThe cultured human hepatoma cell line Hep3B was divided into the blank control group, negative control group, and experimental group. The negative control group and the experimental group were transfected with NC siRNA and Cyclin D1 siRNA by liposomes, and the cells were harvested after 48 h. MTT was used to detect cell proliferation; the flow cytometry was used to observe apoptotic cells and we calculated apoptosis rate; the Caspase-3 protein in cells of each group was detected by immunohistochemistry; the mRNA and protein expression levels of hepatitis B virus x protein (HBx), xeroderma pigmentosum D (XPD), Bcl-2, and Bax in cells of each group were detected by RT-PCR and Western blotting, respectively.ResultsCompared with the blank control group and the negative control group, the cell proliferation ability of the experimental group decreased, the apoptosis rate increased, and the relative expression of Caspase-3 increased (allP<0.01). Compared with the blank control group and the negative control group, the mRNA and protein expression levels of HBx and Bcl-2 in the experimental group were down-regulated, while those of XPD and Bax were up-regulated (allP<0.01).ConclusionThe proliferation of human hepatoma cells transfected with Cyclin D1 siRNA is inhibited and the apoptosis increases, and the mechanism may be related to the down-regulation of HBx and Bcl-2 expression, and up-regulation of XPD and Bax expression.
Keywords: Cyclin D1; hepatocellular carcinoma; cell proliferation; apoptosis; human shear repair genes
肝細胞癌(HCC)是全世界最普遍的惡性腫瘤之一,其發病率和病死率均較高[1]。HCC的發生發展是十分復雜的過程,不僅與抑癌基因失活和癌基因或癌相關基因激活有關,還涉及多種信號轉導通路功能失調[2]。長期慢性乙型肝炎(乙肝)病毒(HBV)感染是導致HCC發病的重要原因之一,這一過程可能與乙肝病毒x蛋白(HBx)對肝細胞周期與凋亡的影響有關[3]。HBx蛋白可通過反式激活細胞啟動子和增強子來增強病毒基因的表達和復制,這有助于病毒的持續性感染[4]。目前尚無效果顯著的方法用于治療HBV相關HCC。Cyclin D1是調控細胞周期G1期(DNA合成前期)的關鍵蛋白,現已證實Cyclin D1與包括肝癌在內的多種惡性腫瘤的發生發展有關[5]。本研究將靶向Cyclin D1基因的小干擾RNA(siRNA)轉染人肝癌細胞株Hep3B細胞,觀察Cyclin D1 siRNA轉染的人肝癌細胞增殖、凋亡變化,并探討其機制。
1 材料與方法
1.1 主要實驗材料 人肝癌細胞Hep3B由本實驗室保存。MEM培養基和胎牛血清購自Gibco公司。陰性對照siRNA(NC siRNA)和Cyclin D1 siRNA均由上海吉凱公司合成,在前期實驗中已證實Cyclin D1 siRNA序列(5′-UUCUCCGAACGUGUCACGUTT-3′)具有沉默效果。NC siRNA序列為5′-ACAAACAGATCATCCGCAA-3′,Cyclin D1 siRNA序列為5′-UUCUCCGAACGUGUCACGUTT-3′。MTT試劑購自Solarbio公司。Annexin V-FITC細胞凋亡檢測試劑盒購自杭州聯科生物公司。TRIzol及脂質體LipofectamineTM2 000均購自Invitrogen公司。Caspase-3 一抗購自Abcam公司。逆轉錄試劑盒購自Fermentas公司。2×濃縮PCR擴增預混液購自天根生物技術有限公司。所用引物由Generay Biotech公司合成。總蛋白提取試劑盒購自北京普利萊基因技術有限公司。Cyclin D1、HBx、Bcl-2、XPD、Bax、β-actin的一抗購自Santa Cruz公司。作為二抗的HRP-Goat anti Mouse IgG購自北京中杉金橋公司。
1.2 細胞培養及Cyclin D1 siRNA轉染 用含雙抗(100 μg/mL的鏈霉素和100 U/mL的青霉素)、10%胎牛血清的MEM培養基培養Hep3B細胞,然后將裝有Hep3B細胞的培養瓶置于5% CO2、37 ℃恒溫孵箱內培養。往6孔板內平鋪細胞,控制細胞密度為1×106/孔,24 h后在顯微鏡下觀察到Hep3B細胞融合率約為90%。將Hep3B細胞分為空白對照組、陰性對照組和實驗組。陰性對照組和實驗組分別通過脂質體轉染NC siRNA和Cyclin D1 siRNA。實驗每組重復6次。siRNA濃度為100 nmol/L,脂質體每孔5 μL。轉染48 h后收獲細胞。經RT-PCR法測得空白對照組、陰性對照組和實驗組Cyclin D1 mRNA相對表達量分別為3.53±0.99、3.64±1.37、0.99±0.62,經Western blotting法測得三組Cyclin D1蛋白相對表達量分別為1.56±0.29、1.62±0.49、0.18±0.12,實驗組Cyclin D1 mRNA及蛋白相對表達量均低于空白對照組和陰性對照組(P均<0.05),說明Cyclin D1 siRNA轉染成功,實驗組Cyclin D1表達下調。
1.3 細胞增殖能力檢測 將人肝癌Hep3B細胞種植于96孔板內,留出空白凋零孔,不添加細胞。每孔內均加入15 mg/mL的MTT溶液20 μL,孵育4 h后棄去上清,再分別往每孔內加入二甲基亞楓(DMSO)150 μL,振蕩10 min。放入酶聯免疫監測儀(Labststems,芬蘭),波長設置為492 nm,測定96孔板內各孔的光密度值(OD值),以此反映細胞增殖能力。
1.4 細胞凋亡率測算 用胰酶消化并收集空白對照組、陰性對照組及實驗組細胞。PBS溶液分別洗滌細胞2次,用Binding Buffer緩沖液(含Ca2+的緩沖液)500 μL進行懸浮。分別往各組細胞中加入PI、Annexin V-FITC染色體熒光各5 μL。流式細胞儀觀察凋亡細胞,計算細胞凋亡率。
1.5 各組細胞中Caspase-3蛋白檢測 采用免疫組化法。先將收獲的細胞固定,石蠟包埋,切片,脫蠟。用3%的過氧化氫阻斷內源性過氧化物酶,然后用Caspase-3的一抗(工作濃度為1∶100)孵育,再用相應的二抗孵育。切片先后用二氨基聯苯胺、蘇木精染色,顯微鏡下觀察,Caspase-3陽性為細胞呈棕黃色或棕褐色染色。根據染色強度和陽性細胞百分比判定結果[6]:黑褐色或棕褐色計3分,棕黃色或深黃色計2分,淡黃色計1分,無明顯著色計0分;陽性細胞百分比>75%計4分,>50%~75%計3分,>25%~50%計2分,>5%~25%計1分,0~5%計0分;上述兩項得分相乘,1~12為Caspase-3蛋白表達陽性。
1.6 各組細胞中HBx、XPD、Bcl-2、Bax mRNA及蛋白檢測
1.6.1 HBx、XPD、Bcl-2、Bax mRNA檢測 采用RT-PCR法。HBx基因上游引物序列為5′-CACTTCGCCTCACCTCTG-3′,下游引物序列為5′-TCGGTCGTTGACATTGCT-3′,產物長度112 bp;Bcl-2基因上游引物序列為5′-AAGCCGGCGACGACTTCT-3′,下游引物序列為5′-GGTGCCGGTTCAGGTACTCA-3′,產物長度258 bp;XPD基因上游引物序列為5′-TCTGCCTCTGCCCTATGAT-3′,下游引物序列為5′-GGTGCCGGTTCAGGTACTCA-3′,產物長度363 bp;Bax基因上游引物序列為5′-GGATGCGTCCACCAAGAA-3′,下游引物序列為5′-GCACTCCCGCCACAAAGA-3′,產物長度386 bp;內參β-actin基因上游引物序列為5′-CGGGAAATCGTGCGTGAC-3′,下游引物序列為5′-TGGAAGGTGGACAGCGAGG-3′,產物長度434 bp。PCR反應體系:上下游引物各1 μL,cDNA 500 ng,2×濃縮的PCR擴增預混液12.5 μL,然后在反應體系內添加去離子水至體系最終體積為25 μL。PCR反應擴增條件:預變性94 ℃ 5 min,1個循環;DNA變性94 ℃ 40 s、引物退火55 ℃ 40 s、DNA聚合酶延伸72 ℃ 55 s,35個循環;最終延伸72 ℃ 7 min,1個循環。PCR反應結束后,取PCR產物5 μL進行瓊脂糖凝膠電泳,后置于凝膠成像儀下觀察并拍照。用Bland Leader3.00凝膠電泳圖像分析軟件分析結果,以目的基因/β-actin比值代表目的基因相對表達量。
1.6.2 HBx、XPD、Bcl-2、Bax蛋白檢測 用RIPA裂解液提取細胞總蛋白,BCA試劑盒測定蛋白濃度,然后取蛋白20 μg進行SDS-聚丙烯酰胺凝膠電泳。將凝膠上分離到的蛋白條帶通過轉移電泳方式轉至硝酸纖維素膜上,3% BSA封閉膜,放于4 ℃環境過夜,然后分別用非標記一抗(工作濃度1∶200)及辣根過氧化物酶標記的二抗進行孵育。使用DAB顯色試劑顯色1~30 min后照相。采用Quantity One4.62分析結果。以目的基因/β-actin比值表示目的蛋白相對表達量。
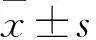
2 結果
2.1 各組細胞增殖能力、凋亡率及Caspase-3蛋白表達比較 與空白對照組和陰性對照組相比,實驗組細胞增殖能力減弱、凋亡率升高、Caspase-3相對表達量增高(P均<0.01)。詳見表1。
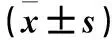
表1 各組細胞增殖能力、細胞凋亡率及Caspase-3蛋白相對表達量
注:與實驗組相比,*P<0.01。
2.2 各組細胞中HBx、XPD、Bcl-2、Bax mRNA及蛋白表達比較 與空白對照組和陰性對照組相比,實驗組HBx、Bcl-2 mRNA及蛋白表達下調,XPD、Bax mRNA及蛋白表達上調(P均<0.05)。詳見表2。
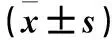
表2 各組HBx、XPD、Bcl-2、Bax基的mRNA和蛋白表達比較
注:與實驗組相比,*P<0.01,#P<0.05。
3 討論
HCC是最常見的惡性腫瘤之一。我國乙肝的高發,使肝癌患者占全世界較大比例[7]。HBx具有多種生物學功能,能夠影響宿主細胞基因表達,從而調節宿主細胞的增殖與分化、影響細胞的信號轉導通路等。HBV相關HCC的發生可能與HBx對肝細胞分裂周期與凋亡的影響有關[8]。HBV相關HCC目前尚無特效治療手段。基因治療具有獨特優勢,可能是HBV相關HCC治療的新方向。
生物體正常的生存、繁殖與細胞周期的準確調控具有密不可分的關系。細胞周期蛋白對細胞周期的各時相均起調控作用,其中參與細胞周期調控的主要因子是Cyclin。細胞周期中G1期的啟動是細胞周期的關鍵,而調控G1期的關鍵蛋白之一是Cyclin D1。Cyclin D1含295個氨基酸,由染色體11q13上的基因編碼[9]。動物模型和細胞實驗均表明,Cyclin D1蛋白過度表達可使細胞G1期縮短,對分裂原的依賴性減弱[10]。正常細胞周期中,Cyclin D1僅在G期呈低水平或恒定表達,而在腫瘤細胞中Cyclin D1呈過度表達,可縮短G1期,導致腫瘤細胞過度增殖。現已證實許多惡性腫瘤的發生發展與Cyclin D1過度表達有關[11]。肝癌的發病同樣與G/S期檢測點缺陷有關[12]。且Cyclin D1高表達的肝癌患者預后不良,而Cyclin D1下調能促進肝癌細胞株Huh7細胞凋亡,使其停滯在G1期[13]。
本研究將靶向Cyclin D1基因的siRNA轉染人肝癌細胞株Hep3B構建Cyclin D1表達下調的肝癌細胞模型,觀察Cyclin D1表達下調對人肝癌細胞增殖、凋亡的影響。本研究結果顯示,與空白對照組和陰性對照組相比,實驗組細胞增殖能力減弱、凋亡率升高、Caspase-3相對表達量增高。Caspase-3是細胞凋亡過程中最主要的終末剪切酶,其活性增強意味著凋亡被誘導[14]。由此可見,Cyclin D1基因表達下調能抑制肝癌細胞的增殖并促進其凋亡。
HBx能整合進入宿主肝細胞的DNA內,從而影響肝細胞的DNA轉錄和蛋白翻譯,繼而影響肝細胞的增殖與分化,影響細胞內信號轉導通路功能等,是HBV致肝癌的重要因素之一[15, 16]。Hep3B細胞是能表達HBx的人肝癌細胞株。本研究發現,Cyclin D1基因表達下調能抑制HBx的表達,提示下調Cyclin D1基因表達也許能降低感染HBV肝細胞惡變的可能性。XPD是轉錄因子ⅡH組成成分之一。許多研究發現XPD參與核苷酸的損傷修復過程,并影響癌基因和抑癌基因的表達,與腫瘤的發生密切相關[17,18]。本課題組前期研究[19]也證實,XPD基因可促進肝癌細胞凋亡并抑制肝癌細胞的生長。Bcl-2、Bax同屬Bcl-2基因家族,而前者是原癌基因,后者是抑癌基因。Bax/Bcl-2可調節細胞增殖與凋亡之間的平衡[20],Bcl-2/Bax比值越大,說明腫瘤細胞的增殖能力越強、凋亡越少。本研究結果顯示,Cyclin D1基因表達下調能抑制肝癌細胞中原癌基因Bcl-2表達,能上調抑癌基因XPD、Bax的表達。這些結果進一步提示,Cyclin D1基因表達下調對肝癌細胞的增殖抑制、促凋亡作用可能與HBx、Bcl-2表達下調和XPD、Bax表達上調有關。
[1] 丁婕妤,王璇,翁苓苓,等.天冬多糖對低氧條件下人肝癌細胞生長、侵襲及遷移的影響[J].山東醫藥,2017,57(14):23-26.
[2] Xu W, Yu J, Wong VW. Mechanism and prediction of HCC development in HBV infection[J]. Best Pract Res Clin Gastroenterol, 2017,31(3):291-298.
[3] Yang SL, Ren QG, Zhang T, et al. Hepatitis B virus X protein and hypoxia inducible factor-1α stimulate Notch gene expression in liver cancer cells[J]. Oncol Rep, 2017,37(1):348-356.
[4] He Z, Yu Y, Nong Y, et al. Hepatitis B virus X protein promotes hepatocellular carcinoma invasion and metastasis via upregulating thioredoxin interacting protein[J]. Oncol Lett, 2017,14(2):1323-1332.
[5] Li Z, Qu L, Luo W,et al. Mig-6 is down-regulated in HCC and inhibits the proliferation of HCC cells via the P-ERK/Cyclin D1 pathway[J].Exp Mol Pathol, 2017,102(3):492-499.
[6] Zhang HL, Zhang H. Withaferin-A Induces Apoptosis in Osteosarcoma U2OS Cell Line via Generation of ROS and Disruption of Mitochondrial Membrane Potential[J]. Pharmacogn Mag, 2017,13(51):523-527.
[7] 袁媛,陳驥,王亞莉.HBeAg陰性慢性乙肝合并肝硬化患者血清HBV-DNA水平與肝功能的關系[J].山東醫藥,2017,57(1):81-83.
[8] Kong F, Hu W, Zhou K, et al. Hepatitis B virus X protein promotes interleukin-7 receptor expression via NF-κB and Notch1 pathway to facilitate proliferation and migration of hepatitis B virus-related hepatoma cells[J]. J Exp Clin Cancer Res, 2016,35(1):172.
[9] Ren K, Li Y, Lu H, et al. miR-3940-5p Functions as a Tumor Suppressor in Non-Small Cell Lung Cancer Cells by TargetingCyclin D1 and Ubiquitin Specific Peptidase-28[J]. Transl Oncol, 2016,10(1):80-89.
[10] Wang WJ,Zhao YM,Yang J,et al.Cyclin D1 polymorphism and oral cancer: a meta-analysis[J]. Mol Biol Rep,2013, 40(1):87-95.
[11] Ferreira-Silva GA, Ortega MM, Banionis MA,et al. A novel ruthenium complex that effectively inhibits ERK activation and cyclin D1 expression in A549 cells[J].Toxicol In Vitro,2017,10(44):382-391.
[12] Steven BH, Curt W. Topology and Control of the Cell-Cycle-Regulated Transcriptional Circuitry[J]. Genetics, 2014,196(1):65-90.
[13] Zhang J, Qin L, Han L, et al. Role of MicroRNA-93 I in Pathogenesis of Left Ventricular Remodeling via Targeting Cyclin-D1[J]. Med Sci Monit, 2017,17(23):3981-3988.
[14] 張立成,周毅.結直腸腺癌組織中EZH2、Caspase-3蛋白的表達變化及意義[J].山東醫藥,2017,57(25):48-50.
[15] Yin D, Wang Y, Sai W, et al. HBx-induced miR-21 suppresses cell apoptosis in hepatocellular carcinoma by targeting interleukin-12[J]. Oncol Rep, 2016,36(4):2305-2312.
[16] 姚雪兵,楊林,朱建蕓,等.野生型及羧基端缺失突變HBx對肝癌細胞增殖的影響[J].廣東醫學,2015,36(24):3742-3745.
[17] Ravegnini G, Nannini M, Simeon V, et al. Polymorphisms in DNA repair genes in gastrointestinal stromal tumours: susceptibility and correlation with tumour characteristics and clinical outcome[J]. Tumour Biol, 2016,37(10):13413-13423.
[18] Wang XC, Wang F, Quan QQ. Roles of XRCC1/XPD/ERCC1 Polymorphisms in Predicting Prognosis of Hepatocellular Carcinoma in Patients Receiving Transcatheter Arterial Chemoembolization[J]. Genet Test Mol Biomarkers, 2016,20(4):176-184.
[19] 丁浩,張吉翔.人著色性干皮病基因D對HepG2細胞Mdm2和Mdm4表達的影響[J].中國病理生理雜志,2014,30(1):48-52.
[20] Zhang S, Qin F, Yang L, et al. Nucleophosmin Mutations Induce Chemosensitivity in THP-1 Leukemia Cells by Suppressing NF-κB Activity and Regulating Bax/Bcl-2 Expression[J]. J Cancer, 2016,7(15):2270-2279.
Changes in proliferation and apoptosis of human hepatocellular carcinoma cells transfected with Cyclin D1 siRNA
ZHANGHongying1,HULilin,YUANWenfeng,DINGHao
(1TheSecondAffiliatedHospitalofNanchangUniversity,Nanchang330006,China)
10.3969/j.issn.1002-266X.2017.35.007
R735.7
A
1002-266X(2017)35-0022-04
2017-06-14)
國家自然科學基金資助項目(81300348);江西省自然科學基金資助項目(20151BAB205100)。
張弘英(1963-),女,副主任醫師,主要從事肝病的研究。E-mail:ladh_2000@163.com
丁浩(1981-),男,博士學歷,副主任醫師,主要從事肝病的研究。E-mail: efydinghao@163.com

