宮頸癌組織長鏈非編碼RNA XIST、小分子RNA miR-101-3p表達變化及其意義
劉麗丹,黃浩梁
(武漢市第一醫院,武漢 430022)
宮頸癌組織長鏈非編碼RNA XIST、小分子RNA miR-101-3p表達變化及其意義
劉麗丹,黃浩梁
(武漢市第一醫院,武漢430022)
目的觀察宮頸癌組織長鏈非編碼RNA(LncRNA)X染色體失活特異轉錄子(XIST)、小分子RNA miR-101-3p表達變化,并探討其臨床意義。方法選取91例宮頸癌患者的宮頸癌組織標本為觀察組,癌旁正常組織(距離宮頸癌組織>5cm且經病例檢查證實為正常組織)標本為對照組。采用實時熒光定量PCR法檢測兩組標本中的XIST、miR-101-3p表達,并分析其與宮頸癌臨床病理參數的關系。結果觀察組、對照組XIST表達量分別為8.97±3.56、7.01±3.82,miR-101-3p表達量分別為8.24±4.22、10.15±3.97。觀察組XIST表達量高于對照組(P<0.05),miR-101-3p表達量低于對照組(P<0.05)。Pearson積矩相關分析結果顯示宮頸癌組織miR-101-3p、XIST表達量呈負相關性(r=-0.716,P<0.05)。腫瘤最大徑≥4 cm、FIGO分期Ⅲ+Ⅳ期、低分化、有淋巴結轉移的宮頸癌組織中miR-101-3p表達量分別低于于腫瘤最大徑<4 cm、FIGO分期Ⅰ+Ⅱ期、中高分化、無淋巴結轉移的宮頸癌組織(P均<0.05),XIST表達量分別高于于腫瘤最大徑<4 cm、FIGO 分期Ⅰ+Ⅱ期、中高分化、無淋巴結轉移宮頸癌組織(P均<0.05)。結論宮頸癌組織XIST表達升高、miR-101-3p表達降低。檢測宮頸組織XIST、miR-101-3p有助于宮頸癌的病情判斷。
宮頸癌;長鏈非編碼RNA;X染色體失活特異轉錄子;小分子RNA;miR-101-3p
目前對腫瘤發生原因的研究已經涉及小分子RNA(miRNA)和長鏈非編碼RNA(LncRNA)[1,2]。
小分子RNA101(miR-101)廣泛存在于真核生物細胞,可作為抑癌因子在乳腺癌[3]、胃癌[4]等惡性腫瘤中異常表達,miR-101-3p是miR-101的一種活性形式[5]。目前尚不清楚宮頸癌組織中miR-101表達變化情況。X染色體失活特異轉錄因子(XIST)表達異常與肺癌和胰腺癌的發生發展有關[6,7]。目前宮頸癌組織中XIST表達變化也不清楚。本課題組前期研究用ELM數據庫分析發現,miR-101和XIST存在4個結合位點,筆者推測二者可能存在相互作用。本研究觀察了宮頸癌組織中miR-1-1-3p、XIST的表達變化,并分析了宮頸癌組織中miR-101、XIST表達與宮頸癌臨床病理參數的關系,旨在明確miR-1-1-3p、XIST在宮頸癌發生發展中的作用及檢測宮頸癌組織miR-1-1-3p、XIST表達的臨床意義。
1 資料與方法
1.1 臨床資料 收集2016年1月~2017年1月收治的91例宮頸癌患者的手術切除宮頸癌組織標本為觀察組,癌旁正常組織標本(距離宮頸癌組織>5 cm且經病例檢查證實為正常組織)為對照組。患者納入標準:①宮頸癌組織病理檢查確定為宮頸癌;②術前未行任何放、化療治療;③術前未接受其它可能影響本研究結果的抗腫瘤藥物治療。排除標準:①妊娠期以及哺乳期的婦女;②心臟功能不全者;③肝、腎功能障礙者;④臨床病歷資料記錄不完整者;⑤合并有其它惡性腫瘤的患者。入組患者年齡39~76(63.24±11.87)歲;腫瘤類型為鱗癌55例,腺癌35例;病灶最大徑<4 cm者49例,≥4 cm者 42例;國際婦產科聯盟(FIGO)分期[8]Ⅰ+Ⅱ期38例,Ⅲ+Ⅳ期53例;分級程度低分化31例,中、高分化60例;有淋巴結轉移33例,無淋巴結轉移58例。本研究已獲我院醫學倫理委員會批準。患者或其家屬已簽署知情同意書。
1.2 miR-101、XIST檢測方法 參照RNA提取試劑盒(諾維贊生物公司)說明書操作提取總RNA。按照逆轉錄試劑盒(諾維贊生物公司)說明書操作進行RNA的反轉錄。反應體系包括總RNA 1 μg、2×RT mix 10 μL、mix 2 μL、oligo dNTPs 1 μL、引物 1 μL共計20 μL。反應條件25 ℃ 5 min,50 ℃ 15 min,85 ℃ 5 min。按照熒光定量PCR試劑盒(諾維贊生物公司)說明書操作進行熒光定量PCR,反應體系包括反轉錄產物2 μL、正向引物2 μL、反向引物2 μL、2×mix 10 μL、純水4 μL,設定38個循環,循環的程序為95 ℃ 30 s、95 ℃ 5 s、60 ℃ 30 s。以GAPDH為內參照。檢測XIST所需引物采用Primer Premier 5.0軟件設計,并由上海生工生物工程公司合成。XIST上游引物序列5′-AATGGAACGGGCTGAGTTTTAG-3′,下游引物序列5′-TCATCCGCTTGCGTTCATAG-3′;內參GAPDH上游引物序列5′-GGAAGGACTCATGACCACAGTCC-3′,下游引物序列5′-TCGCTGTGAAGTCAGAGGAGACC-3′。檢測miR-101-3p所需引物采用TaqMan公司生產的miR-101-3p檢測探針。以2-ΔΔCt表示miR-101、XIST表達量。
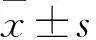
2 結果
2.1 兩組miR-101-3p、XIST表達比較 觀察組、對照組XIST表達量分別為(8.97±3.56)、(7.01±3.82),miR-101-3p表達量分別為(8.24±4.22)、(10.15±3.97)。觀察組XIST表達量高于對照組(P<0.05),miR-101-3p表達量低于對照組(P<0.05)。
2.2 觀察組miR-101-3p、XIST表達量的相關性 Pearson積矩相關分析結果顯示宮頸癌組織miR-101-3p、XIST表達量呈負相關性(r=-0.716,P<0.05)。
2.3 宮頸癌組織miR-101-3p、XIST表達與宮頸癌臨床病理參數的關系 見表1。腫瘤最大徑≥4 cm、FIGO分期Ⅲ+Ⅳ期、低分化、有淋巴結轉移的宮頸癌組織中miR-101-3p表達量分別低于于腫瘤最大徑<4 cm、FIGO分期Ⅰ+Ⅱ期、中高分化、無淋巴結轉移的宮頸癌組織(P均<0.05),XIST表達量分別高于于腫瘤最大徑<4 cm、FIGO分期Ⅰ+Ⅱ期、中高分化、無淋巴結轉移宮頸癌組織(P均<0.05);不同年齡、病理類型宮頸癌組織中miR-101-3p、XIST表達量相比P均>0.05。
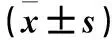
表1 宮頸癌組織XIST、miR-101-3p表達與宮頸癌臨床病理參數的關系
3 討論
miRNA是內源性的非編碼小RNA,廣泛存在于真核生物中,它與惡性腫瘤的發生、發展密切相關,腫瘤細胞中的miRNA異常改變可以介導某些基因的表達,進而調控惡性腫瘤細胞的功能[12]。miR-101作為抑癌因子在乳腺癌[13]、肝癌[14]等惡性腫瘤細胞呈低表達,并調控其增殖、侵襲、轉移等。MiR-101包括miR-101-3P和miR-101-5p兩種成熟的形式,有研究發現miR-101-3p的下調可以促進肝癌細胞的增殖、遷移,并抑制細胞的凋亡[15]。在正常雌性哺乳動物細胞中,XIST是維持兩條X染色體中一條沉默的關鍵因素,其表達異常會導致細胞基因轉錄過程異常而向惡性轉變。文獻報道,XIST表達異常與肺癌、乳腺癌等密切相關[17]。本研究首先觀察了宮頸癌組織miR-101-3p、XIST表達變化,結果顯示,與癌旁組織比較,宮頸癌組織中miR-101-3p表達下調,XIST表達上調,提示miR-101-3p、XIST參與了宮頸癌的發病過程。Sheng等[4]的研究結果顯示,miR-101-3p表達下調參與了肝癌的增殖、遷移。魏偉等[6]的研究發現,XIST在胰腺癌組織中呈高表達,可能參與了胰腺癌的發生、發展過程。亦與本研究結果相呼應。Pearson積矩相關分析結果顯示宮頸癌組織中miR-101-3p與XIST的表達呈負相關。筆者在前期研究中利用ELM數據庫分析發現,miR-101和XIST存在4個結合位點。結合本研究結果,筆者認為XIST、miR-101-3p共同參與了宮頸癌發生過程,但是其中究竟是XIST調控miR-101-3p還是miR-101-3p調控XIST目前尚不清楚。
本研究結果顯示,相對于腫瘤最大徑<4 cm、FIGO分期Ⅰ+Ⅱ期、中高分化、無淋巴結轉移的宮頸癌組織腫瘤最大徑≥4 cm、FIGO分期Ⅲ+Ⅳ期、低分化、有淋巴結轉移的宮頸癌組織中miR-101-3p低表達、XIST高表達更為顯著,說明miR-101-3p、 XIST與宮頸癌患者臨床病理參數密切相關,腫瘤越大、臨床分期越晚、腫瘤分化程度越差以及有區域淋巴結轉移時,兩種蛋白的表達異常更為明顯,提示臨床檢測宮頸組織miR-101-3p、XIST有助于宮頸癌的病情判斷。
綜上所述,宮頸癌組織miR-101-3p表達下降、 XIST表達升高。檢測宮頸癌組織miR-101-3p、 XIST表達有助于判斷患者病情。
[1] Huang L, Huang Z, Fan Y, et al. FOXC1 promotes proliferation and epithelial-mesenchymal transition in cervical carcinoma through the PI3K-AKT signal pathway[J].Am J Transl Res, 2017,9(3):1297-1306.
[2] 劉瀟陽,張詢.中國人群宮頸癌p63蛋白表達的Meta分析[J].診斷病理學雜志,2014,32(5):267-269.
[3] Liu P, Ye F, Xie X, et al. mir-101-3p is a key regulator of tumor metabolism in triple negative breast cancer targeting AMPK[J].Oncotarget, 2016,7(23):35188-35198.
[4] Sheng Y, Li J, Zou C, et al. Downregulation of miR-101-3p by hepatitis B virus promotes proliferation and migration of hepatocellular carcinoma cells by targeting Rab5a[J]. Arch Virol, 2014,159(9):2397-2410.
[5] Cui Y, Zhang F, Zhu C, et al. Upregulated lncRNA SNHG1 contributes to progression of non-small cell lung cancer through inhibition of miR-101-3p and activation of Wnt/β-catenin signaling pathway[J]. Oncotarget, 2017,8(11):17785-17794.
[6] 魏偉,楊波,唐翎.長鏈非編碼RNA XIST在胰腺癌中的表達及意義[J].中國普通外科雜志,2017,26(3):304-310.
[7] Wang H, Shen Q, Zhang X, et al. The long non-coding RNA XIST controls non-small cell lung cancer proliferation and invasion by modulating miR-186-5p[J]. Cell Physiol Biochem, 2017,41(6):2221-2229.
[8] Reisenauer C, Wallwiener D, Brucker SY, et al. Pelvic organ prolapse stage Ⅳ and cervical cancer FIGO Ⅱa[J]. Arch Gynecol Obstet, 2017,295(6):1303-1304.
[9] 趙珊,姚德生,陳軍瑩,等.血清miR-203與宮頸癌臨床病理特征的關系[J].重慶醫學,2014,43(8):972-975.
[10] 韓金利,楊冉,崔志英.宮頸癌患者血清CRP水平與臨床病理特征和預后的關系[J].中國婦幼保健,2015,30(17):2728-2730.
[11] Kurita T, Matsuura Y, Koi C, et al. The relationship between positive peritoneal cytology and the prognosis of patients with uterine cervical cancer[J].Acta Cytol, 2015,59(2):201-206.
[12] Loosen SH, Schueller F, Trautwein C, et al. Role of circulating microRNAs in liver diseases[J]. World J Hepatol, 2017,9(12):586-594.
[13] Wang L, Li L, Guo R, et al. miR-101 promotes breast cancer cell apoptosis by targeting Janus kinase 2[J]. Cell Physiol Biochem, 2014,34(2):413-422.
[14] Xu F, Liao JZ, Xiang GY, et al. MiR-101 and doxorubicin codelivered by liposomes suppressing malignant properties of hepatocellular carcinoma[J].Cancer Med, 2017,6(3):651-661.
[15] Sheng Y, Ding S, Chen K, et al. Functional analysis of miR-101-3p and Rap1b involved in hepatitis B virus-related hepatocellular carcinoma pathogenesis[J]. Biochem Cell Biol, 2014,92(2):152-162.
[16] Hu CE, Du PZ, Zhang HD, et al. Long noncoding RNA CRNDE promotes proliferation of gastric cancer cells by targeting miR-145[J]. Cell Physiol Biochem,2017,42(1):13-21.
[17] Schouten PC, Vollebergh MA, Opdam M, et al. High XIST and low 53BP1 expression predict poor outcome after high-dose alkylating chemotherapy in patients with a BRCA1-like breast cancer[J]. Mol Cancer Ther, 2016,15(1):190-198.
10.3969/j.issn.1002-266X.2017.35.014
R737.3
B
1002-266X(2017)35-0044-03
2017-06-02)
湖北省自然科學基金項目(2015CFB306)。

