響應面優化復合酶法提取干巴菌多糖工藝
張嵐,和勁松,王雪峰,廖國周,普岳紅,葛長榮,范江平,谷大海
(云南農業大學食品科學技術學院,云南昆明650201)
響應面優化復合酶法提取干巴菌多糖工藝
張嵐,和勁松,王雪峰,廖國周,普岳紅,葛長榮,范江平*,谷大海*
(云南農業大學食品科學技術學院,云南昆明650201)
探討應用復合酶法提取干巴菌多糖的最佳工藝條件。以多糖提取率為考察指標,在單因素優化的基礎上,應用Box-Behnken試驗設計優化得出影響因素的最佳參數水平,進而獲得最佳工藝條件。結果表明:復合酶法提取干巴菌多糖的最佳工藝條件為酶解時間64 min,料液比1∶40(mg/L),復合酶濃度0.47%,在此條件下干巴菌多糖提取率為17.87%,提取效果最優。
干巴菌;多糖;復合酶法;響應面分析法;工藝優化
Abstract:The paper was aimed to study the optimal conditions for compound enzyme extraction of polysaccharides of Thelephora ganbajun Zang.The extraction rate of polysaccharides was main value index,based on single factor tests,the optimal parameters of influence factors were optimized by Box-Behnken design,and then the optimal conditions were obtained.The results showed that the optimal extraction conditions were hydrolysis time 64 min,material-liquid ratio 1∶40(mg/L),compound enzyme 0.47%.Under these conditions,the extraction rate of polysaccharides could be up to 17.87%,as well as show the optimal extraction results.
Key words:Thelephora ganbajun Zang;polysaccharide;compound enzymes methods;response surface analysis;processing optimization
多糖作為自然界中含量最多的天然聚合物之一,是生命物質中重要的組成成分,由于其豐富的生物活性以及獨特的生理功能,多糖類化合物在醫藥、石化工業、環保工業以及食品工業中有廣泛的應用,成為當今國內外的研究熱點。食用菌多糖因其具有純天然、無毒害、活性高等特點,擁有巨大的應用價值和較為廣闊的市場前景[1-2]。
干巴菌又名繡球菌,也叫對花菌、馬牙菌等,屬于真菌門、層菌綱、褶菌目、革菌科,主產于云南,是一種珍稀名貴的食藥兩用真菌[3-4]。干巴菌主要分布在云南省昆明、呈貢、安寧、楚雄、保山等地,集中在海拔1 000 m~2 200 m的松林中,是野生食用菌中的上品。已有實驗證明,干巴菌的活性成分中,多糖含量較高,具有抗氧化、增強免疫力等功效[5]。由于干巴菌季節性很強,為云南特有地方性食用菌,僅在云南省尤其是昆明以及其臨近地區有食用習慣[6],因此,國內外對干巴菌的研究極少,可能與原料的產地與產量較少有關。目前針對菌類多糖提取工藝的研究多采用傳統熱水法,多糖難以釋放出來,導致多糖得率較低[7]。而復合酶法可以最大限度的將植物組織分解,提高多糖得率;同時減少多糖結構及生物活性的破壞,已逐漸成為植物活性成分提取工藝的研究熱點[8]。響應面分析法是利用合理的試驗設計方案,通過對回歸方程的分析,優化工藝參數的統計方法[9]。該方法設計合理,結果準確,被越來越多的應用于工藝優化中。因此,本研究采用響應面優化復合酶法提取干巴菌多糖工藝,考察各工藝參數對多糖得率的影響,旨在為干巴菌多糖活性的深入研究及其開發和利用提供一定的理論依據。
1 材料與方法
1.1 材料與試劑
新鮮干巴菌:云南易門康源菌業有限公司,干巴菌經低溫干燥后,粉碎,備用。
纖維素酶、木瓜蛋白酶:Sangon Biotech公司;無水乙醇、葡萄糖、苯酚、濃硫酸:天津市致遠化學試劑有限公司;所用試劑均為分析純。
1.2 儀器與設備
紫外分光光度計:上海翱藝儀器有限公司;AR224CN電子天平:常州奧豪斯儀器有限公司;DKZ-1電熱恒溫水浴鍋:上海精密實驗設備有限公司;EU-K1-20TQ超純水器:南京歐鎧環境科技有限公司;TGC20M離心機:湖南湘立科學儀器有限公司;FW135型粉碎機:天津泰斯特儀器有限公司。
1.3 方法
1.3.1 復合酶法提取干巴菌多糖工藝
干巴菌原料進行干燥粉碎,精確稱取過80目篩的干巴菌粉5 g,按照試驗設計,加入一定料液比及復合酶量,于設定溫度的水浴鍋中,不停攪拌,酶解反應至設定時間,反應結束后,置于沸水浴中滅酶10 min,離心待用。采用苯酚硫酸法[10]測定多糖含量,計算提取率。
1.3.2 標準曲線的繪制[11]
稱取葡萄糖標準品200 mg,向其中加入蒸餾水使其溶解,定容至 100 mL。分別吸取標液 2、4、6、8、10 mL,分別定容至100 mL。再吸取2 mL溶液,然后加入5%苯酚溶液1 mL,迅速加入5 mL濃硫酸,振搖5 min,置沸水浴上加熱15 min,然后置冷水浴中冷卻30 min,以蒸餾水為空白作對照,在490 nm處用分光光度計測量吸光度,以葡萄糖濃度為橫坐標,吸光值為縱坐標,繪制標準曲線,得回歸方程:y=11.656x+0.025 8,R2=0.998 5。
1.3.3 干巴菌多糖提取率測定
精確吸取2 mL粗多糖溶液,然后加入5%苯酚溶液1 mL,迅速加入5 mL濃硫酸,振搖5 min,置沸水浴上加熱15 min,然后置冷水浴中冷卻30 min,以蒸餾水為空白作對照,在490 nm處用分光光度計測量吸光度。根據葡萄糖含量的標準曲線,由樣品溶液的吸光度計算粗多糖提取率。多糖提取率計算式如下:
多糖提取率/%=[(C×V×d)/m]×100
式中:C為測得的樣品溶液的葡萄糖質量濃度,mg/mL;V為樣品液體積,mL;d為稀釋倍數;m為樣品質量,mg。
1.3.4 單因素試驗設計
在復合酶法提取干巴菌多糖過程中,影響多糖提取率最重要的因素為酶解時間、料液比、復合酶濃度。為研究以上因素對多糖提取率的影響規律,試驗對反應條件進行了設置。單因素試驗中,考察酶解時間(40、50、60、70、80 min)、料液比[1∶10、1∶20、1∶30、1∶40、1∶50(mg/L)]復合酶選用(木瓜蛋白酶∶纖維素酶=2∶1)混合酶,考察酶加量(0.2%、0.3%、0.4%、0.5%、0.6%)對干巴菌多糖提取效果的影響。每組試驗重復3次,結果取平均值。
1.3.5 響應面優化最佳提取工藝
在單因素優化的基礎上,應用Box-Behnken試驗設計原理,選取復合酶酶解時間(A)、料液比(B)、復合酶濃度(C)3個對多糖提取率影響較顯著因素,采用三因素三水平的響應面分析法優化干巴菌多糖提取工藝。試驗因素與水平設計見表1。

表1 Box-Behnken試驗設計因素與水平Table 1 Design factors and levels of Box-Behnken experiment
1.4 數據處理
本試驗設計采用Design-Expert8.0統計分析軟件,圖形制作采用Excel數據處理軟件。
2 結果與分析
2.1 單因素試驗結果
2.1.1 酶解時間對干巴菌多糖提取率的影響
固定料液比1∶40(mg/L)、復合酶濃度0.5%、酶解溫度55℃,考察酶解時間對干巴菌多糖提取率的影響,結果見圖1。
由圖1可知,酶解時間在40 min~60 min范圍內,干巴菌多糖的提取率隨時間的延長而增加,在60 min時,多糖提取率達到最大,說明酶解時間在60 min時,酶與底物充分反應。因此,考慮到實際生產問題,選取60 min為最佳酶解時間。
2.1.2 料液比對干巴菌多糖提取率的影響
固定復合酶濃度0.5%、酶解溫度55℃,酶解時間60 min,考察料液比對干巴菌多糖提取率的影響,結果見圖2。
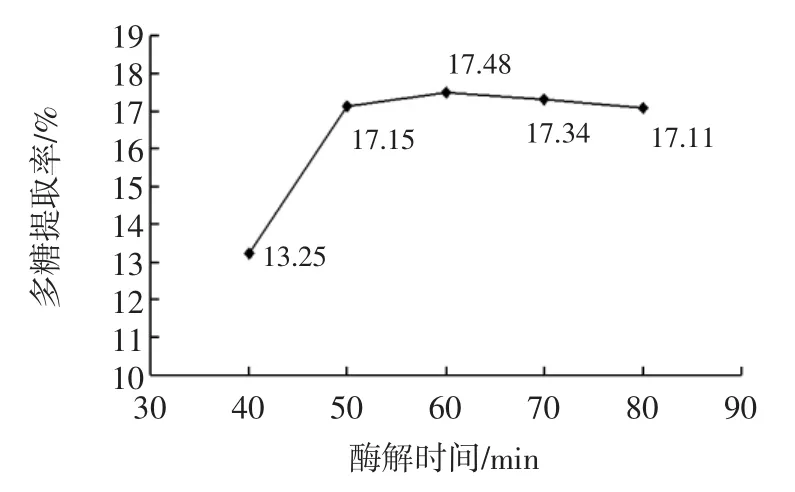
圖1 酶解時間對干巴菌多糖提取率的影響Fig.1 Effect of hydrolysis time on the yield of polysaccharides

圖2 料液比對干巴菌多糖提取率的影響Fig.2 Effect of marerial-liquid ratio on the yield of polysaccharides
由圖2可知,干巴菌多糖提取率在料液比為1∶10(mg/L)~1∶40(mg/L)時,提取率明顯增長,隨著液體量的增大,多糖提取率呈下降趨勢,說明在料液比為1∶40(mg/L)時,多糖已經充分溶解到溶液中,繼續增大料液比可能會導致溶劑量過大而使有效成分流失。因此,選定料液比為1∶40(mg/L)為最佳料液比。
2.1.3 復合酶濃度對干巴菌多糖提取率的影響
固定料液比 1∶40(mg/L)、酶解溫度 55℃、酶解時間60 min,考察復合酶濃度對干巴菌多糖提取率的影響,結果見圖3。
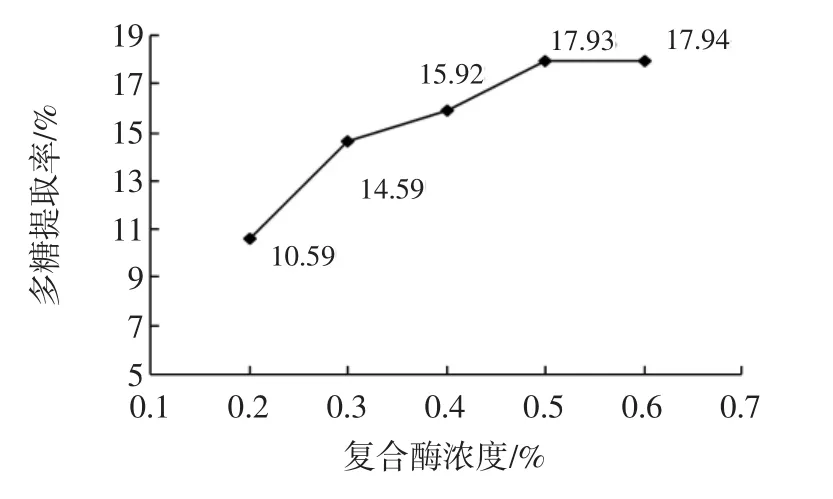
圖3 復合酶濃度對干巴菌多糖提取率的影響Fig.3 Effect of compound enzyme concentration on the yield of polysaccharides
在復合酶濃度為0.2%~0.5%的時候,多糖提取率隨酶濃度的增加而增長,在復合酶濃度達到0.5%以后,多糖提取率趨于平緩,這是由于,在一定酶解條件下,酶濃度不足時,酶濃度越大裂解細胞壁的效率越高,當酶濃度到飽和后,再增加酶濃度對結果的影響就變弱了[12],因此,選取復合酶濃度為0.5%為最佳復合酶濃度。
2.2 響應面優化干巴菌多糖提取工藝
2.2.1 響應面分析方案及結果
在單因素試驗的基礎上,選取酶解時間(A)、料液比(B)、復合酶濃度(C)作為試驗設計的3個自變量,通過響應面試驗設計建立干巴菌多糖提取率與自變量直接的函數關系,進而尋求復合酶法提取干巴菌多糖的最佳提取工藝。用Design-Expert8.0統計分析軟件對數據進行處理。試驗方案及結果見表2。

表2 設計方案與試驗結果Table 2 Experimental design and yield
2.2.2 回歸模型的方差分析
回歸模型的方差分析[13]見表3。

表3 模型的方差分析結果Table 3 Analysis results of analysis of variance of model
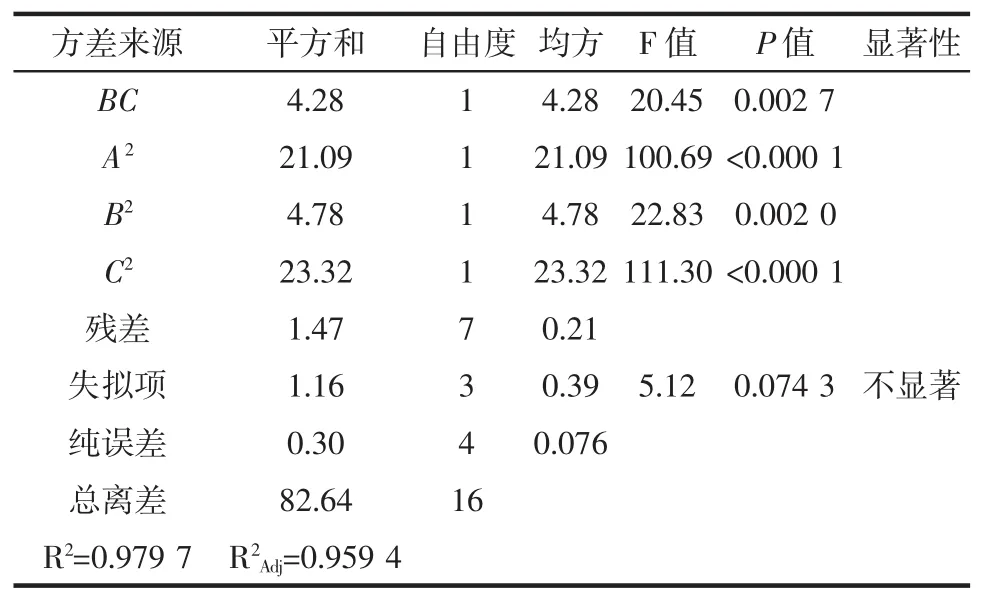
續表3 模型的方差分析結果Continue table 3 Analysis results of analysis of variance of model
由表3可知,模型對試驗擬合良好,模型的P值<0.000 1,表明該試驗模型極顯著。失擬項P=0.074 3>0.05,說明失擬項檢驗不顯著,該回歸模型的總決定系數R2=0.979 7,調整決定系數R2Adj=0.959 4,說明方程對試驗的擬合度較好,能夠較真實地反應試驗結果,可用此模型來分析和預測復合酶提取法提取干巴菌多糖的結果。對表3中數據進行回歸擬合,得到自變量與干巴菌多糖得率(Y)的二次多項回歸方程為:

2.2.3 響應面分析
響應面分析[13]見圖4。


圖4 兩兩因素交互作用對多糖提取率影響的響應面圖Fig.4 Response surface for the effects of processing parameters on the extraction rate of polysaccharides
對模型的方差分析表明,響應曲面越陡說明各因素之間兩兩交互作用越顯著,由圖4可以看出,C(復合酶濃度)與B(料液比)交互作用最為顯著;B(料液比)與A(酶解時間);A(酶解時間)與C(復合酶濃度)次之,此結果與回歸分析結果吻合。可知,復合酶濃度對干巴菌多糖提取率的影響最為顯著。
由圖4可知,復合酶濃度與料液比對干巴菌多糖的影響均成拋物線形,即隨著復合酶濃度與料液比同時增加,多糖提取率呈現先增大后降低趨勢,所以,應用到提取工藝中,可適當增加復合酶濃度與料液比,可以提高干巴菌多糖提取率。而料液比對多糖的提取率的影響大于酶解時間,因為當提取率達到平衡之前,原料與介質之間的濃度差影響表觀速率常數,料液比數值越大,更有利于表觀速率常數維持在較大水平[14],提高干巴菌多糖提取率。而適當延長酶解時間可以提高干巴菌多糖提取率,但是酶解時間過長,會造成提取物自身的水解,或者造成大量目標產物被吸附,從而導致干巴菌提取率下降。因此,在實際生產中,應控制酶解時間在最佳范圍內。
為檢驗響應面優化復合酶法提取干巴菌多糖工藝的可靠性,采用優化后的復合酶法提取工藝條件進行驗證試驗,采用優化后的工藝參數,即酶解時間64 min,料液比 1∶40(mg/L),復合酶濃度 0.47%,在此條件下,干巴菌多糖提取率為17.55%,而模型預測值為17.87%。二者接近,表明運用響應面法優化得到的模型參數準確可靠[15]。
3 結論
本研究采用復合酶法提取干巴菌多糖,該工藝通過酶能使細胞壁破碎的作用,使細胞內的多糖物質可以充分溶出,從而顯著提高了干巴菌多糖的提取工藝。
為進一步優化復合酶法提取干巴菌多糖工藝條件,本試驗考察了酶解時間、料液比、復合酶濃度3個因素對干巴菌多糖提取率的影響。在單因素試驗基礎上,采用響應面優化復合酶法提取干巴菌多糖,得到多項式回歸方程,直觀體現了各試驗因素與試驗結果的相關性,影響干巴菌多糖提取率的工藝因素中,復合酶濃度對干巴菌多糖提取率的影響最為顯著。最終確定復合酶法提取干巴菌多糖的最佳工藝為酶解時間 64 min,料液比 1∶40(mg/L),復合酶濃度 0.47%,在此條件下干巴菌多糖得率為17.87%。而實測值為17.55%,試驗結果為干巴菌多糖的提取以及多糖性質的研究提供了一定的試驗基礎,并能對工業化生產起到指導作用。
[1]Bertozzi CR,Kiessling LL.Chemical glycobiology[J].Science,2001,291(5512):2357-2364
[2]Whitmancm J,Bond Mr,Kohler JJ.Chemical glycobiology[J].Comprehensive Natural ProductsⅡ,2010,6(4):175-224
[3]黃年來.中國大型真菌原色圖鑒[M].北京:中國農業出版社,1998:216-217
[4]傅四清,魏蓉城.干巴菌研究進展[J].林業科技通訊,1997(8):21-23
[5]陸文娟,喻晨.響應面優化提取干巴菌多糖的工藝研究[J].南京師范大學學報,2015,15(3):84-92
[6]桂明英,劉蓓,朱萍,等.干巴菌生態學初步研究[J].西南農業學報[J].西南農業學報,2005,18(3):325-327
[7]YANG Bao,ZHAO Mouming,JOHN S,et al.Effect of ultrasonic treatment on the recovery and DPPH radical scavenging activity of polysaccharides from longan fruit percarp[J].Food Chemistry,2008,106(2):685-690
[8]李小平,陳錦平.油棗多糖的酶法提取及其對多糖分子量分布的影響[J].食品科學,2007,28(8):191-194
[9]ZHONG K,WANG Q.Optimization of ultrasonic extraction of polysaccharides from dried longan pulp using response surface methodology[J].Carbohydrate Polymers,2010,80(1):19-25
[10]張惟杰.糖復合物生化研究技術[M].杭州:浙江大學出版社,1999:455-456
[11]王心詩,邰麗梅,吳素蕊.響應面法優化水提野生銅色牛肝菌多糖工藝[J].中國食用菌,2015,34(1):60-64
[12]董麗輝,范三微,凌慶枝.酶法提取亮菌多糖的研究[J].中國釀造,2012,31(4):51-54
[13]費榮昌.試驗設計與數據處理(第四版)[M].無錫:江南大學出版社,2001:59-63
[14]王占一,張立華.復合酶法提取石榴籽多糖的工藝優化[J].食品科學,2016,37(18):19-25
[15]王根女,蘇平,黃愷婷,等.響應面法優化微波提取紫蘇葉多酚物質[J].中國食品學報,2009,9(5):87-92
Optimization of Compound Enzyme Extraction Technology of Polysaccharide of Thelephora ganbajun Zang via Response Surface Methodology
ZHANG Lan,HE Jin-song,WANG Xue-feng,LIAO Guo-zhou,PU Yue-hong,GE Chang-rong,FAN Jiang-ping*,GU Da-hai*
(College of Food Science and Technology,Yunnan Agricultural University,Kunming 650201,Yunnan,China)
2017-03-30
10.3969/j.issn.1005-6521.2017.20.010
云南省省院省校科技合作專項(2013IB010)
張嵐(1988—),女(漢),碩士,研究方向:食品工程。
*通信作者:范江平(1972—),男(漢),教授,博士,研究方向:食品科學;谷大海(1980—),男(漢),講師,碩士,研究方向:食品科學與工程。

