鈣離子感受蛋白STIM1與Orai1在鈣敏感受體介導鈣內流及NO生成中的相互作用*
王臘梅, 鐘 華, 唐 娜, 龐麗娟, 張春軍, 何 芳△
(石河子大學醫學院 1新疆地方病與民族高發病教育部重點實驗室, 2病理生理教研室, 3病理教研室, 新疆 石河子 832002)
鈣離子感受蛋白STIM1與Orai1在鈣敏感受體介導鈣內流及NO生成中的相互作用*
王臘梅1, 2, 鐘 華1, 2, 唐 娜1, 2, 龐麗娟1, 3, 張春軍1, 2, 何 芳1, 2△
(石河子大學醫學院1新疆地方病與民族高發病教育部重點實驗室,2病理生理教研室,3病理教研室, 新疆 石河子 832002)
目的研究Ca2+感受蛋白[基質相互作用分子1(STIM1)與鈣釋放激活鈣通道蛋白1(Orai1)]在人臍靜脈內皮細胞(HUVECs)鈣敏感受體(CaSR)介導的鈣內流和一氧化氮(NO)生成中的相互作用。方法將CaSR激動劑精胺[鈣池操縱性鈣通道(SOC)和受體操縱性鈣通道(ROC)均激活]單用或與ROC模擬劑12-O-十四烷酰佛波醇-13-醋酸酯(TPA)+CaSR負性變構調節劑Calhex 231(激活ROC、阻斷SOC)、蛋白激酶C(PKC)抑制劑Ro 31-8220和PKCα/β1選擇性抑制劑Go 6976(激活SOC、阻斷ROC)聯合孵育HUVECs;利用免疫熒光技術檢測HUVECs中STIM1和Orai1的蛋白表達和共定位;免疫共沉淀法檢測STIM1和Orai1之間的相互作用;取2~3代HUVECs隨機分為特異性的質粒轉染組(shSTIM1+shOrai1組)、空質粒組(vehicle-STIM1+vehicle-Orai1組)和未轉染組(control組),將3組細胞分別加入上述4組不同藥物刺激,采用熒光探針Fura-2/AM檢測HUVECs中Ca2+濃度的變化,NO熒光探針DAF-FM DA負載方法同步檢測HUVECs中NO生成的變化。結果STIM1和Orai1蛋白表達共定位于胞漿,與control組相比,加入Calhex 231+TPA、Ro 31-8220和Go 6976刺激后,STIM1和Orai1在胞漿中的定位均減少,且二者的相互作用均減弱;在4種不同處理因素作用下,shSTIM1+shOrai1組細胞內Ca2+濃度和NO凈熒光強度均明顯降低(P<0.05)。結論STIM1與Orai1以二元復合物的形式共同調節CaSR,并通過激活SOC和ROC介導鈣內流及NO生成。
基質相互作用分子1; 鈣釋放激活鈣通道蛋白1; 鈣敏感受體; 一氧化氮
鈣離子(calcium ion,Ca2+)是細胞內重要的信號分子,鈣庫的排空可以激活胞外Ca2+的內流,這種鈣內流的方式被稱作鈣池操縱性鈣內流(store-operated calcium entry,SOCE),在傳遞細胞信息方面非常重要。血管內皮細胞持續Ca2+內流可釋放舒張因子如一氧化氮(nitric oxide,NO)以維持血管內環境穩定。血管內皮功能障礙是多種心血管疾病的共同病理機制。在人臍靜脈內皮細胞(human umbilical vein endothelial cells,HUVECs)中,精胺(spermine)可通過激活鈣敏感受體(Ca2+-sensing receptor,CaSR)而引起細胞內鈣離子濃度(intracellular Ca2+concentration,[Ca2+]i)升高及NO的生成。
在生理條件下,鈣池操縱性鈣通道(store-operated calcium calcium channels,SOC)和受體操縱性鈣通道(receptor-operated channels,ROC)作為非興奮細胞介導的胞外Ca2+內流的主要途徑,兩者以協同的方式參與了CaSR激活,進而引發持續Ca2+內流和NO生成[1-2]。本課題組近期的研究逐步揭示了SOCE的分子機制,確定了瞬時受體電位通道1(transient receptor potential channel 1,TRPC1)、基質相互作用分子1(stromal interaction molecule 1,STIM1)和鈣釋放激活鈣通道蛋白1(calcium release-activated calcium channel protein 1,Orai1)均為參與CaSR經SOC和ROC介導的Ca2+內流和NO生成過程中的關鍵分子組件,以SOCE復合體的形式對疾病的發生發展產生作用[3]。亦有研究表明組成SOC亞基的Orai1、TRPC1和STIM1關鍵分子組件和相互作用模式在不同細胞類型有所不同。如在Jurkat細胞Orai1是構成SOC必需的分子組件,敲低TRPC1或TRPC3則不影響SOC和ROC。本研究擬在前期工作的基礎上,試圖闡明STIM1與Orai1在鈣敏感受體介導Ca2+內流和NO生成中的相互作用模式,有助于學者以介導鈣活動相關機制為靶點進行藥物篩選,并為心血管疾病防治提供新思路。
材 料 和 方 法
1實驗材料
健康孕婦剖宮產的新鮮臍帶來自華中科技大學同濟醫學院附屬同濟醫院婦產科(性別和體重不限),該實驗經倫理委員會批準和個人知情同意。
2主要試劑
內皮細胞培養基(Sciencell);蛋白酶抑制劑(Calbichem);G418(Biosharp);去內毒素高純度質粒抽提試劑盒(Omega);LipofectamineTM2000、Fura-2/AM與Opti-MEM(Invitrogen);shRNA(上海吉凱基因化學技術有限公司);BCA蛋白定量試劑盒和DAF-FM DA(NO熒光探針)(Beyotime);ECL發光試劑盒(ThermoBiosharp);鼠抗人STIM1單克隆抗體和鼠抗人Orai1多克隆抗體(Abcam);鼠抗β-actin單克隆抗體(Santa Cruze);II 抗(Protein Tech);其余均為國產分析純試劑。
3主要儀器
CX-102型超凈工作臺(安徽蚌埠凈化設備廠);二氧化碳培養箱(Thermo);Ca2+成像系統FV300、倒置熒光顯微鏡IX-70和激光共聚焦顯微鏡FV300(Olympus)。
4方法
4.1HUVECs的培養 依據參考文獻的方法[4-5]培養HUVECs,在無菌條件下取健康孕產婦剖宮產胎兒的新鮮臍帶。采用胰酶消化法用含10%胎牛血清的ECM培養基(添加100 mg/L青霉素和100 mg/L鏈霉素混合液)原代培養HUVECs,于37 ℃、5% CO2、飽和濕度的培養箱中培養,待細胞生長至90%融合時進行常規傳代。
重組質粒由實驗室前期構建,基因轉染步驟參照LipofectamineTM2000試劑盒說明書進行。結合文獻[6]的方法,取對數生長期的HUVECs接種于6孔板(取2個6孔板鋪板),待細胞融合至85%時,將STIM1 shRNA與Orai1 shRNA聯合轉染至HUVECs中。實驗中1~3孔為轉染STIM1 shRNA和Orai1 shRNA的HUVECs,即實驗組(shSTIM1+shOrai1組);4~6孔為空質粒組(vehicle-STIM1+vehicle-Orai1組);7~9孔為未做任何轉染處理的細胞,即空白對照組(control組)。分別在轉染后的24 h、48 h和72 h于熒光顯微鏡下觀察GFP熒光。同時采用G418進行逐步篩選獲得穩定克隆。
4.2免疫熒光技術檢測HUVECs中STIM1與Orai1的蛋白表達 取于玻片上生長24 h 的HUVECs,PBS溶液沖洗細胞,冰甲醇固定20 min后,0.5% Triton-PBS透化10~15 min,封閉后輕甩去封閉液,滴加相應 I 抗混合液,4 ℃孵育(選用濕盒保持玻片濕度)。次日洗片后滴加對應熒光標記的 II 抗混合液(1∶100稀釋),室溫避光孵育1 h。洗片,1 mg/L DAPI 室溫避光孵育15 min復染細胞核。洗片,滴加防淬滅劑后于熒光顯微鏡下觀察STIM1與Orai1的蛋白表達情況。陰性對照組以PBS代替相應 I 抗孵育,鏡下觀察并記錄結果。
4.3免疫共沉淀法檢測HUVECs中STIM1與Orai1的相互作用 (1)STIM1多克隆抗體沉淀(正向):將2~3代HUVECs接種于放有圓形玻片的培養皿中,待細胞達85%融合,與藥物孵育20 min,加入裂解液充分裂解后,12 000×g離心 3~5 min,取上清,加入 I 抗,4 ℃搖床過夜,按1∶10體積比加 50%的 Protein G Agarose,4 ℃ 搖床上混勻10 min后,1 000 r/min,4 ℃離心15 min,吸除上清液,不能吸掉的Protein G Agarose 用裂解液(500 μL)洗滌沉淀5次,洗滌時離心條件和吸除上清液要求同上。完成最后1次洗滌后去上清,加入SDS蛋白上樣緩沖液中,混勻煮沸5 min, 200×g離心 3 min ,取上清進行SDS-PAGE,用Orai1作為I抗(1∶1 000)進行Western blot分析。(2)Orai1單克隆抗體沉淀(反向):用STIM1作為I抗(1∶1 000)進行Western blot分析,方法同(1)。實驗中用非特異性鼠IgG代替 I 抗沉淀作為對照。
4.4HUVECs中Ca2+濃度的熒光測定 首先將聯合轉染的HUVECs接種于放有圓形玻片的小培養皿中,待細胞融合至85%以上后,分別加入CaSR激動劑精胺及ROC模擬劑(TPA)+CaSR負性變構調節劑Calhex 231、PKC抑制劑Ro 31-8220與PKCα/β1選擇性抑制劑Go 6976。聯合轉染48 h后將Fura-2/AM與含鈣液以1∶499的比例混合后加入,37 ℃孵育細胞后并去酯化處理[6]。激光共聚焦監測熒光的動態變化,分析得出兩激發光的熒光強度比值的變化 (即Δratio)以反映[Ca2+]i。
4.5HUVECs中NO濃度的熒光測定 HUVECs處理同4.4。聯合轉染48 h后按1∶2 000比例加入DAF-FM DA熒光探針稀釋液,37 ℃孵育細胞后室溫避光條件下,在細胞層面實時檢測刺激前后熒光的強弱[6],并通過Ingenuity Pathway Analysis軟件進行分析。
5統計學處理
所有數據采用SPSS 17.0統計軟件進行統計分析。實驗數據用均數±標準誤(mean±SEM)表示,多組間均數比較采用單因素方差分析(one-way ANOVA),各組均數間的兩兩比較采用SNK-q檢驗,以P<0.05為差異有統計學意義。
結 果
1免疫熒光技術觀察HUVECs中STIM1與Orai1的蛋白表達
在激光共聚焦顯微鏡下胞核的DNA染料(DAPI)陽性著色顯示為藍色熒光,STIM1的陽性著色為紅色熒光,Orai1的陽性著色為綠色熒光,橙黃色熒光則代表紅色和綠色熒光的疊加熒光。結果可見正常對照組HUVECs中STIM1和 Orai1蛋白的表達呈陽性,兩者共定位于胞漿,HUVECs分別經Calhex 231+TPA+精胺+Ca2+、Ro 31-8220+精胺+Ca2+和Go 6976+精胺+Ca2+刺激后鏡下的熒光示STIM1和Orai1在胞漿中的定位均減少,兩者的結合也明顯減少,見圖1。
2免疫共沉淀法檢測HUVECs中STIM1與Orai1的相互作用
各處理組正向STIM1/Orai1或反向Orai1/STIM1分別與靜息狀態下的正向STIM1/Orai1或反向Orai1/ STIM1的相對比值的百分數表示STIM1和Orai1相互作用的強弱。與control組和spermine+Ca2+組比較,Calhex 231+TPA+spermine+Ca2+組、Ro 31-8220+spermine+Ca2+組和Go 6976+spermine+Ca2+組中STIM1和Orai1的相互作用減弱(P<0.05),見圖2。
3不同處理因素對聯合轉染后HUVECs中[Ca2+]i和NO的生成的影響
3.1聯合轉染STIM1與Orai1使精胺誘導的HUVECs中[Ca2+]i和NO生成減少 采用脂質體法將shSTIM1與shOrai1同時轉染HUVECs,48 h后用G418進行穩篩,加入精胺處理細胞,與對照組(control組,即精胺+Ca2+組)及空質粒組(精胺+Ca2++vehicle-STIM1+vehicle-Orai1組)相比,實驗組(精胺+Ca2++shSTIM1+shOrai1組)的[Ca2+]iΔratio值和NO凈熒光強度值均明顯降低(P<0.05)。同時沉默STIM1與Orai1基因,能夠使CaSR經SOC和ROC介導的[Ca2+]i和NO生成減少,見圖3。
3.2聯合轉染STIM1與Orai1使TPA+Calhex231誘導的HUVECs中[Ca2+]i和NO生成減少 同3.1的方法加入TPA+Calhex231處理細胞,與對照組(Calhex 231+TPA+精胺+Ca2+組)及空質粒組(Calhex 231+TPA+精胺+Ca2++vehicle-STIM1+vehicle-Orai1組)相比,實驗組(Calhex 231+TPA+精胺+Ca2++shSTIM1+shOrai1組)中[Ca2+]iΔratio值和NO凈熒光強度值均明顯降低(P<0.05)。這說明同時沉默STIM1與Orai1基因能夠使CaSR經ROC介導的[Ca2+]i和NO生成減少,見圖4。
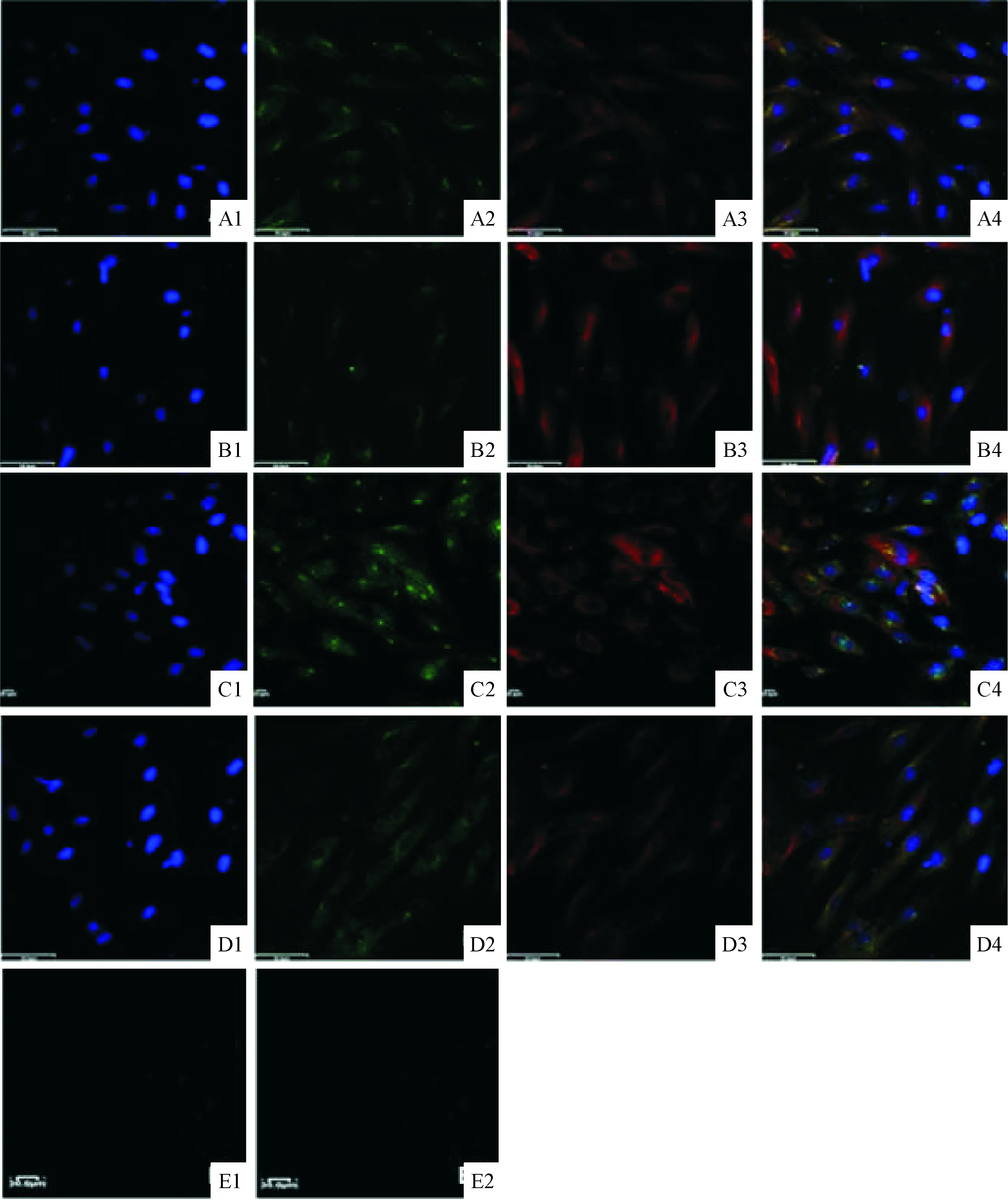
Figure 1. The protein expression of STIM1 and Orai1 in HUVECs were detected by immunocytochemical. A1~A4: protein expression and immunofluoresence of Orail1 and STIM1 for nuclear in HUVECs stimulated by spermine; B1~B4, C1~C4 and D1~D4: protein expression and immunofluoresence of Orail1 and STIM1 stimulated by Calhex 231+TPA+spermine, Ro 31-8220+spermine and Go 6976+spermine, respectively; E1: blank control group; E2: negative control group (×60).
圖1免疫熒光檢測HUVECs中STIM1與Orai1的蛋白表達
3.3聯合轉染STIM1與Orai1使Ro 31-8220介導的的HUVECs中[Ca2+]i和NO生成減少 同3.1的方法加入PKC抑制劑Ro 31-8220處理細胞,與對照組(Ro 31-8220+精胺+ Ca2+組)及空質粒組(Ro 31-8220+精胺+Ca2++vehicle-STIM1+vehicle-Orai1組)相比,實驗組(Ro 31-8220+精胺+Ca2++shSTIM1+shOrai1組)中[Ca2+]iΔratio值和NO凈熒光強度值均明顯降低(P<0.05)。這說明同時沉默STIM1與Orai1基因能夠使CaSR經SOC介導的[Ca2+]i和NO生成減少,見圖5。
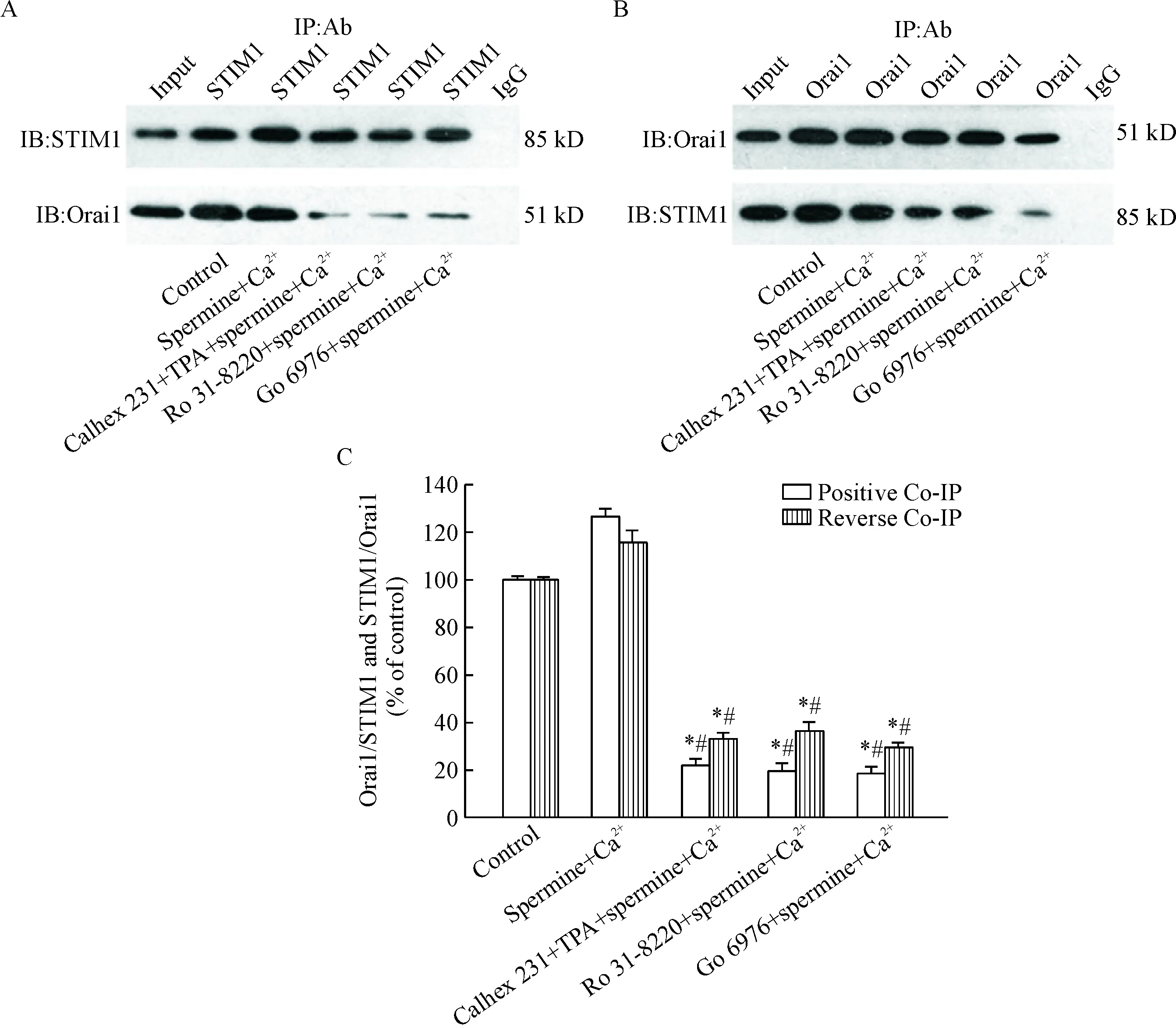
Figure 2. The interaction between STIM1 and Orai1 examined by co-immunoprecipitation (Co-IP). A: positive Co-IP, Orai1 as a resistance; B: reverse Co-IP, STIM1 as a resistance; C: semi-quantity analysis of the interaction. Mean±SEM.n=3.*P<0.05vscontrol group;#P<0.05vsspermine+Ca2+group.
圖2免疫共沉淀法檢測HUVECs中STIM1與Orai1的相互作用
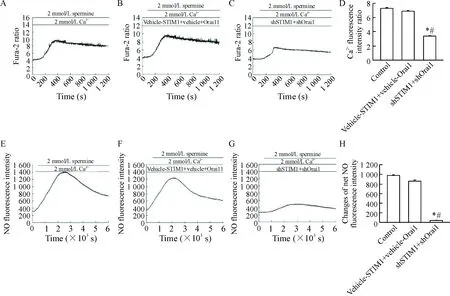
Figure 3. The dynamic changes of intracellular calcium fluorescence intensity ratio (A~D) and NO fluorescence intensity (E~H) after spermine treatment in shSTIM1 and shOrai1 double transfected HUVECs. A and E: control group; B and F: vehicle-STIM1+vehicle-Orai1 group; C and G: shSTIM1+shOrai1 group. Mean±SEM.n=3.*P<0.05vscontrol group;#P<0.05vsvehicle-STIM1+vehicle-Orai1 group.
圖3精胺刺激HUVECs后STIM1與Orai1聯合干擾組Ca2+和NO熒光強度的動態變化
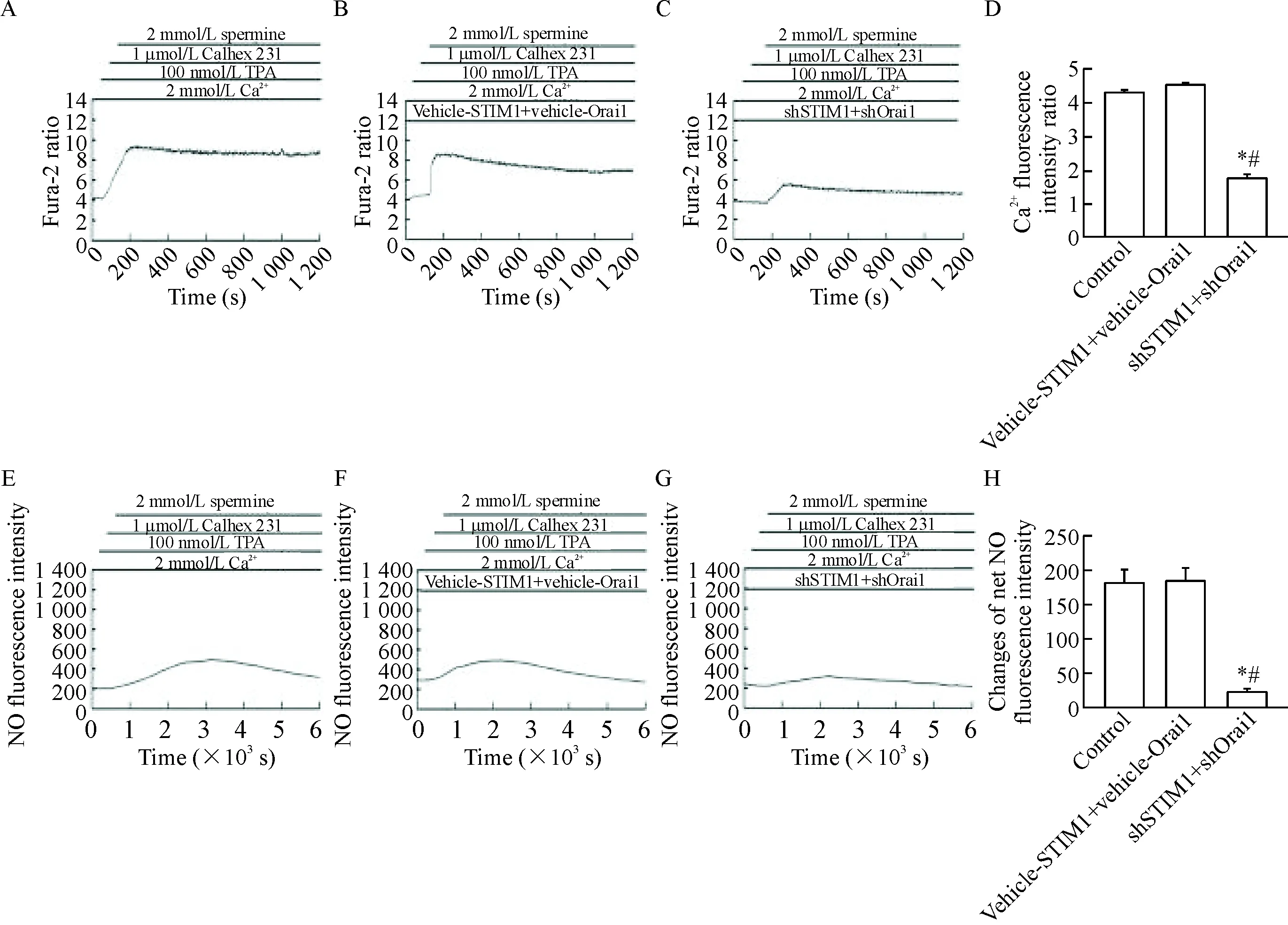
Figure 4. The dynamic changes of intracellular calcium fluorescence intensity ratio (A~D) and NO fluorescence intensity (E~H) after Calhex 231+TPA treatment in shSTIM1 and shOrai1 double transfected HUVECs. A and E: control group; B and F: vehicle-STIM1+vehicle-Orai1 group; C and G: shSTIM1+shOrai1 group. Mean±SEM.n=3.*P<0.05vscontrol group;#P<0.05vsvehicle-STIM1+vehicle-Orai1 group.
圖4TPA+Calhex231刺激HUVECs后STIM1與Orai1聯合轉染組Ca2+和NO熒光強度的動態變化
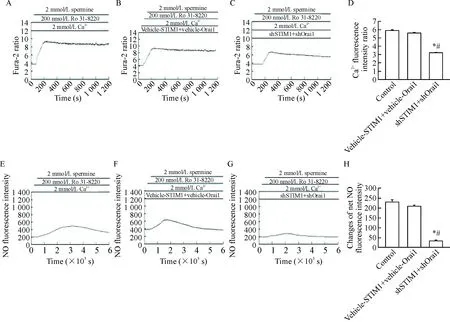
Figure 5. Dynamic changes of intracellular calcium fluorescence intensity ratio (A~D) and NO fluorescence intensity (E~H) after Ro 31-8220 treatment in shSTIM1 and shOrai1 double transfected HUVECs. A and E: control group; B and F: vehicle-STIM1+vehicle-Orai1 group; C and G: shSTIM1+shOrai1 group. Mean±SEM.n=3.*P<0.05vscontrol group;#P<0.05vsvehicle-STIM1+vehicle-Orai1 group.
圖5Ro31-8220刺激HUVECs后STIM1與Orai1聯合轉染組Ca2+和NO熒光強度的動態變化
3.4聯合轉染STIM1與Orai1使Go 6976作用的HUVECs中[Ca2+]i和NO生成減少 同3.1的方法加入PKCα/β1抑制劑Go 6976處理細胞,與對照組(Go 6976+精胺+ Ca2+組)及空質粒組(Go 6976+精胺+Ca2++vehicle-STIM1+vehicle-Orai1組)相比,實驗組(Go 6976+精胺+Ca2++shSTIM1+shOrai1組)中[Ca2+]iΔratio值和NO凈熒光強度值均明顯降低(P<0.05)。這說明同時沉默STIM1與Orai1基因,能夠使CaSR經SOC介導的[Ca2+]i和NO生成減少,見圖6。
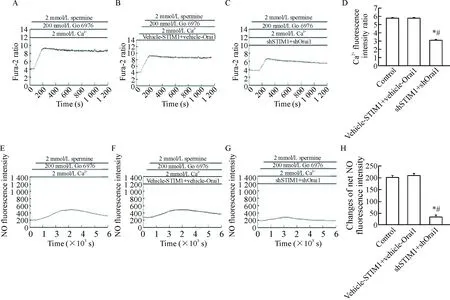
Figure 6. The dynamic changes of intracellular calcium fluorescence intensity ratio (A~D) and NO fluorescence intensity (E~H) after Go 6976 treatment in shSTIM1 and shOrai1 double transfected HUVECs. A and E: control group; B and F: vehicle-STIM1+vehicle-Orai1 group; C and G: shSTIM1+shOrai1 group. Mean±SEM.n=3.*P<0.05vscontrol group;#P<0.05vsvehicle-STIM1+vehicle-Orai1 group.
圖6Go6976刺激HUVECs后STIM1與Orai1聯合轉染中Ca2+和NO熒光強度的動態變化
討 論
心腦血管疾病現已成為危害人類健康和致死的主要因素,其發病率呈現逐年上升的趨勢。隨著人們對STIMs與Orais生物學作用及機制深入研究,發現其在心腦血管疾病的發生發展中發揮重要作用。如STIM1和Orai1作為SOCE的調節蛋白存在于多種細胞中[7],Voelkers等[8]首次證實STIM1和Orai1均表達于心肌細胞,并且是TG 耗竭Ca2+庫后引發SOCE所必須的蛋白質,STIM1基因沉默后,可降低舒張期[Ca2+]i及咖啡因誘發的肌漿網中Ca2+釋放。在內質網STIM1表達水平不變的情況下,當應用一些化學試劑使Orai1蛋白表達減少時,SOCE減弱且通過基因敲除技術分別敲除Orai1和STIM1基因,結果都會導致SOCE作用減弱,提示SOCE作用的減弱與Orai1和(或)STIM1蛋白表達水平降低有直接關系[9]。大量文獻證實在不同細胞由TRPCs、STIMs和Orais三者之間形成的二元或三元復合物調節SOC或ROC介導的生理和病理生理功能。如在HEK293細胞株STIM1與Orai1在內質網膜與細胞膜的結合處激活SOC[10],在腎小球膜細胞TRPC1和TRPC4共同組成SOC功能亞基,并通過STIM1/TRPC4相互作用介導SOC激活[11],在血小板TRPC6與Orai1和STIM1相互作用激活SOC[12]。在大鼠主動脈血管平滑肌細胞研究證實血小板衍生生長因子依賴Orai1/STIM1-SOC介導了平滑肌細胞增殖和遷移[13],STIM1/Orai1構成SOC過度激活參與了自發性高血壓腦卒中大鼠主動脈血管明顯的收縮[14]。TRPCs、肌漿/內質網鈣ATP酶(sarcoplasmic/endoplasmic reticulum Ca2+-ATPase,SERCA)和微管末端結合蛋白1(microtubule end-binding protein 1,EB1)等參與了SOC介導的SOCE,它們與STIMs和Orais構成SOCE復合體[3]。Jardin等[15]在人血小板發現Orai1在介導TRPC1-STIM1相互作用及TRPC1形成鈣通道的激活模式(依賴SOC或ROC)中發揮重要作用。
課題組前期實驗研究表明,在HUVECs中CaSR在介導Ca2+內流、eNOS活性和NO生成中起著重要作用[2]。Ziegelstein等[4]在人的主動脈血管內皮細胞中證實,在CaSR激動劑精胺的刺激下,通過三磷酸肌醇和ryanodine受體敏感的鈣池釋放,可引起[Ca2+]i增加和NO生成,結果提示在此過程中可能有外鈣內流的參與,且外鈣內流涉及的鈣通道相關蛋白STIM1、Orai1作為其關鍵分子組件參與了CaSR激活引發持續Ca2+內流和NO生成等相關心血管疾病的發生、發展。然而STIM1與Orai1二者之間相互作用模式以及功能尚未闡明,因此在這一領域的研究工作也顯得尤為重要。本實驗經免疫熒光技術、免疫共沉淀技術檢測發現在HUVECs中,STIM1與Orai1共定位于胞漿,經Calhex 231+ TPA +精胺+Ca2+、Ro 31-8220+精胺+Ca2+、Go 6976+精胺+Ca2+刺激后,鏡下熒光顯示STIM1與Orai1在胞漿中的定位均減少且相互作用減弱。為了闡明STIM1與Orai1在HUVECs中CaSR介導Ca2+內流及NO生成中的作用,實驗將特異性的STIM1 shRNA與Orai1 shRNA聯合轉染HUVECs,保證沉默基因有效抑制相關表達的同時,用精胺與HUVECs孵育激活SOC和ROC通路,發現在HUVECs中沉默STIM1與Orai1可抑制SOC和ROC通路介導的[Ca2+]i升高和NO生成。隨后分別用Calhex 231+TPA、Ro 31-8220和Go 6976處理細胞,在細胞外含Ca2+的情況下檢測HUVECs中[Ca2+]i與NO生成的變化。實驗結果表明Ca2+內流和NO的生成過程中有SOC和(或)ROC參與,且在HUVECs中同時沉默STIM1與Orai1后對[Ca2+]i和NO生成均有抑制作用。最終證明STIM1與Orai1以二元復合物的形式作為SOC和ROC關鍵組件調節了CaSR途徑介導的鈣內流和NO生成。
在血管系統中CaSR可通過增加[Ca2+]i調節NO的釋放和鉀通道激活,在調節血管張力及高血壓等心血管疾病的發生發展中起著重要的作用,而上述研究又為深入認識血管系統中STIM1和Orai1調節CaSR功能的生理和病生理作用和機制提供了重要理論基礎。未來的研究將更多闡明在心血管系統的不同細胞中STIM1和Orai1的功能、寡聚化模式及調節機制,了解不同細胞中SOC和ROC的結構與調節機制之間的細微差別,進而在分子水平實現對選擇性靶向作用治療臨床心血管疾病的防治提供一個新的途徑。
[1] 王振煥, 胡清華, 鐘 華, 等. 小凹蛋白-1在臍靜脈內皮細胞CaSR介導NO生成中的作用和機制[J]. 中國病理生理雜志, 2011, 27(5):934-938.
[2] 梁 霄, 羅小林, 鐘 華, 等.小干擾RNA沉默細胞外鈣敏感受體抑制人臍靜脈內皮細胞鈣內流和NO生成[J]. 生理學報, 2012, 64(3):289-295.
[3] 劉 青, 林默君.鈣池操縱性鈣通道的激活信號分子與肺動脈高壓[J]. 中國動脈硬化雜志, 2012, 20(3):273-277.
[4] Ziegelstein RC, Xiong Y, He C, et al. Expression of a functional extracellular calcium-sensing receptor in human aortic endothelial cells[J]. Biochem Biophys Res Commun, 2006, 342(1):153 -163.
[5] 陳玉龍, 賈 敏.香煙提取物對人臍靜脈內皮細胞蛋白亞硝基化的影響及機制[J]. 中國動脈硬化雜志, 2016, 24(9):889 -892+938.
[6] 王臘梅, 鐘 華, 趙 慧, 等.Orai3參與了HUVECs外鈣敏感受體介導的鈣內流和NO生成[J]. 中國病理生理雜志, 2014, 30(1):1-10.
[7] 趙 慧, 何 芳.血管疾病治療新靶標:STIM1和Orai1[J]. 中國病理生理雜志, 2013, 29(1):179-182+187.
[8] Voelkers M, Salz M, Herzog N, et al. Orai1 and Stim1 regulate normal and hypertrophic growth in CaSRdiomyocytes[J]. J Mol Cell CaSRdiol, 2010, 48(6):1329-1334.
[9] Galán C, Dionisio N, Smani T, et al. The cytoskeleton plays a modulatory role in the association between STIM1 and the Ca2+channel subunits Orai1 and TRPC1[J]. Biochen Pharmacol, 2011, 82(4):400-410.
[10] Park CY, Hoover PJ, Mullins FM, et al. STIM1 clusters and activates CRAC channels via direct binding of a cytosolic domain to Orai1[J]. Cell, 2009, 136(5):876-890.
[11] Sours-Brothers S, Ding M, Graham S, et al. Interaction between TRPC1/TRPC4 assembly and STIM1 contributes to store-operated Ca2+entry in mesangial cells[J]. Exp Biol Med, 2009, 234(6):673-682.
[12] Jardin I, Gómez LJ, Salido GM, et al. Dynamic interaction of hTRPC6 with the Orai1-STIM1 complex or hTRPC3 mediates its role in capacitative or non-capacitative Ca2+entry pathways[J]. Biochem J, 2009, 420(2):267-276.
[13] Hirano K, Hirano M, Hanada A. Involvement of STIM1 in the proteinase-activated receptor 1-mediated Ca2+influx in vascular endothelial cells[J]. J Cell Biochem, 2009, 108(2):499-507.
[14] Darbellay B, Arnaudeau S, Ceroni D, et al. Human muscle economy myoblast differentiation and excitation-contraction coupling use the same molecular partners, STIM1 and STIM2[J]. J Biol Chem, 2010, 285(29):22437-22447.
[15] Jardin I, Lopez JJ, Salido GM, et al. Orai1 mediates the interaction between STIM1 and hTRPC1 and regulates the mode of activation of hTRPC1-forming Ca2+channels[J]. J Biol Chem, 2008, 283(37):25296 -25304.
(責任編輯: 林白霜, 宋延君)
InteractionbetweenSTIM1andOrai1incalcium-sensingreceptor-mediatedcalciuminfluxandnitricoxidegeneration
WANG La-mei1, 2, ZHONG Hua1, 2, TANG Na1, 2, PANG Li-juan1, 3, ZHANG Chun-jun1, 2, HE Fang1, 2
(1KeyLaboratoryofXinjiangEndemicandEthnicDiseases,MinistryofEducation,2DepartmentofPathophysiology,3DepartmentofPhysiology,MedicalCollegeofShiheziUniversity,Shihezi832002,China.E-mail:fangf2002shz@126.com)
AIM: To investigate the interaction of Ca2+-sensing proteins, stromal interaction molecule 1 (STIM1) and calcium release-activated calcium channel protein 1 (Orai1), in Ca2+-sensing receptor (CaSR)-mediated extracellular Ca2+influx and production of nitric oxide (NO).METHODSHuman umbilical vein endothlial cells (HUVECs) were incubated with CaSR agonist spermine [activating store-operated calcium channels (SOC) and receptor-operated calcium channels (ROC)] alone or combined with CaSR negative allosteric modulator Calhex 231+ROC analogue TPA (activating ROC, blocking SOC), protein kinase C (PKC) inhibitor Ro 31-8220, or PKCα/β1 selective inhibitor Go 6976 (activate SOC, blocking ROC). The protein expression of STIM1 and Orai1 was determined by the method of immunofluorescence. The interaction between STIM1 and Orai1 was examined by co-immunoprecipitation. The second to third passages of HUVECs were divided into STIM1 and Orai1 short hairpin RNA group (shSTIM1+shOrai1 group), vehicle-STIM1+vehicle-Orai1 group and control group, and then incubated with the 4 different treatments above. The intracellular Ca2+concentration ([Ca2+]i) was detected using the fluorescent Ca2+indicator Fura-2/AM. The production of NO was also determined by DAF-FM DA fluorescent probe.RESULTSThe protein expression of STIM1 and Orai1 was located in the cytoplasm. Compared with control group, the localization of STIM1 and Orai1 in the cytoplasm was reduced after the HUVECs were incubated with Calhex 231+TPA, Ro 31-8220 or Go 6976, and the interaction of STIM1 and Orai1 was decreased significantly. The [Ca2+]iand the net NO fluorescence intensity in shSTIM1+shOrai1 group were significantly reduced after the 4 different treatments (P<0.05).CONCLUSIONSTIM1 and Orai1 are components of SOC and ROC in store- and receptor-operated Ca2+entry and NO generation.
Stromal interaction molecule 1; Calcium release-activated calcium channel protein 1; Ca2+-sen-sing receptor; Nitric oxide
R363; R541
A
10.3969/j.issn.1000- 4718.2017.10.007
1000- 4718(2017)10- 1773- 08
2017- 03- 20
2017- 07- 18
國家自然科學基金資助項目(No. 31160239;No. 81160018)
△通訊作者 Tel: 0993-2057166; E-mail: fangf2002shz@126.com
雜志網址: http://www.cjpp.net

