水飛薊素對大鼠腎臟缺血再灌注損傷的保護作用及機制探討
董建,楊潔,史國輝
(華北理工大學附屬醫院 腎內科,河北 唐山 063000)
水飛薊素對大鼠腎臟缺血再灌注損傷的保護作用及機制探討
董建,楊潔,史國輝
(華北理工大學附屬醫院 腎內科,河北 唐山 063000)
目的探索水飛薊素對大鼠腎臟缺血再灌注損傷(IRI)的保護作用及是否與抑制NF-κB活化有關。方法將30只成年雄性SD大鼠隨機為假手術組(S組)、缺血再灌注模型組(IR組)及藥物組(SM組)。全自動生化分析儀檢測血肌酐、血尿素氮,HE染色檢測腎小管損傷程度,免疫組織化學檢測腎臟IL-6及NF-κB p65表達,酶聯免疫吸附法測定腎組織勻漿上清液NF-κB、IL-6濃度。結果IR組血肌酐、尿素氮、組織勻漿細胞核內NF-κB及細胞漿中IL-6水平較S組升高(P<0.05),SM組較IR組降低(P<0.05),IR組腎小管損傷較重,腎臟IL-6、NF-κB p65表達增強。而給藥組腎小管損傷減輕,腎臟IL-6、NF-κB p65表達減弱。結論水飛薊素對大鼠腎臟缺血再灌注損傷具有保護作用,其與抑制NF-κB活化有關。
水飛薊素;大鼠;缺血再灌注損傷;NF-κB
急性腎損傷(acute kidney injury,AKI)的發病率及死亡率較高,全球每年超過1 300萬患者發病,每年大約可引起170萬人死亡[1-2]。腎缺血再灌注損傷(ischemia-reperfusion injury,IRI)是誘發急性腎損傷較為重要的原因,其在休克、腎移植[3-4]、腎動脈血管成形術及造影劑腎病等疾病中較為常見[5-8],并可導致內皮細胞激活及白細胞黏附,影響微血管血流動力學[9]。缺血誘導的炎癥應答常常會引起細胞損傷或壞死[10]。腎臟IRI預后常常較差,目前并未有效的治療方法。核因子 -κB(nuclear factor κB,NF-κB)是在轉錄過程中RNA聚合酶轉錄時所需要的一種輔助因子,由調節多種生物應答的轉錄因子家族構成[11]。NF-κB信號傳導通路的改變會引起多種炎癥性疾病的發生,其中就可出現在腎臟IRI疾病的炎癥反應中[12]。哺乳動物NF-κB家族由5個成員組成:p65(RelA)、c-Rel、RelB、p50/p105(NF-κB1)及 p52/p100(NF-κB2),其形成不同的異源二聚體或同源二聚體[13]。在正常生理狀態時,NF-κB與核轉錄因子κB抑制蛋白(inhibitory kappa B,ⅠκB)在胞質中結合,其活性被抑制,當有外界刺激如創傷、感染等時,ⅠκB會被ⅠκB酶復合物磷酸化而失去抑制作用,ⅠκB開始泛素化,隨后被特定蛋白酶降解,NF-κB變成游離狀態進入細胞核內[14],結合靶向基因的啟動子或增強子區域的特定序列,調節促炎基因等相關基因的轉錄,進而改變多種炎癥相關因子及酶類物質的表達,如白細胞介素6(interleukin-6,IL-6)。同時編碼ⅠκB蛋白使細胞恢復穩態[15]。
水飛薊素是從水飛薊種子中提取的黃酮類混合物,具有明顯的抗炎作用,可以抑制炎癥信號的表達和中性粒細胞的遷移,穩定肥大細胞。過去水飛薊素常常作為保肝藥物使用,近些年發現其對其他臟器同樣有一定的保護作用。TAN等發現水飛薊素可以降低腎IRI大鼠血清肌酐、尿素氮水平[16],但相關研究相對較少且其機制尚不明確。鑒于水飛薊素明顯的抗炎作用、本身無毒副作用和對多種器官的保護作用,其對大鼠腎臟IRI的保護作用及其是否與抑制NF-κB活化有關有待于進一步研究。
1 材料與方法
1.1 實驗動物
健康成年雄性SD大鼠,無特定病原體(SPF)級環境飼養,體重250~290 g[購自北京維通利華實驗動物技術有限公司,合格證號SCXK(京)2009-003],購自華北理工大學動物實驗中心動物房飼養7 d,以適應環境。12 h光照環境,12 h黑暗環境,可自由獲取食物和水。本實驗的動物處理方法經華北理工大學醫學倫理委員會商議后批準。
1.2 儀器與試劑
Olympus電動正置顯微鏡(日本奧林巴斯公司),酶標儀(美國BIO-RAD公司),全自動生化檢測儀(美國Benckman公司),水飛薊素膠囊(德國馬博士大藥廠,生產批號:B1403206),IL-6、NF-κB p65免疫組織化學(免疫組化)試劑盒(購自北京博奧森生物技術有限公司),NF-κB及IL-6酶聯免疫吸附測定(ELISA)試劑盒(購自上海酶聯生物科技有限公司)。
1.3 方法
選用隨機數字法將30只雄性大鼠分為3組,分別為假手術組(S組)、缺血再灌注模型組(IR組)及藥物組(SM組)。各組處理情況:S組及IR組術前給予生理鹽水灌胃7 d,SM組術前給予水飛薊素100 mg/(kg·d)灌胃7 d。術前12 h給予禁食水,腹腔緩慢注射10%水合氯醛(300 mg/kg)麻醉大鼠后,仰臥位固定。劍突下至恥骨聯合上備皮并用安爾碘消毒3次,充分暴露手術區域,手術器械于高壓蒸汽滅菌器內120℃,40 min滅菌。術中使用生理鹽水浸濕紗布保護腹腔臟器,同時注意保暖。手術切口3~4 cm,腹中線逐層切開皮膚、皮下組織、肌肉及腹膜,逐層打開腹腔。IR組、SM組結扎右側輸尿管及右側腎動靜脈,摘取右側腎臟,無創動脈夾阻斷左側腎臟血液供應,夾閉左側腎動靜脈40 min,再灌注24 h后,給予10%水合氯醛腹腔注射再次麻醉大鼠,逐層打開腹腔,留取血液樣品及腎組織。S組不給予缺血再灌注處理,其余步驟與其他組相同。取出各組左側腎臟后分別沿冠狀面和矢狀面切成4分,一部分立即放入4%多聚甲醛中固定12~24 h,包埋制成蠟塊,放于4℃冰箱冷凍中保存。一部分腎臟迅速放入-180℃液氮罐中速凍,后保存在-80℃低溫冰箱中,用于組織勻漿的制備,組織勻漿上清液保存于-20℃。用含有促凝集的真空管抽取下腔靜脈血3.5 ml,放入4℃冰箱中。應用Benckman全自動生化檢測儀測量血清肌酐及尿素氮濃度;HE染色后,在Olympus電動正置顯微鏡下觀察腎病組織病理學改變;免疫組織化學染色檢測NF-κB p65在細胞核中的表達及IL-6在細胞漿中的表達;ELISA檢測腎組織勻漿細胞核NF-κB及細胞漿IL-6濃度。
1.4 統計學方法
數據分析采用SPSS 17.0統計軟件,計量資料以均數±標準差(±s)表示,采用方差分析,兩兩比較用LSD-t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 腎功能檢測結果
各組大鼠腎臟缺血再灌注40 min后,各組大鼠血肌酐濃度變化差異有統計學意義(F=198.993,P=0.000),兩兩比較經LSD-t檢驗,IR組血肌酐濃度高于S組(t=19.938,P=0.000),但SM組血肌酐濃度較IR 組低(t=9.377,P=0.000),但高于 S組(t=10.561,P=0.000)。各組大鼠血尿素氮濃度變化差異有統計學意義(F=450.588,P=0.000),IR 組血尿素氮濃度高于 S組(t=30.472,P=0.000),但 SM 組血尿素氮濃度較IR組低(t=20.183,P=0.000)。見表1。
2.2 腎臟病理結果
S組腎小球、腎小管清晰可見,結構完整,無異常改變。IR組鏡下可見腎組織皮髓質交界區大量腎小管腫脹、壞死,刷狀緣脫落,部分腎小管阻塞,腎間質有大量中性粒細胞浸潤。SM組腎小管腫脹較輕,無壞死及未見腎基膜破裂及刷狀緣脫落,腎間質僅有少量中性粒細胞浸潤。見圖1。
2.3 免疫組織化學觀察結果
IR組腎組織中包漿IL-6、胞核NF-κB p65表達水平高于S組,SM組包漿IL-6、胞核NF-κB p65表達較IR組降低,但仍高于S組。見圖2、3。
表1 各組大鼠血肌酐及血尿素氮濃度比較 (n=10,±s)

表1 各組大鼠血肌酐及血尿素氮濃度比較 (n=10,±s)
注:1)與 S組比較,P <0.05;2)與 IR 組比較,P<0.05
組別血肌酐/(μmol/L)血尿素氮/(mmol/L)S 組(n=10) 46.67±5.20 6.02±0.42 IR 組(n=10) 151.51±15.521) 27.59±2.511)SM 組(n=10) 102.21±12.121) 13.31±1.011)2)F值 198.993 450.588 P值 0.000 0.000
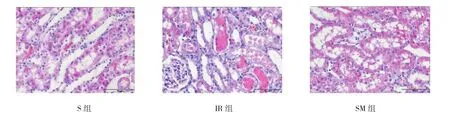
圖1 各組大鼠腎小管染色結果比較 (HE×400)
2.4 ELISA檢測結果
各組大鼠細胞核NF-κB濃度變化差異有統計學意義(F=95.892,P=0.000),IR 組細胞核 NF-κB濃度高于 S組(t=13.694,P=0.000),但SM組NF-κB濃度較IR組低(t=8.639,P=0.000),但高于S組(t=5.055,P=0.000)。各組大鼠細胞質IL-6濃度變化差異有統計學意義(F=1618.489,P=0.000),IR 組細胞質IL-6濃度高于 S組(t=56.892,P=0.000),SM組 IL-6濃度高于 S組(t=28.022,P=0.000),SM 組IL-6濃度較IR組低(t=28.870,P=0.000)。見表2。
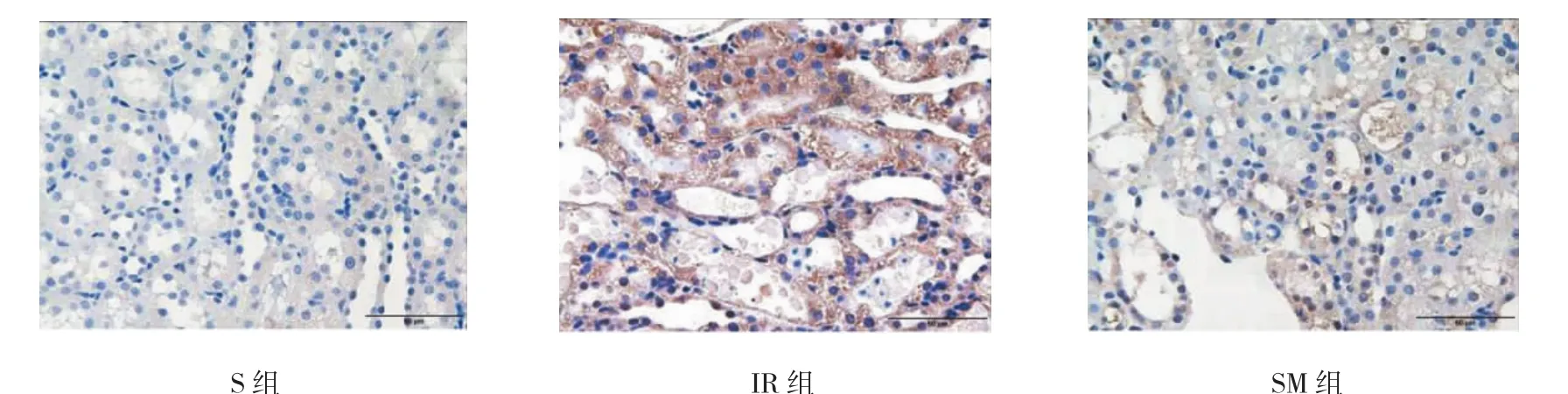
圖2 各組大鼠IL-6的表達 (免疫組織化學×400)
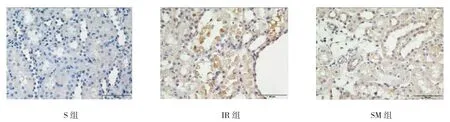
圖3 各組大鼠NF-κB p65的表達 (免疫組織化學×400)
表2 各組大鼠腎臟細胞核NF-κB及細胞漿IL-6濃度比較 (n=10,ng/g,±s)
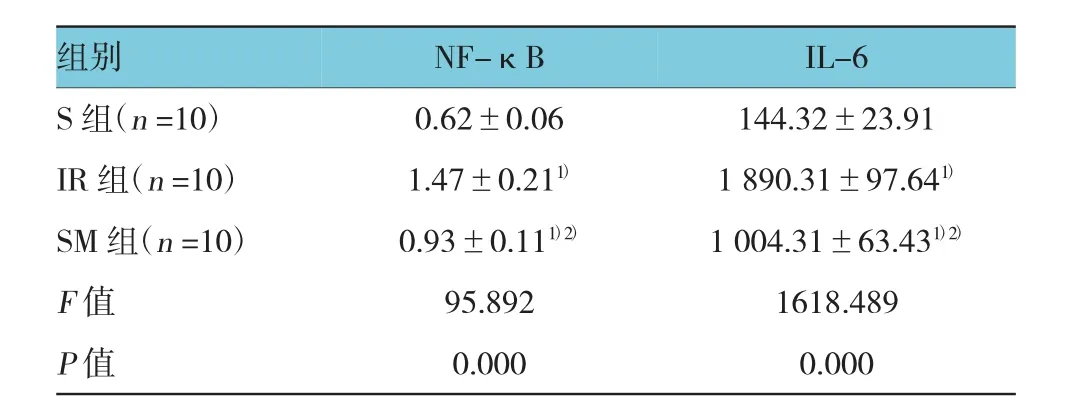
表2 各組大鼠腎臟細胞核NF-κB及細胞漿IL-6濃度比較 (n=10,ng/g,±s)
注:1)與 S組比較,P <0.05;2)與 IR 組比較,P <0.05
組別 NF-κB IL-6 S 組(n=10) 0.62±0.06 144.32±23.91 IR 組(n=10) 1.47±0.211) 1 890.31±97.641)SM 組(n=10) 0.93±0.111)2) 1 004.31±63.431)2)F值 95.892 1618.489 P值 0.000 0.000
3 討論
在正常腎臟組織中,炎癥因子水平較低,但在病理狀態下易急劇升高,腎小球濾過率快速下降與腎小管、腎小球的變化伴隨間質性炎癥有關[17],IRI可以通過誘發內皮細胞功能紊亂、刺激白細胞介導炎癥反應、降低微小血管的血流量引起急性腎損傷[18]。建立缺血再灌注損傷模型很多,該損傷均與炎癥反應有較為密切的關系。炎癥是導致腎臟IRI的主要因素[19],大量的炎癥介質與腎臟IRI有關,如IL-6可以激活中性粒細胞、淋巴細胞及單核巨噬細胞等向損傷部位聚集,發生炎癥反應損傷腎組織。在缺血再灌注損傷后,TNF-α抑制劑減輕炎癥改變[20]。在HgCl2介導的大鼠急性腎損傷模型中,腎臟IL-19的表達水平較高[21]。在遭受IRI的細胞懸液中,模型組中的TNF-α、IL-6和單核細胞趨化蛋白 -1(monocyte chemotactic protein 1,MCP-1)濃度高于對照組[22]。在本實驗中,IR組腎組織中IL-6的表達升高,而在SM組IL-6表達降低。
一直以來,NF-κB通路被認為是典型的促炎信號通路,很大程度上被細胞因子、趨化因子及黏附分子等促炎基因的表達影響[23],NF-κB可以被多種致病因素活化,有文獻報道,NF-κB在缺血時活化,再灌注12 h開始升高,2~3 d達到頂峰[24]。預先給予大鼠NF-κB抑制劑不僅抑制由IR引起的NF-κB的活化,且阻止MCP-1 mRNA的表達,表明NF-κ B在IRI炎癥的開始占有重要角色[25]。轉錄因子p65是NF-κB家族中的一員,可以調節大多數NF-κB靶基因[26],p65基因敲除大鼠只會有較弱的外周炎癥反應[27]。本研究結果顯示,術前給予大鼠水飛薊素灌胃7 d,與IR組相比,SM組降低血清肌酐、血清尿素氮及中性粒細胞的浸潤,改善了腎功能,減輕腎小管損傷,免疫組織化學檢測細胞核NF-κBp65及細胞漿IL-6表達水平較IR降低,ELISA檢測腎組織勻漿細胞核NF-κB及細胞漿IL-6濃度SM組偏低,表明水飛薊素可以改善腎功能,抑制NF-κB的活化,進而降低IL-6的表達。
綜上所述,目前研究可以證實水飛薊素對大鼠腎臟缺血再灌注損傷具有保護作用其可能與抑制NF-κB活化有關。臨床腎缺血再灌注損傷患者病情較為復雜,常常合并多種疾病,且目前并未明確有效保護腎臟IRI的藥物應用于臨床,而本實驗發現水飛薊素可以改善大鼠腎功能、減輕腎臟損傷,其與抑制NF-κB的活化有關,此外水飛薊素還對心臟、腦、胃及腸IRI有保護作用,更適合臨床應用。但水飛薊素是否可以通過影響ⅠκB的活性抑制NF-κB活化還需進一步研究。
[1]MEHTA R L,CERD?J,BURDMANN E A,et al.International society of nephrology's 0by25 initiative for acute kidney injury(zero preventable deaths by 2025):a human rightscasefor nephrology[J].Lancet,2015,385(9987):2616-2643.
[2]BELLOMO R,KELLUM J A,RONCO C.Acute kidney injury[J].Lancet,2012,380(9843):756-766.
[3]JANG H R,KO G J,WASOWSKA B A,et al.The interaction between ischemia-reperfusion and immune responses in the kidney[J].J Mol Med(Berl),2009,87(9):859-864.
[4]SEMENTILLI A,FRANCO M.Renal acute cellular rejection:correlation between the immunophenotype and cytokine expression of the inflammatory cells in acute glomerulitis,arterial intimitis,and tubulointerstitial nephritis[J].Transplant Proc,2010,42(5):1671-1676.
[5]FRIEDERICKSEN D V,van DER MERWE L,HATTINGH T L,et al.Acute renal failure in the medical ICU still predictive of high mortality[J].S Afr Med J,2009,99(12):873-875.
[6]MANSANO A M,VIANNA P T,FABRIS V E,et al.Prevention of renal ischemia/reperfusion injury in rats using acetylcysteine after anesthesia with isoflurane[J].Acta Cir Bras,2012,27(4):340-345.
[7]MORGAN C J,GILL P J,LAM S,et al.Peri-operative interventions,but not inflammatory mediators,increase risk of acute kidney injury after cardiac surgery:a prospective cohort study[J].Intensive Care Med,2013,39(5):934-941.
[8]SHIMIZU S,SAITO M,KINOSHITA Y,et al.Nicorandil ameliorates ischaemia-reperfusion injury in the rat kidney[J].Br J Pharmacol,2011,163(2):272-282.
[9]BONVENTRE J V,ZUK A.Ischemic acute renal failure:an inflammatory disease[J].Kidney Int,2004,66(2):480-485.
[10]GLODOWSKI S D,WAGENER G.New insights into the mechanisms of acute kidney injury in the intensive care unit[J].J Clin Anesth,2015,27(2):175-180.
[11]YAN R,LI Y,ZHANG L,et al.Augmenter of liver regeneration attenuates inflammation of renal ischemia/reperfusion injury through the NF-kappa B pathway in rats[J].Int Urol Nephro,2015,47(5):861-868.
[12]FRANTZ S,TILLMANNS J,KUHLENCORDT P J,et al.Tissue-specific effects of the nuclear factor kappa B subunit p50 on myocardialischemia-reperfusion injury[J].Am J Pathol,2007,171(2):507-512.
[13]GHOSH S,HAYDEN M S.Celebrating 25 years of NF-κB research[J].Immunol Rev,2012,246(1):5-13.
[14]HINZ M,ARSLAN S ?,SCHEIDEREIT C.It takes two to tango:IκBs,the multifunctional partners of NF-κB[J].Immunol Rev,2012,246(1):59-76.
[15]NATOLI G.NF-κB and chromatin:ten years on the path from basic mechanisms to candidate drugs[J].Immunol Rev,2012,246(1):183-192.
[16]TAN J,HU J,HE Y,et al.Protective role of silymarin in a mouse modelofrenalischemia-reperfusion injury[J].Diagn Pathol,2015,10(1):198.
[17]LAMEIRE N H,BAGGA A,CRUZ D,et al.Acute kidney injury:an increasing global concern[J].Lancet,2013,382(9887):170-179.
[18]MUNSHI R,HSU C,HIMMELFARB J.Advances in understanding ischemic acute kidney injury[J].BMC Med,2011,9(1):11.
[19]BONVENTRE J V,WEINBERG J M.Recent advances in the pathophysiology of ischemic acute renal failure[J].J Am Soc Nephrol,2003,14(8):2199-2200.
[20]GERLACH U A,ATANASOV G,WALLENTA L,et al.Shortterm TNF-alpha inhibition reduces short-term and long-term inflammatory changes post-ischemia/reperfusion in rat intestinal transplantation[J].Transplantation,2014,97(7):732-739.
[21]HSU Y H,LI H H,SUNG J M,et al.Interleukin-19 mediates tissue damage in murine ischemic acute kidney injury[J].PLoS One,2013,8(2):e56028.
[22]DONG X,SWAMINATHAN S,BACHMAN L A,et al.Resident dendritic cells are the predominant TNF-secreting cell in early renal ischemia-reperfusion injury[J].Kidney Int,2007,71(7):619-628.
[23]LAWRENCE T.The nuclear factor NF-kappa B pathway in inflammation[J].Cold Spring Harb Perspect Biol,2009,1(6):a001651.
[24]MARKó L,VIGOLO E,HINZE C.Tubular epithelial NF-κB activity regulates ischemic AKI[J].J Am Soc Nephrol,2016,27(9):2658-2669.
[25]SUNG F L,ZHU T Y,AU-YEUNG K K,et al.Enhanced MCP-1 expression during ischemia/reperfusion injury is mediated by oxidative stress and NF-kappa B[J].Kidney Int,2002,62(4):1160-1170.
[26]GASPARINI C,FELDMANN M.NF-κB as a target for modulating inflammatory responses[J].Curr Pharm Des,2012,18(35):5735-5745.
[27]LUO J G,ZHAO X L,XU W C,et al.Activation of spinal NF-κB/p65 contributes to peripheral inflammation and hyperalgesia in rat adjuvant-induced arthritis[J].Arthritis Rheumatol,2014,66(4):896-906.
Protective effect of Silymarin on renal ischemia-reperfusion injury in rats
Jian Dong,Jie Yang,Guo-hui Shi
(Department of Nephrology,North China University of Science and Technology Affiliated Hospital,Tangshan,Hebei 063000,China)
ObjectiveTo investigate the protective effect of Silymarin on renal ischemia-reperfusion injury(IRI)and its underlying inhibiting mechanism towards nuclear factor κB(NF-κB).MethodsA total of 30 male sprague-dawley(SD)rats were randomly divided into three groups:sham operation(S)group,IRI (IR)group and IRI plus Silymarin(SM)group.Serum creatinine(Cr)and blood urea nitrogen(BUN)were analyzed with automatic biochemical analyzer.Hematoxylin-eosin (HE)staining was performed for histological grading of kidney injury.Expression of interleukin 6 (IL-6)and NF-κB p65 was identified by Immunohistochemical staining and Enzyme-linked immunosorbent assay (ELISA).ResultsCirculating Cr,BUN,NF-κB and IL-6 were elevated significantly in the IR group compared with those in the S group (P<0.05),and those in the SM group (P<0.05).Animals in the IR group experienced obvious increase of renal tubular damage and expression of IL-6 and NF-κB,which were ameliorated with treatment of Silymarin.ConclusionsInactivation of NF-κB signaling pathway mediates protective effect of Silymarin on renal ischemia-reperfusion.
Silymarin;rat;ischemia-reperfusion injury;NF-κB
R692
A
10.3969/j.issn.1005-8982.2017.24.004
1005-8982(2017)24-0017-05
2017-03-07
史國輝,E-mail:saint40@sina.com
(王榮兵 編輯)

