脂多糖介導的TLR4信號通路在膀胱癌免疫逃逸中的作用及其機制
吳高亮 周偉敏 齊雪亮 胡 涌 黃 驥 郝 超
(江西省腫瘤醫院泌尿外科,江西 南昌 330029)
脂多糖介導的TLR4信號通路在膀胱癌免疫逃逸中的作用及其機制
吳高亮 周偉敏 齊雪亮 胡 涌 黃 驥 郝 超
(江西省腫瘤醫院泌尿外科,江西 南昌 330029)
目的探討脂多糖介導的Toll樣受體(TLR)4信號通路活化在膀胱癌(BC)T24細胞系免疫逃逸中的作用及其機制。方法取對數生長期T24細胞,使用1 μg/ml的脂多糖分別刺激該細胞0、6、12、24 h,采用流式細胞儀檢測細胞表面TLR4的表達量,采用RT-PCR檢測細胞中程序性死亡配體-1(PD-1,又稱B7-H1)mRNA的表達,采用酶聯免疫吸附法(ELISA)檢測細胞中B7-H1 蛋白的表達,分析TLR4表達與B7-H1 mRNA及其蛋白的相關性。結果TLR4陽性率隨刺激時間的增長而上調,且在12 h時達到最高值,24 h時表達略有降低,但仍較高。6、12、24 h時TLR4陽性率與0 h時比較差異有統計學意義(Plt;0.05)。RT-PCR及ELISA結果顯示B7-H1 mRNA及蛋白的表達隨刺激時間的增長而上調,且在12 h時達到最高值,24 h時表達略有降低,但仍較高。與0 h時比較,6 h和24 h T24細胞B7-H1 mRNA及蛋白表達量增高(Plt;0.05),12 h 顯著增高(Plt;0.01)。TLR4與B7-H1 mRNA呈正相關(r=0.785,P=0.002),TLR4與B7-H1 蛋白呈正相關(r=0.825,P=0.012)。結論脂多糖能活化TLR4信號通路,并上調B7-H1 mRNA及其蛋白的表達,可能參與BC細胞免疫逃逸,為BC的靶向治療提供新思路。
Toll樣受體4;程序性死亡配體-1;蛋白表達;膀胱癌;免疫逃逸
膀胱癌(BC)是發病率最高的泌尿系統惡性腫瘤,可分為表淺性BC(Ta~1及原位癌Tis)和浸潤性BC(T2~4)兩大類,其中浸潤性BC占總體的80%,具有易發生轉移、預后較差、術后生存率較低等特點〔1〕初次治愈后復發率高達70%~80%。Toll樣受體(TLR)4是一種免疫調節因子,參與機體免疫應答的起始階段,正常情況下僅表達于機體免疫細胞表面,病理狀態下表達于多種惡性腫瘤細胞表面〔2〕。程序性死亡配體(PD)-1又稱B7-H1,可以通過與受體PD-1的結合對某些細胞因子的分泌和T細胞的增殖產生抑制作用,或與腫瘤細胞的免疫逃逸密切相關〔3〕。目前,關于TLR4信號通路和B7-H1在肺癌、套細胞淋巴癌細胞等中的免疫逃逸過程已有報道〔4,5〕,但是在BC細胞中的免疫逃逸機制鮮見報道。本文利用脂多糖介導的TLR4信號通路活化,研究TLR4信號通路和B7-H1在BC免疫逃逸中的作用及其機制。
1 材料與方法
1.1實驗材料
1.1.1細胞及試劑 人BC細胞系T24細胞(中國科學院典型培養物保藏委員會細胞庫),青霉素、鏈霉素(Sigma公司),胎牛血清、胰蛋白酶、培養液 RPMI1640培養基(HyClone 公司),Trizol reagent(Invitrogen公司),鼠抗人TLR4單克隆抗體(Biolegend公司),RT-PCR試劑盒(LifeInvitrogen公司),PCR引物由LifeInvitrogen公司合成。PierceTM BCA Protein Assay Kit(Thermo公司),B7-H1 ELISA kit(LifeInvitrogen)。
1.1.2實驗儀器 流式細胞儀(BD Biosciences),Real-Time PCR System(model 7500,Applied Biosystems,Carlsbad,CA,USA),PCR System 9700(GeneAmp),酶標儀(BIO-RAD Model680,Japan),低溫高速離心機(Centrifuge 5810 R,eppendorf)。
1.2實驗方法
1.2.1細胞培養 使用RPMI1640培養基(含10%胎牛血清、濃度為100 U/ml青霉素和100 μg/ml硫酸鏈霉素),在溫度37℃,體積分數為5%的CO2飽和濕度的恒溫培養箱中對BC T24細胞進行常規培養,每2 d按照1∶2或1∶3的比例傳代。
1.2.2TLR4信號通路活化 取對數生長期T24細胞,0.25%胰酶消化完全后,加入適當的完全培養基終止消化,1 500 r/min離心3 min,棄去上清后,以新鮮完全培養液重新懸浮,細胞計數儀計數,將細胞懸浮液稀釋至1.5×105cells/ml,以2 ml/孔接種于6孔培養板中,24 h后加入含有1 μg/ml的脂多糖,繼續孵育0、6、12和24 h。
1.2.3流式細胞儀檢測TLR4表達 按時間點收集細胞,0.25%胰蛋白酶消化后,加入適當的完全培養基終止消化,1 500 r/min離心3 min,棄去上清,冰磷酸鹽緩沖液(PBS)洗滌,重復3次,加入PE標記的鼠抗人TLR4單克隆抗體,在4℃的溫度下避光孵育30 min,孵育完畢后,冰PBS洗滌3次,將細胞團塊完全懸浮于冰PBS中,加入200 μl 4%多聚甲醛固定細胞,采用流式細胞儀檢測TLR4表達。
1.2.4RT-PCR測定B7-H1 mRNA表達 按時間點取脂多糖孵育結束的6孔板,棄去上清,加入1 ml/孔的Trizol裂解液,裂解細胞,按照相分離-沉淀RNA-洗滌RNA-RNA再溶解的步驟,提取各組T24細胞中總RNA。測量各組總RNA濃度,分別取等量的總RNA逆轉錄合成cDNA。測量逆轉錄后的各組cDNA濃度,分別取等量的cDNA進行RT-PCR,設定條件:50℃ 2 min,95℃ 10 min。40個循環:95℃ 15 s,60℃ 1 min。B7-H1上游引物序列:5′-GCCGATACAAGCGAATTA-3′,下游引物序列:5′-TCTCAGTGTGCTGGTCTGGTCACAT-3′,以甘油醛-3-磷酸脫氫酶(GAPDH)為內參,上游引物序列:5′-TCATGGGTGTGAACCATGAGAA-3′,下游引物序列:5′-GGCATGGACTGTGGTCATGAG-3′,采用PCR System 9700進行分析,運用2-△△Ct法相對定量檢測各組 mRNA 的表達量。
1.2.5ELISA測定B7-H1蛋白表達 按時間點取脂多糖孵育結束的6孔板置于冰上,棄去上清,用冰PBS洗3遍,再加入1 ml/孔的冰PBS,用細胞刮仔細完全地刮下細胞。將刮下的含有細胞的PBS液轉移離心管內,3 000 r/min,4℃離心5 min,棄去上清液,加入250 μl/孔的混合裂解液,反應30 min。反應完畢后,12 000 r/min,4℃離心10 min,取上清液。測定牛血清蛋白標準品(BCA)的標準曲線,計算各組樣品的總蛋白濃度。各組樣品取等量的總蛋白,按照B7-H1 ELISA試劑盒的規定步驟處理蛋白,用酶標儀測量各孔的吸光度,根據測定的B7-H1蛋白標準曲線,計算各組樣品對應的蛋白濃度。
1.3統計學方法 應用SPSS17.0軟件進行χ2、t檢驗、Spearman相關性分析。
2 結 果
2.1脂多糖刺激時間對TLR4表達的影響 以1 μg/ml的脂多糖分別刺激T24細胞0、6、12、24 h,流式細胞儀檢測結果顯示TLR4陽性率隨刺激時間的增長而上調,且在12 h時(27.76%,3 551/12 790)達到最高值,24 h時(22.49%,3 057/13 590)表達略有降低,但仍較高。6 h(14.65%,1 856/12 672)、12 h、24 h時TLR4陽性率與0 h(3.55%,533/15 024)時比較差異有統計學意義(Plt;0.05)。
2.2B7-H1 mRNA及蛋白表達結果 B7-H1 mRNA、蛋白的表達隨刺激時間的增長而上調,且在12 h時達到最高值,24 h時表達略有降低,但仍較高。與0 h時比較,6 h和24 h T24細胞B7-H1 mRNA、蛋白表達量增高(Plt;0.05),12 h顯著增高(Plt;0.01)。見表1。
2.3相關性分析 TLR4與B7-H1 mRNA、蛋白呈正相關(r=0.785,0.825;P=0.002,0.012)。
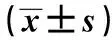
表1 B7-H1 mRNA、蛋白表達結果
與0 h比較:1)Plt;0.05,2)Plt;0.01
3 討 論
細胞介導的細胞免疫是一種機體抗腫瘤免疫的形式〔6〕,腫瘤抗原被機體免疫系統識別和提呈,對特異性細胞起到活化作用,進而殺傷腫瘤細胞。羅斌等〔7〕研究發現,腫瘤細胞可以通過缺如某些免疫分子和(或)異常表達,導致特異性細胞處于免疫耐受或無反應狀態,進而避開機體的免疫殺傷作用,這種現象既是免疫逃逸。隨著分子生物學的不斷發展和蛋白組學技術的研究深入,BC發生發展相關的特異性蛋白因子逐漸被發現,包括存活素(survivin)、凋亡抑制蛋白(livin)等〔8,9〕。Rosborough等〔10〕在研究中利用基因沉默(RNAi)技術,采用載有survivin siRNA的脂質體對原位BC小鼠模型進行治療,可發現在治療的3 w內,survivin mRNA的表達較治療前降低了70%,且腫瘤體積也有所降低,說明分子靶向survivin可作為臨床治療BC的新思路。livin是凋亡抑制蛋白(IAP)家族的新發現的一員,研究表明轉染livin的反義寡核苷酸于BC細胞中可抑制livin的表達及細胞增殖,同時激活細胞凋亡過程中最主要的終末剪切酶caspase-3,促進癌細胞凋亡。這些因子雖然被發現,但是其在BC的發生、發展、轉移過程中的作用機制和相互作用尚未完全明確,因此本次研究信號通路及相關蛋白表達,以期為BC的靶向治療提供依據。
B7家族分子在多種造血干細胞惡性腫瘤、實體瘤和浸潤性免疫細胞中均表達,研究發現膀胱腫瘤中存在共刺激因子B7-H1的高表達。本研究說明脂多糖的確可以活化TLR4信號通路,增加T24細胞表面TLR4的表達量。且TLR4的影響下B7-H1 mRNA及蛋白表達升高,TLR4與B7-H1 mRNA及蛋白表達呈正相關。B7-H1是新近發現的共刺激因子,其與T細胞、B細胞表面的PD-1分子結合,可提供抑制性信號,抑制兩者的活化和增殖,并可誘導細胞毒性T細胞(CTL)凋亡。Huang等〔11〕研究發現抑制體外培養的BC T24細胞系細胞外信號調節激酶、C-Jun N端激酶(ERK、JNK)信號通路后,TLR4介導的B7-H1表達上調作用被削弱,提示絲裂原活化蛋白激酶(MAPK)信號通路的活化可能參與了B7-H1相關的膀胱腫瘤免疫逃逸過程。另外還有研究證實B7-H1可誘導Treg表面的Fas/FasL表達上調,促進白細胞介素-10(IL-10)的分泌以誘導活化的細胞凋亡〔12〕。還有研究〔13〕發現,自然殺傷(NK)細胞在B7-H1表達缺失的情況下仍能增強CTL的殺傷作用,阻斷B7-H1后則可增強鼠結腸炎性免疫應答。
1李 哲,魏素菊,劉風玲,等.循環腫瘤細胞監測早期膀胱癌微轉移的價值〔J〕.腫瘤防治研究,2015;42(7):740-2.
2Rajaiah R,Perkins DJ,Ireland DD,etal.CD14 dependence of TLR4 endocytosis and TRIF signaling displays ligand specificity and is dissociable in endotoxin tolerance〔J〕.Proc Natl Acad Sci U S A,2015;112(27):8391-6.
3Bardoli AD,Afshar M,Viney R,etal.The PD-1/PD-L1 axis in the pathogenesis of urothelial bladder cancer and evaluating its potential as a therapeutic target〔J〕.Future Oncol,2016;12(5):595-600.
4郜 亮,馮向先.Toll樣受體4在惡性黑色素瘤中的表達及其介導腫瘤免疫逃逸的機制〔J〕.中華實驗外科雜志,2015;32(6):1387-90.
5Wang L,Qian J,Lu Y,etal.Immune evasion of mantle cell lymphoma:expression of B7-H1 leads to inhibited T-cell response to and killing of tumor cells〔J〕.Haematologica,2013;98(9):1458-66.
6張 荻,陳宜恬,李榮榮,等.CD_4~+CD_(25)~+Treg細胞介導的腫瘤免疫機制探析〔J〕.中華中醫藥學刊,2014;35(12):2886-9.
7羅 斌,田建輝,劉嘉湘,等.循環腫瘤細胞免疫逃逸的研究進展〔J〕.中華腫瘤防治雜志,2015;22(23):1856-60.
8黃益恒,周 念,徐 勛,等.聯合檢測特異性核基質蛋白-4、膀胱癌抗原在膀胱癌早期診斷中的意義〔J〕.實用醫學雜志,2014;30(22):3608-10.
9晉學飛,吳 冰,譚九峰,等.生存素、Livin和zeste同源物-2在膀胱癌組織中的表達〔J〕.中華實驗外科雜志,2015;32(6):1230-2.
10Rosborough BR,Ra?ch-Regué D,Matta BM,etal.Murine dendritic cell rapamycin-resistant and rictor-independent mTOR controls IL-10,B7-H1,and regulatory T-cell induction〔J〕.Blood,2013;121(18):3619-30.
11Huang X,Chen Y,Chung CS,etal.Identification of B7-H1 as a novel mediator of the innate immune/pro-inflammatory response as well as a possible myeloid cell prognostic biomarker in sepsis〔J〕.J Immunol,2014;192(3):1091-9.
12林 城,陳 雄,劉靜南,等.PD-1/PD-L1信號通路在非小細胞肺癌免疫逃逸及其治療中的研究進展〔J〕.中國肺癌雜志,2014;17(10):734-40.
13李旭宏,王曉波,余少鴻,等.NK細胞上清液提高CTL細胞對肝癌細胞殺傷力的研究〔J〕.檢驗醫學與臨床,2016;13(z1):62-5.
〔2017-01-19修回〕
(編輯 袁左鳴)
R73
A
1005-9202(2017)22-5528-03;
10.3969/j.issn.1005-9202.2017.22.018
江西省自然科學基金資助項目(No.20161BAB205271)
吳高亮(1978-),男,碩士,副主任醫師,主要從事泌尿系腫瘤研究。

