α-突觸核蛋白通過Rab5B下調海馬神經元膜表面NMDA受體含量及其介導的Ca2+內流和內向電流
于文嬌 楊巍巍,3,4 李 昕,3,4 李旭冉 陳 敏 于 順,3,4*
(1.首都醫科大學宣武醫院神經生物學研究室,北京市老年病醫療研究中心,北京 100053;2.首都醫科大學帕金森病臨床診療與研究中心,北京 100053;3.帕金森病北京市重點實驗室和教育部神經變性病重點實驗室,北京 100053;4.國家老年疾病臨床醫學研究中心,北京 100053;5.桂林醫學院附屬醫院神經科學實驗室,廣西桂林 541001)
·Alpha-突觸核蛋白的致病機制·
α-突觸核蛋白通過Rab5B下調海馬神經元膜表面NMDA受體含量及其介導的Ca2+內流和內向電流
于文嬌1, 2楊巍巍1, 2,3,4李 昕1, 2,3,4李旭冉1, 2陳 敏1, 5*于 順1, 2,3,4*
(1.首都醫科大學宣武醫院神經生物學研究室,北京市老年病醫療研究中心,北京 100053;2.首都醫科大學帕金森病臨床診療與研究中心,北京 100053;3.帕金森病北京市重點實驗室和教育部神經變性病重點實驗室,北京 100053;4.國家老年疾病臨床醫學研究中心,北京 100053;5.桂林醫學院附屬醫院神經科學實驗室,廣西桂林 541001)
目的研究α-突觸核蛋白(α-synuclein,α-Syn)對原代海馬神經元膜表面N-甲基-D-天門冬氨酸(N-methyl-D-aspartate,NMDA)受體含量和功能的影響及其機制。方法細胞外添加基因重組α-Syn,使其進入原代培養神經元細胞內,觀察敲減Rab5B基因前后神經元膜表面NMDA受體(NMDAR)和Rab5B表達的變化;NMDA激活NMDAR,活細胞工作站測定神經元Ca2+內流變化,全細胞膜片鉗記錄內向跨膜電流變化。結果α-Syn增加神經元Rab5B的表達,減少膜表面NMDAR含量,并因而抑制NMDA引起的Ca2+內流及內向跨膜電流;敲減Rab5B可逆轉α-Syn對NMDAR的下膜作用及功能的影響。結論α-Syn通過上調Rab5B而下調海馬神經元膜表面NMDAR含量及其介導的Ca2+內流及內向電流。
α-突觸核蛋白;NMDA受體;Rab5B;神經元;海馬
α-突觸核蛋白(α-synuclein,α-Syn)異常表達存在于老化和某些神經系統退行性疾病如阿爾茨海默病(Alzheimer’s disease,AD)、帕金森病(Parkinson’s disease,PD)、路易體癡呆(dementia with Lewy body,DLB)患者的腦中[1]。老化和上述變性腦均存在記憶功能下降或障礙的表現[2]。海馬是與記憶密切相關的神經結構。以往研究[3-6]表明,海馬神經元表面與記憶密切相關的谷氨酸受體——N-甲基-D-天門冬氨酸受體(N-methyl-D-aspartate receptors,NMDARs)在老化和變性腦中發生顯著的變化,但其機制不清楚。筆者以往研究[7]表明,α-Syn的異常表達可以促進多巴胺神經元膜表面NMDARs的內在化,導致膜表面NMDARs減少,這一作用與α-Syn上調Rab5B表達有關。Rab5B是一種小的GTPases蛋白,是NMDARs內在化所必需的蛋白[8]。鑒于老化和變性腦的海馬結構存在α-Syn的異常積聚,筆者推測,海馬神經元膜表面NMDARs的變化可能與α-Syn有關。本研究將利用原代培養大鼠海馬神經元觀察α-Syn對神經元膜表面NMDARs內在化及功能的影響,并分析Rab5B的作用。
1 材料與方法
1.1 材料
健康出生12 h內Wistar新生大鼠,購自中國人民解放軍軍事醫學科學實驗動物中心,實驗動物許可證號:SCXK-2014-004。杜恩斯組織勻漿器(Wheaton Kimble公司,美國);Neurobasal A培養基、B27、DMEM培養基(Gibco公司,美國);胎牛血清(FBS,Berlin公司,美國);NMDA、MK-801(Sigma公司,美國);Rab5B反義寡核苷酸(百恩維公司,中國);NMDAR NR1抗體(Abcam公司,美國);Rab5B抗體(Santa Cruz公司,美國);Fluo4-AM(東仁化學公司,日本)。
Hank’s平衡鹽溶液A(HBSS,不含Ca2+、Mg2+)(mmol/L):NaCl 0.14,KCl 0.54×10-2,葡萄糖0.006,KH2PO40.44×10-3,Na2HPO40.33×10-3,調整pH至7.2;Hank’s平衡鹽溶液B(HBSS,不含Mg2+)(mmol/L):NaCl 0.14,KCl 0.54×10-2,葡萄糖 1,KH2PO40.44×10-3,Na2HPO40.33×10-3,CaCl20.13×10-2,調整pH至7.2。電極內液(mmol/L):CsCl 70,NaCl 10,4-羥乙基哌嗪乙磺酸(HEPES)10,EGTA 10,ATP 2,GTP 0.2,調整pH至7.3;細胞外液(mmol/L):NaCl 150,KCl 5,CaCl21.4,葡萄糖 10,HEPES 5,河豚毒素(TTX)0.000 3,木防儀苦毒素(picrotoxin)0.1,NBQX 0.01,士的寧(trychnine)0.1,調整pH至7.3,調整滲透壓至330 mOsm。
活細胞工作站(Leica公司,德國);玻璃微電極拉制儀(Narishige公司,日本);膜片鉗放大器(Multiclamp 700B)(HEKA公司,德國),數據采樣板(Digidata 1322A)和數據采集分析軟件(pClamp 9.2)(Molecular Devices公司,美國);MiniAnalysis軟件包(Synaptosoft公司,美國)。
1.2 方法
1.2.1 重組人α-Syn的制備
基因重組人α-Syn的表達和純化根據本室已建立的方法進行[7]。純化后的蛋白分別用SDS-PAGE和Western blotting法進行鑒定,BCA法定量后備用。
1.2.2 海馬原代神經元培養
原代神經元培養方法根據已建立的方法[9]進行:將新生鼠斷頭,剝離鼠腦后于顯微鏡下分離并剪碎雙側海馬,胰蛋白酶消化30 min后,用含10%(體積分數)FBS的DMEM培養基終止消化。玻璃滴管火焰拋光后,輕柔吹打分散細胞,計數細胞密度。以2 × 105個/cm2密度接種到多聚賴氨酸包被的35 mm培養皿中,于37 ℃,5%(體積分數) CO2的培養箱內培養。待神經元貼壁后,改用Neurobasal A、B27無血清培養基繼續培養,每3 d換半液,培養10~12 d。
1.2.3 Rab5B反義寡核苷酸的制備
Rab5B反義寡核苷酸(antisense sequence,AS)及擾亂順序的寡核苷酸(scrambled sequence,SS),其序列分別是:5′-GCTGTGCTTCTGCTAGTCATTTCAAGAG AATGACTAGCAGAAGCACAGCTTTTTTCTCGAGG-3′和5′-GATCCCTCGAGAAAAAAGCTGTGCTTCTGCTA GTCATTCTCTTGAAATGACTAGCAGAAGCACAGC-3′。
1.2.4 細胞免疫熒光檢測
細胞用PBS漂洗后,預冷的4%(質量分數)多聚甲醛固定細胞30 min,含有1%(體積分數)Triton-X 100的PBST溶液室溫孵育30 min,1%(質量分數) BSA封閉1 h。加入抗NMDAR NR1抗體(1∶1 000)或抗Rab5B抗體(1∶1 000),于4 ℃反應過夜。PBST洗3次,每次10 min。加入熒光二抗(1∶5 000),室溫反應2 h。PBST洗3次,每次10 min。激光共聚焦顯微鏡觀察。
1.2.5 細胞內Ca2+濃度的測定
細胞培養皿置于活細胞工作站載物臺上,激發光波長為488 nm,發射光波長為515 nm,固定參數后每10 s掃描一次,掃描180s作為基線。加入NMDA(100μmol/L)及甘氨酸(10μmol/L),繼續掃描目的細胞內的Ca2+熒光強度改變,圖像由隨機軟件分析處理(Leica公司,德國)。胞內的Ca2+熒光強度變化用Fluo-4與Ca2+結合后的熒光強度比值表示。計算公式:熒光強度變化=Ft/F0(Ft:添加NMDA后第t秒神經元內的熒光復合物的熒光強度,F0:基線水平的神經細胞內的熒光復合物的熒光強度[7])。
1.2.6 全細胞膜片鉗記錄細胞膜電流及給藥
采用常規全細胞記錄模式[10],記錄細胞的電信號,輸入膜片鉗放大器,而后經由模數轉換儀輸入到計算機,經10 Hz濾波,采樣頻率為2~3 Hz。記錄信號的監測、儲存及通過記錄點擊給予細胞的指令電壓以及分析處理由Axon軟件pClamp 8.0和Clampfit 8.0完成。全細胞記錄在22~24 ℃室溫環境下進行,連續記錄30 min以上。
通過軟件控制正壓給藥系統(DAD-12 Superfusion System)的通道灌注NMDA(100 μmol/L)、Glycine(10 μmol/L)。使用HL-2型恒流泵進行細胞外灌注沖洗細胞,以終止藥物作用。
1.3 統計學方法
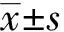
2 結果
2.1 Rab5B參與α-Syn引起的神經元膜表面NMDAR 亞單位NR1的內在化
免疫熒光標記顯示,沒有α-Syn處理的神經元(PBS組),NR1主要分布于神經元的膜表面。外加α-Syn處理后,神經元膜表面NR1顯著減少,胞質中的NR1明顯增多,提示NR1發生內在化。單純轉染Rab5B SS和Rab5B AS的神經細胞,NR1也主要分布于神經元的膜上。用α-Syn處理Rab5B SS轉染神經元,膜表面的NR1顯著減少,胞質中的NR1明顯增多,而在Rab5B AS轉染神經元,α-Syn使NR1內在化的作用消失,提示α-Syn促進NMDAR NR1的內在化的作用需要Rab5B的參與(圖1)。
2.2 Rab5B參與α-Syn抑制NMDA受體介導的Ca2+內流
活細胞工作站結果顯示(n=5),NMDA引起 [Ca2+]i快速而顯著增加,NMDA的這一作用被NMDA受體特異性阻斷劑MK-801完全阻斷。事先用α-Syn處理神經元后,則 NMDA引起的[Ca2+]i增加的作用明顯受到抑制,而用Rab5B-AS抑制Rab5B表達后,α-Syn抑制[Ca2+]i增加的作用被消除(圖2)。
2.3 Rab5B參與α-Syn抑制NMDA受體介導的跨膜內向電流
將鉗制電壓設定為-75 mV條件下時,NMDA受體介導的內向電流隨受體特異性激動劑NMDA濃度的增加而增加(圖3)。α-Syn處理細胞后,NMDA受體介導的內向電流受到抑制,且此抑制作用在Rab5B AS轉染細胞后消失(圖4)。
3 討論
本研究結果表明,利用外加重組α-Syn處理海馬神經元后,可使神經元膜表面NMDARs亞單位NR1減少,胞質含量增加。鑒于NR1是構成NMDAR的必需亞單位,其在神經元膜表面的減少意味著完整的具有功能的NMDARs發生了內在化。筆者以往的研究[11]表明,將α-Syn添加到細胞外,α-Syn可以迅速進入細胞并引起細胞內α-Syn含量增加,由此推測,細胞外添加α-Syn導致的NMDARs的內在化,很可能是α-Syn進入細胞內引起的。作為支持這一推測的證據,在α-Syn過表達的神經細胞中,NMDARs也發生內在化。由于Rab5B蛋白是內吞機制中的關鍵蛋白,能夠促進細胞膜表面蛋白的內在化[8],筆者推測,α-Syn引起的海馬神經元膜表面NMDARs的內在化可能有Rab5B的參與。為了證明這一點,筆者利用小干擾RNA敲減Rab5B,觀察α-Syn對NMDARs內在化的影響。結果顯示,敲減Rab5B后,α-Syn引起的NMDARs內在化明顯受到抑制。
如前所述,神經元膜表面NR1亞單位的減少意味著膜表面功能性NMDARs的減少。由于NMDARs在通道開放情況下可以介導Na+和Ca2+的內流和由此引起的內向電流,筆者分別利用活細胞工作站和膜片鉗技術研究了α-Syn處理和非處理神經元NMDARs特異性激動劑NMDA對Ca2+內流和內向跨膜電流的影響。在無α-Syn處理的神經元,NMDA引起細胞內Ca2+濃度快速而顯著增加,同時可以記錄到NMDARs介導的內向電流,NMDA的這一作用呈濃度依賴性。而在α-Syn處理神經元,NMDA引起細胞內Ca2+濃度增加以及NMDAR介導的內向電流明顯受到抑制。這一結果提示,α-Syn引起了NMDARs功能的變化,這一變化很可能是通過促進NMDARs的內在化從而導致神經元膜表面功能性的NMDARs減少。由于α-Syn的上述作用可因敲減Rab5B而被明顯抑制,因此推測Rab5B參與了α-Syn引起的NMDARs內在化過程。

圖1 Rab5B在α-Syn所致細胞膜表面NR1內在化中的作用Fig.1 The role of Rab5B in α-Syn-induced NR1 internalization
Representative immunofluorescence images showing NR1 (red),Rab5B SS or AS (green),and DAPI (blue).Cells were incubated separately with α-Syn (10 μmol/L) for 24 h or LV-GFP-Rab5B AS for 3 days,with or without added α-Syn.Other batches of cells were treated with corresponding vehicles,PBS and LV-GFP-Rab5B SS,either in the presence or absence of α-Syn.Each batch of cells was then stained for immunofluorescence microscopy and nuclei were counterstained with DAPI.Images were captured under a 100×objective with equal exposure times to allow direct comparison.Each of the three independent replicates was assessed from three to ten random fields of view.n=5 in each group,bar=10 μm.NR1: N-methyl-D-aspartate receptors1;PBS: phosphate buffered saline;α-Syn: α-synuclein;SS: scrambled sequence;AS: antisense sequence;GFP: green fluorescent protein.

圖2 α-Syn對于NMDA引起的[Ca2+]i增加的影響Fig.2 Effect of α-Syn on NMDA-induced elevation of [Ca2+]i
Cells were transfected with Rab5B SS or Rab5B AS for three days,and then treated with α-Syn (10μmol/L) for 24 h before observing NMDAR-mediated Ca2+influx.Cells were stained Ca2+indicator fluo4-AM.A: Dynamic changes in [Ca2+]i as indicated by fluorescence intensity (Ft/F0);B: Statistical peak values of [Ca2+]i before and after NMDA stimulation.n=5 in each group;*P<0.05,**P<0.01;α-Syn: α-synuclein;NMDA:N-methyl-D-aspartate;HBSS:Hank’s balanced salt solution;SS: scrambled sequence;AS: antisense sequence;Ft: fluorescence of the indicator at t second;F0: fluorescence of the indicator at 0 second;[Ca2+]i: Ca2+influx.

圖3 α-Syn對不同濃度的NMDA誘發內向跨膜電流的影響Fig.3 The effect of α-Syn on currents evoked by NMDA of different concentrations
Whole cell patch clamp experiments were used to record NMDA receptor-mediated currents in cultured hippocampal neurons.Batches of cells were treated as described above.A,BCurrents in α-Syn-treated cells(10 μmol/L) were decreased at a range of agonist concentrations (0,10,20,50,100,200 and 500μmol/L) and returned to robust levels on addition of LV-GFP-AS (n=5,*P<0.05,**P<0.01vsPBS-treated group,#P<0.05vsα-Syn group);α-Syn: α-synuclein;NMDA:N-methyl-D-aspartate;SS: scrambled sequence;PBS: phosphate buffered saline;AS: antisense sequence.

圖4 α-Syn抑制NMDA受體介導的內向電流Fig.4 α-Syn reduced NMDAR-mediated inward currents
A: Trace of NMDA receptor-mediated currents in each batch of cells.B: Bar graphs shows the normalized currents after NMDA stimulation.n=5 in each group;*P<0.05;α-Syn: α-synuclein;NMDA:N-methyl-D-aspartate;PBS: phosphate buffered saline;SS: scrambled sequence;AS: antisense sequence.
本研究為老化和某些神經退行性疾病腦的海馬神經元膜表面NMDARs變化的機制提供了實驗依據。
[1] Yu S,Ueda K,Chan P.Alpha-synuclein and dopamine metabolism[J].Mol Neurobiol,2005,31(1-3): 243-254.
[2] Aarsland D,Creese B,Politis M,et al.Cognitive decline in Parkinson disease[J].Nat Rev Neurol,2017,13(4):217-231.
[3] Horak M,Holubova K,Nepovimova E,et al.The pharmacology of tacrine at N-methyl-d-aspartate receptors[J].Prog Neuropsychopharmacol Biol Psychiatry,2017,75:54-62.
[4] Hall H,Reyes S,Landeck N,et al.Hippocampal Lewy pathology and cholinergic dysfunction are associated with dementia in Parkinson’s disease[J].Brain,2014,137(Pt 9): 2493-2508.
[5] Ullman M T,Pullman M Y.A compensatory role for declarative memory in neurodevelopmental disorders[J].Neurosci Biobehav Rev,2015,51: 205-222.
[6] Foster T C,Kyritsopoulos C,Kumar A.Central role for NMDA receptors in redox mediated impairment of synaptic function during aging and Alzheimer’s disease[J].Behav Brain Res,2017,322(Pt B):223-232.
[7] Cheng F,Li X,Li Y,et al.alpha-Synuclein promotes clathrin-mediated NMDA receptor endocytosis and attenuates NMDA-induced dopaminergic cell death[J].J Neurochem,2011,119(4):815-825.
[8] Arnett A L,Bayazitov I,Blaabjergm,et al.Antisense oligonucleotide against GTPase Rab5b inhibits metabotropic agonist DHPG-induced neuroprotection[J].Brain Res,2004,1028(1): 59-65.
[9] 王鵬,李昕,陳予東,等.α-突觸核蛋白寡聚體抑制大鼠原代培養神經元突起早期生長[J].首都醫科大學學報,2014,35 (5): 587-591.
[10] Wu H Y,Yuen E Y,Lu Y F,et al.Regulation of N-methyl-D-aspartate receptors by calpain in cortical neurons[J].J Biol Chem,2005,280(22): 21588-21593.
[11] Yin J,Han J,Zhang C,et al.C-terminal part of alpha-synuclein mediates its activity in promoting proliferation of dopaminergic cells[J].J Neural Transm (Vienna),2011,118(8):1155-1164.
α-SynucleinreducessurfaceexpressionsofNMDAreceptorsandNMDA-invokedCa2+influxandinwardcurrentbyupregulationofRab5Binculturedprimaryhippocampalneurons
Yu Wenjiao1,2,Yang Weiwei1,2,3,4,Li Xin1,2,3,4,Li Xuran1,2,Chen Min1,5*,Yu Shun1,2,3,4*
(1.DepartmentofNeurobiology,XuanwuHospital,CapitalMedicalUniversity,BeijingInstituteofGeriatrics,Beijing100053,China;2.ClinicalCenterforParkinson’sDisease,CapitalMedicalUniversity,Beijing100053,China;3.BeijingKeyLaboratoryforParkinson’sDiseaseandKeyLaboratoryofNeurodegenerativeDiseases,MinistryofEducation,Beijing100053,China;4.NationalClinicalResearchCenterforGeriatricDisorders,Beijing100053;5.LaboratoryofNeuroscience,AffiliatedHospitalofGuilinMedicalUniversity,Guilin541001,GuangxiZhuangAutonomousRegion,China)
ObjectiveTo investigate the effects of α-synuclein(α-Syn) on surface expressions and functions of N-methyl-D-aspartate (NMDA) receptors (NMDARs) in cultured primary hippocampal neurons.MethodsIncreased intracellular α-Syn levels were realized by extracellular addition of recombinant human α-Syn to the culture medium of rat primary hippocampal neurons.Expressions of surface NMDARs and Rab5B were observed by fluorescence immunocytochemistry and Western blotting.Rab5B antisense oligonucleotides were applied to suppress Rab5B expression.Live cell imaging system and whole-cell patch-clamp recording were used to record NMDA-evoked Ca2+influx and inward currents.ResultsNeurons treated with α-Syn displayed increased Rab5B,decreased surface NMDARs,and reduced NMDA-evoked Ca2+influx and inward currents.The above α-Syn effects were inhibited by suppression of Rab5B expression.Conclusionα-Syn reduces the surface expression and functions of NMDARs by increasing Rab5B expression.
α-synuclein;NMDA receptor;Rab5B;neuron;hippocampus
國家自然科學基金(81371200,81071014,81401042),北京市醫院管理局“使命”計劃專項經費資助(SML20150803),北京市科學技術委員會資助(Z161100005116011,Z171100000117013),北京市衛生和計劃生育委員會“老年重大疾病關鍵技術研究”(PXM2017_026283_000002),廣西自然科學基金(2014GXNSFAA118197)。This study was supported by National Natural Science Foundation of China (81371200,81071014,81401042),Beijing Municipal Administration of Hospitals’ Mission Plan (SML20150803),Beijing Municipal Science &Technology Commission (Z161100005116011,Z171100000117013),Beijing Municipal Commission of Health and Family Planning (PXM2017_026283_000002),Natural Science Foundation of Guangxi (2014GXNSFAA118197).
*Corresponding authors,E-mail:yushun103@163.com,chenmin790830@163.com
時間:2017-12-13 21∶29
http://kns.cnki.net/kcms/detail/11.3662.R.20171213.2129.066.html
10.3969/j.issn.1006-7795.2017.06.018]
Q189
2017-10-23)
編輯 陳瑞芳

