基于造影目測結果評估冠狀動脈分叉病變介入治療中分支閉塞風險評分系統的研究
何源,張冬,陳昌喆,宋晨曦,尹棟,豐雷,朱成剛,徐波,竇克非
冠心病研究
基于造影目測結果評估冠狀動脈分叉病變介入治療中分支閉塞風險評分系統的研究
何源,張冬,陳昌喆,宋晨曦,尹棟,豐雷,朱成剛,徐波,竇克非
目的:基于冠狀動脈造影量化分析(QCA)研究結果,建立根據冠狀動脈造影目測結果評估分叉病變介入治療中分支閉塞風險的評分系統。 方法:既往我們對以分支即興支架置入策略行冠狀動脈分叉病變介入治療的患者造影資料進行QCA,形成了RESOLVE評分系統。本研究納入RESOLVE研究全部1 545例患者(共1 601處病變),將RESOLVE評分系統中根據QCA結果計分項改為造影目測評估結果,評價造影目測評估結果和原QCA結果一致性;比較主支血管支架置入后分支閉塞[定義為冠狀動脈造影提示心肌梗死溶栓治療臨床試驗(TIMI)血流等級下降]組(n=11,共118處病變)與無分支閉塞組(n=1 431,共1 483處病變)各評分預測因素的造影目測評估結果,并參照RESOLVE評分的計分方法形成V-RESOLVE評分。評價V-RESOVE評分的區分度、擬合優度及不同積分對應分支閉塞發生率,并比較V-RESOLVE評分和RESOLVE評分對分叉病變介入治療中分支閉塞風險的診斷價值。 結果:將RESOLVE評分中QCA分析計分項改為造影目測評估結果,與QCA分析結果的一致性為一般至中等(加權Kappa值0.22~0.44);分支閉塞組術前分叉核直徑狹窄程度、主支血管支架置入前分支血管狹窄程度較無分支閉塞組更高,分叉角度、主支/分支血管管徑比較無分支閉塞組更大(P均<0.01);由此建立的V-RESOLVE評分的受試者工作特征(ROC)曲線下面積為0.76[95%可信區間(CI):0.71~0.80],與RESOLVE評分ROC曲線下面積(0.77,95%CI:0.72~0.81)之間的差異無統計學意義(P=0.74,Hosmer-Lemeshow法P=0.17);根據V-RESOLVE評分四分位數間研究對象分支閉塞情況,定義評分≥12分患者為高危患者,其分支閉塞發生率明顯高于非高危(評分<12分)患者(16.7% vs 4.3%,P<0.01);V-RESOLVE評分與RESOLVE評分定義的非高危患者(4.3% vs 3.4%)和高危患者中分支血管閉塞發生率(16.7% vs 18.0%)間的差異均無統計學意義(P值分別為0.22和0.60)。 結論:本研究通過冠狀動脈造影目測評估結果建立的V-RESOLVE評分系統可預測分叉病變介入治療中分支閉塞風險。
冠狀動脈疾病;危險性評估;評分系統
冠狀動脈分叉病變介入治療的比例占經皮冠狀動脈介入治療(PCI)總量的15%~20%,一直是PCI中的難點[1,2],其中如何避免重要分支血管閉塞是分叉病變介入治療的一大挑戰。基于QCA數據建立的RESOLVE評分是分叉病變介入治療中分支閉塞風險的有效預測工具[3]。該評分系統納入了6項分支閉塞的獨立預測因素,包括2項冠狀動脈造影目測評估結果,即術前主支血管斑塊與分支血管位置關系、支架置入前主支血管心肌梗死溶栓治療臨床試驗(TIMI)血流等級和4項冠狀動脈造影量化分析(QCA)結果,即術前分叉核直徑狹窄程度、術前分叉角度、術前主支/分支血管直徑比和主支血管支架置入前分支血管狹窄程度。采用QCA分析造影結果盡管能較客觀地評價病變嚴重程度[4],但分析過程費時,并且不能提供實時評價結果,使RESOLVE評分在分叉病變介入治療實踐中的指導價值受到局限。
本研究旨在基于RESOLVE評分建立完全由造影目測評估結果預測分叉病變介入治療中分支閉塞風險的工具,即V-RESOLVE評分系統。
1 資料與方法
研究對象:本研究將RESOLVE研究納入的患者及分叉病變作為研究對象,連續篩選我院2012-01至2012-07期間成功行PCI的7 007例患者,排除290例選擇性雙支架置入治療患者,入選1 545例有分叉病變(定義為冠狀動脈狹窄處連接分支血管或冠狀動脈狹窄累及重要分支冠狀動脈,重要分支定義參照歐洲分叉俱樂部定義標準[5],原則上參考直徑≥1.5 mm)的患者,共計1 601處分叉病變。
資料收集:收集入選患者冠狀動脈造影和手術資料。對所有研究對象基線和預擴張后冠狀動脈造影資料分別進行QCA和目測評估。QCA由計算機分析系統(Qangio XA, version 7.3, Medis, Leiden,Netherlands)進行,對研究對象基線和術中預擴張后造影資料進行測量并計算RESOLVE評分中術前分叉核狹窄程度、術前分叉角度、術前主支/分支血管管徑比和主支支架置入前分支血管狹窄程度結果。目測評估由阜外醫院核心實驗室一名具有豐富造影影像學分析經驗的技術員,在對研究對象先前QCA結果和分支閉塞情況全盲條件下獨立回顧。分叉核定義為從血管開始分出分支血管到界嵴的分叉中心節段[6],分叉角度定義為主支遠端和分支血管夾角,主支/分支血管直徑比計算公式為1/2(主支血管分叉近端參考直徑+主支血管分叉遠端參考直徑)/分支血管參考直徑。
分支血管閉塞風險評分建立方法:將RESOLVE評分系統中根據QCA結果計分的4個計分項(術前分叉核狹窄程度、術前分叉角度、術前主支/分支血管管徑比和主支血管支架置入前分支血管狹窄程度)改為目測評估結果,計分方法參考RESOLVE評分系統不變,比較目測評估結果與QCA結果的一致性,并形成V-RESOLVE評分(表1)。評價V-RESOLVE評分診斷冠狀動脈分叉病變介入治療中分支血管閉塞的區分度、擬合優度,并根據不同積分對應的分支閉塞發生率,進行評分的危險分層。進一步比較V-RESOLVE評分與RESOLVE評分診斷區分度和對應不同危險度患者分支血管閉塞風險情況。
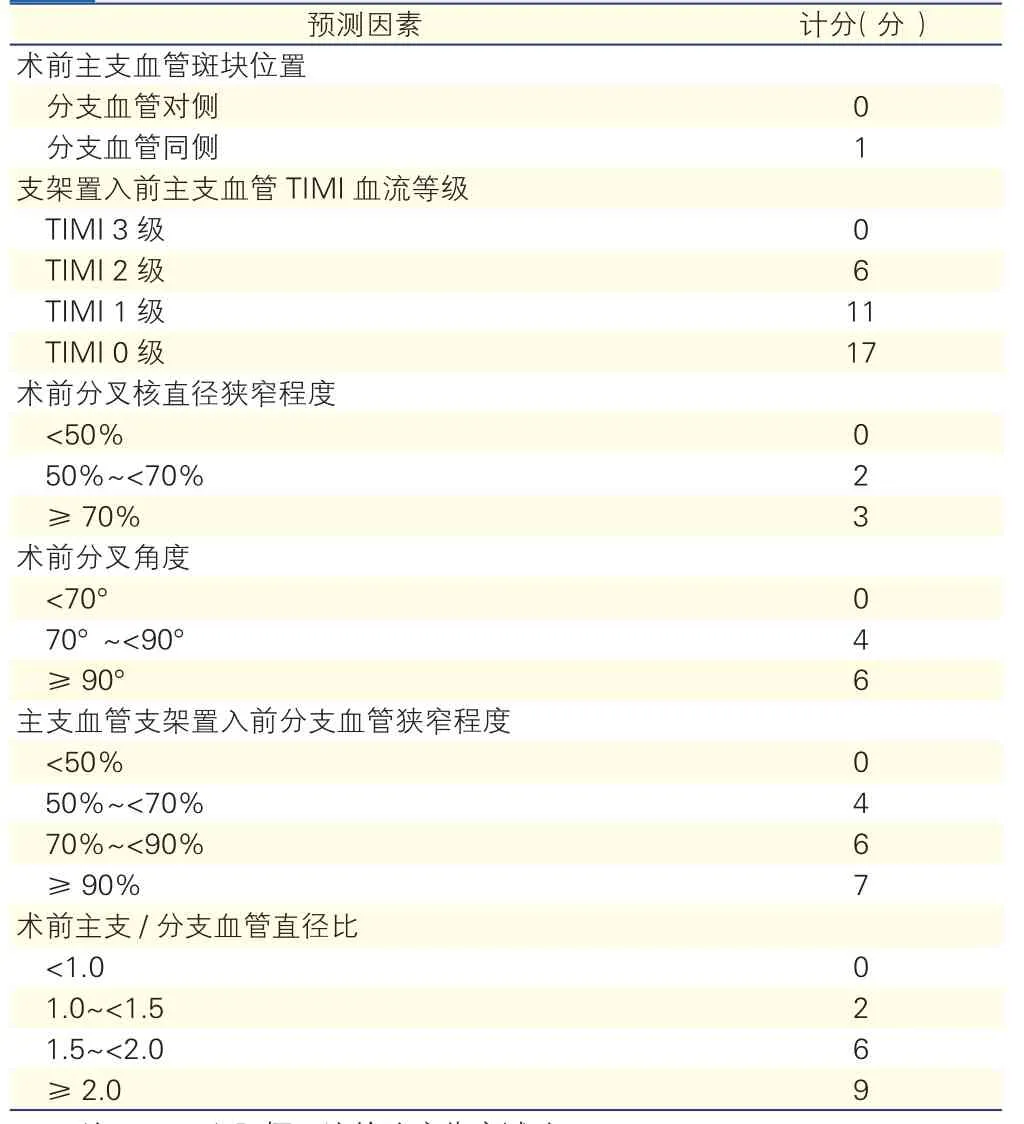
表1 V-RESOLVE評分系統風險預測因素及計分
診斷標準與分組方法:分支血管閉塞定義為冠狀動脈造影提示TIMI血流等級下降。以主支血管支架置入后是否發生分支閉塞分為分支閉塞組114例患者(118處病變)和無分支閉塞組1 431例患者(1 483處病變)。
介入治療和圍術期用藥:患者的介入治療策略和器械均由術者決定。圍術期抗血小板和抗凝藥物使用根據手術情況并參照PCI指南。術前均予患者氯吡格雷300 mg和阿司匹林300 mg;術后建議所有患者終生服用阿司匹林(100 mg/d),并至少服用1年氯吡格雷(75 mg/d)。
統計學方法:所有數據應用SAS9.4統計軟件進行分析。計量資料用均數±標準差表示,并通過獨立樣本t檢驗進行比較,計數資料用百分比表示并以χ2檢驗或Fisher精確檢驗進行比較。造影目測評估與QCA結果的一致性檢驗用加權kappa值評價[7],一般認為kappa值>0.8一致性好,0.61~0.80一致性較好,0.41~0.60一致性中等,0.21~0.4一致性一般,<0.20一致性差。以受試者工作特征(ROC)曲線下面積評價診斷區分度[8],以Hosmer-Lemeshow擬合優度檢驗(HL)評價診斷一致性[8,9],以重分類改善指標(NRI)和綜合判別改善程度(IDI)比較兩種評分系統間診斷區分度的優劣[10]。P<0.05認為差異有統計學意義。
2 結果
2.1 兩組患者RESOLVE評分系統中QCA計分項改為目測評估結果后的情況比較(表2)
本研究全部1 601處分叉病變造影目測評估結果與對應原QCA結果[11]比較顯示,術前分叉核直徑狹窄程度的一致性一般(加權Kappa值=0.22)、主支/分支血管管徑比一致性一般(加權Kappa值=0.22)、主支血管支架置入前分支血管狹窄程度一致性一般(加權Kappa值=0.24)、術前分叉角度一致性中等(加權Kappa值=0.44)。分支閉塞組和無分支閉塞組造影目測評估結果顯示,分支閉塞組術前分叉核直徑狹窄程度、主支血管支架置入前分支血管狹窄程度較無分支閉塞組更高,術前分叉角度、術前主支/分支血管直徑比較無分支閉塞組更大(P均<0.01)。
表2 兩組患者分叉病變分支閉塞預測因素的目測評估結果比較
注:-:無
2.2 V-RESOLVE評分的構建和診斷能力評價(圖1)
參考RESOLVE評分系統計分項和計分方法,根據目測評估結果,計算研究對象分支閉塞風險積分,形成V-RESOLVE評分。以主支支架置入后是否發生分支血管閉塞作為狀態變量,以V-RESOLVE評分由低到高作為檢驗變量,繪制ROC曲線(圖1)。ROC 曲 線 下 面 積 為 0.76(95%CI:071~0.80,P<0.01)。V-RESOLVE評分 HL P值為 0.17,提示擬合優度良好。
V-RESOLVE評 分 范 圍 為0~43分。 按 照V-RESOLVE評分四分位數,將本研究對象分為Q1(0~3 分)組、Q2(4~7 分)組、Q3(8~11 分)組、Q4(≥12分)組,四組的分支閉塞發生率依次為 1.54%(7/456)、4.80% (18/375)、7.22% (27/374)、16.67% (66/396)。Q4組較Q1組、Q2組、Q3組的分支血管閉塞的比值比(OR)依次為13.33(95%CI:6.02~29.41)、4.65(95%CI:2.65~8.20)、2.67(95%CI:1.66~4.27)。將 Q1~Q3 評分范圍(0~11 分)患者定義為非高危患者,Q4評分范圍(12~43分)患者定義為高危患者。高危患者分支血管閉塞發生率顯著高于非高危患者(16.7% vs 4.3%,P<0.01)。

圖1 V-RESOLVE評分系統受試者工作特征曲線
2.3 V-RESOLVE評分和RESOLVE評分的ROC曲線下面積和診斷區分度比較(圖2)
V-RESOLVE評分ROC曲線下面積(0.76,95%CI:071~0.80)與 RESOLVE 評分的 ROC 曲線下面積(0.77,95%CI:0.72~0.81)相比,差異無統計學意義(P=0.74)。RESOLVE評分較V-RESOLVE評分的NRI為15.4%,IDI為0.9%,兩種評分的診斷區分度差異無統計學意義(P均<0.05)。V-RESOLVE評分非高危患者與RESOLVE評分非高危患者(RESOLVE評分0~9分)分支血管閉塞發生率(4.3% vs 3.4%)以及V-RESOLVE評分高危患者與RESOLVE評分高危患者(RESOLVE評分10~43分)分支血管閉塞發生率(16.7% vs 18.0%)之間的差異均無統計學意義(P均<0.05)。
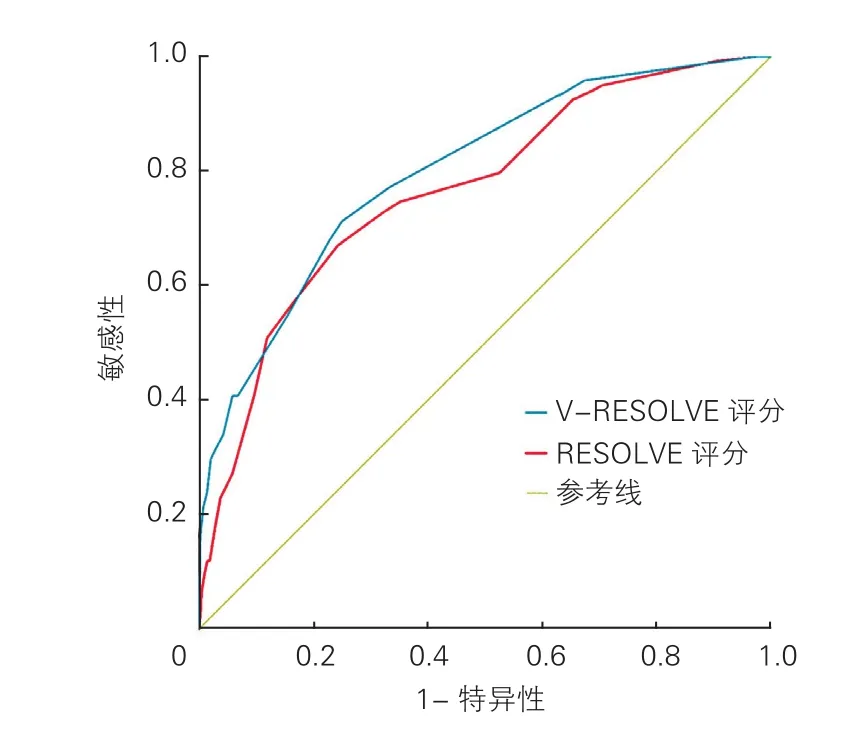
圖2 V-RESOLVE評分系統與RESOLVE評分系統受試者工作特征曲線比較
3 討論
本研究建立了完全由造影目測評估結果預測冠狀動脈分叉病變介入治療中分支閉塞風險的V-RESOLVE評分系統,該系統由基于QCA分析結果的RESOLVE評分系統得來,同樣包括6個預測因素,具有較好的區分度和校準度,以<12分和≥12分作為V-RESOVE評分區分非高危患者和高危患者診斷分界點時,高危患者分支血管閉塞發生率明顯高于非高危患者;與RESOLVE評分相比,V-RESOLVE評分系統的ROC曲線下面積無顯著差異,NRI和IDI提示兩評分系統間無明顯優劣差距,可認為在預測分支血管閉塞風險方面兩評分系統效能相當;V-RESOLVE評分與RESOLVE評分對應危險分組患者的分支閉塞發生率無顯著差異,提示兩評分系統在區分分支閉塞風險高危患者上同樣有效。以上結果為V-RESOLVE評分用于冠狀動脈分叉病變介入臨床實踐提供了依據。
分支閉塞的病理生理學機制較復雜,目前認為斑塊移位或界嵴移位可能是分支閉塞的主要機制[12]。V-RESOLVE評分中的分支血管閉塞預測因素與RESOLVE評分[3]一致,主支血管分叉部位斑塊位于分支同側、主支血管TIMI血流等級下降、術前分叉核直徑狹窄程度高、主支/分支血管直徑比大的分叉病變在介入治療中更容易發生嚴重的斑塊移位壓迫分支血管開口,從而增加了分支血管閉塞風險。分叉角度增大增加分支閉塞風險,與先前研究結果[13]一致。大分叉角度可致分支血流分流阻力增加及分叉核斑塊負荷增大,也可增加術中錨定導絲進入分支血管的難度,以上原因都有可能增加大分支角度分叉病變介入治療時分支閉塞可能。
此前有研究提示,與QCA軟件分析結果相比,目測評估造影的方法在分析分叉病變方面,其結果穩定性和準確性較差[14]。本研究中,目測評估和QCA分析術前分叉核狹窄程度、術前分叉角度、術前主支/分支血管直徑比和支架置入前分支血管狹窄程度結果一致性提示為一般至中等(加權Kappa值 0.22~0.44),優于 Shin 等[15]報道的歐洲分叉俱樂部專家目測評估與QCA一致性分析結果(kappa=0.109),這也可解釋為何V-RESOLVE評分與RESOLVE評分的診斷能力相當。但V-RESOLVE評分高危(≥12分)患者的診斷分界點高于RESOLVE評分高危(≥10分)患者,可能原因是:術者目測評估需要行PCI的病變時,往往會傾向于較QCA分析結果高估病變嚴重程度。Nallamothu等[16]的研究提示,目測評估較QCA分析結果可將病變直徑狹窄程度高估8.2%。而在V-RESOLVE評分與RESOLVE評分中,有兩項風險預測因素與血管直徑狹窄程度相關,因此有可能是目測評估結果對病變的高估造成了V-RESOLVE評分中高危患者的診斷分界點更高。
本研究有以下局限性。首先,本研究V-RESOLVE評分目測僅由一名有豐富造影影像學分析經驗的觀察人員獨立完成,其目測評估結果可能較為接近QCA結果,后續研究中尚需進一步比較本評分系統在不同觀察經驗的不同觀察者之間的結果一致性,以檢驗本評分系統的應用價值。其次,本研究為單中心回顧性研究,并且可能存在未知混雜因素,尚需多中心、前瞻性研究進一步驗證V-RESOLVE評分在臨床實踐中的應用價值。最后,V-RESOLVE評分僅能給出分支閉塞發生可能性的相關信息而非主支血管支架置入后分支血管閉塞發生率的準確值。因此,V-RESOLVE評分并不是分叉介入治療決策的唯一參考。術者仍應結合分支血管臨床意義和術中實際情況,選擇分叉病變介入治療的合適策略。未來需要隨機對照臨床研究來驗證V-RESOLVE評分在臨床實踐中的應用價值。
綜上所述,V-RESOLVE評分系統是根據目測評估冠狀動脈分叉病變造影結果進行分支閉塞風險分層的有效工具,計算簡便,其在介入治療術者和冠狀動脈分叉病變患者人群中的表現尚待進一步證實。
[1] Steigen TK, Maeng M, Wiseth R, et al. Randomized study on simple versus complex stenting of coronary artery bifurcation lesions: the Nordic bifurcation study. Circulation, 2006, 114: 1955-1961.
[2] Iakovou I, Schmidt T, Bonizzoni E, et al. Incidence, predictors, and outcome of thrombosis after successful implantation of drug-eluting stents. JAMA, 2005, 29: 2126-2130.
[3] 何源, 張冬, 尹棟, 等. 冠狀動脈分叉病變介入治療中分支閉塞風險模型及評分系統的研究. 中國循環雜志, 2015, 30: 827-832.
[4] Grundeken MJ, Ishibashi Y, Ramcharitar S, et al. The need for dedicated bifurcation quantitative coronary angiography (QCA)software algorithms to evaluate bifurcation lesions. EuroIntervention,2015, 11(Suppl V): V44-49.
[5] Louvard Y, Medina A, Stankovic G. Definition and classification of bifurcation lesions and treatments. EuroIntervention, 2010, 6(Suppl J):J31-35.
[6] Janssen JP, Rares A, Tuinenburg JC, et al. New approaches for the assessment of vessel sizes in quantitative (cardio-)vascular X-ray analysis. Int J Cardiovasc Imaging, 2010, 26: 259-271.
[7] Landis JR, Koch GG. The measurement of observer agreement for categorical data. Biometrics, 1977, 33: 159-174.
[8] Cook NR. Use and misuse of the receiver operating characteristic curve in risk prediction. Circulation, 2007, 115: 928-935.
[9] Hosmer DW, Hosmer T, Le Cessie S, et al. A comparison of goodnessof-fit tests for the logistic regression model. Stat Med, 1997, 16: 965-980.
[10] Steyerberg EW, Vickers AJ, Cook NR, et al. Assessing the performance of prediction models: a framework for traditional and novel measures.Epidemiology, 2010, 21: 128-138.
[11] Dou K, Zhang D, Xu B, et al. An angiographic tool for risk prediction of side branch occlusion in coronary bifurcation intervention: the RESOLVE score system (Risk prEdiction of Side branch OccLusion in coronary bifurcation interVEntion). JACC Cardiovasc Interv, 2015, 8:39-46.
[12] Koo BK, Waseda K, Kang HJ, et al. Anatomic and functional evaluation of bifurcation lesions undergoing percutaneous coronary intervention. Circ Cardiovasc Interv, 2010, 3: 113-119.
[13] 劉倩倩, 張冬, 楊浩瀚, 等. 血管分叉角度對冠狀動脈分叉病變介入治療中分支血管閉塞的影響. 中國循環雜志, 2016, 31: 108-112.
[14] Girasis C, Onuma Y, Schuurbiers JC, et al. Validity and variability in visual assessment of stenosis severity in phantom bifurcation lesions: a survey in experts during the fifth meeting of the European Bifurcation Club. Catheter Cardiovasc Interv, 2012, 79: 361-368.
[15] Shin DH, Koo BK, Waseda K, et al. Discrepancy in the assessment of jailed side branch lesions by visual estimation and quantitative coronary angiographic analysis: comparison with fractional flow reserve. Catheter Cardiovasc Interv, 2011, 78: 720-726.
[16] Nallamothu BK, Spertus JA, Lansky AJ, et al. Comparison of clinical interpretation with visual assessment and quantitative coronary angiography in patients undergoing percutaneous coronary intervention in contemporary practice: the Assessing Angiography (A2) project.Circulation, 2013, 127: 1793-1800.
Scoring System for Predicting the Risk of Side Branch Occlusion Based on Angiographic Visual Estimation in Coronary Bifurcation Intervention
HE Yuan, ZHANG Dong, CHEN Chang-zhe, SONG Chen-xi, YIN Dong, FENG Lei, ZHU Cheng-gang, XU Bo, DOU Ke-fei.
Department of Cardiology, National Center for Cardiovascular Disease and Fuwai Hospital, CAMS and PUMC, Beijing (100037),China
DOU Ke-fei, Email: fwdoukefei@126.com
Objective: To establish a scoring system for predicting the risk of side branch occlusion(SBO) in coronary bifurcation intervention based on visual estimation of quantitative coronary angiography (QCA).
Methods: RESOLVE scoring system was developed from QCA. A total of 1 545 patients with 1 601 bifurcation lesions by RESOLVE study were enrolled. Based on RESOLVE scoring system, visual estimation was conducted to compare the consistency. According to SBO occurrence after main branch stent implantation, our research was divided into 2 groups: SBO group, which was defined by coronary angiography confirmed TIMI grade decreasing, n=114 patients with 118 lesions and Non-SBO group, n=1 431 patients with 1 483 lesions. Using RESOLVE scoring method as reference,V-RESOLVE scoring system was established, the discrimination, goodness-of-fit and V-RESOLVE score for the incidence of SBO were assessed;the diagnostic value for predicting the risk of SBO in coronary bifurcation intervention was compared between 2 scoring systems.
Results: The consistency between visual and QCA was from fair to moderate (weighted Kappa=0.22-0.44). Compared with Non-SBO group, SBO group had the higher degrees of pre-operative bifurcation stenosis and side branch stenosis before main branch stent implantation; larger bifurcation angle and vessel diameters in main/side branches, all P<0.01. The area of V-RESOLVE under ROC curve was 0.76(95%CI 0.71-0.81) which was similar to the area of RESOLVE under ROC curve:0.77 (95% CI 0.72-0.81), P=0.74, Hosmer-Lemeshow P=0.17. The patients were categorized into 2 conditions by V-RESOLVE: high risk (V-RESOLVE score≥12)and non-high risk (V-RESOLVE score<12), the incidence of SBO was higher in high risk patients (16.7% vs 4.3%), P<0.01. The incidences of SBO were similar in non-high risk patients by V-RESOLVE and RESOLVE (4.3% vs 3.4%), P=0.22 and in high risk patients (16.7% vs 18.0%), P=0.60.
Conclusion: V-RESOLVE scoring system may predict the risk of SBO in patients with coronary bifurcation intervention.
Coronary artery disease; Risk assessment; Scoring system
首都臨床特色應用研究基金(Z141107002514096);北京協和醫學院“協和青年基金”(3332016130)
100037 北京市,北京協和醫學院 中國醫學科學院 國家心血管病中心 阜外醫院 冠心病診治中心
何源 博士研究生 主要從事心血管內科研究 Email:hey2013yuanh@163.com 通訊作者:竇克非 Email:fwdoukefei@126.com
R54
A
1000-3614(2017)12-1158-05
10.3969/j.issn.1000-3614.2017.12.004
(Chinese Circulation Journal, 2017, 32:1158.)
2017-07-27)
(編輯:朱柳媛)

