英夫利西單抗治療克羅恩病的療效、安全性觀察及影響因素分析Δ
陳禾鳳,楊婉花,姚瑋艷(1.上海交通大學醫學院附屬瑞金醫院藥劑科,上海0005;.上海交通大學醫學院附屬瑞金醫院消化內科,上海 0005)
英夫利西單抗治療克羅恩病的療效、安全性觀察及影響因素分析Δ
陳禾鳳1*,楊婉花1#,姚瑋艷2(1.上海交通大學醫學院附屬瑞金醫院藥劑科,上海200025;2.上海交通大學醫學院附屬瑞金醫院消化內科,上海 200025)
目的:觀察英夫利西單抗(IFX)治療克羅恩病(CD)的療效和安全性,探討其影響因素。方法:采用回顧性研究法,選擇2015年1-12月于我院住院行IFX治療的CD患者120例作為研究對象。所有患者均給予注射用IFX 5 mg/kg靜脈滴注,分別于0、2、6周及以后每隔8周給予相同劑量,持續用藥。比較患者用藥前后的體質量、C反應蛋白(CRP)、紅細胞沉降率(ESR)、白細胞計數(WBC)、內鏡下黏膜愈合情況等療效指標,丙氨酸轉氨酶(ALT)、天冬氨酸轉氨酶(AST)、堿性磷酸酶(AKP)、γ-谷氨酰轉肽酶(γ-GT)、總膽紅素(TB)、直接膽紅素(DB)、尿肌酐(Cr)等肝腎功能指標,以及ADR發生時間、累及器官/系統、臨床表現和轉歸;分析其影響因素。結果:與用藥前比較,患者用藥后的體質量顯著增加,ESR顯著下降,差異均有統計學意義(P<0.05);且二者變化值呈顯著正相關(r=0.275,P=0.016)。78.57%的患者經腸鏡評估示黏膜愈合。患者用藥前后的AST、AKP和Cr比較,雖然差異均有統計學意義(P<0.05),但升高幅度較小,AST均未超過正常值上限2倍,AKP僅1例超過正常值上限2倍,Cr均未超過正常值上限。患者用藥前后的CRP、WBC及其余肝腎功能指標比較,差異均無統計學意義(P>0.05)。24例患者有ADR記錄,發生率為20.00%,累及呼吸、消化、皮膚黏膜、機體防御等器官/系統,多表現為上呼吸道感染、肝功能指標異常等;其中10例(41.67%)因ADR延遲給藥,6例(25.00%)停藥。規律/首次用藥患者的ESR達標率(78.21%)高于有間歇用藥史者(57.14%),但差異無統計學意義(P>0.05);合用美沙拉嗪對患者AST、AKP水平是否上升有顯著影響(P=0.002)。結論:IFX可顯著增加CD患者體質量、降低ESR、改善黏膜愈合情況,療效明確。建議CD患者規律使用IFX。IFX總體安全性良好,但可能引起輸液反應、肝功能指標短暫升高,故輸液期間應嚴密監測患者情況,尤其是對有合并用藥(美沙拉嗪等)的患者應監測肝功能。
英夫利西單抗;克羅恩病;療效;安全性;影響因素
克羅恩病(CD)是一種慢性非特異性疾病,與潰瘍性結腸炎統稱為炎癥性腸病(IBD)。該病好發于青壯年,可累及消化道各部位,臨床表現常見腹痛、腹瀉、腸梗阻,并發癥多,且反復發作、遷延不愈,嚴重影響患者的生存質量。英夫利西單抗(IFX)是首個用于治療CD的生物制劑[1],適用于傳統治療效果不佳的中重度活動性CD和瘺管型CD[2]。自2007年IFX于我國上市,已積累了一部分治療風濕性疾病的臨床觀察報道[3-4],但治療IBD的相關報道有限[5],且以CD患者為研究對象的臨床觀察例數通常較少。本研究回顧性分析了120例IFX治療CD的臨床療效及藥品不良反應(ADR),以期為臨床合理用藥提供依據。
1 資料與方法
1.1 納入與排除標準
納入標準:臨床診斷和用藥方案符合《炎癥性腸病診斷與治療的共識意見(2012年·廣州)》[6]、《英夫利西治療克羅恩病的推薦方案(2011年)》[7]、《建立我國炎癥性腸病診治中心質量控制指標的共識》[8]。
排除標準:有活動性感染、腸道CD合并纖維狹窄性梗阻且不伴有炎性反應活動證據的患者。
1.2 研究對象
按照上述標準,納入2015年1-12月(設為“觀察期”)于我院住院行IFX治療的120例CD患者的病歷。其中,男性79例(65.83%),女性41例(34.17%);年齡≤16歲者11例,17~40歲者99例,>40歲者10例,平均年齡(27.93±8.96)歲;病變部位:回腸末段47例,結腸15例,回結腸58例;25例合并瘺管;2例累及上消化道;31例有IBD相關手術史;2例合并強直性脊柱炎;94例為觀察期內啟用IFX,17例為觀察期前已開始規律應用IFX,9例有間歇給藥史(即觀察期前有IFX用藥史,停藥半年以上,重新按0、2、6周開始給藥);IFX給藥次數為1~8次/人,共計(576±1.46)次,平均(4.81±1.46)次/人;有52例患者同時聯用美沙拉嗪、硫唑嘌呤、甲氨蝶呤或糖皮質激素等其他IBD治療藥物,其中43例聯合1種藥物、7例聯合2種藥物、2例聯合3種藥物。
1.3 治療方法
所有患者均給予注射用IFX(商品名:類克,荷蘭Janssen Biologics B.V.,注冊證號:S20120012,規格:100 mg/支)5 mg/kg靜脈滴注,分別于0、2、6周及以后每隔8周給予相同劑量,持續用藥。每支藥品用10 mL無菌注射用水溶解,再用0.9%氯化鈉注射液稀釋至250 mL;滴注時間不得少于2 h。
1.4 觀察指標
通過醫院信息系統查閱患者病歷,結合國家《藥品不良反應/事件報告表》,使用Excel 2007軟件記錄患者的性別、年齡、診斷、過敏史、IFX用藥史、合并用藥、IFX給藥次數及每次給藥劑量等一般資料,體質量、C反應蛋白(CRP)、紅細胞沉降率(ESR)、白細胞計數(WBC)、內鏡下黏膜愈合情況等療效指標,丙氨酸轉氨酶(ALT)、天冬氨酸轉氨酶(AST)、堿性磷酸酶(AKP)、γ-谷氨酰轉肽酶(γ-GT)、總膽紅素(TB)、直接膽紅素(DB)、尿肌酐(Cr)等肝腎功能指標,以及ADR發生時間、臨床表現和轉歸。其中,若所測指標值高于正常值上限則標為“異常”,異常率=用藥后指標異常例數/總例數×100%。ADR按現行的《藥品不良反應報告和監測管理辦法》[9]進行相關性及嚴重程度評估。因患者持續用藥,本研究中“用藥后”指的是觀察期內最后一次用藥后。
1.5 統計學方法
采用SPSS 19.0軟件對數據進行統計分析。計量資料以x±s表示,根據是否符合正態分布采用t檢驗或非參數秩和檢驗;計數資料以例數或百分比表示,采用χ2檢驗或Fisher確切概率檢驗;相關性分析采用Pearson和Spearman分析。P<0.05為差異有統計學意義。
2 結果
2.1 療效指標
與用藥前比較,患者用藥后的體質量顯著增加(P<0.001),ESR顯著下降(P=0.018),差異均有統計學意義;用藥前后的CRP和WBC比較,差異均無統計學意義(P>0.05)。相關性分析結果表明,ESR變化值與體質量變化值呈顯著正相關(r=0.275,P=0.016)。CRP、ESR、WBC的異常率從用藥前的25.00%~38.61%下降至用藥后的3.26%~23.53%。14例患者于6次用藥后再次行腸鏡評估,有11例(78.57%)示黏膜愈合。患者用藥前后療效指標比較見表1。
2.2 肝腎功能指標
用藥前,患者肝腎功能指標的異常率僅為0~3.96%;用藥后,除Cr外所有肝腎功能指標的異常率均有上升,為3.03%~9.59%。患者用藥前后的AST(P=0.029)和AKP(P=0.006)比較,差異均有統計學意義;用藥前后的Cr比較,差異雖然也有統計學意義(P=0.010),但均未超過正常值上限(97 μmol/L),故異常率為0;其余肝腎功能指標比較,差異均無統計學意義(P>0.05),詳見表2。
2.3 ADR
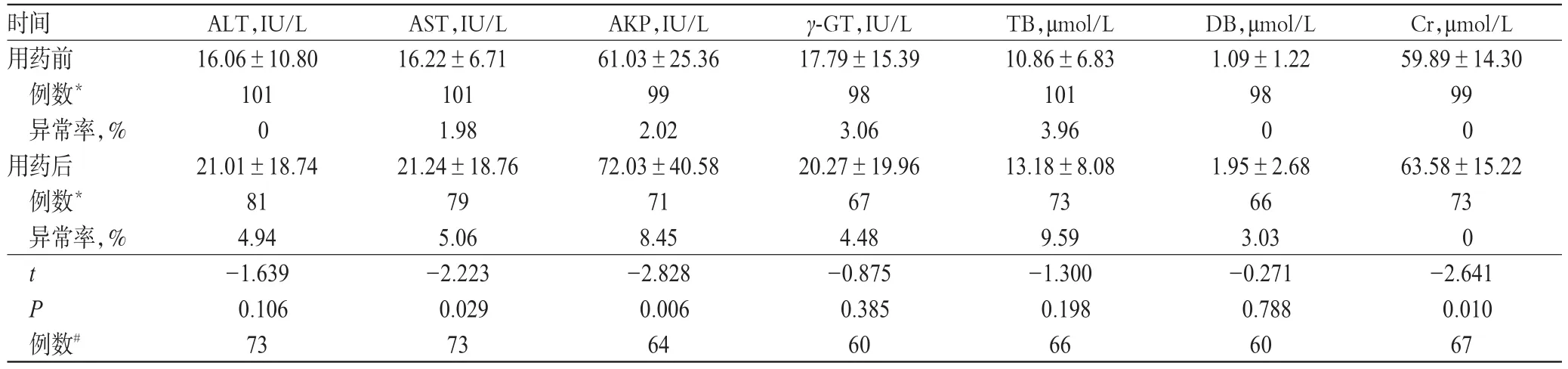
表2 患者用藥前后肝腎功能指標比較(x±s)Tab 2Comparison of liver and renal function indexes before and after medication(x±s)
2.3.1 基本情況 24例患者的病歷中有ADR記錄,發生率為20.00%(24/120)。其中,在第2、3次用藥后有10例(41.67%)患者發生ADR,在第1、5次用藥后各有4例(16.67%)患者發生ADR,其他ADR發生時間分別為第4次(3例,12.50%)、第6次(2例,8.33%)、第9次(1例,4.17%)用藥后;有7例(29.17%)ADR在用藥后1 d內發生。ADR臨床表現涉及呼吸、消化、皮膚黏膜、機體防御等器官/系統,詳見表3。
2.3.2 臨床轉歸 24例發生ADR的患者中,10例(41.67%)因ADR而延遲給藥,6例(25.00%)停藥[其中5例為皮膚黏膜及心血管系統相關ADR(20.83%)]。5例(20.83%)未作處理自行好轉;19例(79.17%)使用藥物對癥處理,其中5例(20.83%)因ADR住院檢查、治療或留院觀察,延長住院時間1~18 d。經處理后,患者ADR癥狀均較前有所改善,復查指標基本恢復正常;僅有1例存在反復血壓波動,出院后經門診隨訪治療后病情穩定。
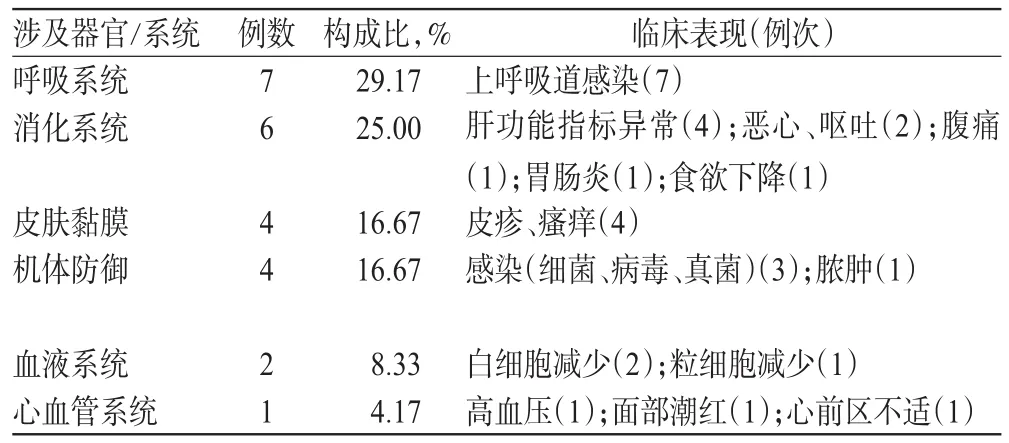
表3 IFX致ADR累及器官/系統及臨床表現Tab 3 Organs/systems involved in IFX-induced ADR and clinical manifestations
2.4 影響因素分析
ESR、體質量及肝腎功能影響因素分析結果分別見表4、表5。由表4可知,雖然差異無統計學意義(P>0.05),但規律/首次用藥患者的ESR達標率為78.21%(61/78),高于有間歇用藥史者(57.14%,4/7);規律/首次用藥患者的體質量增加率也較有間歇用藥史者更高[72.73%(80/110)vs.44.44%(4/9)]。由表5可知,合用美沙拉嗪對患者AST、AKP水平是否上升有顯著影響(P=0.002),其他因素對患者肝腎功能的影響不顯著。
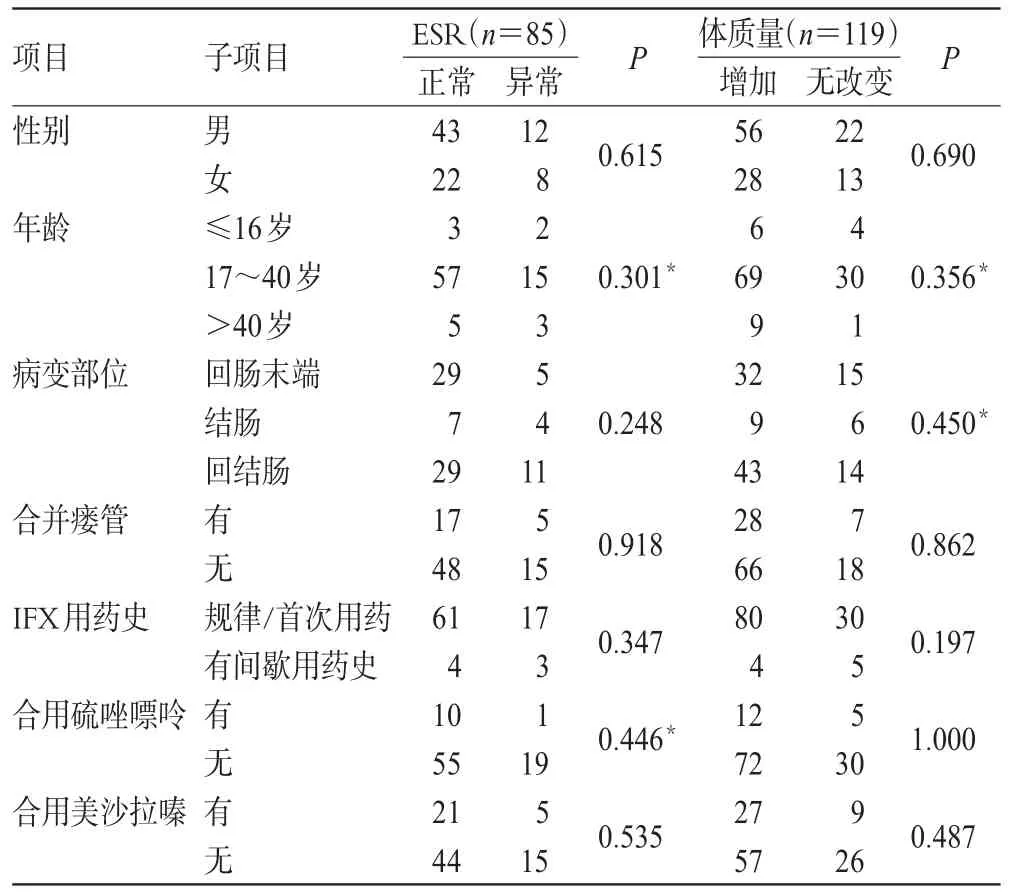
表4 ESR、體質量影響因素分析結果Tab 4 Analysis results of influential factors of ESR and body weight
3 討論
ACCENTⅠ、ACCENTⅡ、REACH等多個大型臨床試驗及國內外多項臨床研究已證實IFX對CD的緩解率可達36%~88%[10-11]。CRP、ESR、WBC等炎癥指標作為評估CD活動度的重要參數[6],被臨床廣泛應用。本研究結果顯示,患者應用IFX后,CRP、ESR、WBC的異常率從用藥前的25.00%~38.61%下降至用藥后的3.26%~23.53%,與既往研究[10]結果基本一致。營養不良是CD常見的全身癥狀,本研究中患者應用IFX后,體質量明顯增加,且與ESR下降呈顯著正相關,進一步證明了IFX的療效。此外,內鏡下黏膜是否愈合是CD治療效果的客觀評價指標[12],本研究中78.57%的患者可達到黏膜愈合,充分證實了IFX可促進腸道黏膜愈合、改善臨床癥狀。
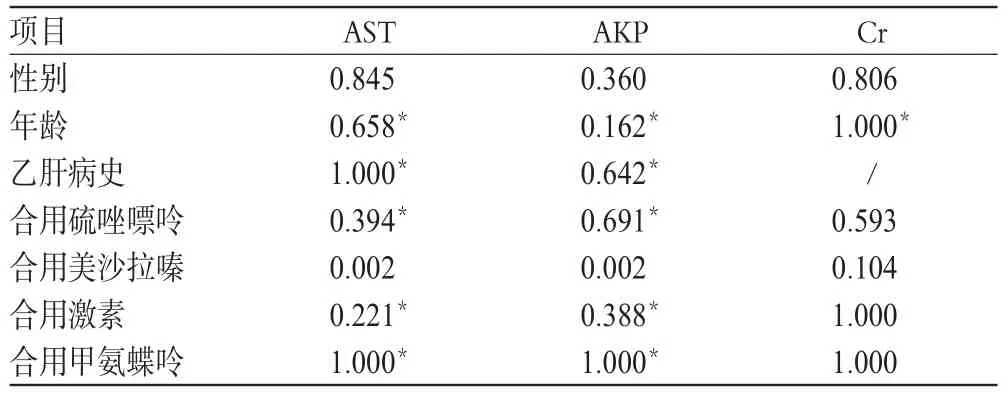
表5 肝腎功能影響因素分析結果(P)Tab 5 Analysis result of influential factors for liver and renal function(P)
IFX是人鼠嵌合免疫球蛋白(Ig)G1分子,可引發免疫原性,形成抗體,中和IFX的生物學效應。國外研究顯示,經IFX規律治療的患者腸道較有間歇用藥史者的黏膜愈合率更高、手術率更低且生存質量更高[13-14]。因本研究中有間歇用藥史者的樣本量有限,故未進一步分析其與內鏡下腸道黏膜愈合的相關性。但據報道,約8%~60%的IBD患者在用藥過程中(尤其是間斷按需給藥時)會產生抗體[15],而當抗IFX抗體(ATI)存在時,IFX的清除率將提高2.7倍[16]。因此,有間歇用藥史者可能因產生更多的抗體而影響療效。本研究結果顯示,雖然差異無統計學意義,但規律/首次用藥患者的ESR達標率和體質量增加率均較有間歇用藥史者更高。然而IFX作為生物制劑,價格昂貴,考慮到患者的經濟負擔,按療程間歇給藥在國內并不少見,臨床在權衡利弊時應充分考慮藥物療效、產生抗體風險及患者的經濟水平。
輸液反應、感染、肝毒性等是IFX常見的ADR,甚至可導致停藥[17]。本研究觀察期間發生24例ADR,主要包括感染、肝功能指標異常及皮膚黏膜的輸液反應,ADR構成比及表現與既往研究[3-5]結果類似。其中,皮膚黏膜及心血管系統相關ADR均為給藥后速發型輸液反應,占所發生ADR的20.83%,與國內外約20%的總體發生率[18]相近。雖然例數僅為5例,但均導致患者停用IFX,對疾病治療造成影響。因此,輸液期間及輸液后均需對患者進行監護,如有異常,及時處理。
單抗藥物可使免疫調節細胞和肝細胞因子功能表達異常,引起細胞因子釋放綜合征,導致肝功能指標暫時升高[19]。本研究中,患者用藥前后的AST、AKP和Cr比較,雖然差異均有統計學意義,但升高幅度較小,AST均未超過正常值上限的2倍,AKP僅1例超過正常值上限2倍,Cr均未超過正常值上限,肝損傷分級屬于1級(輕度肝損傷)[20],經口服保肝藥治療后轉歸較好,未影響IFX給藥。影響因素分析結果顯示,合用美沙拉嗪對患者AST、AKP水平是否上升有顯著影響。肝功能指標異常是IFX常見的ADR之一,美沙拉嗪、硫唑嘌呤等CD治療藥物也可能引起轉氨酶升高[18],因此對于同時使用IFX及美沙拉嗪等的患者,尤其是長期用藥患者,應加強肝功能監測,以保障用藥安全。
IFX可抑制機體體液免疫、細胞免疫和天然免疫,增加CD患者感染風險,主要為嚴重細菌感染、機會性感染。本研究中所有患者用藥前均已經過詳細體檢、X光片、T-Spot檢查及乙/丙型肝炎病毒檢查,期間未發現結核及肝炎復發,主要發生的感染事件為上呼吸道感染,治療后均恢復正常。有研究表明,年齡(≥65歲)是IBD患者使用生物制劑發生嚴重感染的高危因素[21],提示治療期間應密切監測患者情況,嚴格把握給藥指征。
綜上所述,IFX可顯著增加CD患者的體質量、降低ESR、改善黏膜愈合情況,療效明確。建議CD患者應規律使用IFX,以保證療效。為保障用藥安全,給藥前應對患者進行活動性感染篩查,輸液過程中嚴密監測患者情況;除了少見且嚴重的輸液反應外,每次用藥前需監測患者的血常規、肝腎功能;對有合并用藥(美沙拉嗪等)的患者更應密切跟蹤肝功能指標變化。下一步研究可完善療效評估指標、擴大樣本量,對IFX長期療效及安全性的影響因素及相關性進行深入探討。
[1]Brynskov J,Nielsen OH,Ahnfelt-Ronne I,et al.Cytokines(immunoinflammatory hormones)and their natural regulation in inflammatory bowel disease(Crohn’s disease and ulcerative colitis):a review[J].Dig Dis,1994,12(5):290-304.
[2]Derkx B,Taminiau J,Radema S,et al.Tumour-necrosisfactor antibody treatment in Crohn’s disease[J].Lancet,1993,342(8864):173-174.
[3]李峰,晉紅中.119例英夫利西單抗不良反應的文獻分析[J].中國藥物警戒,2016,13(4):229-232.
[4]馮莉霞,朱劍,張江林,等.英夫利西單抗治療風濕性疾病的安全性評價[J].中國藥房,2015,26(17):2356-2358.
[5]范如英,盛劍秋,陸曉娟,等.英夫利西單抗對炎癥性腸病的療效及安全性分析[J].胃腸病學和肝病學雜志,2013,22(9):898-900.
[6]中華醫學會消化病學分會炎癥性腸病學組.炎癥性腸病診斷與治療的共識意見:2012年·廣州[J].中華內科雜志,2012,51(10):818-831.
[7]中華醫學會消化病學分會炎癥性腸病學組.英夫利西治療克羅恩病的推薦方案:2011年[J].中華消化雜志,2011,31(12):822-824.
[8]中華醫學會消化病學分會炎癥性腸病學組.建立我國炎癥性腸病診治中心質量控制指標的共識[J].中華內科雜志,2016,55(7):568-571.
[9]衛生部.藥品不良反應報告和監測管理辦法[S].2011-05-04.
[10]Nanda KS,Cheifetz AS,Moss AC.Impact of antibodies to infliximab on clinical outcomes and serum infliximab levelsin patientswith inflammatory boweldisease(IBD):a meta-analysis[J].Am J Gastroenterol,2013,108(1):40-47.
[11]宓林,于曉峰,鄒健.英夫利昔治療炎癥性腸病的國內研究系統回顧[J].國際消化病雜志,2013,33(4):279-282.
[12]Baert F,Moortgat L,Van Assche G,et al.Mucosal healing predicts sustained clinical remission in patients with early-stage Crohn’s disease[J].Gastroenterology,2010,138(2):463-468.
[13]Rutgeerts P,Diamond RH,Bala M,et al.Scheduled maintenance treatment with infliximab is superior to episodic treatment for the healing of mucosal ulceration associated with Crohn’s disease[J].Gastrointest Endosc,2006,63(3):433-442.
[14]Lichtenstein GR,Yan S,Bala M,et al.Remission in patients with Crohn’s disease is associated with improvement in employment and quality of life and a decrease in hospitalizations and surgeries[J].Am J Gastroenterol,2004,99(1):91-96.
[15]Ben-Horin S,Mazor Y,Yanai H,et al.The decline of anti-drug antibody titres after discontinuation of anti-TNFs:implications for predicting re-induction outcome in IBD[J].Aliment Pharmacol Ther,2012,35(6):714-722.
[16]Ternant D,Aubourg A,Magdelaine-Beuzelin C,et al.Infliximab pharmacokinetics in inflammatory bowel disease patients[J].Ther Drug Monit,2008,30(4):523-529.
[17]周有連,陳燁.英夫利昔單抗治療炎癥性腸病的療效及影響因素分析[J].南方醫科大學學報,2013,33(12):1833-1838.
[18]周笑甜,冉志華.英夫利昔單抗治療炎癥性腸病的研究進展[J].胃腸病學,2009,14(11):691-694.
[19]黃奇,繆應雷.炎癥性腸病中藥物性肝損傷的研究進展[J].胃腸病學和肝病學雜志,2014,23(7):727-730.
[20]于樂成,茅益民,陳成偉.藥物性肝損傷診治指南[J].臨床肝膽病雜志,2015,31(11):1752-1769.
[21]Cottone M,Kohn A,Daperno M,et al.Advanced age is an independent risk factor for severe infections and mortality in patients given anti-tumor necrosis factor therapy for inflammatory bowel disease[J].Clin Gastroenterol Hepatol,2011,9(1):30-35.
Efficacy and Safety Observation of Infliximab in the Treatment of Crohn’s Disease and Analysis of Influential Factors
CHEN Hefeng1,YANG Wanhua1,YAO Weiyan2(1.Dept.of Pharmacy,Ruijin Hospital,Shanghai Jiaotong University School of Medicine,Shanghai 200025,China;2.Dept.of Gastroenterology,Ruijin Hospital,Shanghai Jiaotong University School of Medicine,Shanghai 200025,China)
OBJECTIVE:To observe therapeutic efficacy and safety of infliximab(IFX)in the treatment of Crohn’s disease(CD),and to investigate its influential factors.METHODS:In retrospective study,a total of 120 CD patients
IFX treatment in our hospital during Jan.-Dec.2015 were selected as research objects.All patients were given IFX for injection 5 mg/kg intravenously at 0,2nd,6th week and later every 8 weeks continously.Therapeutic efficacy indexes(body weight,CRP,ESR,WBC,mucosal healing under endoscope),liver and renal indexes(ALT,AST,AKP,γ-GT,TB,DB,Cr),the occurrence time of ADR,organs/systems involved,clinical manifestations and outcomes were compared before and after treatment.Influential factors were analyzed.RESULTS:Compared with before medication,body weight of patients were increased significantly,while ESR were decreased significantly,with statistical significance(P<0.05).There was positively correlation between above two indexes(r=0.275,P=0.016).Mucosal healing was found in 78.57%of patients by colonoscopy.There was statistical significance in the levels of AST,AKP and Cr before and after treatment(P<0.05),but those indexes were increased slightly.AKP exceeded 2 times the upper limit of normal value in only 1 case,but AST did not exceed 2 times the upper limit of normal limit,Cr did not exceed the upper limit of normal value.There was no statistical significance in CRP,WBC or other liver and renal function indexes before and after treatment(P>0.05).There were 24 cases of ADR with incidence of 20.00%.Respiratory system,digestive system,skin mucous membrane,body defense and other organs/systems were involved,mainly manifestating as uper respiratory tract infetion,liver function indexes order etc.Ten patients(41.67%)delayed the treatment,and 6 cases(25.00%)discontinued.Standard rate of ESR in patients with regular/primary medication(78.21%)was higher than those with intermittent medication history(57.14%),but without statistical significance(P>0.05).Combined use of mesalazine had no significant effect on the increase of AST and AKP(P=0.002).CONCLUSIONS:IFX significantly increases body weight of CD patients,decreases ESR and improves mucosal healing.It shows definite therapeutic efficacy.It is suggested that CD patients should use IFX regularly.The overall safety of IFX is good,but it may cause transfusion reaction and transient increase of liver function index.So,the patient’s condition should be closely monitored during the infusion.[especially for liver function of those with drug combination(mesalazine,etc.)]
Infliximab;Crohn’s disease;Therapeutic efficacy;Safety;Influential factor
R969.3
A
1001-0408(2017)35-4947-05
DOI10.6039/j.issn.1001-0408.2017.35.14
上海市臨床藥學重點專科建設項目
*主管藥師,碩士研究生。研究方向:臨床藥學。電話:021-64370045。E-mail:chf40626@rjh.com.cn
#通信作者:主任藥師,碩士生導師,碩士。研究方向:臨床藥學。電話:021-64370045。E-mail:yangwanhuaxy@163.com
2017-02-09
2017-05-10)
(編輯:胡曉霖)

