QuEChERS結合超高效液相色譜-串聯質譜法同時測定番茄中噻蟲嗪、噻蟲胺、螺蟲乙酯及其代謝物殘留
劉 炎,歐陽迪慶,葉玉鳳,王成秋,焦必寧,趙其陽,張耀海,敖 艷,王海燕
(1.農業部柑桔產品質量安全風險評估實驗室(重慶),中國農業科學院柑桔研究所/西南大學柑桔研究所,重慶 400712;2.西南大學 食品科學學院,重慶 400715;3.農業部柑桔及苗木質量監督檢驗測試中心,重慶 400712;4.國家柑桔工程技術研究中心,重慶 400712;5.柑桔學重慶市重點實驗室,重慶 400712;6.重慶市畜牧科學院,重慶 402460)
QuEChERS結合超高效液相色譜-串聯質譜法同時測定番茄中噻蟲嗪、噻蟲胺、螺蟲乙酯及其代謝物殘留
劉 炎1,3,歐陽迪慶1,3,葉玉鳳1,3,王成秋1,2,3,4*,焦必寧1,2,3,4,5*,趙其陽1,3,張耀海1,3,敖 艷2,3,王海燕6
(1.農業部柑桔產品質量安全風險評估實驗室(重慶),中國農業科學院柑桔研究所/西南大學柑桔研究所,重慶 400712;2.西南大學 食品科學學院,重慶 400715;3.農業部柑桔及苗木質量監督檢驗測試中心,重慶 400712;4.國家柑桔工程技術研究中心,重慶 400712;5.柑桔學重慶市重點實驗室,重慶 400712;6.重慶市畜牧科學院,重慶 402460)
建立了QuEChERS-UPLC-MS/MS法快速同時檢測番茄中噻蟲嗪及其代謝產物(噻蟲胺)、螺蟲乙酯及其4種代謝產物(BYI08330-enol-glucoside、BYI08330-mono-hydroxy、BYI08330-enol和BYI08330-ketohydroxy)殘留的分析方法。樣品經乙腈提取,NaCl和無水MgSO4除水后,經N-丙基乙二胺(PSA)和C18粉末凈化,用超高效液相色譜-串聯質譜(UPLC-MS/MS)分析,采用多反應離子監測模式(MRM)檢測,基質匹配標準溶液外標法定量。7種目標物質在0.2~2 000 μg/L質量濃度范圍內均具有良好的線性關系(r2≥0.999 2),在0.002、0.02、0.20、2.00 mg/kg 加標水平下的平均回收率為79.9%~104%,相對標準偏差(RSD)為0.94%~6.4%,方法定量下限(LOQ)為0.002 mg/kg。該方法快速簡便、靈敏度高、重現性好,能滿足番茄中噻蟲嗪、噻蟲胺和螺蟲乙酯及其代謝產物殘留的快速檢測和確證要求。
QuEChERS法;超高效液相色譜-串聯質譜法;農藥殘留;番茄
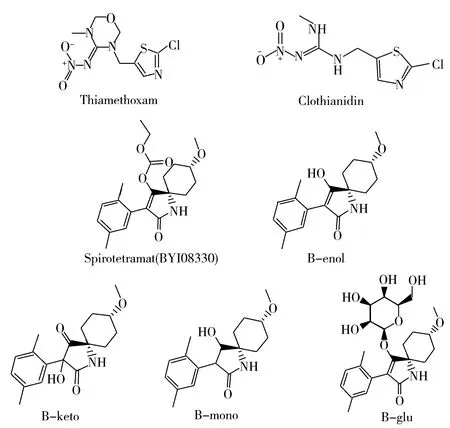
圖1 噻蟲嗪、噻蟲胺、螺蟲乙酯及其代謝物的結構Fig.1 Structures of thiamethoxam,clothianidin,spirotetramat and its metabolites
番茄(SolanumlycopersicumL.)是世界第一大蔬菜作物,我國的番茄產量約占世界的1/3[1]。隨著全球氣候變化、結構調整和設施農業的快速發展,煙粉虱在番茄上的危害逐年增加,造成其傳播的番茄黃化曲葉病毒病日益加重[2]。目前主要采用化學法防治煙粉虱,但吡蟲啉等常規殺蟲劑會造成抗藥性,因此廣譜、高效、低毒、安全的新型殺蟲劑正逐漸受到關注。根據中國農藥信息網的數據,噻蟲嗪、噻蟲胺以及螺蟲乙酯已被登記用于防治番茄上的煙粉虱。
噻蟲嗪、噻蟲胺、螺蟲乙酯及其代謝物(結構式見圖1)作為高毒農藥的替代品種,可有效防治半翅目、鞘翅目和某些鱗翅目害蟲。毒理研究表明:噻蟲嗪、噻蟲胺對哺乳動物、鳥類和水生生物具有低毒性,對蜜蜂具有高毒性[3];螺蟲乙酯的主要代謝產物對鳥類和哺乳動物具有低急性和短期毒性,其代謝物的毒性均等于或低于母體化合物;也有研究表明,大鼠的雄性生殖毒性可能是由代謝物B-enol引起[4]。由于噻蟲嗪在植物體內可轉化為噻蟲胺,所以JMPR評估報告中噻蟲嗪的膳食評估殘留物包括噻蟲嗪和噻蟲胺[3],螺蟲乙酯的膳食評估殘留物包括螺蟲乙酯、B-enol、B-glu、B-mono和B-keto[4]。我國規定番茄中噻蟲胺的最大殘留限量為1 mg/kg,但尚未制定噻蟲嗪的限量標準;規定番茄中螺蟲乙酯及其烯醇類代謝產物的臨時最大殘留限量為1 mg/kg[5],但未包括螺蟲乙酯其他的代謝物殘留。
目前國內外測定噻蟲嗪、噻蟲胺和螺蟲乙酯殘留主要采用液相色譜法(HPLC)[6-7]和液相色譜-質譜法(LC-MS)[8-12]等,也有較少關于氣相色譜法(GC)[13-15]和氣相色譜-質譜法(GC-MS)[16]的報道,前處理方法大多采用固相萃取法(SPE),也有研究采用QuEChERS方法。但尚未見同時檢測番茄中噻蟲嗪、噻蟲胺和螺蟲乙酯及其4種代謝物的方法報道。因此,研究建立高效準確、同時測定以上幾種農藥殘留的檢測方法,對于保障食品安全、進行農藥安全性評價具有重要意義。
本研究以改進的QuEChERS結合UPLC-MS/MS技術,建立了快速檢測番茄中的噻蟲嗪、噻蟲胺和螺蟲乙酯及其代謝物等7種殺蟲劑殘留的分析方法。重點對樣品量和凈化條件等進行了優化,并將此方法應用于柑橘、節瓜、蘋果和茄子中上述殺蟲劑殘留的測定。本方法簡單方便、易于操作,能夠滿足番茄中噻蟲嗪、噻蟲胺和螺蟲乙酯及其代謝物殘留量快速檢測和確證的要求,并為我國制定噻蟲嗪和螺蟲乙酯的代謝物在番茄中的最大殘留限量提供參考依據。
1 實驗部分
1.1 儀器、試劑與樣品
Agilent 1290-6495液相色譜串聯質譜儀(美國Agilent公司);Milli-Q A10 超純水儀(美國Millipore公司);CL31/CL31R 多用途離心機(美國Thermo Fisher公司);KQ5200DE型數控超聲波清洗器(昆山市超聲儀器有限公司)等。
標準品:噻蟲嗪(純度99.0%),噻蟲胺(純度99.0%),螺蟲乙酯(BYI08330,純度98.5%),B-glu(純度98.6%),B-mono(純度98.2%),B-enol(純度99.6%),B-keto(純度94.8%),均購于德國Dr.Ehrenstorfer GmbH;乙腈、甲醇(色譜純,德國CNW Technologies GmbH);N-丙基乙二胺(PSA,德國 CNW Technologies GmbH );超純反相C18填料(加拿大SiliCycle公司);氯化鈉和無水硫酸鎂(分析純,國藥集團化學試劑有限公司);甲酸(分析純,重慶川東化工有限公司)。
番茄、柑橘、節瓜、蘋果、茄子樣品購于當地超市。
1.2 實驗方法
1.2.1超高效液相色譜條件色譜柱:Agilent ecipes plus C18液相色譜柱(1.8 μm,2.1 mm×50 mm);柱溫40 ℃;流動相:0.1%甲酸水溶液(A)-甲醇(B);梯度洗脫程序:0~0.2 min,10% B;0.2~6.0 min,10%~90% B;6.0~8.0 min,90% B;8.0~8.1 min,90%~10% B;8.1~9.0 min,10% B。進樣量:3 μL;流速:0.3 mL/min。
1.2.2質譜條件離子化模式:電噴霧離子源,正離子模式(ESI+);質譜掃描方式:多反應監測(MRM);干燥氣溫度250 ℃,干燥氣流速14 L/min,氮氣壓力30 psi,鞘氣溫度375 ℃,鞘氣流速12 L/min,毛細管電壓4 000 V,噴嘴電壓500 V,iFunnel parameters高壓為200 V,低壓100 V。7種農藥的監測離子、錐孔電壓、碰撞能量等質譜參數如表1所示。
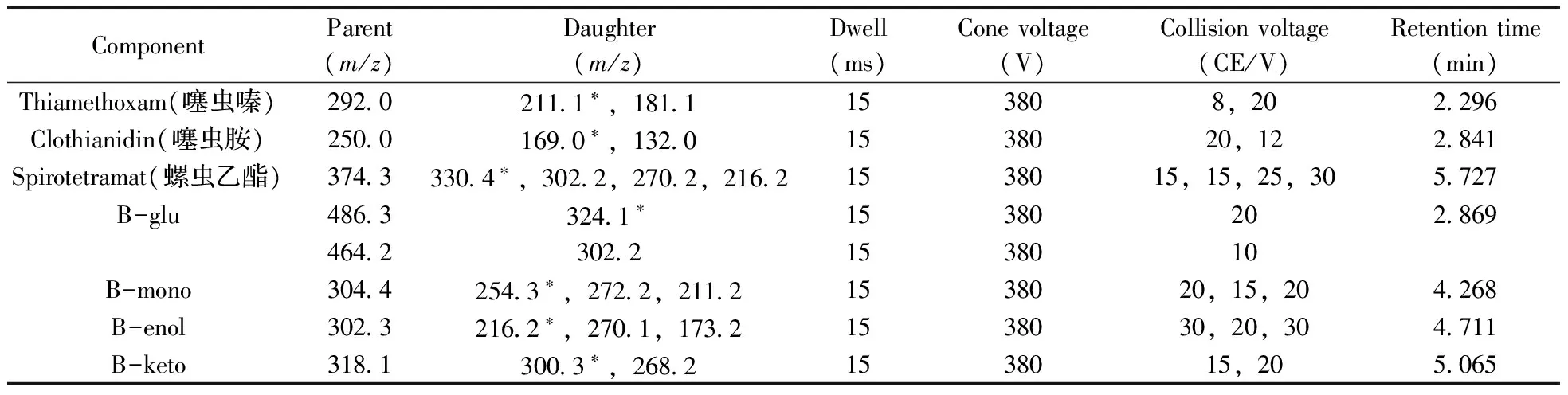
表1 7種農藥的串聯質譜測定參數Table 1 MS /MS parameters for the seven pesticides
* quantification ion
1.2.3標準溶液的配制標準工作液:分別準確稱取 10 mg(精確至 0.01 mg) 農藥標準品,用甲醇溶解并定容至10.0 mL,配成1 000 mg/L標準工作液,于-50 ℃避光保存。用甲醇將標準儲備液逐級稀釋配成2、1、0.5、0.1、0.05、0.01、0.005、0.001、0.000 2 mg/L的 7種農藥的系列混合標準溶液,置于-50 ℃保存。
基質空白標準溶液:以不含7種農藥的番茄果實為材料,利用本實驗前處理方法制備番茄的基質空白溶液。分別移取適量的 20、10、5、1、0.5、0.1、0.05、0.01、0.002 mg/L 的混合標準溶液,用基質空白溶液稀釋成一系列質量濃度為 2、1、0.5、0.1、0.05、0.01、0.005、0.001、0.000 2 mg/L的基質空白標準溶液,在優化條件下測定,分別得到番茄中7種農藥的標準曲線。
1.2.4樣品前處理方法準確稱取5.00 g(精確至0.01 g) 番茄勻漿樣品于50 mL離心管中,加入5.00 mL乙腈,超聲波提取20 min,加入2.0 g MgSO4和0.5 g NaCl,劇烈振搖1 min,10 000 r/min離心5 min。取上清液2 mL轉入已加有25 mg PSA和25 mg C18的4 mL 聚四氟乙烯離心管中,振蕩混合1 min,3 000 r/min離心5 min。取上清液過0.22 μm有機濾膜,濾液經 UPLC-MS/MS分析。
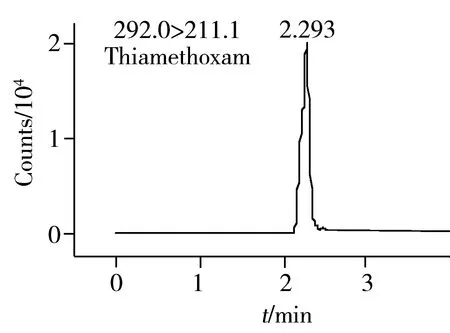
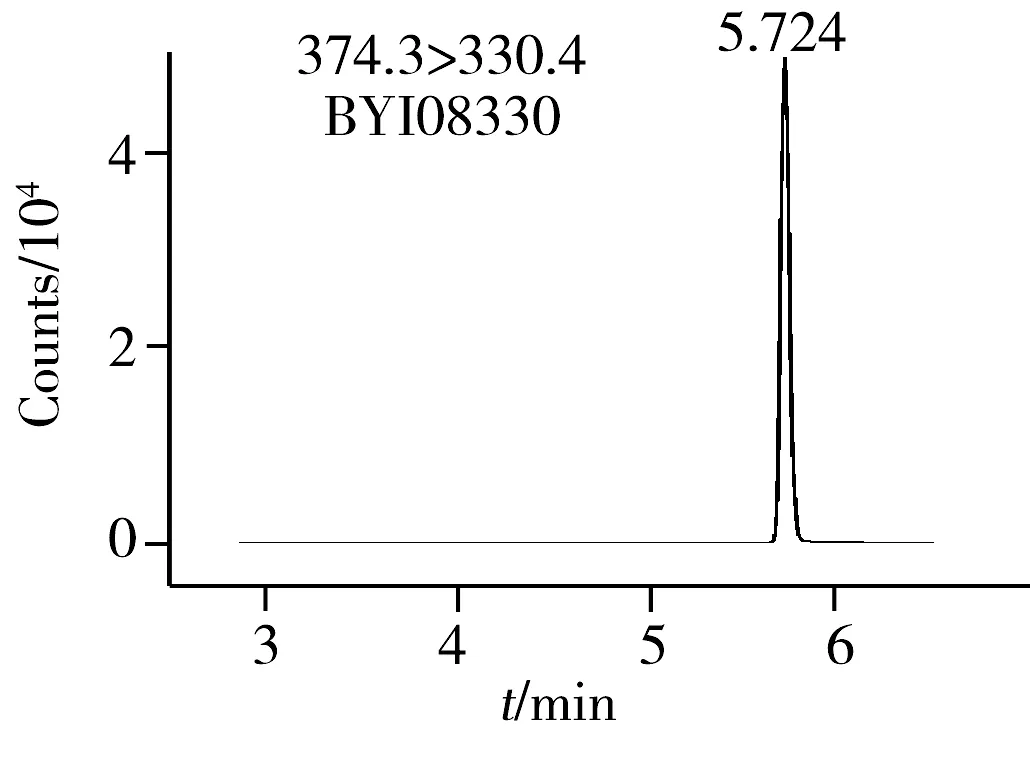

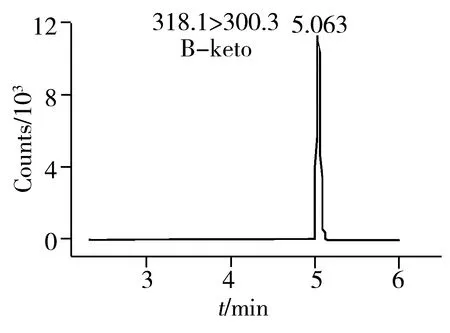
圖2 0.2 mg/L 7種農藥的UPLC-MS/MS MRM色譜圖Fig.2 UPLC-MS/MS MRM chromatograms of 7 pesticides

圖3 不同樣品量對番茄中噻蟲嗪和螺蟲乙酯及其代謝物加標回收率的影響Fig.3 Effects of different sample amounts on the recovery of thiamethoxam and spirotetramat and their metabolites in tomato
2 結果與討論
2.1 色譜條件優化
選擇Agilent ecipes plus C18(1.8 μm,2.1 mm×50 mm)色譜柱進行分離,在優化色譜條件下,以含0.1%甲酸的純水溶液和純甲醇溶液為流動相可獲得較好的分離度及較高的響應值,各種農藥的保留時間見表1。圖2為0.2 mg/L番茄基質標準溶液的MRM離子色譜圖。
2.2 前處理條件的優化
2.2.1稱樣量QuEChERS方法中,稱樣量一般為10.0 g[17-19],本實驗考察了稱樣量(3.0、5.0、10.0 g)對7種農藥回收率的影響,實驗結果見圖3。結果表明,稱樣量過少或過多均會影響回收率;當稱樣量為5.0 g時,7種農藥的回收率均最佳。隨著稱樣量的增加,有機溶劑等試劑耗材的成本也會增加,因此本實驗選取最佳稱樣量為5.0 g。
2.2.2吸附劑PSA去除有機酸的效果較好,但去除色素、甾醇和維生素的效果一般;C18去除維生素、色素和甾醇的能力較好,但對少部分農藥有一定的吸附。歐盟[20]和AOAC[21]在QuEChERS方法中,一般采用1 mL提取上清液中加入25 mg PSA或25 mg C18。本實驗比較了單一PSA和C18以及PSA-C18混合對回收率的影響。結果表明,對單一PSA而言,B-mono和B-enol的回收率會隨著吸附劑用量的增加而提高,其他農藥則相反,但PSA的最小使用量為50 mg時,螺蟲乙酯、B-glu、B-enol和B-keto的回收率均低于70%。對單一C18而言,7種農藥的回收率基本隨著吸附劑用量的增加而升高,但C18的最大使用量為100 mg時,B-glu的回收率仍不足70%。Li等[8]指出,PSA量對農藥的回收率產生負面影響,即隨著PSA添加量的增加目標物的回收率會有所下降;GCB和C18的用量對目標物的提取效率沒有顯著影響。當使用PSA-C18混劑后,B-mono和B-enol的回收率會隨著添加量的增加先升高后降低,而其他農藥的回收率反而降低;當PSA+C18為25 mg+25 mg時,所有目標物的回收率均可達到70%~110%。因此,本實驗選擇加入25 mg PSA 和25 mg C18的混合凈化劑。
2.3 基質效應
基質效應是由共洗脫基質組分引起的分析信號的抑制或增強現象,已被廣泛研究并被認為是食品樣品LC-MS/MS定量分析中的誤差源[22]。本研究使用基質匹配的校準標準物來補償基質溶液中目標農藥的基質效應。計算基質效應的公式如下:

ME為正值表明基質效應增強,反之減弱。一般當基質效應增強或抑制超過10%,則認為基質效應對定量檢測具有顯著影響,不可忽略[10]。從表2可看出,除了B-glu和B-mono外(|ME|<10%),其余5種農藥的ME絕對值均大于10%,表明這5種農藥的基質減弱效應明顯。為確保結果的準確性,本文采用基質標準工作液為基準進行校正。
2.4 方法評價
2.4.1線性關系與檢出限在優化的前處理和色譜條件下,對系列質量濃度的基質空白混合標準溶液進行檢測,其線性范圍等結果見表2。結果表明,7種農藥的質量濃度(x,μg/L)在0.2~2 000 μg/L范圍內與其積分峰面積(y)呈良好的線性關系,r2≥0.999 2。當實際樣品殘留量超過此線性范圍時,應對樣品溶液適當稀釋后再進行定量測定。在信噪比(S/N)為3時,7種農藥的檢出限(LOD)為0.03~1.6 μg/kg。
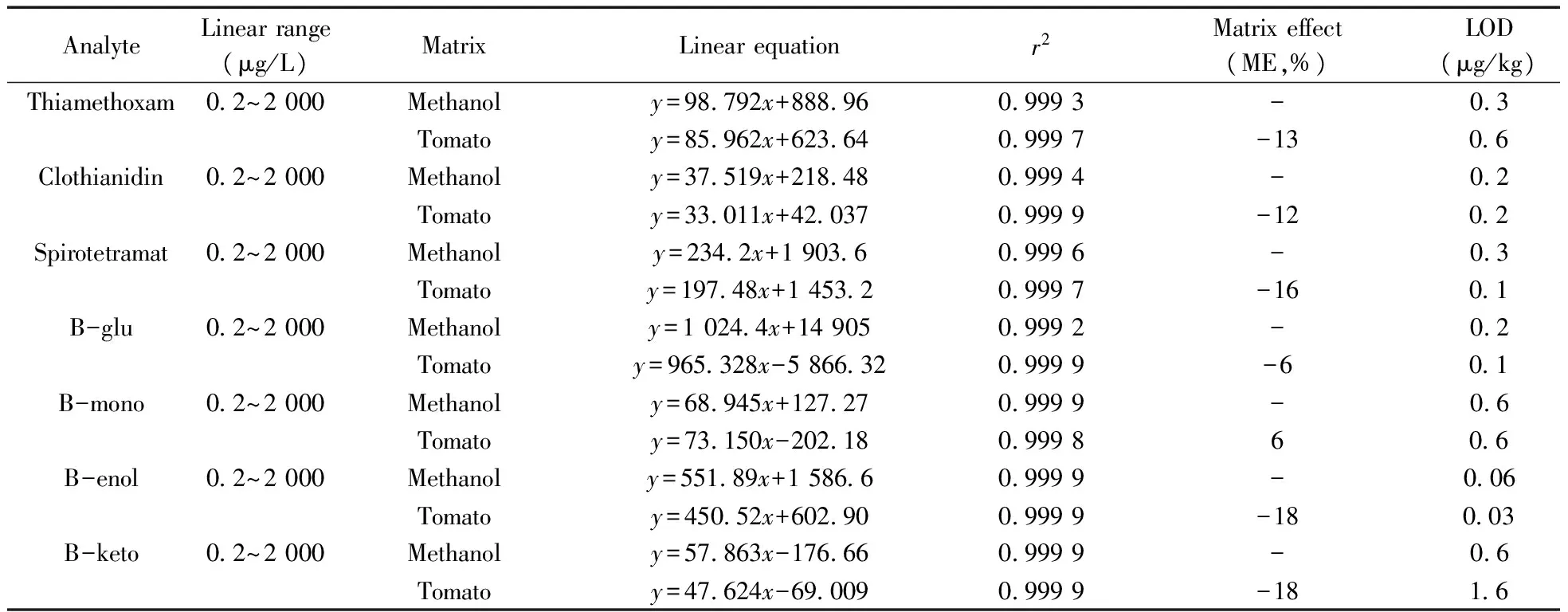
表2 7種農藥的線性范圍、線性方程、相關系數、基質效應和檢出限Table 2 Linear ranges,regression equations,correlation coefficients,matrix effect and limits of detection(LODs) for seven pesticides
-:no data
2.4.2回收率與精密度分別在空白番茄樣品中添加0.002、0.02、0.20、2.00 mg/kg水平的混標溶液,每個添加濃度平行測定5次,進行加標回收率試驗。7種農藥的平均回收率為79.9%~104%,相對標準偏差(RSD)為0.94%~6.4%(表3)。以最低加標濃度可知,7種農藥的定量下限(LOQ)為0.002 mg/kg。結果表明,本方法具有較高的回收率和精密度,滿足農藥多殘留檢測要求。
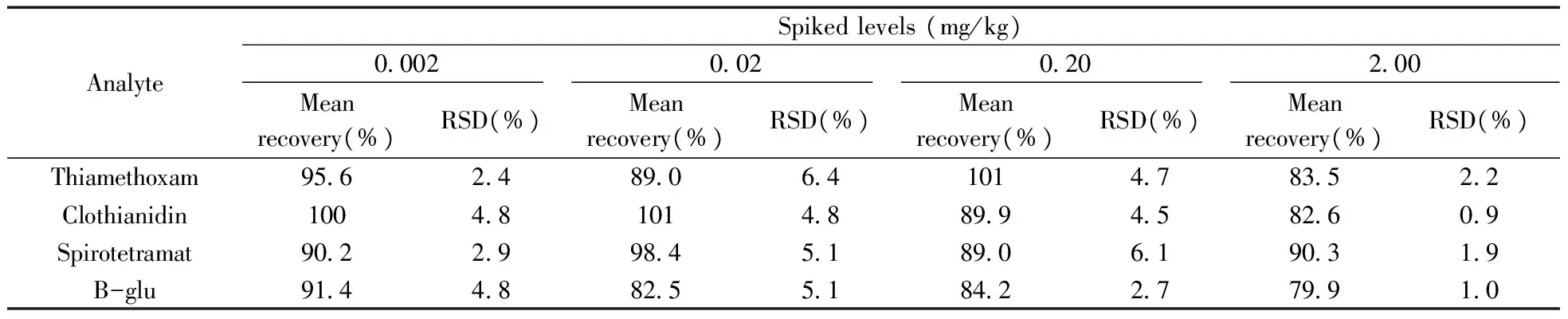
表3 7種農藥的平均回收率和相對標準偏差Table 3 Mean recoveries and relative standard deviations of 7 pesticides
(續表3)

AnalyteSpikedlevels(mg/kg)0 0020 020 202 00Meanrecovery(%)RSD(%)Meanrecovery(%)RSD(%)Meanrecovery(%)RSD(%)Meanrecovery(%)RSD(%)B-mono86 44 01024 899 81 186 42 4B-enol84 12 31042 01012 889 31 5B-keto91 64 295 94 694 73 692 91 4
2.5 與其他前處理方法的比較
表4對比了本方法與文獻方法的優缺點,由表可知,同樣使用QuEChERS技術,本方法的試劑和凈化劑用量相對更少,成本更低。并且本方法可同時測定7種農藥,總體回收率相對較好,RSD較小,能滿足實際樣品的分析測定要求。

表4 QuEChERS方法測定7種農藥與其他樣品前處理方法的比較Table 4 Comparison of QuEChERS methods for the determination of 7 pesticides and other sample pretreatment methods
2.6 方法應用
將本方法應用于柑橘、節瓜、蘋果、茄子中7種目標農藥殘留量的測定,通過在這4種空白基質中加入0.2、1.0、5.0、10.0、50.0、100.0、500.0、1 000.0、2 000.0 μg/L的7種農藥混標,獲得7種農藥的溶劑標準曲線和相關系數,并計算各基質的基質效應,結果見表5。由表可知,4種基質中7種農藥大多數表現為抑制作用,在實際樣品測定時需用基質匹配標準曲線進行定量。分別在柑橘、節瓜、蘋果和茄子空白勻漿樣品中添加0.20 mg/kg 的混標溶液,各平行測定5次,進行加標回收率實驗,結果見表5。不同樣品基質中7種農藥的平均回收率為71.1%~102%,RSD為0.61%~6.1%。4種基質中農藥的回收率基本滿足農藥殘留分析的要求。
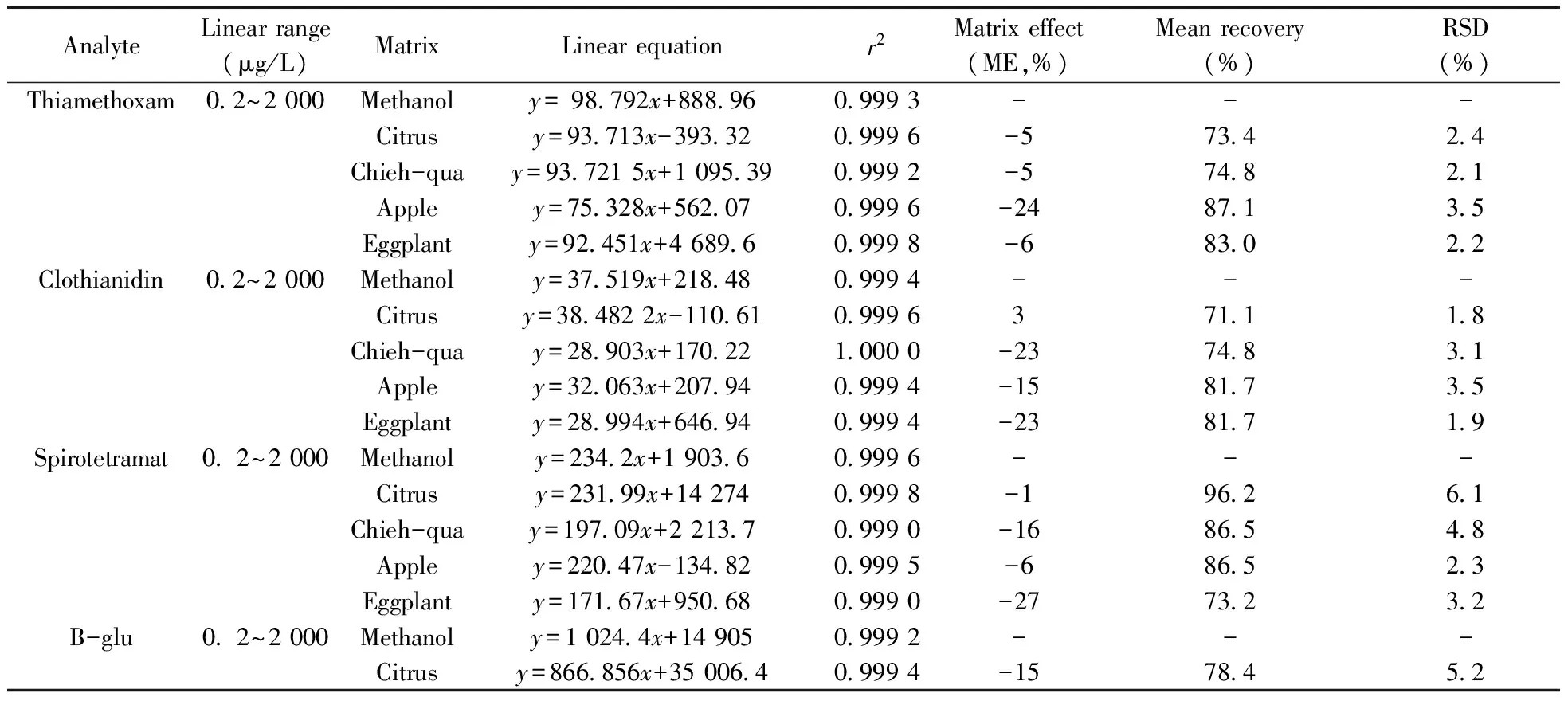
表5 7種農藥測定方法的應用Table 5 Application of seven pesticide determination methods
(續表5)

AnalyteLinearrange(μg/L)MatrixLinearequationr2Matrixeffect(ME,%)Meanrecovery(%)RSD(%)Chieh-quay=994 84x+2770 20 9998-374 81 5Appley=1101 52x+2744 40 9999876 42 5Eggplanty=1036 278x+11236 140 9991177 73 0B-mono0 2~2000Methanoly=68 945x+127 270 9999---Citrusy=67 876x-466 440 9995-279 85 0Chieh-quay=50 558x-194 210 9998-2781 71 3Appley=53 076x-182 250 9998-2387 03 0Eggplanty=55 248x-10 420 9997-2077 82 2B-enol0 2~2000Methanoly=551 89x+1586 60 9999---Citrusy=574 53x-4290 30 9994482 70 61Chieh-quay=459 76x-1771 10 9999-1773 12 1Appley=507 26x-426 250 9997-885 91 9Eggplanty=417 85x+943 520 9995-2473 21 7B-keto0 2~2000Methanoly=57 863x-176 660 9999---Citrusy=46 949x-303 840 9994-1986 54 4Chieh-quay=51 473x-424 760 9991-111023 3Appley=52 904x-176 430 9993-985 52 6Eggplanty=48 577x+202 60 9999-1680 61 5
-:no data
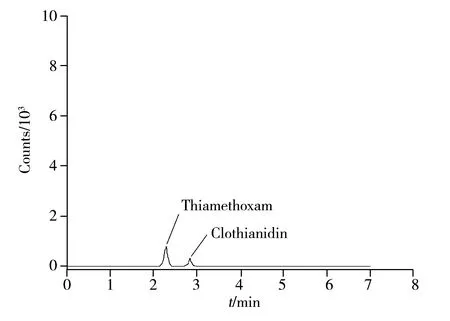
圖 4 番茄樣品的色譜圖Fig.4 Chromatogram of a tomato sample
采用本方法檢測市售20份番茄、20份節瓜、20份蘋果、20份茄子樣品,其中節瓜中未檢出上述7種農藥,番茄有1份樣品檢出噻蟲嗪和噻蟲胺,蘋果有1份樣品檢出噻蟲嗪,茄子有2份樣品檢出噻蟲嗪,檢出量為0.003~0.027 mg/kg,但均未超標。圖4為檢出農藥的市售番茄樣品的色譜圖。
3 結 論
本研究采用優化后的QuEChERS結合UPLC-MS/MS技術,建立了快速檢測番茄中噻蟲嗪、噻蟲胺、螺蟲乙酯及4種代謝產物殘留的方法。本方法具有操作簡單、快速、靈敏度高、檢出限低和重現性好等優點,能滿足番茄中噻蟲嗪、噻蟲胺、螺蟲乙酯及4種代謝產物同時檢測的要求。該方法同時適用于柑橘、節瓜、蘋果、茄子中上述7種農藥殘留的檢測,有較高的應用推廣價值。
[1] Gouvêa M M,Freitas D M,Rezende J A,Watanabe L F,Louren?o A L.Phytoparasitica,2017,45(1):95-101.
[2] Fang Y,Jiao X G,Xie W,Wang S L,Wu Q J,Shi X B,Chen G,Su Q,Yang X,Pan H P,Zhang Y J.ScientificReports,2013,3(2876):1-5.
[3] Authority E F S.EfsaJournal,2012,10(11):2990.
[4] Authority E F S.EfsaJournal,2016,14(3):4429.
[5] GB 2763-2016.Maximum Residue Limits for Pesticides in Food.National Food Safety Standards (食品中最大殘留限量.國家食品安全標準).
[6] Malhat F M,Watanabe H,Loutfy N M,Ahmed M T.Toxicological&EnvironmentalChemistry,2014,96(2):318-327.
[7] Gong Y,Huang W,Zhang Y F,Li J Z.AsianJournalofChemistry,2012,24(11):5289-5291.
[8] Li S S,Liu X G,Dong F S,Xu J,Xu H Q,Hu M F,Zheng Y Q.FoodChem.,2016,192:893-899.
[9] Iwafune T,Ogino T,Watanabe E.J.Agric.FoodChem.,2014,62(13):2790-2796.
[10] Zhu Y L,Liu X G,Xu J,Dong F S,Liang X Y,Li M M,Duan L F,Zheng Y Q.J.Chromatogr.A,2013,1299:71-77.
[11] Wang D,Hou C J,Zhao E C,Jia C H.J.Instrum.Anal.(王東,侯傳金,趙爾成,賈春虹.分析測試學報),2015,34(6):681-685.
[12] Zhan X P,Chen J B,Ma L,Huang L Q,Zhao L,Yu S H.J.Instrum.Anal.(占繡萍,陳建波,馬琳,黃蘭淇,趙莉,余淑紅.分析測試學報),2016,35(4):476-481.
[13] Li L,Jiang G Q,Liu C Y,Liang H Y,Sun D L,Li W.FoodControl,2012,25(1):265-269.
[14] Hafez R O,Singh B.JournalofInsectScience,2016,29(1):25-31.
[15] Zhang F,Zhang X Z,Luo F J,Chen Z M,Sun W J,Liu G M,Lou Z Y.J.Instrum.Anal.(張芬,張新忠,羅逢健,陳宗懋,孫威江,劉光明,樓正云.分析測試學報),2013,32(4):393-400.
[16] Melo A,Cunha S C,Mansilha C,Aguiar A,Pinho O,Ferreira I M.FoodChem.,2012,135(3):1071-1077.
[17] Anastassiades M,Lehotay S J,tajnbaher D,Schenck F J.J.AOACInt.,2003,86(2):412-431.
[18] Lehotay S J,Kok A D,Hiemstra M,Bodegraven P V.J.AOACInt.,2005,88(2):595-614.
[19] Xie W,Han C,Qian Y,Ding H Y,Chen X M,Xi J Y.J.Chromatogr.A,2011,1218(28):4426-4433.
[20] Determination of Pesticide Residues Using GC-MS and/or LC-MS (/MS) Following Acetonitrile Extraction/Partitioning and Clean-up by Dispersive SPE-QuEChERS Method.EN 15662.2008.
[21] AOAC Official Method 2007.01 Pesticide Residues in Foods by Acetonitrile Extraction and Partitioning with Magnesium Sulfate Gas Chromatography/Mass Spectrometry and Liquid Chromatography/Tandem Mass Spectrometry.AOAC International,2007.
[22] Niessen W M A,Manini P,Andreoli R.MassSpectrometryReviews,2006,25(6):881-899.
[23] Ramadan G,Shawir M,El-Bakary A,Abdelgaleil S.ChileanJournalofAgriculturalResearch,2016,76(1):129-133.
[24] Zhang Y,Xu J,Dong F S,Liu X G,Li X G,Li Y B,Wu X H,Liang X Y,Zheng Y Q.Anal.Methods,2013,5(6):1449-1455.
[25] Mohapatra S,Kumar S,Prakash G S.Environ.Monit.Assess.,2015,187(632):1-12.
Analysis of Thiamethoxam,Clothianidin and Spirotetramat and Their Metabolites Residues in Tomato Using QuEChERS Method with Ultra Performance Liquid Chromatography-Mass Spectrometry
LIU Yan1,3,OUYANG Di-qing1,3,YE Yu-feng1,3,WANG Cheng-qiu1,2,3,4*,JIAO Bi-ning1,2,3,4,5*,ZHAO Qi-yang1,3,ZHANG Yao-hai1,3,AO Yan2,3,WANG Hai-yan6
(1.Laboratory of Risk Assessment for Citrus Quality and Safety,Ministry of Agriculture,Citrus Reserch Institute,Chinese Academy of Agricultural Sciences/Southwest University,Chongqing 400712,China;2.College of Food Science,Southwest University,Chongqing 400715, China;3.Quality Supervision and Testing Center for Citrus and Seedling,Ministry of Agriculture,Chongqing 400712,China;4.National Center for Citrus Engineering,Chongqing 400712,China;5.Chongqing Key Laboratory of Citrus,Chongqing 400712,China;6.Chongqing Academy of Animal Science,Chongqing 402460,China)
In this study,an analytical method was established for the determination of thiamethoxam and its metabolites clothianidin,spirotetramat and its four metabolites such as BYI08330-enol-glucoside,BYI08330-ketohydroxy,BYI08330-enol and BYI08330-mono-hydroxy residues in tomatoes using QuEChERS cleanup with ultra-performance liquid chromatography-tandem mass spectrometry(UPLC-MS/MS).The residues in samples were extracted with acetonitrile,dehydrated with anhydrous magnesium sulfate and sodium chloride,then purified with primary secondary amine (PSA) sorbent and C18,finally detected by ultra-performance liquid chromatography-tandem mass spectrometry(UPLC-MS/MS) under the multi-reactive ion monitoring mode(MRM) and quantified by external standard method.The results showed that good linearities for the seven analytes i.e.thiamethoxam,clothianidin,spirotetramat,BYI08330-enol-glucoside,BYI08330-mono-hydroxy,BYI08330-enol and BYI08330-ketohydroxy were observed in the concentration range of 0.2-2 000 μg/L with the correlation coefficients(r2) not less than 0.999 2. The limits of quantification(LOQs) were 0.002 mg/kg.The average recoveries at the fortified levels of 0.002,0.02,0.20 and 2.00 mg/kg were in the range of 79.9%-104% with the relative standard deviations of 0.94%-6.4%.With the advantages of rapidness,simplicity,high sensitivity and good reproducibility,the method is suitable for the determination of thiamethoxam,clothianidin,spirotetramat and their four metabolites residues in tomatoes.
QuEChERS;UPLC-MS/MS;pesticide residues;tomato
2017-07-24;
2017-08-21
2017年國家柑桔及熱帶作物產品質量安全風險評估項目(GJFP2017004);國家現代農業(柑桔)產業技術體系建設項目 (CARS-26)
*
焦必寧,研究員,研究方向:果蔬貯藏加工技術與質量安全,Tel:023-68349046,E-mail:jiaobining@citrus.cn
王成秋,副研究員,研究方向:食品安全與質量控制,Tel:023-68349046,E-mail:citruszhx@163.com
10.3969/j.issn.1004-4957.2017.12.003
O657.63;O657.7
A
1004-4957(2017)12-1431-08

