陽離子交換凈化/氣相色譜-質譜法與氣相色譜法測定蔬菜水果中15種三唑類農藥殘留
許天鈞,蘇建峰
(1.遼東學院 化學工程學院,遼寧 丹東 118003;2.福建中檢華日食品安全檢測有限公司,福建 福州 350008)
陽離子交換凈化/氣相色譜-質譜法與氣相色譜法測定蔬菜水果中15種三唑類農藥殘留
許天鈞1,蘇建峰2*
(1.遼東學院 化學工程學院,遼寧 丹東 118003;2.福建中檢華日食品安全檢測有限公司,福建 福州 350008)
采用離子交換凈化法,建立了蔬菜水果中15種三唑類農藥殘留測定的前處理方法。樣品用乙腈提取,加入氯化鈉均質,離心分層后取部分乙腈層經溶劑轉換后過陽離子交換柱凈化,所得凈化液經濃縮定容后供氣相色譜儀(GC)和氣相色譜-質譜儀(GC-MS)分析。氣相色譜-質譜法采用選擇離子掃描方式(SIM),外標法定量。結果表明,在最優條件下15種三唑類農藥的定量下限(S/N≥10)均可達到0.01 mg/kg,在0.01、0.05、0.10 mg/kg三個加標水平下的回收率為68%~102%,相對標準偏差為2.4%~16.2%。實驗特別考察了該凈化方法在氣相色譜-電子捕獲檢測器(ECD)上的適用性,發現各種蔬菜水果(包括蔥屬蔬菜)均可獲得干擾極少的ECD譜圖。方法簡單、快速,適用于多種蔬菜水果中15種三唑類農藥殘留的測定。
固相萃取;氣相色譜法;氣相色譜-質譜法;三唑類殺菌劑;三唑類植物生長調節劑;蔬菜水果
三唑類農藥是一類影響細菌甾醇類生物合成并破壞其細胞膜功能的高效、廣譜、低毒的內吸性殺菌劑,被廣泛應用于蔬菜水果等農作物的種植中,是目前銷售量最大、最有發展前景的一類殺菌劑。除抑菌作用外,該類化合物還具有極強的調節植物生長、提高植物抵抗不良環境傷害的生理效應。
目前應用于食品中三唑類農藥殘留檢測的前處理方法主要是常規農藥多殘留分析方法和分子印跡法[1-2],常規農藥多殘留分析方法(包括專屬三唑類[3-5]和跨種類[6-12])采用極性、非極性固相萃取柱或復合固相萃取柱(Carb/PSA、Carb/NH2等)凈化,如GB 23200.8-2016[13](其前一版為GB/T 19648-2006,方法原理和步驟均一致),或者將吸附劑采用粉末的形式進行凈化,如QuEChERS法。本研究發現,由于三唑類農藥在化學結構上均是主鏈上帶取代苯基和1,2,4-三唑基團化合物,其中1,2,4-三唑基團在適當pH值條件下可結合質子形成陽離子,經條件優化后可采用陽離子交換法對三唑類農藥進行前處理凈化,供氣相色譜-質譜儀(GC-MS)分析,效果良好。該前處理凈化方案應用于食品中三唑類農藥殘留檢測的研究尚未見文獻報道。
本實驗還考察了該前處理凈化方案在氣相色譜/電子捕獲檢測器(GC/ECD)上的適用性。特別地,由于蔥屬蔬菜樣品中含有大量的烷基硫代半胱氨酸、亞砜類化合物等及其活性酶,在制樣后會產生大量硫基干擾物質[12,14-15],這些干擾物在ECD檢測器上響應值很大,使用常規前處理方法凈化得到的樣品譜圖均密布有大小不一的干擾峰,無法進行定性定量分析。本前處理方法能夠實現三唑類農藥和大量硫基干擾物質的分離,所得凈化效果適用于ECD檢測,可應用于部分三唑類農藥的測定,滿足高通量樣品的檢測需求。
1 實驗部分
1.1 儀器與試劑
7890A-5975C氣相色譜-質譜聯用儀(美國Agilent公司);Clarus 680氣相色譜儀(美國PerkinElmer公司);DB-5MS毛細管柱(30 m×0.25 mm×0.25 μm)、HP-5毛細管柱(30 m×0.32 mm×0.25 μm)均購于美國Agilent公司;T-18basic均質器(德國IKA公司);4 000 r/min低速離心機(德國Sigma公司);旋轉蒸發儀(德國Heidolph公司);氮吹儀(上海安譜DC-12);三唑酮、四氟醚唑、戊菌唑、三唑醇、多效唑、腈菌唑、芐氯三唑醇、氟硅唑、乙環唑、丙環唑、戊唑醇、三氟苯唑、氟環唑、聯苯三唑醇和苯醚甲環唑15種標準品純度均≥98%,購自德國Dr. Ehrenstorfer公司;陽離子交換固相萃取小柱(60 mg/3 mL,美國Thermo公司);所用溶劑和試劑均為分析純或色譜純;實驗用水為三重過濾去離子水。
1.2 實驗方法
1.2.1樣品處理制備:大蔥、菠菜、大白菜、春菜、青蔥、黃瓜、荷蘭豆、西紅柿、蘋果、香蕉樣品購于農貿市場,取各樣品約500 g置于制樣均質器中攪碎,備用。
提取:稱取10 g(精確至0.01 g)攪碎混勻樣品至50 mL離心管中,加入20 mL乙腈,15 000 r/min均質15 s,加入3 g氯化鈉,繼續均質15 s,旋上蓋子充分振蕩,4 000 r/min 離心10 min,移取上層乙腈10 mL至雞心瓶中,40 ℃減壓旋轉蒸發至近干,用3 mL含2%甲酸的甲醇-水(體積比1∶1)溶解殘渣(必要時配合超聲),所得溶液待凈化。
凈化:將陽離子交換柱置于玻璃離心管上,依次用3 mL甲醇、3 mL含2%甲酸的甲醇-水(1∶1)活化,將上述提取液過柱,再依次用3 mL含2%甲酸的甲醇-水(1∶1)、3 mL甲醇淋洗雜質,棄去淋洗液,最后用5 mL 0.5%氨水-甲醇洗脫,收集洗脫液于40 ℃氮氣吹干,用丙酮-正己烷(體積比1∶9)定容至1 mL,加入少量無水硫酸鎂,渦旋5 s后吸取上清液過濾膜后裝瓶,待測。

圖1 標準溶液的選擇掃描總離子流色譜圖Fig.1 SIM chromatogram of standard solution
1.2.2色譜-質譜條件氣相色譜-質譜條件:載氣為氦氣(純度99.999%),恒流模式,流速為1.0 mL/min,進樣口溫度260 ℃,進樣量1 μL,不分流進樣。色譜-質譜接口溫度280 ℃,離子源溫度230 ℃,四極桿溫度150 ℃,離子化方式EI,電子能量70 eV,倍增器電壓在自動調諧后加400 V。15種三唑類農藥的色譜分離譜圖見圖1,色譜質譜相關參數見表1。
氣相色譜條件:載氣為氮氣(純度99.999%),流速2.0 mL/min,進樣口溫度260 ℃,進樣量1 μL,不分流進樣,檢測器溫度300 ℃。
程序升溫:初始柱溫60 ℃,保持1 min,以20 ℃/min升至150 ℃,再以15 ℃/min升至230 ℃,最后以 25 ℃/min升至280 ℃,保持5 min。

表1 選擇離子監測待測農藥的保留時間、定量離子、定性離子Table 1 Retention time,quantitative and qualitative ions for SIM acquisition
2 結果與討論
2.1 樣品前處理條件的選擇
三唑類農藥在乙腈、丙酮、乙酸乙酯中均有較高的溶解度,對于食品基質中的農藥殘留,一般選用具有一定極性強度的溶劑或溶劑組合時提取效率較高。丙酮雖然提取效率高,但基質中大量雜質也被提取出來,給凈化帶來困難。乙酸乙酯在提取時與水分層,無協同效應,且對于新鮮果蔬的滲透效果一般。乙腈通用性強,對三唑類農藥溶解度大,可溶入的雜質量適中,且乙腈與樣品中自帶的水具有協同效應,形成乙腈-水混合提取液,在對目標物的溶解、對樣品基質的充分滲透和控制溶入的雜質量方面均具有很好的效果,故選用乙腈提取果蔬中三唑類農藥。加入氯化鈉均質,利用氯化鈉的鹽析作用,除去水和水溶性雜質,同時還可沉淀蛋白,提高三唑類農藥在有機相中的分配比。離心后的溶液最上層是乙腈層,中間是樣品殘渣與乙腈的混合層,下層為飽和氯化鈉水溶液,氯化鈉應過量,確保水溶液中鹽的濃度達到飽和,以保證鹽析的效果。移取部分上清液即可凈化,操作簡單迅速。
提取液經鹽析分配后采用陽離子交換柱凈化,陽離子交換柱中的鍵合基團能夠保留離子化的三唑類農藥,通過淋洗去除主要干擾物后,再用堿性溶液洗脫三唑類農藥。實驗中先用甲醇洗去小柱中的干擾物并使鍵合官能團打開,再用含2%甲酸的甲醇-水(1∶1)繼續活化并平衡。選用含2%甲酸的甲醇-水(1∶1)溶液溶解殘留物并上柱(若溶液渾濁,應將其高速離心后取澄清液上柱,以防未溶解的顆粒堵塞小柱或影響其中官能團的吸附與解吸附規律),溶解液中2%甲酸與水配合,使三唑類農藥結合質子,呈陽離子形態。實驗發現甲酸比例過高(5%)時雜質增多,凈化效果下降;比例過低(0.5%)時方法耐受性下降,在應對不同種類樣品時,質子化效率不穩定將導致回收率波動。依次采用指定溶液淋洗雜質后以0.5%的氨水-甲醇洗脫,定容時加入少量無水硫酸鎂,可確保樣液的無水環境,避免對毛細管柱造成傷害。
2.2 結果分析
2.2.1氣相色譜-質譜測定結果凈化后的樣液供氣相色譜-質譜儀(GC-MS)分析,經優化選擇監測離子,各待測物的定量離子基本無干擾,部分定性離子有干擾,干擾幅度尚能滿足其定性的要求。采用本法處理的荷蘭豆樣品(檢出丙環唑0.045 mg/kg)和春菜樣品(檢出苯醚甲環唑0.11 mg/kg)的選擇監測提取離子流色譜圖見圖2。樣品經本法凈化后,所得各提取離子流色譜圖總體較優,丙環唑的定性離子m/z173色譜圖中有干擾峰,但其響應值不高,且保留時間與丙環唑不重疊,不影響定性,其它離子色譜圖中基本無干擾峰,經儀器自動計算,m/z259、261、265、323、325的信噪比(S/N)均超過200。
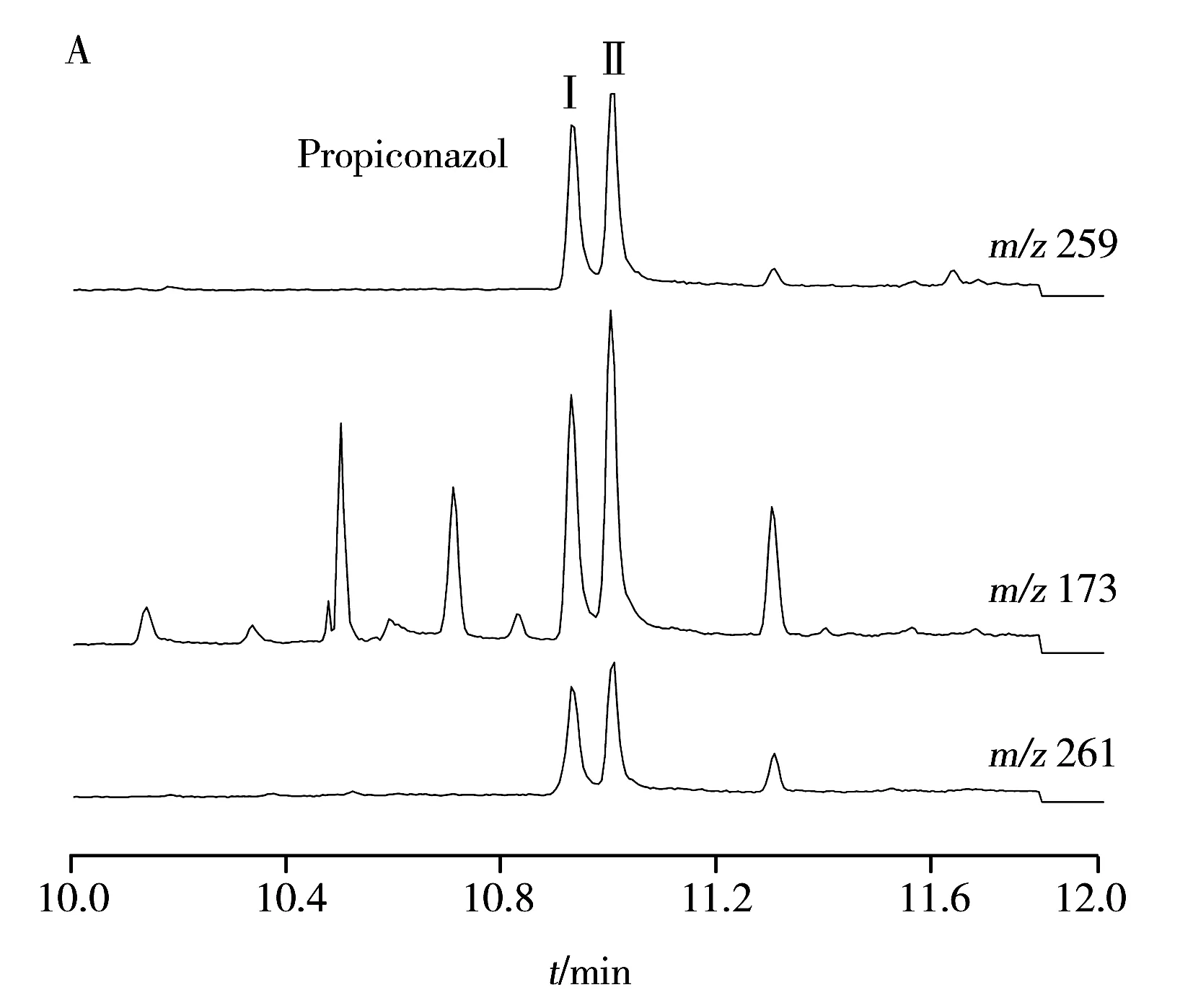
2.2.2氣相色譜測定結果實驗考察了本凈化方法在氣相色譜/電子捕獲檢測器(GC/ECD)上的適用性。由于蔥屬蔬菜樣品含有大量的烷基硫代半胱氨酸、亞砜類化合物等及其活性酶,在完整的細胞內,酶與底物是分隔存在的。在制樣過程中,細胞受損傷,酶作用于底物,產生大量揮發性硫基干擾物,是蔥屬蔬菜樣品基質干擾的主要來源,且干擾物的含量遠高于農殘含量,在ECD檢測器上響應值很大,因此這類樣品被認為是極難分析的樣品[12,14-15]。目前主要采用在制樣前用磷酸或微波處理的方法來鈍化樣品中的活性酶[12],降低干擾,但磷酸處理法適用范圍較窄,且不好解決采樣代表性與稱樣精確度之間的矛盾,而微波處理法對實驗條件要求比較苛刻,易導致農藥降解,故本研究亦未采用。實驗對以下兩種方法進行對照研究(圖3):①GB 23200.8-2016中的前處理方法(圖3B),雖然該法中后續測試儀器為氣相色譜質譜聯用儀,但其中的Envi-18、Carb/NH2凈化法代表了目前固相萃取法凈化的主流;②QuEChERS凈化法(圖3C),代表了目前粉末分散凈化的主流方法。圖3B和C雖然基線、干擾峰數量大小等不完全相同,但其干擾均過大。實際上,目前的常規前處理方案處理大蔥樣品時,所得的ECD譜圖均呈現與圖3B和C類似的干擾。原因是常規凈化方法中未針對蔥屬蔬菜中含有的大量揮發性硫基干擾物質進行特別凈化,所以這些干擾物進入ECD檢測器后產生眾多干擾峰,無法進行定性定量分析。本法(圖3A)針對三唑類農藥中1,2,4-三唑基團在適當pH值條件下可結合質子形成陽離子的特點,優化吸附解吸附條件,可以針對性地除去這些干擾物質,獲得很好的凈化效果。
對于一般蔬菜水果(如菠菜、黃瓜、西紅柿等),使用本法與常規前處理方法所得的ECD譜圖無較大變化,只是總體雜質峰略少。這是因為對于一般蔬菜水果,其主要雜質使用常規前處理方法即可獲得良好的凈化效果,故結果差別不大。
由于有些三唑類農藥在ECD檢測器上無響應或響應極低,并且部分三唑類農藥性質相近,無法完全分離,所以GC/ECD法測定三唑類農藥有其固有缺陷。本實驗同時測定15種三唑類農藥多殘留,在GC/ECD上既有無響應值的,也有重疊的,故本研究僅給出本前處理的凈化方案在GC/ECD上適用性的考察結論,作為GC-MS法的補充。
對于GC/ECD法的應用,在確認所測三唑類農藥標準溶液在GC/ECD上有足夠響應值的前提下,本研究得出以下結論:①作為初篩方法(與標準溶液對照,若相應保留時間處無色譜峰,則初篩未檢出,若有色譜峰,則應使用GC-MS法進行確證);②僅作為少量幾個三唑類農藥的定量分析方法。

圖3 不同前處理方法所得大蔥樣品的GC/ECD色譜圖Fig.3 Chromatograms of GC/ECD from scallion with different pretreatment methodsA:this method;B:GB 23200.8-2016 method;C:QuEChERS method

圖4 空白大蔥樣品(a)及加標水平為0.05 mg/kg大蔥樣品(b)的GC/ECD色譜圖Fig.4 Chromatograms of GC/ECD from blank scallion(a) and blank scallion spiked with 0.05 mg/kg mix standards(b)
圖4給出了空白大蔥和大蔥加標樣品的譜圖,從圖中信號與基線對比可見,對于選擇性不高的ECD檢測器來說,大蔥樣品能夠獲得非常滿意的凈化效果。
2.3 方法線性范圍、定量下限、回收率與精密度
采用標準溶液測試,15種三唑類農藥在0.01~1.0 mg/L范圍內線性關系良好,r2>0.98。以加標樣品10倍信噪比(S/N≥10)確定方法定量下限(LOQ),各農藥的LOQ均可達到0.01 mg/kg。采用大蔥、黃瓜、蘋果樣品進行加標回收率實驗,加標水平為0.01、0.05、0.10 mg/kg,測定結果見表2,15種三唑類農藥回收率在68%~102%之間。本實驗采用基質標準曲線對基質效應進行了考察,發現15種三唑類農藥的基質效應對回收率的影響均在13%以內,其中苯醚甲環唑的基質效應相對略強,在8%~13%之間,其它14種三唑類農藥的基質效應均不明顯,這主要得益于前處理的良好凈化效果。目標物的RSD為2.4%~16.2%,其中添加水平為0.01 mg/kg樣品的RSD值總體略大,這是由于濃度很低時,三唑類農藥在前處理和儀器測定時波動性增大,導致精密度有所降低,但仍處于可接受范圍內,0.05、0.10 mg/kg添加水平的精密度則有明顯提高,總體RSD≤16.2%,結果滿意。

表2 方法定量下限、回收率和精密度(n=6)Table 2 LOQ,recovery and RSD of the method(n=6)
(續表2)

No.CompoundLOQ(mg/kg)Spiked(mg/kg)ScallionCucumberAppleRecovery(%)RSD(%)Recovery(%)RSD(%)Recovery(%)RSD(%)3Pencnazole0 010 01905 7854 8868 90 05885 5817 1898 70 10893 9887 4893 14Triadimenol0 010 017212 17416 27110 40 05739 47013 7758 80 107010 26910 2688 55Paclobutrazol0 010 01897 4846 8727 60 05815 9817 1794 50 10824 1854 4775 16Myclobutanil0 010 01866 8809 0928 00 05876 6848 9895 90 10885 5874 2866 07Diclobutrazole0 010 01919 1918 58910 80 05855 7924 9936 70 10862 6846 1906 38Flusilazole0 010 01888 7837 7887 30 05928 0925 0847 20 10824 7875 4834 09Etaconazole0 010 01825 3787 3757 50 05875 8844 6844 80 10775 4893 2892 510Propiconazol0 010 01877 0779 4826 90 05766 8786 4897 10 10817 5892 8816 111Tebuconazole0 010 01789 4726 87611 30 057310 1794 5818 90 10826 6787 0837 212Fluotrimazole0 010 01948 3837 4938 80 05839 0846 6916 40 10827 1886 3884 413Epoxiconazole0 010 01918 1968 91026 70 05936 7895 5975 40 10973 7943 0952 414Bitertanol0 010 019413 710210 29915 00 05939 7898 88712 10 108810 0908 4899 915Difenoconazole0 010 0110010 21019 79211 70 05915 1995 8936 00 10903 6896 9856 7
2.4 實際樣品分析
用本方法對市售大蔥、菠菜、大白菜、春菜、青蔥、黃瓜、荷蘭豆、西紅柿、蘋果、香蕉樣品各3份進行測定,結果在1份春菜和1份大白菜樣品中檢出苯醚甲環唑,含量分別為0.11 mg/kg和0.38 mg/kg,1份菠菜樣品中檢出氟硅唑0.44 mg/kg,1份荷蘭豆樣品中檢出丙環唑0.045 mg/kg,其中春菜和荷蘭豆樣品譜圖見圖2,其它樣品均未檢出相關農藥殘留。
3 結 論
本研究針對三唑類農藥中1,2,4-三唑基團在適當pH值條件下可結合質子形成陽離子的特點,通過優化吸附解吸附條件,建立了陽離子交換凈化/氣相色譜-質譜法測定蔬菜水果中15種三唑類農藥殘留的分析方法,效果良好。通過對本法在GC/ECD上的適用性考察發現,本前處理方法對于蔥屬蔬菜中含有的大量揮發性硫基干擾物質具有很好的凈化效果,有效解決了目前農殘分析中“調味蔬菜樣品檢測”的難點,除了應用于三唑類農藥外,對其他相關農藥也具有一定的借鑒意義。
[1] Hu Y Y,Xu H Q,Yao J,Lü Y N,Song W,Li W J,Han F,Zheng P.Chin.J.Anal.Chem.(胡艷云,徐慧群,姚劍,呂亞寧,宋偉,李文靜,韓芳,鄭平.分析化學),2014,42(2):227-232.
[2] Gao L,Li Y L,Liu B,Gao W H.JournaloftheChineseCerealsandOilsAssociation(高林,李亞麗,劉博,高文惠.中國糧油學報),2016,31(10):131-136.
[3] Ge N,Liu X M,Li X M,Huang X Z,Wu Y P,Li J,Liu Y M.J.Instrum.Anal.(葛娜,劉曉茂,李學民,黃學者,吳艷萍,李金,劉永明.分析測試學報),2011,30(12):1351-1355.
[4] Li J G,Wang Y F,Shi J W,Jiang L,Yao X P,Fang L Y.Chin.J.Chromatogr.(李繼革,王玉飛,施家威,蔣麗,姚潯平,方蘭云.色譜),2012,30(3):262-266.
[5] Wang F,Li T,Ma C.Chin.J.Chromatogr.(王菲,李彤,馬辰.色譜),2013,31(3):191-199.
[6] Su J F,Zhong M S,Chen J,Guo X,Chen J X,Liang Z,Liu J J.J.Instrum.Anal.(蘇建峰,鐘茂生,陳晶,郭昕,陳勁星,梁震,劉建軍.分析測試學報),2015,34(6):625-638.
[7] Pang G F,Cao Y Z,Zhang J L,Fan C L,Liu Y M,Li X M,Jia G Q,Li Z Y,Shi Y Q,Wu Y P,Guo T T.J.Chromatogr.A,2006,1125:1-30.
[8] Pang G F,Fan C L,Chang Q Y,Li Y,Kang J,Wang W W,Cao J,Zhao Y B,Li N,Li Z Y,Chen Z M,Luo F J,Lou Z Y.J.AOACInt.,2013,96(4):887-896.
[9] Fan C L,Chang Q Y,Pang G F,Li Z Y,Kang J,Pan G Q,Zheng S Z,Wang W W,Yao C C,Ji X X.J.AOACInt.,2013,96(2):432-440.
[10] Hou X H,Zheng X,Zhang C L,Ma X W,Ling Q Y,Zhao L S.J.Chromatogr.B,2014,969:123-127.
[11] Liu D,Min S G.J.Chromatogr.A,2012,1235:166-173.
[12] Su J F,Lu S Y,Chen J,Chen J X,Liang Z,Liu J J.Chin.J.Chromatogr.(蘇建峰,盧聲宇,陳晶,陳勁星,梁震,劉建軍.色譜),2011,29(7):643-655.
[13] GB 23200.8-2016.National Food Safety Standards-Determination of 500 Pesticides and Related Chemicals Residues in Fruits and Vegetables by Gas Chromatography-Mass Spectrometry(食品安全國家標準 水果和蔬菜中500種農藥及相關化學品殘留量的測定 氣相色譜-質譜法).
[14] Ji S J,Liu C J,Sato M,Li D X,Li J Q.Phys.Test.Chem.Anal.:Chem.Anal.(紀淑娟,劉長江,佐藤元昭,李冬秀,李俊奇.理化檢驗-化學分冊),2006,42(11):914-917.
[15] Zhang H,Chen Z L,Yang G S,Wang W Z,Li X Q,Li R J,Wu Y J.FoodChem.,2008,108(1):322-328.
Determination of 15 Triazole Pesticides in Vegetables and Fruits by Gas Chromatography and Gas Chromatography-Mass Spectrometry
XU Tian-jun1,SU Jian-feng2*
(1.School of Chemical Engineering,Eastern Liaoning University,Dandong 118003,China;2.Fujian CCIC-Fairreach Food Safety Testing Co.,Ltd.,Fuzhou 350008,China)
A method was developed for the determination of 15 triazole pesticides in vegetables and fruits by gas chromatography(GC) and gas chromatography-mass spectrometry(GC-MS) with ion exchange column.The samples were pretreated quickly,then extracted with acetonitrile after sodium chloride homogenization,separated by liquid-liquid partition.The clear supernatant purified by solid phase extraction with ion exchange column was ready for GC-ECD and GC-MS analysis.Determinations were performed by using selected ion monitoring(SIM) mode,and external standard method was used for quantification.After optimizing the conditions for pretreatment and determination,the method was convenient and rapid.Under the optimal conditions,the quantitation limits of the method(S/N≥10) were 0.01 mg/kg.The recoveries at spiked levels of 0.01,0.05,0.10 mg/kg were in the range of 68%-102% with the relative standard deviations of 2.4%-16.2%.Besides,the pretreatment has a good purification effect in GC-ECD chromatogram.The method is easy,rapid and sensitive,and could meet the requirements for the analysis of 15 triazole pesticides in vegetables and fruits.
solid phase extraction(SPE);gas chromatography;gas chromatography-mass spectrometry;triazole fungicides;triazole plant growth mediations;vegetables and fruits
2017-08-22;
2017-09-25
遼寧省科技廳項目(2016LD0112)
*
蘇建峰,高級工程師,研究方向:食品中污染物殘留分析,E-mail:sujianfeng2005@163.com
10.3969/j.issn.1004-4957.2017.12.009
O657.7;O657.63
A
1004-4957(2017)12-1469-07

