羧芐西林鈉無菌原料藥熱原控制的風險評估
柴依群
(上海上藥新亞藥業有限公司新先鋒制藥廠,上海201203)
0 引言
熱原是指臨床上引起哺乳動物發熱反應的物質。在羧芐西林鈉無菌原料藥的質量標準中,熱原是一個重要的質量考察項目。若熱原檢查不合格,則表明藥品生產過程中的無菌保證措施出現了很嚴重的問題。
2010年版GMP引入了質量風險管理的理念,它是依據科學知識及經驗對質量風險進行評估,以保證產品質量。羧芐西林鈉無菌原料藥的熱原污染可能來源于原輔料、生產過程、生產環境、生產設備及人員操作等方面。
本文主要從羧芐西林鈉無菌原料藥的生產工藝(包括生產過程、生產設備、人員操作等)著手,對羧芐西林鈉無菌原料藥生產的熱原污染風險進行評估和分析。
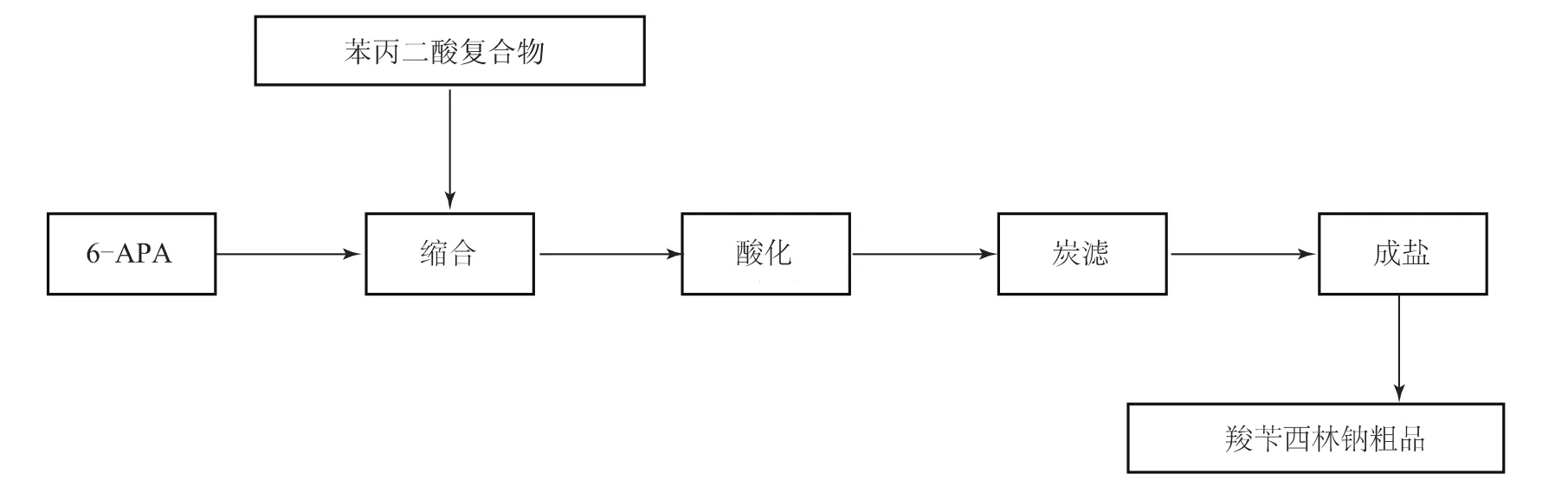
1 羧芐西林鈉無菌原料藥的生產工藝流程
根據羧芐西林鈉無菌原料藥的工藝規程,該產品的生產過程由兩大步驟組成:第一步為羧芐西林鈉(粗品)的合成工藝;第二步為羧芐西林鈉無菌原料藥的精制凍干工藝。
羧芐西林鈉(粗品)的合成工藝流程如圖1所示,羧芐西林鈉無菌原料藥的精制凍干工藝流程如圖2所示。
2 羧芐西林鈉無菌原料藥生產工藝的風險評估與分析方法
根據羧芐西林鈉無菌原料藥兩個不同生產工藝的特點,對照羧芐西林鈉(粗品)合成工藝與羧芐西林鈉無菌原料藥精制凍干工藝流程,對工藝中可能引入熱原的每一個風險點進行識別、分析與評估。
對于已識別的風險點,可使用常用的失敗模式效果分析(FMEA)這一風險評估工具進行風險分析。失敗模式效果分析是一種對工藝的失敗模式及其對結果和/或產品性能可能產生的潛在影響的評估工具。一旦失敗模式被建立,就可通過降低風險來消除、減少或控制潛在的失敗[1]。
FEMA風險得分=嚴重性×可能性×可測定性。其中,嚴重性、可能性、可測定性的評分標準如表1所示。通過風險得分的計算,可以找出風險等級高的風險點,并采用一系列的控制措施,使高風險點降低到可接受水平。根據表1標準,其風險得分可接受標準:分數≤9。
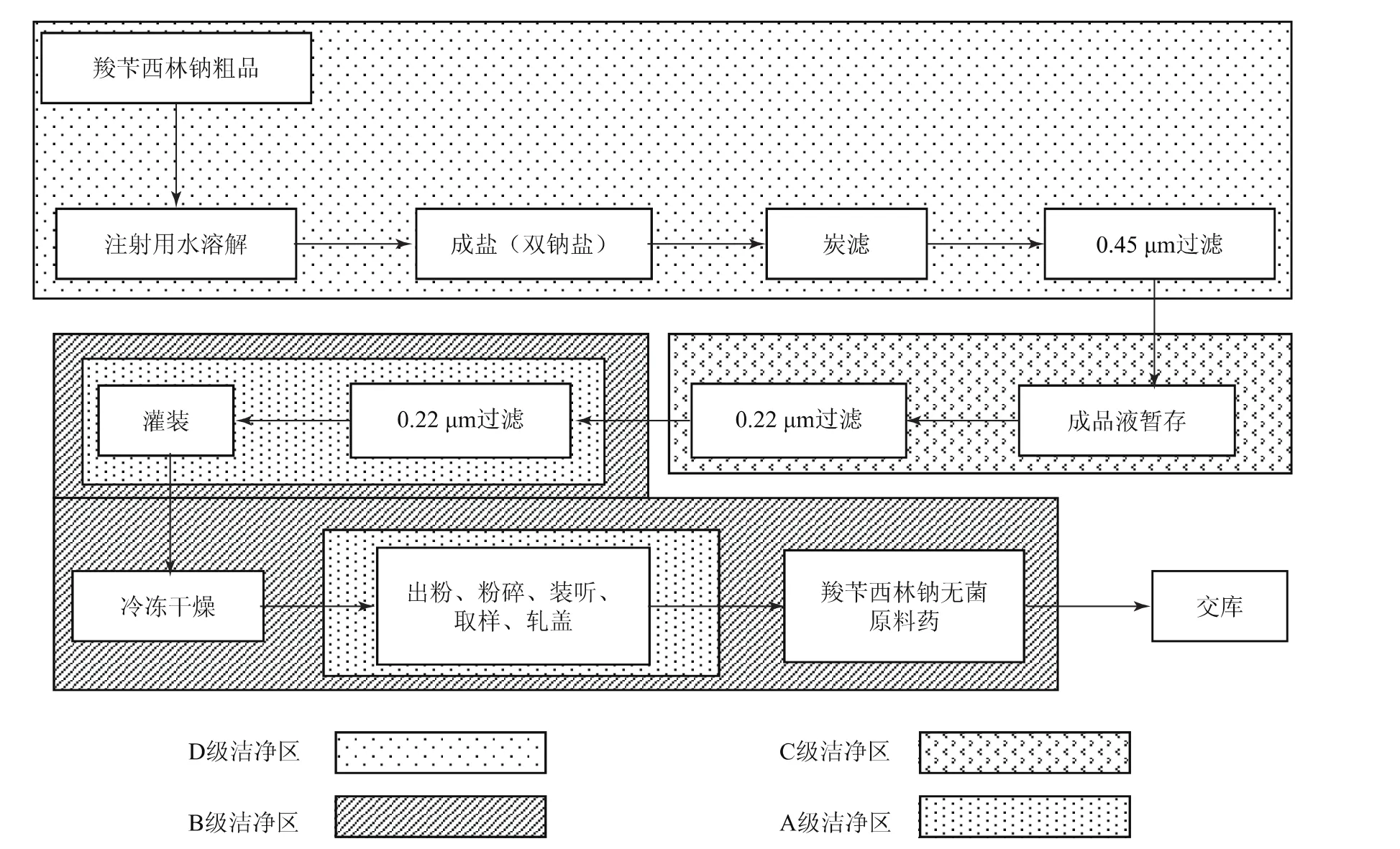
圖2 羧芐西林鈉無菌原料藥的精制凍干工藝流程

表1 嚴重性、可能性、可測定性的評分標準
3 羧芐西林鈉無菌原料藥熱原控制的風險評估
3.1 羧芐西林鈉(粗品)合成工藝各關鍵點的熱原風險評估
表2為羧芐西林鈉(粗品)合成工藝各關鍵點的熱原風險評估結果。
從表2可看出:對羧芐西林鈉(粗品)合成工藝中縮合、酸化、炭濾及成鹽的熱原風險判斷,羧芐西林鈉(粗品)合成工藝過程中雖有引入熱原和微生物污染的可能,但由于其生產過程基本在強酸環境下進行,且最終羧芐西林鈉粗品的pH值=3.0~5.0,為強酸性,對熱原具有一定的破壞能力,因此,羧芐西林鈉(粗品)合成工藝中的各熱原控制關鍵點為低風險點。
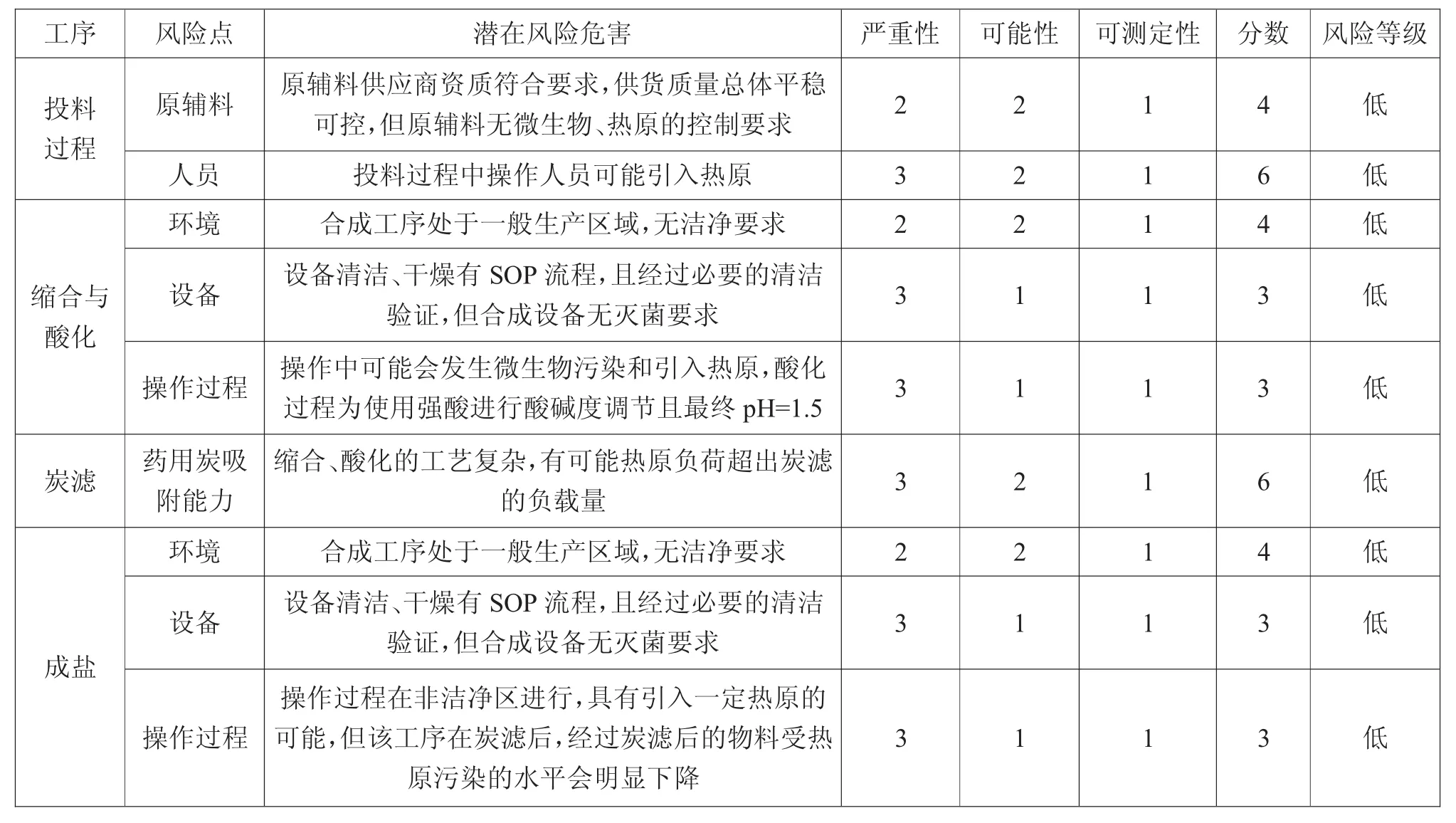
表2 羧芐西林鈉(粗品)合成工藝各關鍵點的熱原風險評估結果
3.2 羧芐西林鈉無菌原料藥精制凍干工藝各關鍵點的熱原風險評估
3.2.1 羧芐西林鈉無菌原料藥的精制凍干工藝
羧芐西林鈉無菌原料藥的生產工藝主要包括精制成鹽(雙鈉鹽)、凍干兩大部分。其中,成鹽(雙鈉鹽)過程在炭濾前進行,凍干過程在炭濾后進行。由于炭濾操作是羧芐西林鈉無菌原料藥生產工藝中的重要步驟,對熱原的去除具有關鍵性作用,因此,將炭濾工序作為劃分羧芐西林鈉無菌原料藥工藝風險評估的關鍵點。考慮到整個工藝中的絕大部分操作都在炭濾后進行,且炭濾前的主要物料(羧芐西林鈉粗品)的熱原檢測結果符合要求,因此本文把工藝中熱原風險評估的重點放在炭濾之后的所有工藝步驟上。
3.2.1.1 成鹽(雙鈉鹽)工藝
成鹽(雙鈉鹽)工藝在炭濾之前,其整個操作過程在D級潔凈區中進行,操作步驟簡單,且該工藝所用的主要物料(羧芐西林鈉粗品)經檢驗,其熱原符合要求。因此,在成鹽(雙鈉鹽)工藝中引入熱原的可能性極小。
3.2.1.2 凍干工藝
凍干工藝在炭濾之后,包括料液過濾、灌裝、冷凍干燥、出粉、粉碎、包裝等多個步驟,其工藝操作均在潔凈區中進行,但步驟復雜,設備繁多,且操作過程中人為干預的部分較多。
此外,由于凍干工藝處于炭濾之后,且與羧芐西林鈉無菌原料藥的最終質量有直接關系,所以對其所涉及的生產設備、人員操作均有很高的要求。雖然所有設備均經過確認、驗證,直接接觸藥品的人員操作也被盡可能避免,但仍有以下環節可能會引入熱原污染。
3.2.2 羧芐西林鈉無菌原料藥精制凍干工藝各關鍵點的熱原風險評估
從以上分析可知,熱原在羧芐西林鈉無菌原料藥精制凍干工藝的各關鍵點的重點在凍干工藝器具及設備管路清洗、灌裝、出料等環節。
3.2.2.1 首次風險評估
表3為羧芐西林鈉無菌原料藥凍干工藝器具及設備管路清洗、灌裝、出料等關鍵點的熱原風險評估結果。
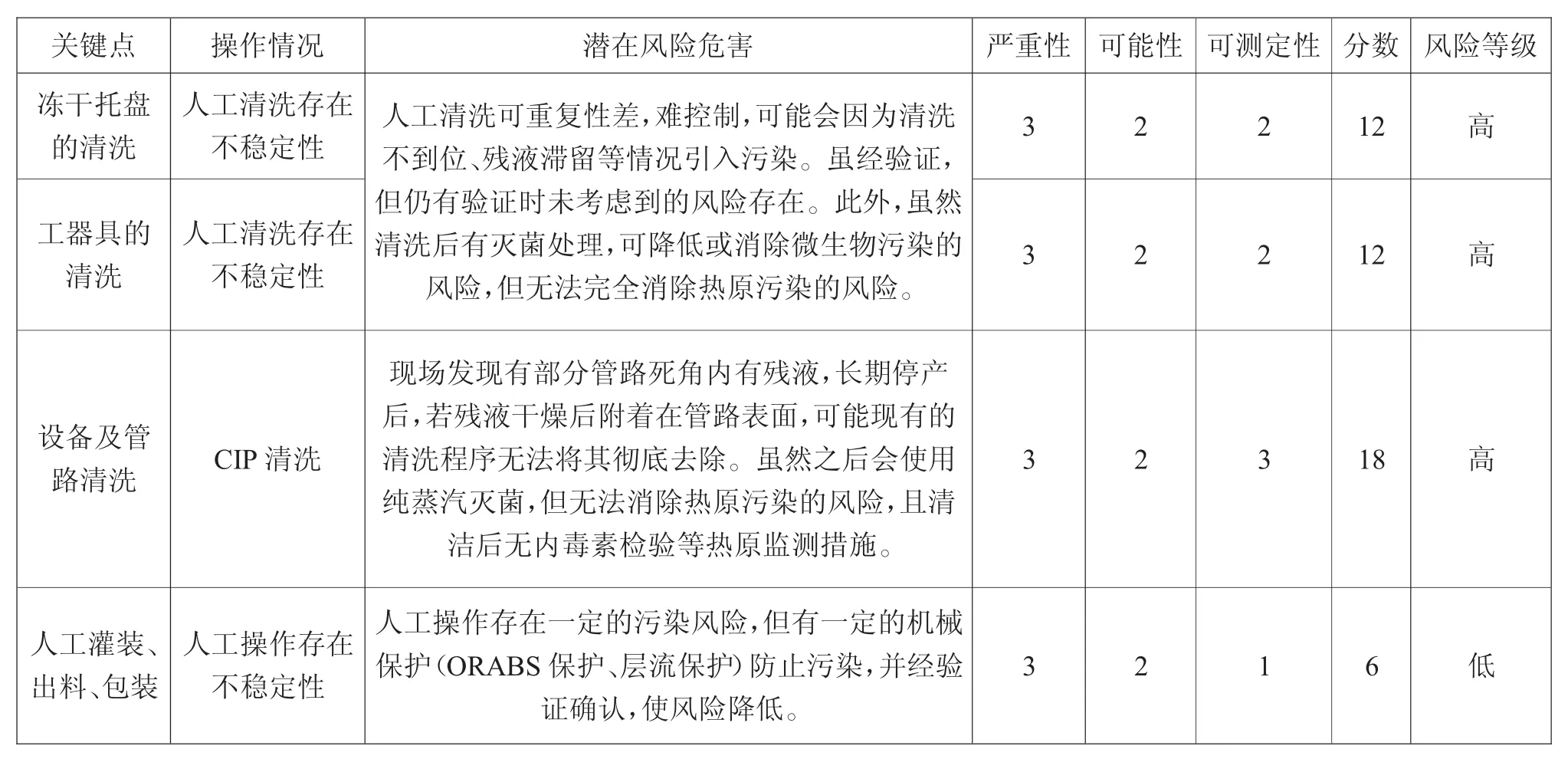
表3 凍干工藝器具及設備管路清洗、灌裝、出料等關鍵點的熱原風險評估結果
從表3可以看到:分數≥9的關鍵點有凍干托盤的清洗、工器具的清洗及設備與管路的清洗。
3.2.2.2 風險控制措施與二次風險評估
從以上分析可知,熱原在羧芐西林鈉無菌原料藥凍干工藝的高風險點為凍干托盤的清洗、工器具的清洗及設備與管路的清洗,應采取相應的風險控制措施,并對所采取的風險控制措施進行二次FMEA分析。
表4為羧芐西林鈉無菌原料藥凍干工藝關鍵點的熱原風險控制措施與二次風險評估結果。
從表4可看出:二次FMEA評估分析的結果表明,熱原污染風險控制在可接受的范圍內。對于熱原的風險控制措施必須有標準化文件,并對相關人員進行培訓,使制定的風險控制措施能真正得到落實。
4 風險回顧
在完成羧芐西林鈉無菌原料藥有關熱原方面的風險評估后,按照風險評估管理的理念,需設定羧芐西林鈉無菌原料藥熱原控制的風險評估回顧周期,其宗旨是回顧風險控制措施的落實與執行情況,檢驗控制措施是否在可接受限度內,是否會影響原來控制措施落實的因素。
5 結語
本文以羧芐西林鈉無菌原料藥中的熱原控制為研究對象,從粗品合成與精制凍干兩個工藝步驟著手,介紹了羧芐西林鈉無菌原料藥的生產工藝,又以此兩個工藝步驟為劃分依據,對羧芐西林鈉無菌原料藥的熱原控制關鍵點的風險進行了識別和分析,并提出了降低熱原污染風險的措施。
結論:(1)羧芐西林鈉(粗品)合成工藝的各關鍵點為熱原污染的低風險點;(2)羧芐西林鈉無菌原料藥凍干工藝中的器具及設備管路清洗、灌裝、出料等關鍵點為熱原污染的高風險點。針對上述各關鍵風險點,只要采取相應的風險控制措施,就能有效降低羧芐西林鈉無菌原料藥的熱原污染風險。
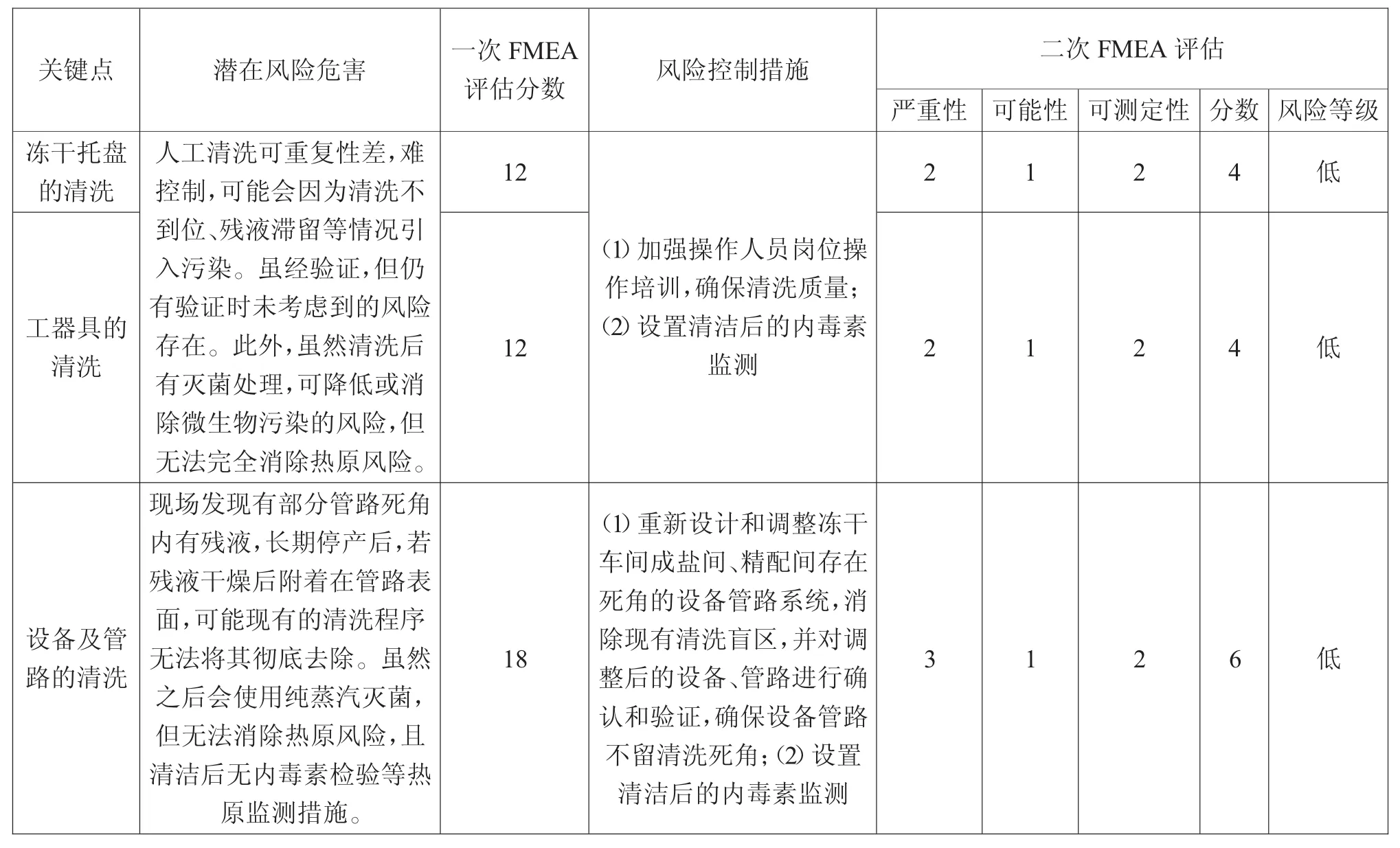
表4 凍干工藝關鍵點的熱原風險控制措施與二次風險評估結果
[1]國家食品藥品監督管理局藥品認證管理中心.藥品GMP指南·質量管理體系[M].北京:中國醫藥科技出版社,2011:210.

