缺血性腦卒中后血管性癡呆的MRI影像特點研究
區尚之 楊少民 歐陽裕鋒
作為缺血性腦卒中的常見并發癥之一, VaD是僅次于阿爾茨海默病(AD)的認知功能障礙第二大病因, 但不同于AD的病理發展特質, VaD多具有可預防性, 因而早期診斷至關重要。MRI是診斷腦損傷不可或缺的影像學方法, 對灶區位置的結構與功能判定均具有較高的診斷價值。對此, 本研究旨在分析缺血性腦卒引起的VaD在MRI中的影像特征, 為臨床診斷提供指導, 現報告如下。
1 資料與方法
1.1 一般資料 回顧性分析2015年1月~2017年5月本院收治的60例缺血性腦卒中后VaD患者(觀察組)和同期體檢的60例健康志愿者(對照組)的臨床資料。其中觀察組男38例, 女22例;年齡56~79歲, 平均年齡(68.6±8.4)歲;小學及以下12例, 中學或中專37例, 大專及以上11例;簡易精神狀態檢查量表(MMSE)[1]評分為(14.6±2.1)分。觀察組納入標準:①符合VaD相關診斷標準者[2];②存在缺血性腦卒中疾病史者;③年齡50~80歲。對照組中男35例,女25例;年齡50~76歲, 平均年齡(66.1±7.8)歲;小學及以下11例, 中學或中專36例, 大專及以上13例;MMSE評分為(26.3±2.5)分。排除標準:①腦卒中發病前已存在認知功能障礙疾病者;②臨床資料不全者;③無法配合檢查者;④診斷為阿爾茲海默病、帕金森病、腦積水、腦腫瘤等其他中樞神經系統疾病;⑤有開顱手術史或嚴重頭顱外傷史者。兩組一般資料比較, 差異無統計學意義(P>0.05), 具有可比性。
1.2 方法 兩組選取并佩戴合適的頭線圈, 采用PHILIPS公司生產的ACHIEVA 1.5t型MRI系統進行檢測(矩陣320 mm×224 mm, 視場 2 4 cm, 重復時間 6 ~10 s, 回波時間約 7 2 ms), 通過T1WI及T2WI行序列掃描;通過時間飛躍法(TOF)進行MRA(翻轉角度240°, 有效層厚0.9 mm), 采集橫斷位140層數據圖像進行重建得到三維血管重建圖像。每次掃描時間約為3 min 40 s, 影像資料均導入計算機, 由2位經驗豐富的醫師采用雙盲法進行分析。
1.3 觀察指標 比較兩組WML情況(ARWMCrs)及影像特點差異。
1.4 評估標準 WML情況評估標準采用ARWMCrs[3]評價,分別評估左右腦額葉、頂枕葉、顳葉、幕下結構、基底核共5個部分的病變情況, 0分:無病損;1分:局灶性病損;2分:至少2處局灶性病損;3分:病損連接成片。WML率=1分+2分+3分。
1.5 統計學方法 采用SPSS19.0統計學軟件對數據進行統計分析。計量資料以均數±標準差(±s)表示, 采用t檢驗;計數資料以率(%)表示, 采用χ2檢驗。P<0.05表示差異具有統計學意義。
2 結果
2.1 WML情況 觀察組大腦左右側額葉、頂枕葉、顳葉、幕下結構、基底核WML率均明顯高于對照組, 差異具有統計學意義(P<0.05), 其中左側頂枕葉及額葉WML最為突出,WML率可達91.7%(55/60)與95.0%(57/60)。見表1。
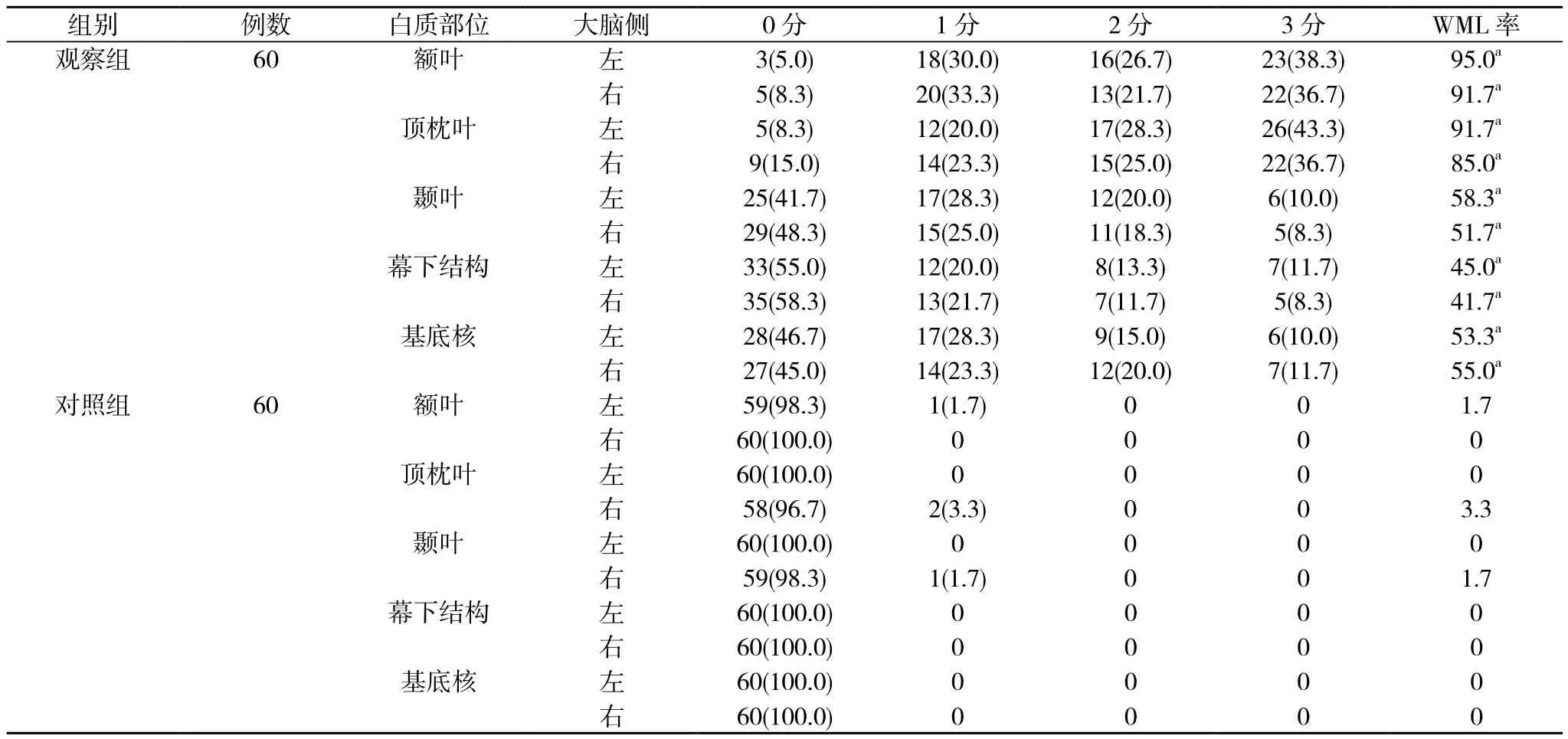
表1 兩組ARWMCrs評級結果比較[n(%), %]
2.2 影像特點 觀察組多見廣泛的WML, 由矢狀梯度回波序列T1WI可見額葉、頂葉、枕葉存在多發軟化灶, 橫軸面梯度回波序列T1WI多見內囊膝部有小軟化灶, 灶區直徑<1 cm, 弛豫時間較長且其T2WI信號更強;皮質厚度大多未見減少, 但可見海馬溝回間距及側腦室體部寬度增加;MRA多見單側椎動脈狹窄, 深穿支動脈及基底動脈顯示微梗死,雙側前動脈硬化程度較高。對照組影像基本未見WML, 各組織寬度及MRA血管顯影形態均屬正常。
3 討論
由于缺血性腦卒中患者發病后腦組織缺血、缺氧性壞死, 極易造成進行性的中樞神經元功能性缺失, 繼而導致出現VaD, 引發患者記憶、語言、情感、人格等多方面的精神障礙, 對其日常生活造成極為惡劣的影響。目前早期VaD主要通過MRI、腦電圖(EEG)、電子計算機斷層掃描(CT)、彩色多普勒超聲(TCD)及各種與發病機制有關的生物標志物水平進行診斷, 其中MRI由于具備高軟組織分辨率而應用最為廣泛, 本研究就其影像特點予以如下討論。
WML作為VaD的主要病理進程, 對患者認知功能影響最為直接, 有研究指出, VaD患者執行功能損傷較AD患者更為嚴重, 其關鍵原因就在于WML引起的額葉-皮層下環路被破壞, 造成自尾狀核背外側至蒼白球、黑質紋狀體的投射過程受阻[4-9]。本研究結果顯示, 觀察組WML明顯較對照組更嚴重, 且病變主要集中與左側頂枕葉與額葉, 究其原因可能與上述部位細胞對代謝紊亂較為敏感有關。本研究還發現多數患者MRI影像橫軸面梯度回波序列T1WI多見內囊膝部有小軟化灶, 弛豫時間較長且其T2WI信號更強, 提示患者存在腔隙性腦梗死, 但對照組也可檢測出少量相似信號,故單憑MRI對腔隙性腦梗死存在誤診, 可結合其他方式進行判定。
隨著白質纖維之間聯系的破壞, 極易對皮層造成繼發性損傷, 且伴隨有白質軸索及髓鞘的脫失, 進而引發腦萎縮,加快疾病進程。據相關文獻報道, 腦室旁白質包含下縱束、扣帶回、上下行枕額纖維束等可聯系大腦各部分的神經纖維束[5], 一旦出現灶點, 可迅速波及皮層及皮層下, 引發腦萎縮。本研究發現觀察組皮質厚度大多未見減少, 但可見海馬溝回間距及側腦室體部寬度明顯大于對照組, 這表明VaD早期的腦萎縮主要表現在海馬萎縮與側腦室擴張, 究其原因與缺血性腦卒中對海馬神經元脫失影響較大有關。此外, 本研究還發現觀察組MRA檢查結果多見單側椎動脈狹窄, 深穿支動脈及基底動脈顯示微梗死, 雙側前動脈硬化程度較高,提示腦血管狹窄、閉塞、硬化對VaD影響極大, 大腦前動脈受累是其發病的關鍵因素。楊運旗等[10]已在研究中證實上述結論, 認為前動脈血管病變可破壞額葉皮質及皮質下結構的纖維聯系, 還對海馬及丘腦參與的記憶環路功能造成嚴重破壞。
綜上所述, MRI可作為早期診斷VaD的有效手段, 針對WML判定較為準確, 對腔隙性腦梗死、腦萎縮、腦血管造影的影像特點突出, 具有較高應用價值。
[1] 李娜, 張華.缺血性小血管病與血管性癡呆的相關性研究.寧夏醫科大學學報, 2012, 34(3):252-256.
[2] 美國精神醫學學會.精神障礙診斷與統計手冊.北京:北京大學出版社, 2016:22-26.
[3] 于潔, 王海麗, 周麗麗, 等.腦白質病變程度對認知功能的影響.中國腦血管病雜志, 2013, 10(12):653-656, 658.
[4] 李鴻梅.缺血性腦卒中后血管性癡呆的影響因素分析.中國醫藥導報, 2015, 12(1):48-51.
[5] 童宣霞, 王龍, 周霞, 等.腦萎縮對皮質下缺血性血管病患者認知功能的影響.中華醫學雜志, 2016, 96(1):14-19.
[6] 趙艷紅.缺血性卒中后血管性癡呆的MRI特點及相關危險因素分析.寧夏醫科大學, 2014.
[7] 趙艷紅, 張華.缺血性卒中后血管性癡呆的MRI特點分析.寧夏醫學雜志, 2014, 36(4):325-327.
[8] 陳偉平.急性缺血性腦卒中后血管性癡呆的相關研究.中山大學, 2006.
[9] 王蒙.缺血性腦卒中后血管性癡呆的相關因素研究.延邊大學,2011.
[10] 楊運旗, 阮守宇, 王婕, 等.DWI、MRA在急性腦缺血中的聯合診斷價值.西南國防醫藥, 2012, 22(4):398-401.

