芽孢皮層裂解酶的提取與SDS-PAGE分析
孫靜,賀曉光,張津瑜,杜文斌,章中
(寧夏大學農學院,寧夏銀川750021)
芽孢的殺滅是食品殺菌的關鍵任務。芽孢是細菌營養體在缺乏營養的環境條件下形成的休眠態,可以休眠幾萬年以上而復活,對各種殺菌處理(如輻照、超高壓、熱、超聲波、微波、化學物質等)有極強的抗性[1]。然而,當萌發條件適宜時,芽孢便迅速萌發、出芽生長,一旦其恢復到營養細胞狀態便喪失了對外界脅迫的抵抗力[2-3]。許多因素能誘導芽孢萌發,如營養素、超高壓、陽離子表面活性劑、機械擦傷、外源DPA、外源裂解酶、細胞壁碎片等等[4-5]。自然界中芽孢的萌發多是由一些營養類的萌發劑觸發,包括氨基酸、糖類和嘌呤核苷類等,也可以由多種營養萌發劑聯合觸發[6]。
在芽孢萌發而轉變成營養體的過程中,皮層裂解酶會將芽孢皮層肽聚糖水解,這是芽孢萌發過程中的一個重要步驟[7]。皮層裂解酶是芽孢所特有的酶,專一地水解芽孢皮層肽聚糖,在休眠的芽孢中,皮層裂解酶不表現出活性,當芽孢萌發時,皮層裂解酶會通過某種機制被激活并將皮層肽聚糖水解[8]。高壓熱殺菌技術(High-pressure thermal sterilization,HPTS)將壓力和溫度結合起來殺菌,對細菌芽孢有良好的殺滅作用[9]。有研究推測,HPTS很可能會影響皮層裂解酶的活性,在某些壓力和溫度條件下,皮層裂解酶可能會被激活,導致芽孢皮層水解,進而使得芽孢結構被破壞[10]。然而,要驗證高壓熱處理是否能激活芽孢皮層裂解酶,首先要提取皮層裂解酶,測定分子量,為皮層裂解酶的分離及純化打下基礎,進而對皮層裂解酶進行HPTS處理,從而揭示HPTS殺滅芽孢的機理,闡明HPTS對皮層裂解酶結構和活性的影響。
本試驗使用DPA、L-丙氨酸、肌苷等來誘導芽孢萌發,芽孢萌發后皮層裂解酶會釋放到萌發液中,經透析處理,從萌發液中提取芽孢皮層裂解酶粗酶液,再進行SDS-PAGE電泳分析其分子量并測定其活性。本文對皮層裂解酶的最佳提取方法及電泳條件進行優化,建立適宜于枯草芽孢桿菌芽孢皮層裂解酶的提取條件和SDS-PAGE電泳技術,確定皮層裂解酶粗酶液中各蛋白分子量,為皮層裂解酶的進一步分離純化提供材料和依據。
1 材料與方法
1.1 材料與試劑
1.1.1 菌種
枯草芽孢桿菌(Bacillus subtilis):中國普通微生物菌種保藏管理中心(CGMCC),編號As 1.433。
1.1.2 主要試劑
2,6-吡啶二羧酸(DPA):分析純,美國 Sigma公司;L-丙氨酸、肌苷:上海瑞永生物科技有限公司;30%丙烯酰胺溶液:北京雷根生物科技有限公司;4×Tris/SDS分離膠緩沖液(pH8.8)、4×Tris/SDS濃縮膠緩沖液(pH6.8):上海雙螺旋生物科技有限公司;過硫酸銨溶液、TEMED、甘氨酸:北京博奧拓達科技有限公司;寬范圍預染蛋白質分子量標準:Thermo Scientific;無水乙醇、磷酸氫二鈉、磷酸二氫鈉:天津市大茂化學試劑廠,均為分析純。
1.1.3 培養基
促芽孢生長錳鹽營養瓊脂培養基:向普通營養瓊脂培養基中加入MnSO4·H2O(使得培養基中Mn2+的濃度為50 mg/L),調pH值,滅菌,備用。
1.2 儀器與設備
AL204型電子天平、FE28型pH計:梅特勒-托利多儀器(上海)有限公司;DSX-280B型高壓滅菌鍋:上海申安醫療器械廠;XMTD-6000型電子恒溫不銹鋼水浴鍋:上海宜昌儀器紗篩廠;LRH系列生化培養箱:上海一恒科學儀器有限公司;GL-10C型冷凍離心機:上海安亭科學儀器廠;722型可見分光光度計:上海馳唐電子有限公司;DYCZ-24DN型電泳槽:北京六一生物科技有限公司;DYY-6C型電泳儀電源:北京市六一儀器廠。
1.3 方法
1.3.1 枯草芽孢桿菌芽孢的培養及菌懸液制備
芽孢的制備方法來自文獻[11]。菌種用營養瓊脂培養基活化3代以上后,接入試管斜面促芽孢生長培養基上劃線培養。在37℃培養7 d后,用接種環和無菌去離子水將試管斜面上的芽孢洗滌收集到離心管里。然后用冷的無菌去離子水離心洗滌芽孢3次。離心條件為7 000 r/min、4℃、15 min。離心后將上清液和沉淀的上部一起倒掉。純化后的芽孢重懸在無菌去離子水中,濃度約為1.5×109CFU/mL,放在4℃下保存,一個月內使用。試驗前將枯草芽孢桿菌芽孢調整到1.5×108CFU/mL左右。
1.3.2 皮層裂解酶的提取[12-15]
1.3.2.1 DPA誘導芽孢萌發提取皮層裂解酶
將芽孢濃度稀釋至1.5×108CFU/mL左右,將DPA濃度設定為10、15、20 mmol/L。將芽孢置于6倍體積的不同濃度萌發液中,放置于32℃的水浴鍋中處理,每10 min測定一次OD600值。處理50 min后再經離心(8 000 r/min、10 min、4℃),將上清液在4℃透析處理24 h,對照液為2 L、75 mmol/L、pH值為7.0的磷酸鈉緩沖液,緩沖液中含有1 mmol/L的EDTA、1 mmol/L的巰基乙酸鈉。透析后的酶液進行超濾濃縮。對照組為1 mL芽孢懸浮液加入6 mL無菌水。
1.3.2.2 肌苷誘導芽孢萌發提取皮層裂解酶
將芽孢濃度稀釋至1.5×108CFU/mL左右,將肌苷濃度設定為10、30、50 mmol/L。其他操作同1.3.2.1。
1.3.2.3 L-丙氨酸誘導芽孢萌發提取皮層裂解酶
將芽孢濃度稀釋至1.5×108CFU/mL左右,將L-丙氨酸濃度設定為10、30、50mmol/L。其他操作同1.3.2.1。
1.3.2.4 L-丙氨酸結合肌苷誘導芽孢萌發提取皮層裂解酶
將芽孢置于6倍體積的、pH=7.0的、30 mmol/L的磷酸鈉緩沖液中,緩沖液中含有10 mmol/L的L-丙氨酸和4 mmol/L的肌苷。32℃下培養,每10 min測定一次OD600值。其他操作同1.3.2.1。
1.4 電泳樣品的處理
取0.8 mL濃縮后的酶液,加入0.2 mL 5×SDSPAGE蛋白上樣緩沖液,混合蛋白樣品和蛋白上樣緩沖液(5×)。沸水浴加熱5 min,以充分變性蛋白。置冰上5 min,使用前10 000 r/min離心1 min。
1.5 聚丙烯酰胺垂直板電泳
1.5.1 染色液、脫色液及電泳液的配制[16-17]
染色液:考馬斯亮藍R-250 1 g,乙醇45%,冰乙酸10%,加水定容至1 000 mL,過濾后使用。
脫色液:冰乙酸10%,乙醇30%。
5×蛋白質電泳緩沖液:Tris 15.1 g,甘氨酸94 g,SDS 5 g,用蒸餾水定容至1 000 mL,使用時用蒸餾水稀釋5倍。
1.5.2 分離膠、濃縮膠的配制
按表1、表2比例分別配制10%、12%的分離膠和5%的濃縮膠[18]。
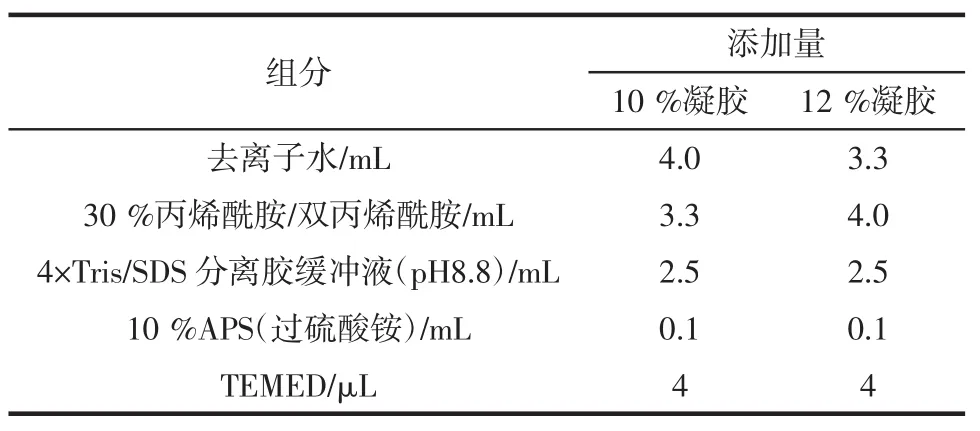
表1 5%分離膠的配制Table 1 The preparation of the 5%separation gel

表2 5%濃縮膠的配制Table 2 The preparation of the 5%spacer gel
1.5.3 電泳
SDS-PAGE參考郭堯君等[18]的方法。采用10%、12%的分離膠及5%的濃縮膠。上樣量為5、10、15 μL。電泳時,在濃縮膠中電壓控制為80 V,走過濃縮膠后電壓調為120 V。凝膠板上的樣品溴酚藍的條帶走至距底端1 cm時,停止電泳,取下凝膠,在染色器皿中加入100 mL染色液,加蓋,過夜染色。脫色液脫色,每3 h換一次脫色液,脫色至染色的凝膠經脫色后能清晰顯示出蛋白條帶為止。
1.6 測量蛋白質分子量[19]
用卡尺測量溴酚藍指示劑和蛋白遷移距離,計算相對遷移率(Rm)=蛋白質遷移距離/溴酚藍指示劑遷移距離,以Rm為橫坐標,標準蛋白質的分子量對數為縱坐標,進行線形回歸,再由標準曲線求得目標蛋白的分子量。
1.7 皮層裂解酶活性的測定
1.7.1 脫芽孢衣芽孢的制備
脫芽孢衣芽孢的制備參照Makino[14]的研究,并做相應的修改。將枯草桿菌芽孢用30 mmol/L SDS、0.2 mol/L 2-巰基乙醇、pH=10.0、0.1 mol/L硼酸鹽緩沖液在40℃下處理,處理4 h~8 h。再用冷的無菌去離子水離心洗滌5次。離心條件為7 000 r/min、4℃、15 min。洗滌后的脫芽孢衣芽孢重懸在無菌去離子水中,濃度約為 1.5×108CFU/mL。
1.7.2 酶活性的測定
在32℃下,通過測定脫芽孢衣芽孢懸浮液的OD600值的減少量來評價酶的活性[14]。取4 mL透析后的粗酶液,于32℃培育20 min,對照組為4 mL無菌水32℃下培育20 min,再向各組中加入1 mL脫芽孢衣芽孢懸浮液,在32℃下反應80 min,每10 min測一次OD600值。
1.8 數據分析方法
所有試驗都重復3次,實驗結果均以平均值±標準差表示。用SPSS 20.0軟件對實驗結果進行統計分析,用Origin 7.0軟件進行作圖。
2 結果與分析
2.1 不同萌發劑對枯草芽孢桿菌芽孢萌發的影響
2.1.1 DPA對芽孢萌發的影響
芽孢萌發時,其核心部分水化,導致其折光性發生變化,萌發后其OD600值顯著下降,并且下降的程度與芽孢萌發率的高低有顯著的相關關系,下降的程度越高,芽孢的萌發率就越高,因此芽孢懸浮液OD600值的變化被廣泛的用于評價芽孢的萌發程度[20]。
DPA對芽孢萌發的影響見圖1。
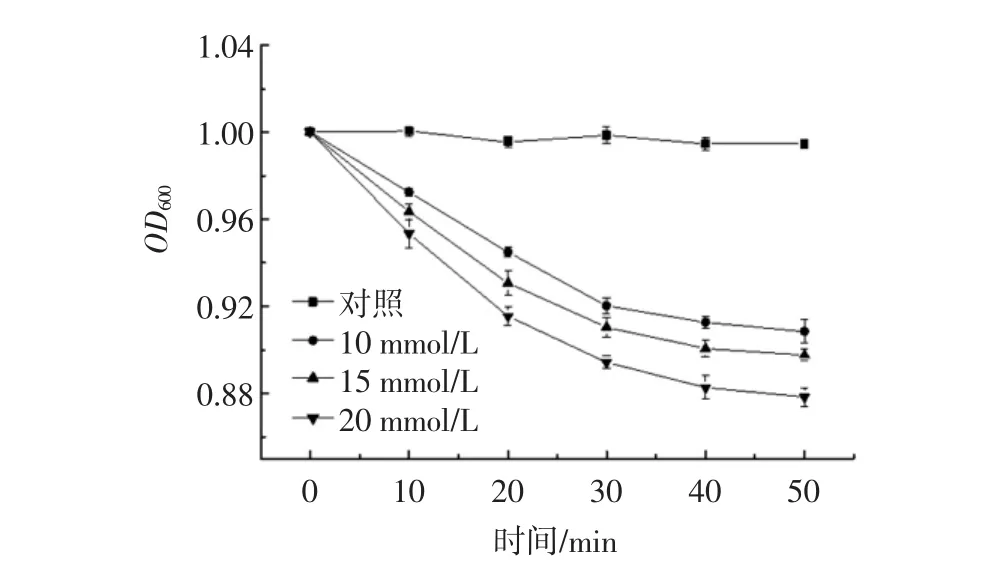
圖1 DPA對芽孢萌發的影響Fig.1 Effect of DPA on germination of spores
從圖1可知,與對照相比,加入DPA的樣品OD600值均有所下降;在前30 min時,OD600值迅速降低,30 min~40 min時OD600值下降趨勢減緩,而40 min~50 min時,OD600值基本不變,說明當加入DPA時,芽孢在30 min內能迅速萌發,30 min~50 min萌發速率逐漸減弱;隨著DPA濃度的逐漸增大,OD600值下降程度也逐漸增大,當DPA濃度達到20 mmol/L時,OD600值下降最多,即芽孢萌發程度最大。
2.1.2 L-丙氨酸對芽孢萌發的影響
L-丙氨酸對芽孢萌發的影響見圖2。
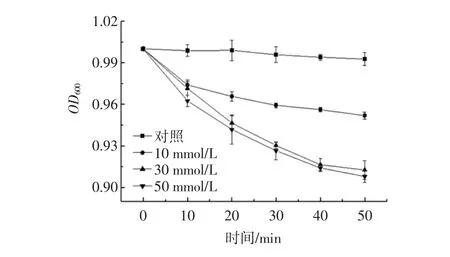
圖2 L-丙氨酸對芽孢萌發的影響Fig.2 Effect of L-alanine on germination of spores
從圖2可以看出,L-丙氨酸濃度為30、50 mmol/L的樣品,在前40 min時OD600值迅速降低,40 min~50 min時,OD600值下降趨勢減慢;而L-丙氨酸濃度為10 mmol/L的樣品,OD600值在前10 min內迅速降低,10 min~50 min OD600值下降趨勢逐漸減緩;說明當加入L-丙氨酸時,芽孢能在較短時間內萌發,隨著時間的延長,萌發速率逐漸減弱;隨著L-丙氨酸濃度的不斷增大,OD600值下降趨勢逐漸最大,說明芽孢的萌發程度隨著L-丙氨酸濃度增大而逐漸增大。
2.1.3 肌苷對芽孢萌發的影響
肌苷對芽孢萌發的影響見圖3。
由圖3可以看出,在前30 min時,OD600值迅速降低,30 min~50 min時,肌苷濃度為10、30 mmol/L的樣品OD600值下降趨勢減緩,而肌苷濃度為50 mmol/L的樣品,30 min~50 min時,OD600值仍有明顯的下降趨勢,但較前30 min下降趨勢有所減小,說明當加入肌苷時,芽孢在30 min內能迅速萌發;隨著肌苷濃度的逐漸增大,OD600值下降程度也逐漸增大,當肌苷濃度達到50 mmol/L時,OD600值下降最多,即芽孢萌發程度最大。
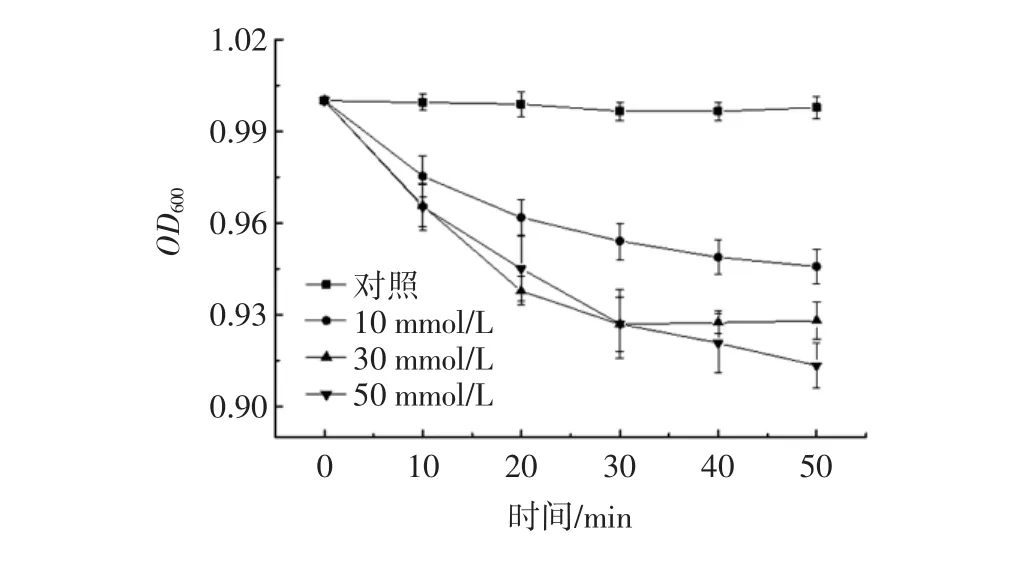
圖3 肌苷對芽孢萌發的影響Fig.3 Effects of inosine on germination of spores
2.1.4 L-丙氨酸結合肌苷對芽孢萌發的影響
L-丙氨酸結合肌苷對芽孢萌發的影響見圖4。
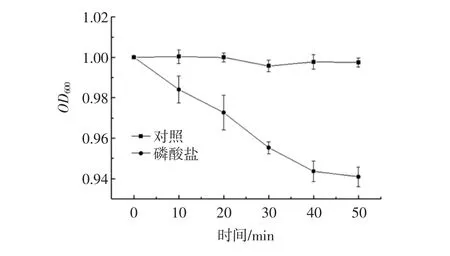
圖4 L-丙氨酸結合肌苷對芽孢萌發的影響Fig.4 Effect of L-alanine combined with inosine on germination of spores
從圖4可知,加入L-丙氨酸結合肌苷(緩沖液中含有10 mmol/L的L-丙氨酸和4 mmol/L的肌苷)的樣品與對照組相比,OD600值有極顯著的降低(P<0.01);隨著培育時間的延長,OD600值逐漸降低,前40 min OD600值下降趨勢明顯,40 min~50 min時,下降趨勢減弱。
對各因素誘導芽孢萌發的效果進行了差異顯著性分析,DPA誘導芽孢萌發的效果顯著高于其他3種芽孢萌發誘導劑(P<0.05)。因此本試驗選用DPA誘導芽孢萌發來提取皮層裂解酶。
2.2 枯草芽孢桿菌芽孢皮層裂解酶粗酶SDS-PAGE電泳結果
對皮層裂解酶粗酶進行SDS-PAGE電泳分析,由于酶的濃度較低,在凝膠板上并未看到蛋白條帶,將酶液進行超濾濃縮后再次進行SDS-PAGE電泳分析,結果如圖5。
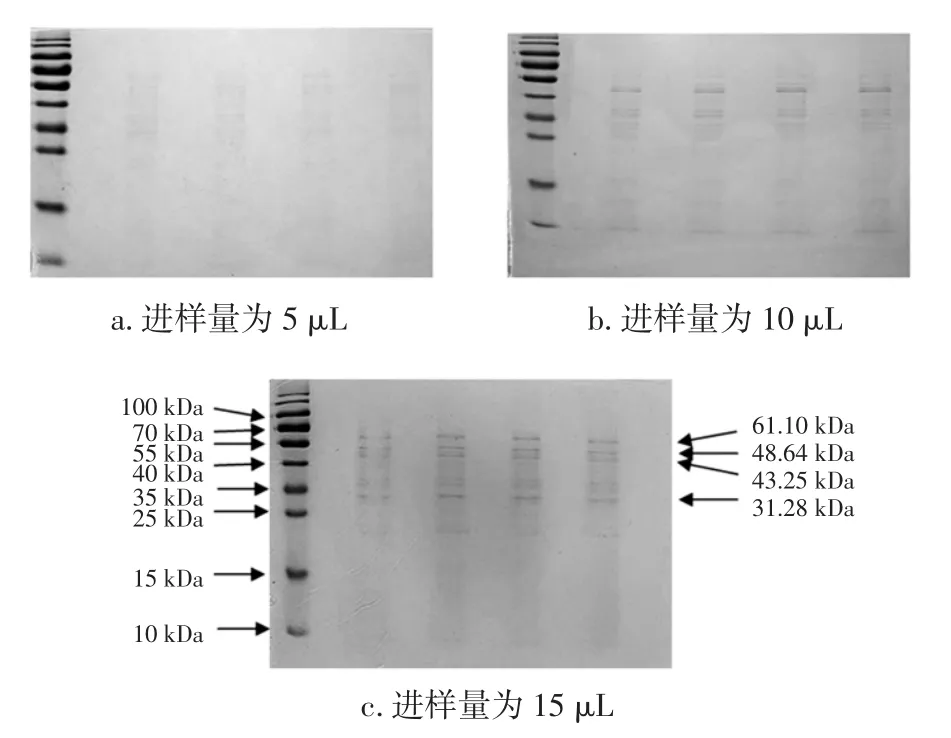
圖5 分離膠濃度為12%的SDS-PAGE電泳圖Fig.5 SDS-PAGE electrophoresis of the separation gel concentration of 12%
由圖5可以看出,進樣量為5 μL時,只能看到蛋白跑過的印跡,無明顯可見條帶,進樣量為10 μL時,能大致看到蛋白條帶,但條帶仍不清晰,隨著進樣量的逐漸增大,蛋白條帶逐漸清晰,增大進樣量至15 μL,能看到清晰的蛋白條帶;但各條帶之間的距離很小,整體分離效果并不良好。
調節分離膠濃度為10%,結果如圖6。
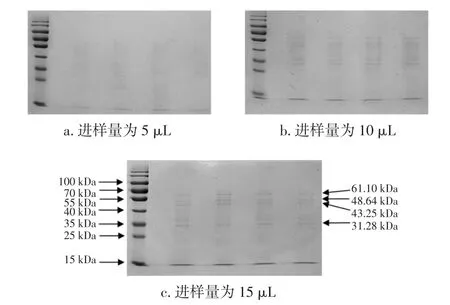
圖6 分離膠濃度為10%的SDS-PAGE電泳圖Fig.6 SDS-PAGE electrophoresis of the separation gel concentration of 10%
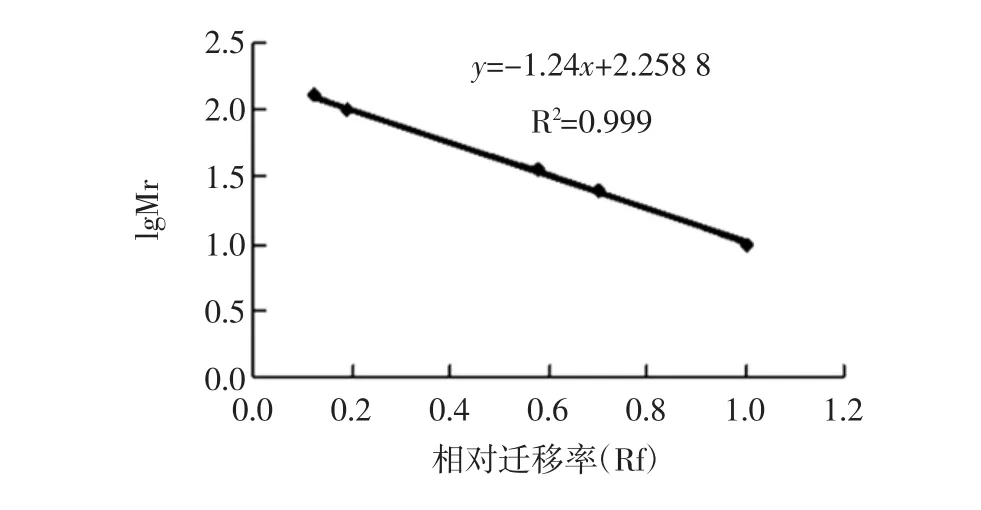
圖7 蛋白質分子量標準曲線Fig.7 Standard curve of molecular weight of protein
可以看出,各蛋白條帶間距明顯拉開,分離效果較好。電泳時,在相對較高濃度分離膠系統中,由于凝膠孔徑相對較小,樣品分子的移動速度因受阻較大而減緩,遷移率就相對較低,對于較大分子量的蛋白而言,所受阻力較大,分離效果較差;在相對較低濃度分離膠系統中,由于凝膠孔徑相對較大,樣品分子的移動只是稍受阻礙,對于較大分子量的蛋白而言,遷移速度較快,遷移率較高,分離效果較好。從圖5-c和6-c可以看出,10%與12%的凝膠系統相比,分子量為48.64 kDa和43.25 kDa的兩種蛋白,在10%的凝膠系統中分離效果更好。所得的PAGE圖像中有多條蛋白條帶,但條帶的強弱有所不同,有4條蛋白條帶較為清晰,通過蛋白質分子量標準曲線(見圖7)可得出,皮層裂解酶粗酶液中蛋白分子量大約分別為:61.10、48.64、43.25、31.28 kDa。Makino[14]分離純化蠟樣芽孢桿菌芽孢萌發時放出的一種皮層裂解酶,經SDS-PAGE電泳法測得皮層裂解酶分子量大約為24 kDa;Miyata[13]純化梭狀芽孢桿菌S40芽孢皮層裂解酶得到的皮層裂解酶分子量為31.0 kDa;Simon[21]在研究一種萌發專一性的巨大芽孢桿菌皮層裂解酶的純化和性質時,純化出的皮層裂解酶分子量為29 kDa。本試驗所提取的皮層裂解酶粗酶液中,尚不能確定哪一種蛋白質為皮層裂解酶,后期將根據圖6c中分離出來的4種蛋白質的分子量,選擇合適的分離純化手段,將皮層裂解酶進一步分離純化出來。
2.3 酶活性的測定
為確定所提取到的粗酶液中確實含有皮層裂解酶,檢測了粗酶液的皮層裂解活性,結果如圖8所示。
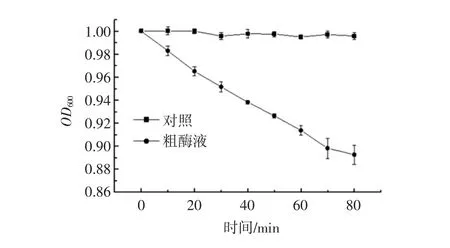
圖8 酶活性的測定Fig.8 Determination of enzyme activity
與對照相比,加入粗酶液的脫芽孢衣芽孢懸浮液的OD600值有極顯著下降(P<0.01),說明粗酶液中含有皮層裂解酶,但具體哪種分子量的蛋白質為皮層裂解酶還需進一步的分離純化和鑒定。本文的試驗結果可為進一步分離純化皮層裂解酶提供基礎。
3 結論
通過研究發現:DPA、L-丙氨酸、肌苷及L-丙氨酸結合肌苷對枯草芽孢桿菌芽孢均有誘導萌發的作用。DPA誘導枯草芽孢桿菌芽孢萌發效果最好,很低濃度的DPA就能迅速誘導芽孢萌發。提取出的皮層裂解酶粗酶液經透析、超濾濃縮后進行SDS電泳,進樣量從5 μL 逐漸增大到 15 μL,當進樣量增大至 15 μL 時,在凝膠板上能看到清晰的蛋白條帶;10%的凝膠系統上的條帶較12%的相比,各條帶間距更大,整體分離效果更好,因此選擇10%的分離膠濃度更為合適。通過蛋白質分子量標準曲線可得出,皮層裂解酶粗酶液中蛋白分子量大約分別為:61.10、48.64、43.25、31.28 kDa,可根據以上試驗結果選擇進一步分離純化皮層裂解酶的手段和條件。
[1] 章中,楊宏偉,胡濟美,等.化學物質輔助超高壓處理對枯草桿菌芽孢的作用[J].中國食品學報,2015,15(5):47-53
[2]YASUDA Y,TOCHIKUBO K.Spore Germination and Outgrowth[J].Journal of Antibacterial&Antifungal Agents Japan,1997,25:333-348
[3] 程琴,黃庶識,陳麗梅.芽孢桿菌孢子萌發機理的研究進展[J].生命科學,2010(9):878-885
[4]SHAH I M,LAABERKI M H,POPHAM D L,et al.A eukaryoticlike Ser/Thr kinase signals bacteria to exit dormancy in response to peptidoglycan fragments[J].Cell,2008,135:486-496
[5]章中.熱和化學因素輔助超高壓對枯草桿菌芽孢的滅活研究[D].北京:中國農業大學,2013
[6] 高志奇,劉先凱,王恒樑.炭疽芽孢桿菌芽孢萌發研究進展[J].軍事醫學科學院院刊,2014(10):833-836
[7] MAKINO S,MORIYAMA R.Hydrolysis of cortex peptidoglycan during bacterial spore germination.[J].Medical Science Monitor International Medical Journal of Experimental&Clinical Research,2002,8(8):RA119-127
[8]BLACK E P,SETLOW P,HOCKING A D,et al.Response of spores to high-pressure processing[J].Comprehensive Reviews in Food Science and Food Safety,2007,6(4):103-119
[9] ZHANG Z,JIANG B,LIAO X,et al.Inactivation of Bacillus subtilis spores by combining high-pressure thermal sterilization and ethanol[J].International Journal of Food Microbiology,2012,160(2):99-104
[10]REINEKE K,MATHYS A,HEINZ V,et al.Mechanisms of endospore inactivation under high pressure[J].Trends in Microbiology,2013,21(6):296-304
[11]GAO Y L,JU X R,JIANG H H.Studies on inactivation of Bacillus subtilis spores by high hydrostatic pressure and heat using design of experiments[J].Journal of Food Engineering,2006,77(3):672-679
[12]GOMBAS D E,LABBE R G.Extraction of spore-lytic enzyme from Clostridium perfringens spores[J].Journal of General Microbiology,1981,126(1):37-44
[13]MIYATA S,MORIYAMA R,SUGIMOTO K,et al.Purification and partial characterization of a spore cortex-lytic enzyme of Clostridium perfringens S40 spores[J].Bioscience Biotechnology&Biochemistry,1995,59(59):514-515
[14]MAKINO S,ITO N,INOUE T,et al.A spore-lytic enzyme released from Bacillus cereus spores during germination[J].Microbiology,1994,140(2):1403-1410
[15]王一曉.熱和化學物質最佳誘導枯草桿菌芽孢萌發條件的研究[D].銀川:寧夏大學,2016
[16]黃體冉,張國慶,王文平,等.SDS-聚丙烯酰氨凝膠電泳法測定蛋白質相對分子質量的改良和優化[J].高校實驗室工作研究,2016(3):63-66
[17]謝喜珍,林娟,謝勇,等.海洋來源瓊膠酶的分離純化及酶學性質研究[J].中國生物工程雜志,2017,37(1):46-52
[18]郭堯君.蛋白質電泳實驗技術[M].北京:科學出版社,2005:186-189
[19]伊金玲.產甲殼素酶菌株HD002的篩選鑒定、發酵條件優化、酶的分離純化及酶學性質研究[D].青島:中國海洋大學,2010
[20]MINH H N T,DANTIGNY P,PERRIER-CORNET J M,et al.Germination and inactivation of Bacillus subtilis,spores induced by moderate hydrostatic pressure[J].Biotechnology&Bioengineering,2010,107(5):876-83
[21]FOSTER S J,JOHNSTONE K.Purification and properties of a germination-specific cortex-lytic enzyme from spores of Bacillus megaterium KM.[J].The Biochemical Journal,1987,242(2):573-579

