體外模擬消化對藍莓皮渣粗提物抗氧化成分及其活性的影響
周笑犁,吳珊珊,林棟,杜斌,陳敏,張婷
(1.貴陽學院食品與制藥工程學院,貴州貴陽550005;2.貴州省果品加工工程技術研究中心,貴州貴陽550005)
在生物體內,活性氧和抗氧化防御系統總是處在一個動態平衡的過程中,一旦這個平衡被破壞,那些具有高反應活性的活性氧基團能夠直接造成人體生物膜系統的損傷,從而導致正常細胞的裂解死亡[1-2];過剩的自由基還會誘導氧化應激現象,氧化體內的蛋白質、脂肪和核酸等[3],抗氧化物質則能在一定程度上保護生物機體免遭活性氧基團的破壞。藍莓為杜鵑花科(Ericaceae)越橘屬(Vaccinium.spp)植物,主要分布于我國山東、吉林、遼寧、江蘇、貴州等地區;據報道藍莓果實能夠減緩衰老,預防腦神經老化,增強記憶力,預防心血管病,增強自身免疫力等功效[4-6]。藍莓果實中含有豐富的花色苷、多酚,它們作為一種良好的抗氧化劑,能有效抑制氧自由基的產生或清除氧自由基,已有較多的研究證明了其活性[7-8]。
近年來,利用體外消化模型研究生物活性物質越來越受到國內外的關注。相對于研究物質體內的消化,體外模擬消化是一種較為簡單、有效的模擬消化過程,不僅可以在某種程度上反映物質在體內的變化情況,而且體外研究法消耗財力少,還具有易于操控等優勢[9-10]。但目前關于藍莓果實中活性物質在體內消化過程中的變化情況我們還了解甚少,特別是對于富含活性成分的果皮渣這一加工副產物。本文嘗試通過體外模擬胃腸消化方法,評價藍莓果皮渣粗提物在消化過程中活性物質的變化規律,及其抗氧化活性,以期對藍莓及其加工副產物的抗氧化活性進行更全面科學的評價,為藍莓加工副產物-果皮渣在醫藥、營養及保健食品中的應用提供一些參考。
1 材料與方法
1.1 試驗原料
藍莓皮渣干粉是在貴州省果品加工工程技術研究中心經藍莓鮮果制作果汁后所剩的皮渣副產物,再經干燥粉碎;α-淀粉酶(3 700 U/g,生化試劑)、胃蛋白酶(3 000 U/g,生化試劑)、胰酶(4 000 U/g,生化試劑):上海金穗生物科技有限公司;膽汁(生化試劑):Ruibio;氯化鈣、氯化鉀、福林酚、無水乙醇、磷酸氫二鈉、磷酸二氫鈉、鐵氰化鉀、碳酸鈉、硝酸鋁、碳酸氫鈉、三氯乙酸、三氯化鐵、硫酸亞鐵、水楊酸、雙氧水均為分析純。
1.2 儀器設備
UV-2550紫外分光光度計:日本島津公司;TDL-16RH離心機:上海安亭科學儀器廠;烘箱:天津市泰斯特儀器有限公司;PHS-3C pH計:上海雷磁;SHB-III循環水真空泵:上海亞榮生化儀器廠;SHA-B數顯水浴恒溫振蕩器:常州澳華恩斯儀器有限公司。
1.3 試驗方法
1.3.1 藍莓皮渣粗提物
稱取50 g的藍莓皮渣干粉,用100 mL 95%乙醇-0.1%HCl溶液(1∶1,體積比)作為提取液,在40℃下超聲提取,冷卻后進行抽濾,再將濾渣進行重提兩次,合并濾液即為皮渣粗提物。
1.3.2 體外模擬消化[11]
體外模擬消化試驗,包含體外模擬胃消化和腸消化兩部分。體外模擬腸消化是在唾液和胃消化的基礎上,再進行腸消化。
1.3.2.1 消化液的配制[9-10]
體外模擬胃液:稱取135mg胃蛋白酶(3000U/mL)加入500 mL胃電解質溶液,混合均勻,用1 mol/L HCl調pH值至2。
體外模擬腸液:向90 mL腸電解質溶液中加入90 mL胰酶和膽汁溶液,搖晃均勻,用1 mol/L NaHCO3調節pH值至7。
胃電解質溶液:稱取 3.1 g NaCl、1.1 g KCl、0.15 g CaCl2、0.6 g NaHCO3用去離子水溶解并定容至1 L。
腸電解質溶液:稱取 5.4 g NaCl、0.65 g KCl、0.33 g CaCl2用去離子水溶解并定容至1 L。
1.3.2.2 模擬胃消化
取一定量藍莓皮渣粗提物,分別稀釋2、5、10倍,即為高、中、低濃度粗提液。分別取3種濃度的粗提液加入α-淀粉酶/CaCl2溶液(模擬唾液),混合均勻,在37℃水浴恒溫振蕩器里消化10 min;然后加入體外模擬胃液(對照組為不添加胃蛋白酶的胃電解質溶液),并調節樣品組和對照組pH2.0,避光于37℃和100 r/min搖床中模擬胃消化培養,分別在消化0.5、1、2 h后取樣品,6 000 r/min下離心10 min,取上清液于-20℃凍存,以備后面分析用。
1.3.2.3 模擬腸消化
經過唾液和胃消化后的消化液中加入體外模擬腸液(對照組為不添加胰酶和膽汁的腸電解質溶液),此時即為模擬腸消化前。然后用1 mol/L NaHCO3調節樣品組和對照組pH值至7.2,繼續置于100 r/min,37℃的搖床中模擬腸消化培養,分別在消化 0.5、1、2、3、4 h后取樣品,在6 000 r/min下離心10 min,取上清液于-20℃凍存,以備后面分析用。
1.3.3 消化液抗氧化成分分析
1.3.3.1 花色苷含量的測定[8]
將消化液分別用NaAc緩沖液和KCl緩沖液稀釋,于黑暗處靜置20 min后在分光光度計上分別測定樣品在510 nm和710 nm處的吸光度進行計算:A=(A510-A700)pH1.0-(A510-A700)pH4.5;則粗提物樣品液中花色苷的濃度為:C/(mg/mL)=(A×MW×DF)/(ε×1)。
式中:MW為樣品中主要花色苷的分子量,MW=449.2;DF為稀釋因子;ε為樣品中主要花色苷的摩爾吸收率,ε=26 900。
1.3.3.2 多酚含量測定
參考福林法[8],移取模擬胃、腸消化液1 mL于比色管中,各加入福林酚試劑3 mL,搖勻后避光放置30 s,再各加入12%Na2CO3溶液6.0 mL,以沒食子酸為標準品,在760 nm處測定吸光度。
1.3.3.3 黃酮的測定
取0.5 mL模擬胃、腸消化液,各加入0.4 mL 5%Na2CO3溶液,搖勻,放置5 min后加入0.4 mL的10%Al(NO3)3溶液,定容至10 mL。室溫下放置15 min,在波長510 nm處測定吸光值。以蘆丁為標準品,采用硝酸鋁-亞硝酸鈉比色法測定總黃酮含量[12]。
1.3.4 消化液抗氧化活性分析
1.3.4.1 還原能力的測定
采用普魯士藍法[13],移取1 mL模擬胃、腸消化液,依次加入0.2 mol/L磷酸鹽緩沖液(pH6.6)2.5 mL和質量分數1%六氰合鐵酸鉀溶液2.5 mL,放入50℃水浴20 min,快速冷卻,再加入10%三氯乙酸2.5 mL,3 000 r/min下離心10 min,移取上清液2.5 mL,依次加入2.5 mL蒸餾水,0.5 mL 0.1%三氯化鐵溶液,充分搖勻,靜置10 min后,在波長為700 nm處測定其吸光值。
1.3.4.2 清除羥自由基(·OH)活性
在帶塞試管中依次加入2 mL 9 mmol/L FeSO4、2 mL 9 mmol/L水楊酸和3 mL模擬胃、腸消化液,最后分別加入2 mL 8.8 mmol/L H2O2啟動反應,在37℃水浴中反應1 h,于波長510 nm處測量吸光值[14],清除率/%=[A0-(Ai-Ai0)]/A0×100。
式中:A0為樣品濃度為0 mg/mL時的吸光值;Ai為加入樣品時的吸光值;Ai0為對應樣品中無顯色劑時的吸光值。
1.3.5 試驗數據分析與統計
數據用平均值±標準差表示。用SPSS17.0進行統計分析,以p<0.05作為差異顯著性判斷標準。
2 結果與分析
2.1 體外模擬消化過程中藍莓皮渣粗提物抗氧化成分的變化
2.1.1 花色苷
藍莓皮渣粗提物模擬胃腸道消化過程中花色苷含量的變化如圖1所示。
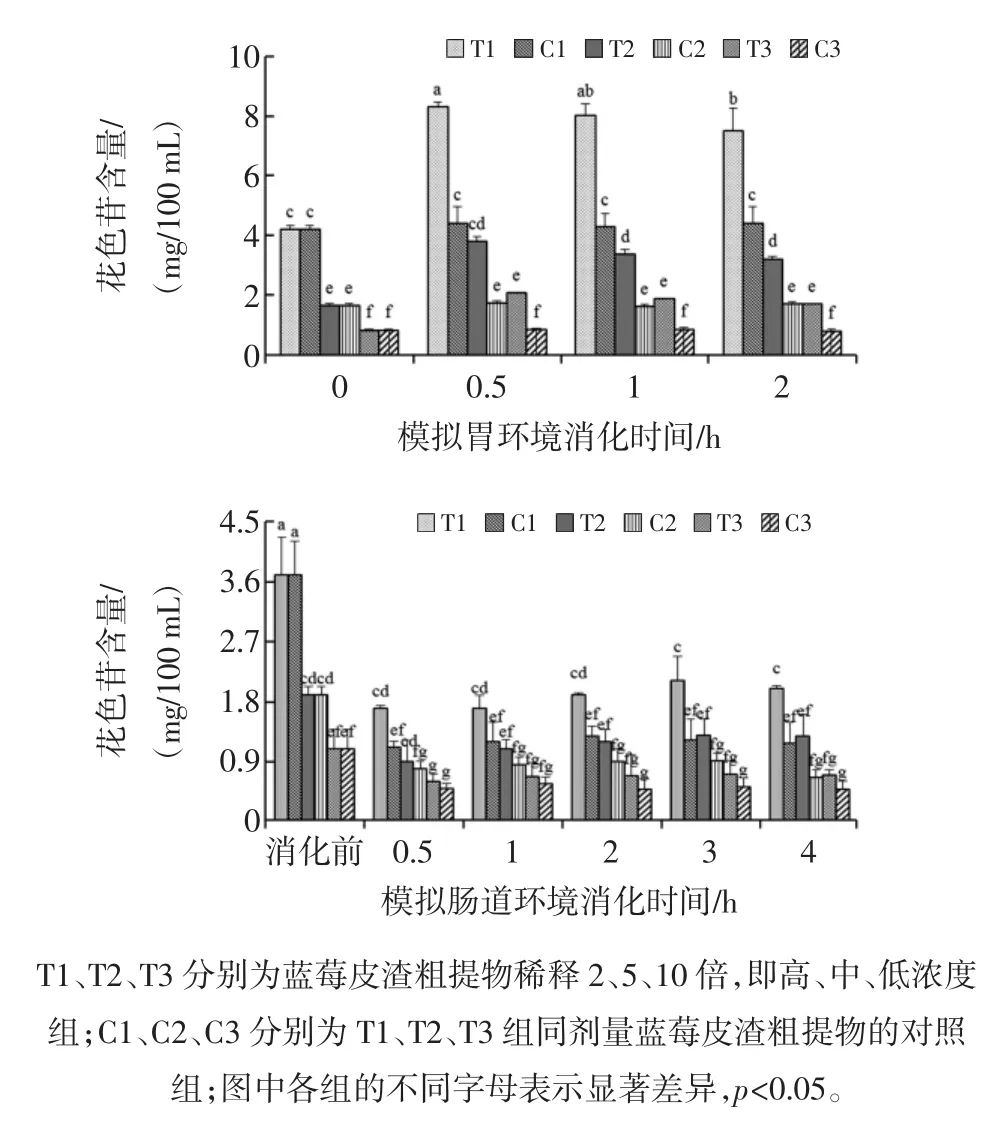
圖1 體外模擬胃腸消化對藍莓皮渣粗提物花色苷釋放量的影響Fig.1 Effect of in vitro simulated gastric and intestinal digestion on anthocyanin released from digested crude extract of blueberry pomace
由圖1可知,較消化前,不同濃度的粗提物經胃消化后花色苷均有了顯著的提高(p<0.05);在模擬胃消化過程中,花色苷含量均顯著增加再減少,在胃消化30 min時各組含量呈現最大峰值;并比相應濃度的對照組(未加胃蛋白酶消化)花色苷含量也顯著增加(p<0.05),而3個不同劑量的對照組花色苷釋放量在模擬消化前后均無顯著變化(p>0.05)。
模擬胃消化2 h結束后進行腸消化,各組花色苷含量迅速且顯著降低(p<0.05),直到模擬腸道環境消化2 h左右,高、中、低濃度的粗提物花色苷含量輕微增加,但均低于消化前的含量,且隨著消化時間的延長又逐漸減少,而3個不同劑量的對照組花色苷釋放量在模擬腸道消化前后均顯著減少(p<0.05)。藍莓皮渣粗提物在模擬胃環境中花色苷含量的提高可能是胃蛋白酶消化的酸性環境(pH2.0)引起的,在該環境下添加的酶促進了花色苷的釋放,可能花色素與蛋白質復合物中的蛋白質在胃蛋白酶的作用下水解從而失去了束縛被釋放;而對照組中花色苷由于酸性條件下較為穩定,變化不顯著(p>0.05);但在模擬腸道環境中花色苷含量有所降低可能由于所存在的一些酶或是pH值變化使得花色苷含量和存在形式發生變化。有研究表明葡萄在腸胃消化后會損失90%的花色苷[15],而楊梅最高會損失59.3%[16],這與本試驗的結果較一致,藍莓皮渣粗提物經胃消化后其中花色苷可增加一倍,而經腸道消化后比消化前損失了近50%,與其他幾種活性成分相比,花色苷在胃腸消化后的損失更加顯著。
2.1.2 多酚
多酚化合物普遍存在于水果、蔬菜、堅果和谷物中[17],是廣泛存在于植物中的次級代謝產物,可以有效清除自由基、抑制脂質過氧化,具有抗氧化、抗菌等多種生物活性[18-19]。模擬胃腸道消化過程中藍莓皮渣粗提物多酚含量的變化如圖2所示。
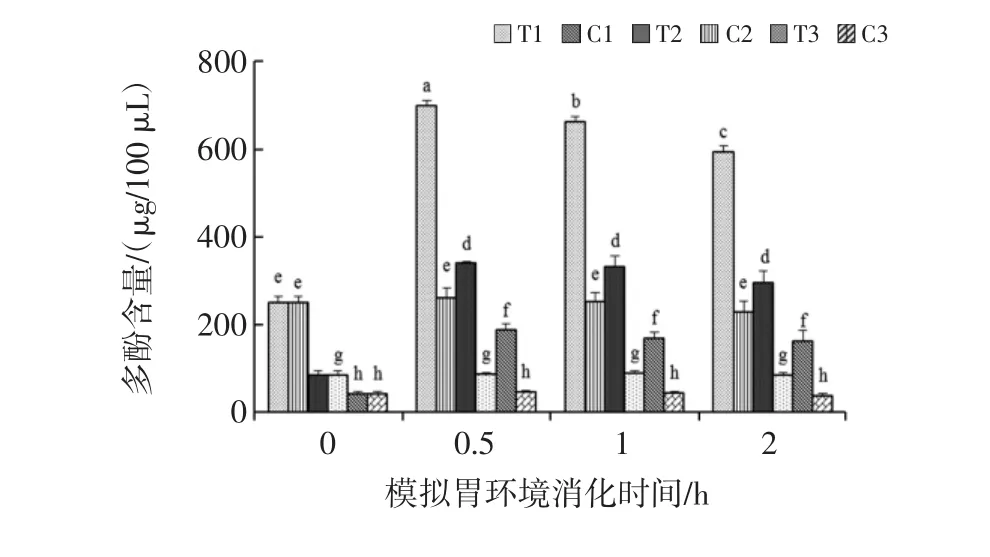
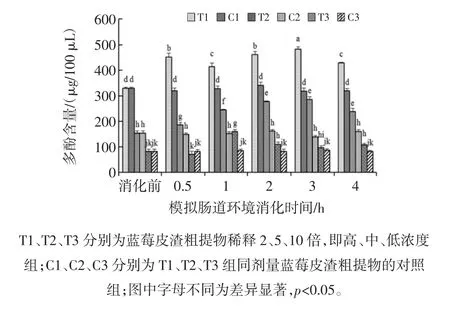
圖2 體外模擬胃腸消化對藍莓皮渣粗提物多酚釋放量的影響Fig.2 Effect of in vitro simulated gastric and intestinal digestion on phenolics released from digested crude extract of blueberry pomace
由圖2可知,3組不同劑量的粗提物經胃消化后多酚含量呈先上升,在30 min時其含量達到最大,隨之含量略有下降并趨于穩定;模擬胃消化過程中高、中、低濃度提取物組多酚的最大釋放量分別為胃消化0 h的 2.8、3.9、4.3倍(p<0.05);對照組的多酚含量在模擬胃消化2.0 h內的變化沒有顯著性差異(p>0.05),表明胃蛋白酶的消化使藍莓皮渣粗提物中的多酚物質進一步釋放出來。李俶報道了由于酚類化合物單體之間形成一定的相互作用,增加了其在胃腸液內的穩定性[20]。在黑枸杞體外消化過程中發現酶解和pH值的變化更能夠讓酚酸從結合態分解為自由態[11]。
而經模擬腸道消化時,藍莓皮渣粗提物中多酚隨著消化時間的增加而逐漸增大,高、中濃度組在2 h~3 h時達到最大后趨于穩定,而低劑量組則較早(1 h~2 h)達到最大多酚量后趨于穩定。在胃消化和腸消化階段藍莓皮渣多酚比消化前和對照組均顯著增加(p<0.05),可能是模擬消化液中的消化酶(淀粉酶、胃蛋白酶與胰酶)逐步破壞了食物基質的細胞壁,促進了游離酚類的逐步釋放[21-22]。至于腸消化階段的多酚含量較胃消化階段顯著降低,這與麩皮體外消化多酚的變化情況較一致,卻不同于全麥和精面多酚的釋放規律[2];也有關于葡萄進行體外消化的研究發現,酚酸、花青素和白藜蘆醇在腸液條件下降解[3,15]。因此在本試驗腸道模擬消化環境,胰酶可能繼續使結合態多酚釋放為游離態,但酚酸和花青素對消化酶或者腸道環境敏感產生不穩定而發生降解,因而腸液消化組的多酚含量沒有表現出明顯的增加。
2.1.3 黃酮
體外模擬胃腸消化過程中藍莓皮渣粗提物黃酮釋放量的變化情況如圖3所示。
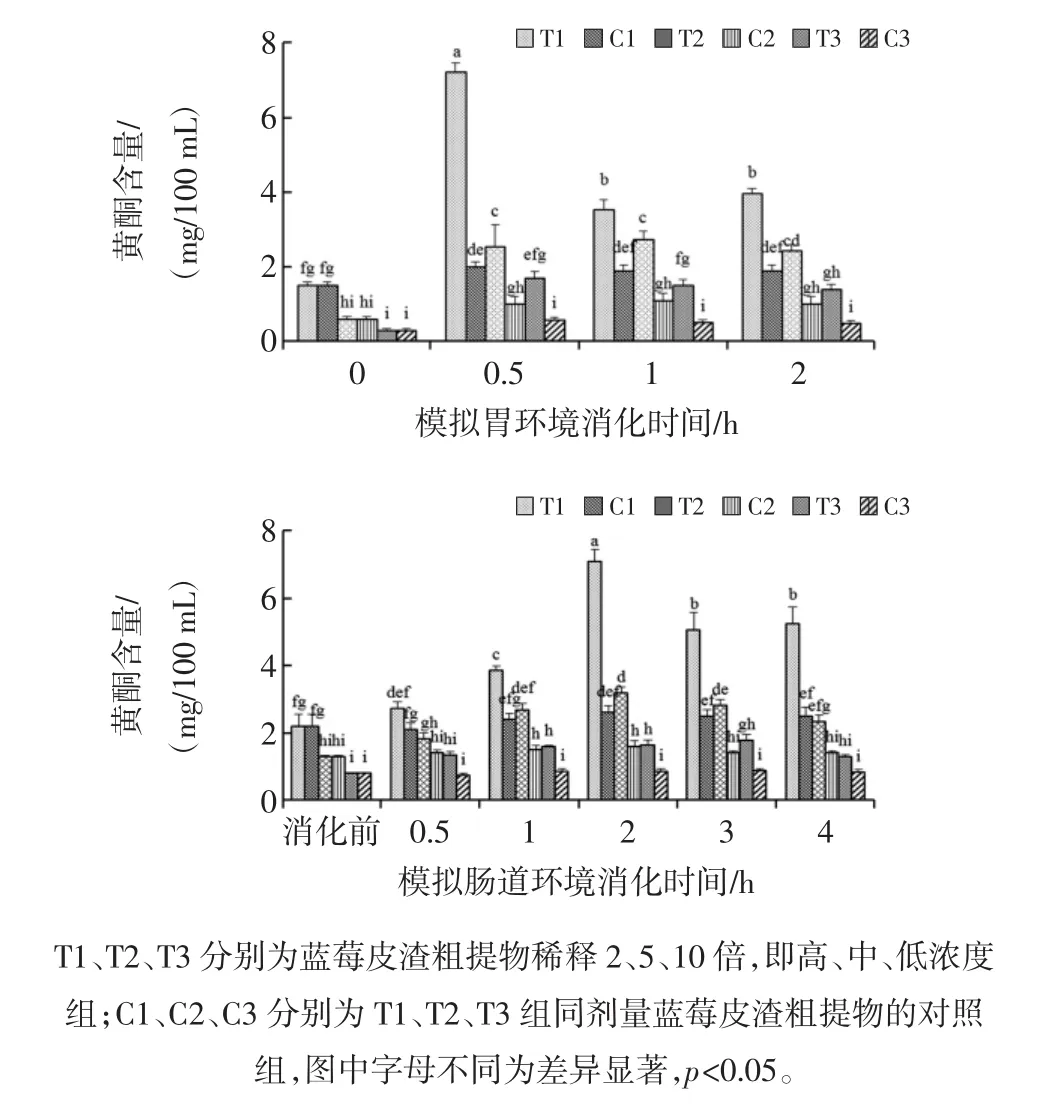
圖3 體外模擬胃腸消化對藍莓皮渣粗提物黃酮釋放量的影響Fig.3 Effect of in vitro simulated gastric and intestinal digestion on flavonoid released from digested crude extract of blueberry pomace
與模擬胃消化0 h相比,3組不同劑量藍莓皮渣粗提物的黃酮釋放量在0.5 h內顯著升高(p<0.05),隨之下降,可能是隨著消化時間的延長,穩定性差的組分發生了降解,消化1 h后黃酮釋放量趨于穩定,對照組的黃酮釋放量在模擬胃消化過程中也有一定的增加,這表明胃蛋白酶和胃酸對黃酮的釋放均具有一定的作用,這與芒果、蘋果中黃酮經胃消化后的釋放趨勢一致[3,23]。
經模擬腸道環境消化后,腸消化組中藍莓皮渣粗提物的黃酮含量逐漸上升,2 h后黃酮含量達最大值,是胃0 h黃酮含量的4.63倍,是腸消化前(胃消化反應但未進行腸消化)的3.2倍。空白組的黃酮含量在模擬腸消化過程中無顯著變化(p>0.05),表明在模擬腸消化過程中,黃酮類植物化學物釋放增加的主要貢獻來自胰酶和膽汁的作用。黃酮類物質也屬于多酚中具有抗氧化活性很高的一類物質,而本試驗中黃酮的變化和多酚略有差異,說明在體外消化過程中,不同的多酚物質在pH值和酶的作用下發生了不同的變化。并且黃酮與上述兩種活性成分在模擬胃腸道的釋放量相比,在腸道環境中更為穩定。
2.2 體外模擬消化過程中藍莓皮渣粗提物抗氧化活性的變化
2.2.1 還原能力
體外模擬胃腸消化對藍莓皮渣粗提物還原能力的影響見圖4。
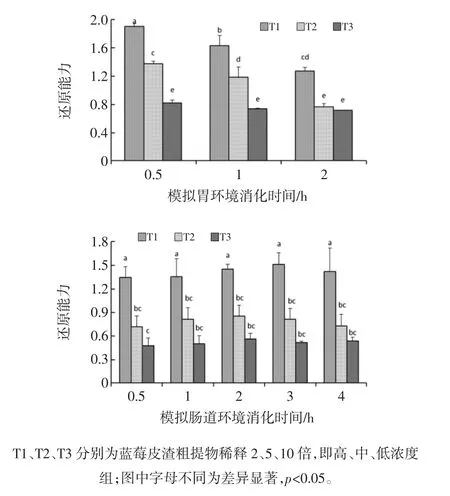
圖4 體外模擬胃腸消化對藍莓皮渣粗提物還原能力的影響Fig.4 Effect of in vitro simulated gastric and intestinal digestion on reducing power from digested crude extract of blueberry pomace
從圖4可以看出,藍莓皮渣粗提物在模擬胃消化后,其還原能力在初始消化的30 min最大,隨著胃消化時間的延長,其還原能力逐漸下降,尤其是高濃度組在30 min時的還原能力顯著高于消化1 h和2 h,也顯著高于其他各組(p<0.05)。模擬腸道消化環境中,隨著消化時間的延長,各組還原能力呈先增加再減少,在消化2 h~3 h時,各組樣品均能呈現較強的還原能力;模擬腸道消化的藍莓皮渣粗提物的還原能力均低于模擬胃液中的還原能力。這可能與胃消化后藍莓皮渣粗提物中花色苷、多酚的含量顯著增加有關,而腸道環境處于中性使得花色苷等活性成分的結構發生變化,從而導致活性的降低。無論在模擬胃液或模擬腸液中,隨著藍莓皮渣粗提物濃度的下降,其還原能力也隨之減小。
2.2.2 清除羥自由基能力
體外模擬胃腸消化對藍莓皮渣粗提物羥自由基的影響見圖5。
從圖5可以看出,模擬胃腸道消化過程中,高濃度提取物組的羥自由基清除率均高于低濃度組。藍莓皮渣粗提物胃液消化組羥自由基清除率在消化0.5 h內達到最大,在消化1 h~2 h保持穩定,這和其他抗氧化成分的變化基本一致;藍莓皮渣粗提物經胃腸消化組分的抗氧化能力提高,其原因可能與經胃腸消化后組分中多酚和花色苷含量的顯著增加有關。模擬人體腸環境中,各組羥自由基清除率有所降低,消化過程中呈先上升,2 h后基本趨于平緩的變化趨勢,可能經過模擬人體腸環境處理后花色苷、多酚等活性成分發生大量損失使得活性降低;抗氧化活性是所有活性成分發揮協同和拮抗作用的結果,胃腸環境的變化可能影響了活性成分的結構和相互作用[3]。
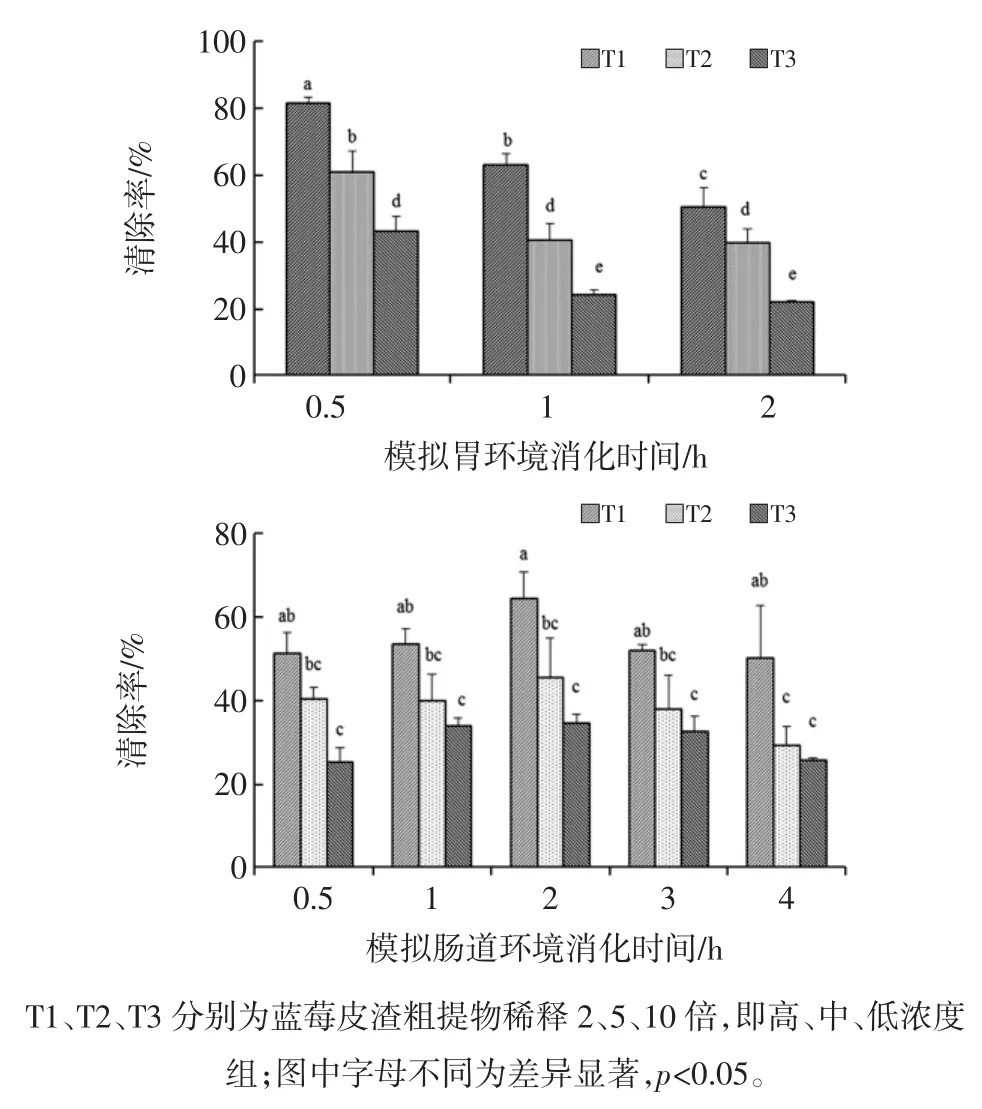
圖5 體外模擬胃腸消化對藍莓皮渣粗提物羥自由基的影響Fig.5 Effect of in vitro simulated gastric and intestinal digestion on the hydroxyl free radical scavenging activity from digested crude extract of blueberry pomace
3 結論
消化系統是生物體的營養攝入系統,食物與消化液之間的相互作用極其復雜。從一方面來說,消化液會破壞細胞結構,促進食物中活性物質的釋放;從另一方面來講,消化液同時也會對活性物質本身造成一定程度的破壞[2-3,21]。由于研究胃腸道消化吸收對食物的影響存在很多困難,因此通過體外模擬胃腸道消化成為研究食品在胃腸消化吸收常用的手段之一[10,20]。目前對于藍莓生物活性研究,包括黃酮、色素、多酚等,均采用傳統的有機溶劑提取法,但此種方法測定的活性成分含量與人體消化吸收的含量之間存在著較大的差異,不足以準確反映藍莓營養成分的實際價值,鄭影已對不同提純度的藍莓模擬消化后的抗氧化進行了研究[4]。任何一種生物活性物質在發揮其作用之前,都要經過人體的胃腸道消化,而消化也會對多酚化合物的生物活性產生影響。尤其是藍莓皮渣中的活性成分豐富,因此本文采用了體外消化法對藍莓皮渣活性成分和抗氧化活性進行了研究。
本研究結果表明,多酚、花色苷等活性成分經胃消化后含量顯著升高,3個不同劑量樣品組中多酚、花色苷和黃酮釋放量在消化0.5 h內顯著升高,這可能是由于部分蛋白質在胃蛋白酶的作用下水解為小分子多肽,從而被大分子蛋白質包圍的多酚被釋放出來;或胃蛋白酶減弱了部分酚酸與細胞壁間的酯鍵,使酚酸從細胞壁中脫離;也可能是胃蛋白酶破壞了多酚—蛋白質結構,使得多酚脫離了蛋白質分子的束縛[22]。對照組中的花色苷和多酚活性成分消化前后無顯著差異,可見酸堿環境對他們的釋放無明顯影響,胃蛋白酶和胃酸對黃酮的釋放均具有一定的作用。而從酸性的胃環境過渡到溫和的堿性腸道環境中,由于pH值的變化,會造成生物可利用多酚,尤其是花色苷減少。模擬腸道環境的酶可能作用于結合態的酚類物質,中性或偏堿性多酚可以在腸液介質中穩定存在(如槲皮素),而酸性多酚大量降解或異構為其它堿性條件下穩定的形式,在腸道中各活性成分的多少也就取決于其釋放量和降解量的高低。本試驗中藍莓皮渣粗提物中黃酮比多酚和花色苷在腸液中穩定,沒有出現顯著的降低,雖然黃酮仍屬于多酚,但沒有在多酚中表現出來,有可能是消化過程中釋放的黃酮類物質占多酚的總含量比較少,或者黃酮降解、轉化產生的物質不影響多酚含量的測量。粗提物在模擬消化過程中抗氧化活性的變化規律與多酚的釋放規律基本一致,雖然腸道中黃酮的量較高,但可能其在消化過程中的釋放增加不足以引起抗氧化活性的顯著變化。由于原材料本身物質的不同,各活性成分含量及抗氧化活性在模擬消化過程中的變化情況不完全一樣。但為了能深入分析藍莓皮渣經胃腸消化后釋放出的活性成分否被人體吸收,還需要利用細胞模型和動物模型來做進一步的研究。
[1] Neal O,Liu RH.Health benefits of whole grain phytochemicals[J].Critical Reviews in Food Science and Nutrition,2010,50:193-208
[2] 劉冬,萬紅霞,趙旭,等.小麥不同部位在體外模擬消化過程中抗氧化活性的變化規律[J].現代食品科技,2016,32(4):94-99
[3] 彭夢雪,從彥麗,劉冬.模擬胃腸消化評價蘋果多酚、黃酮及抗氧化活性的相關性[J].現代食品科,2016,32(1):122-129
[4] 鄭影,何玉龍,鄭洪亮,等.藍莓花色苷體外及模擬人體胃腸環境的抗氧化活性研究[J].食品與生物技術學報,2014,33(7):736-740
[5] 李穎暢,李冰心,孟良玉,等.圣云藍莓花色苷不同組分的體外抗氧化性和穩定性[J].食品科學,2012,33(9):105-109
[6] 陳介甫,李亞東,徐哲.藍莓的主要化學成分及生物活性[J].藥學學報,2010,45(4):422-429
[7] 周笑犁,杜斌,周艷,等.藍莓皮渣花色苷粗提物的抗氧化性[J].食品與發酵工業,2017,43(6):181-186
[8] 周笑犁,陳麗,王瑞,等.藍莓不同部位常規營養成分及活性物質的比較分析[J].食品工業科技,2016,37(8):283-289
[9] BLANQUET S,EVELIJIN Z,BEYSSAC E,et al.A dynamic artificial gastrointestinal system for studying the behavior of orally administered drug dosage forms under various physiological conditions[J].Pharmaceutical Research,2004,21(4):585-591
[10]閔芳芳,聶少平,萬宇俊,等.青錢柳多糖在體外消化模型中的消化與吸收[J].食品科學,2013,34(21):24-29
[11]樓舒婷,林雯雯,孫玉敬,等.黑果枸杞中多酚的體外消化及其抗氧化性研究[J].食品工業科技,2015,36(11):66-70
[12]Kim IS,Yang MR,Lee OH,et al.Antioxidant activities of hot water extracts from various spices[J].International Journal of Molecular Sciences,2011,12(6):4120-4131
[13]齊美娜.紫色馬鈴薯中花色苷的提取、產品研制及其抗氧化活性的研究[D].哈爾濱:東北農業大學,2013
[14]李穎暢,孟憲軍.藍莓花色苷抗氧化活性的研究[J].食品與發酵工業,2007,33(9):61-64
[15]Tagliazucchi D,Verzelloni E,Bertolini D,et al.In vitro bioaccessibility and antioxidant activity of grape polyphenols[J].Food Chemistry,2010,120(2):599-606
[16]Huang HZ,Sun YJ,Lou ST,et al.In vitro digestion combined with cellular assay to determine the antioxidant activity in Chinese bayberry(Myrica rubra Sieb.et Zucc.)fruits:A comparison with traditional methods[J].Food Chemistry,2014,146:363-370
[17]Costa P,Grevenstuk T,Costa AMRD,et al.Antioxidant and anticholinesterase activities of Lavandula viridis L’Hér extracts after in vitro gastrointestinal digestion[J].Industrial Crops&Products,2014,55:83-89
[18]Roleira FMF,Tavares-Da-Silva EJ,Varela CL,et al.Plant derived and dietary phenolic antioxidants:anticancer properties[J].Food Chemistry,2015,183:235-258
[20]李俶,王謝祎,翟宇鑫,等.多酚化合物體外模擬消化的穩定性分析[J].食品科學,2016,37(13):1-5
[21]Gumienna M,Lasik M,Czarnecki Z.Bioconversion of grape and chokeberry wine polyphenols during simulated gastrointestinal in vitro digestion[J].International Journal of Food Science and Nutrition,2011,62(3):226-233
[22]熊云霞.體外模擬消化對蘋果和梨的抗氧化活性及抗癌細胞增殖活性影響的研究[D].廣州:華南理工大學,2013
[23]胡義東,文良娟.體外模擬胃腸消化對芒果抗氧化成分及其活性的影響[J].南方農業學報,2014,45(9):1652-1656

