鯉魚魚鱗中甲殼素的提取
高倩倩
(吉林農業科技學院食品工程學院,吉林吉林132101)
甲殼素(Chitin)是一種天然高分子聚合物,它是屬于直鏈的氨基多糖[1],別名為甲殼質或幾丁質等。通常采用β-1,4糖苷鍵形式連接,也稱為N-乙酰-葡萄糖胺的聚糖[2]。這種高分子聚合物不溶于水、稀酸、稀堿、濃堿,也不溶于一般的有機溶劑,可溶于濃HCl、H2SO4、H3PO4和無水HCOOH,主鏈易發生降解。甲殼素在食品、醫藥科學、材料、農業、微生物學、免疫學等方面應用廣泛[3],具有提高人體免疫力、抗癌抑制癌、癌細胞轉移等作用,另外,對于高血壓、糖尿病、肝腎病、肥胖等癥狀也特別適用。
天然多糖的種類繁多,既可以顯酸性也可以顯堿性,其中一種多糖─殼聚糖,化學名稱為:聚葡萄糖胺(1,4)-2-氨基-B-D,顯堿性的,所以稱之為堿性多糖,殼聚糖是由甲殼素脫乙酰基后得來的產物[4],主要包括糖類、維生素、脂肪、蛋白質和無機鹽[5]。具有降血脂、降血糖、降血壓等多種保健功效。
鯉魚是一種淡水魚,種類多、量產高、分布廣,養殖歷史悠久。副產物魚鱗通常被廢棄掉,不但浪費資源,也會污染環境[6-7]。魚鱗中含有蛋白質及多種維生素和脂肪,也含有鈣、鐵、鋅等微量元素,以及豐富的甲殼素和多種不飽和脂肪酸[8],對于減少膽固醇在血管壁上的累積有一定的作用,因此,在預防高血壓、心臟病及動脈硬化等疾病方面有一定功效[9]。目前,工業化生產中,對于甲殼素/殼聚糖的提取,主要集中在蝦蟹等原料上[10-12],如從小龍蝦中提取甲殼素和殼聚糖,但是從鯉魚魚鱗中提取甲殼素/殼聚糖研究很少,至今未見報道。本試驗以常見的鯉魚魚鱗為主要原料,采用酸堿法提取甲殼素,再脫乙酰基制備殼聚糖,通過不同的單因素確定甲殼素的最佳提取工藝,擴展了甲殼素和殼聚糖的來源,為全方位利用副產物鯉魚魚鱗提供重要參考依據。
1 材料與方法
1.1 試驗材料
鯉魚魚鱗:吉林市西安路創業大市場;濃HCl、NaOH、KMnO4、草酸、乙醇(95%):文理學院化學實驗室提供。
1.2 試驗儀器
101A-2E型數顯式電熱恒溫水浴鍋:上海實驗儀器廠有限公司;SX-2-4-10型箱式電阻爐:上海均珂儀器科技有限公司;ZHT型自動恒溫電熱套:常州金南儀器制造有限公司;DHG-9420A型電熱恒溫鼓風干燥箱:上海高致精密儀器有限公司;SHB-Ⅲ型循化水式多用真空泵:天津科諾儀器設備有限公司;FA1104N型電子天平:金諾天平儀器有限公司;PHB-4型酸度計:北京時代新維測控設備有限公司。
1.3 試驗方法
1.3.1 甲殼素的提取
將鯉魚魚鱗反復沖洗,去除表面附著物,放入電熱恒溫鼓風干燥箱100℃烘干備用。
魚鱗中的礦物質去除:將干魚鱗在常溫下分別與不同濃度的HCl溶液反應,用玻璃棒充分攪拌直至無氣泡產生為止。傾去酸液,水洗至中性。
魚鱗中的蛋白質去除:向平底燒瓶中加入不同濃度的NaOH溶液,水浴加熱(T=70℃)。傾去堿液,靜置冷卻,水洗2次,酸度計調節溶液呈中性,抽濾,獲得甲殼素粗品。
精制甲殼素:將KMnO4溶液加入到平底燒瓶中,用天平稱取甲殼素粗品,每升KMnO4溶液(0.1 mol/L)中加入5 g粗品。浸泡1 h,漏斗過濾,洗滌,再向平底燒瓶中加入草酸溶液,每升草酸溶液中加入10 g粗品。將其置于水浴鍋中加熱(T=70℃),直到樣品全部變為白色,靜置,當燒瓶溫度達到室溫時,水洗至中性,將其置于恒溫鼓風干燥箱中干燥(T=60℃,t=24 h),制得白色的甲殼素固體。
1.3.2 甲殼素提取條件的優化
設計單因素試驗,分析各個因素:HCl、NaOH溶液濃度和處理時間對甲殼素提取率以及礦物質脫除率的影響。
1)HCl溶液濃度對提取率的影響:稱取干魚鱗5 g左右,分別取不同濃度(0.6、0.8、1.0、1.2、1.4 mol/L)的HCl溶液浸泡魚鱗30 min,將HCl溶液倒掉,水洗至中性,烘干稱重后放入平底燒瓶中,加入1.0 mol/L NaOH溶液,水浴加熱(T=70℃,t=7 min),靜置冷卻,水洗至中性,加入 KMnO4溶液(5 g/L)浸泡 1 h,過濾,將樣品水洗至瓶內水接近無色,再加入草酸溶液(10 g/L),水浴加熱(T=70℃),使樣品全部變為白色,靜置冷卻,置于恒溫鼓風干燥箱中60℃干燥24 h,稱重。計算此次操作中礦物質脫除率和甲殼素的提取率。
2)HCl溶液浸泡時間對提取率的影響:用1)中提取率最高的那組HCl溶液濃度(即1 mol/L)浸泡鯉魚魚鱗,分別在室溫下浸泡 20、25、30、35、40 min,方法同上。
3)NaOH溶液濃度對提取率的影響:稱取干魚鱗5 g左右于燒杯中,用1 mol/L的HCl溶液浸泡去除礦物質,分別用 0.6、0.8、1.0、1.2、1.4 mol/L 的 NaOH 溶液在70℃水浴中處理蛋白質,靜置,當燒瓶溫度達到室溫時,水洗至中性,其他方法同上。
4)NaOH溶液處理時間對提取率的影響:稱取干魚鱗5 g左右,1 mol/LHCl溶液浸泡,再用1 mol/L NaOH 在 70 ℃水浴中分別反應 6、7、8、9、10 min,靜置,當燒瓶溫度達到室溫時,水洗至中性,方法同上,稱重。計算此次操作中的甲殼素提取率。
1.3.3 甲殼素灰分的測定:參照文獻[13]
①坩堝灼燒:取4支坩堝洗凈,放入馬弗爐(T=580℃)中灼燒0.5 h。斷電冷卻,T=250℃左右,用坩堝鉗將坩堝取出,放入到干燥器(干燥劑為硅膠)中冷卻0.5 h。②稱樣品(甲殼素)1 g~2 g左右。③樣品的灼燒:將兩支裝有甲殼素的坩堝至于馬弗爐內300℃灼燒1 h,使其完全炭化,再升高溫度至580℃時加熱1 h,冷卻至250℃以下,再取出置于干燥器中,冷卻1 h,用電子天平稱重。根據公示計算灰分的含量。

式中:X為灰分含量,%;m1為坩堝與灰分的總質量,g;m2為坩堝的質量,g;m3為坩堝與樣品的總質量,g。
1.3.4 甲殼素脂肪含量的測定:參照文獻[14]
準確稱取一定量的甲殼素樣品置于索式提取器中,在圓底燒瓶中加入適量乙醇、人造沸石,安裝索式抽提器。先通水后通電,將電熱套調制200 V左右進行2 h的反應,蒸餾濃縮,回收乙醇,取樣烘干并稱重。根據公式計算脂肪的含量。(文獻用乙醚,有毒)
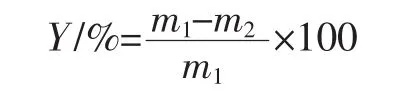
式中:Y為脂肪含量,%;m1為反應前甲殼素的質量,g;m2為反應后甲殼素的質量,g。
1.3.5 殼聚糖的制備
殼聚糖的制備參照喬德亮的方法并進行修改,具體過程如下:稱取一定量按優化工藝提取的甲殼素,于燒杯中,加入1 mol/L NaOH溶液,水浴加熱10 min,溫度80℃[15],使甲殼素脫乙酰基,靜止冷卻至室溫,將NaOH溶液傾倒掉,樣品水洗至中性,用真空抽濾泵抽濾,烘干得到黃色的殼聚糖[16]。
2 結果與分析
2.1 提取甲殼素試驗條件的優化分析
HCl溶液濃度對甲殼素提取率及礦物質脫除率的影響見圖1。

圖1 HCl溶液濃度對甲殼素提取率及礦物質脫除率的影響Fig.1 Effects of HCL concentration on chitin yield rate and mineral removal rate
由圖1可知,在HCl溶液濃度增大的過程中,甲殼素的提取率出現了先升高后降低的現象,在1 mol/L處達到峰值。礦物質脫除率趨于穩定上升狀態,增大HCl溶液的濃度有助于去除鯉魚魚鱗中的礦物質,但一直增大HCl溶液的濃度,甲殼素的提取率也隨之下降,會破壞鯉魚魚鱗中甲殼素,因此單因素試驗中1 mol/LHCl溶液濃度甲殼素提取率最高。
HCl溶液浸泡時間對甲殼素提取及礦物質脫除率的影響見圖2。
由圖2可知,隨著HCl溶液處理魚鱗時間增加,甲殼素的提取率先升高,在30 min處達到峰值,隨后開始下降。礦物質脫除率趨于穩定上升狀態,但在HCl溶液處理時間30 min處開始緩慢下降。由此而知HCl溶液處理時間增加有助于去除鯉魚魚鱗中的礦物質,但HCl溶液處理時間增加甲殼素的提取率也隨之下降,會破壞魚鱗中甲殼素,因此單因素試驗中HCl溶液處理鯉魚魚鱗時間為30 min

圖2 HCl溶液浸泡時間對甲殼素提取及礦物質脫除率的影響Fig.2 Effects of soaking time within HCL solution on chitin yield rate and mineral removal rate
NaOH溶液濃度對甲殼素提取率的影響見圖3。

圖3 NaOH溶液濃度對甲殼素提取率的影響Fig.3 Effects of NaOH concentration on chitin yield rate
由圖3得知,NaOH濃度為0.6 mol/L~1.0 mol/L時,甲殼素的提取率逐漸上升,但是變化幅度不大。超過1 mol/L時,曲線變化幅度大,迅速降低。原因是魚鱗中蛋白質等在NaOH溶液的作用下被分解。濃度越大,甲殼素也會被分解,由此可見,因此單因素試驗中NaOH溶液濃度為1 mol/L時,甲殼素提取率最高。
NaOH溶液處理時間對甲殼素提取率的影響見圖4。
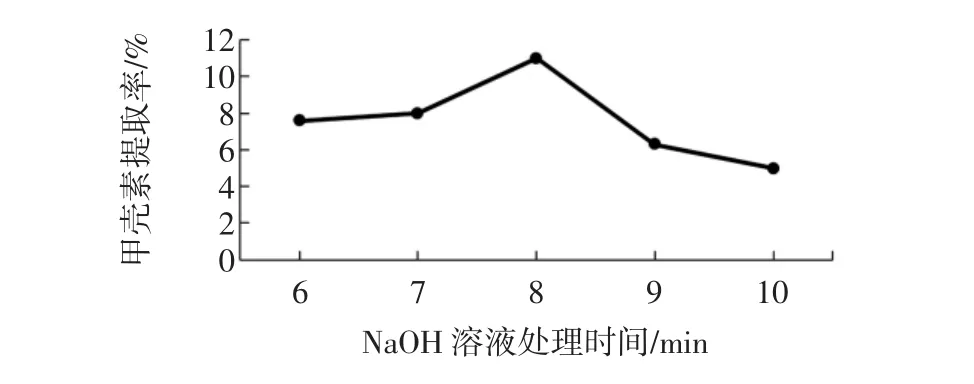
圖4 NaOH溶液處理時間對甲殼素的影響Fig.4 Effects of processing time within NaOH solution on chitin
由圖4可知,NaOH溶液處理時間在6 min~8 min時甲殼素提取率逐漸升高,但隨著反應時間增加,曲線又有所下降,原因是魚鱗中的蛋白質等被分解使其質量減少,甲殼素也會隨著反應時間的增加而水解。所以單因素試驗中鯉魚魚鱗在NaOH溶液中最佳處理時間為8 min,甲殼素提取率最高。
由上述4個圖可知,鯉魚魚鱗中甲殼素的提取較佳工藝為用1 mol/L的HCl溶液在室溫下浸泡30 min,1 mol/LNaOH溶液在70℃水浴中處理8 min,甲殼素提取率11.72%。
2.2 鯉魚魚鱗中甲殼素提取率的響應面試驗優化分析
2.2.1 鯉魚魚鱗中甲殼素提取率的響應面試驗結果
試驗因素編碼水平表見表1,響應面試驗設計及結果見表2。

表1 響應面試驗因素水平表Table 1 The response surface test factors level table

表2 響應面試驗設計及結果Tabie 2 Design and results of the response test
利用Design Expert V 8.0.4響應面軟件進行二次多元回歸擬合,得出鯉魚魚鱗中甲殼素提取率對4個單因素的二次回歸模型:
甲殼素提取率Y=+11.72+0.45A+0.63B+0.40C+0.29D-1.13AB-1.08AC-0.30AD-0.30BC-0.38BD-0.88CD-0.72A2-0.48B2-0.61C2-0.35D2
對甲殼素響應面設計模型進行響應面試驗方差分析,分析結果見表3。
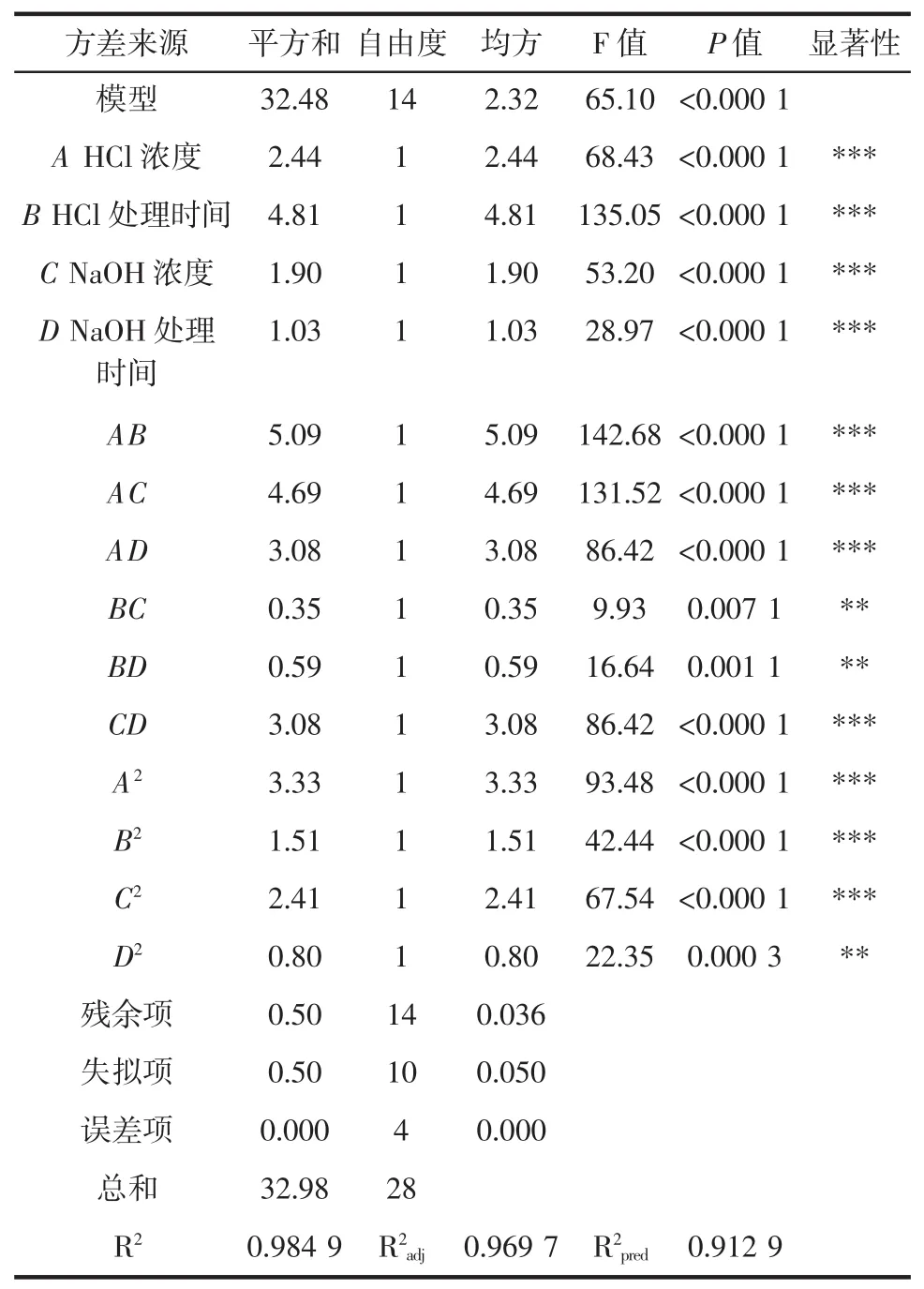
表3 響應面試驗方差分析Table 3 Response surface analysis of variance
由表3可以看出,P<0.000 1,說明模型具有差異極顯著水平,回歸方程結果與試驗結果比較吻合,誤差項不明顯,說明試驗誤差小。方差分析結果說明,回歸模型中差異極顯著項有 A、B、C、D、AB、AC、AD、CD、A2、B2、C2,差異高度顯著項有 BC、BD、D2。模型的調整確定系數為98.49%,矯正決定系數為96.97%,修正決定系數為91.29%,R2adj與R2pred數值基本接近,說明響應值的變化有91%都可以通過該模型來解釋,方程擬合程度較好。R2adj與R2pred的值是合理的。由P值和F值可以看出,鯉魚魚鱗中甲殼素提取率影響的4個因素順序為:HCl溶液處理時間>HCl溶液濃度>NaOH溶液濃度>NaOH溶液處理時間。

圖5 HCl溶液濃度與HCl溶液處理時間交互作用對甲殼素提取率的影響Fig.5 Effects of the interaction with HCL concentration and processing time within HCL solution on chitin yield rate

圖7 HCl溶液濃度與NaOH溶液處理時間交互作用對甲殼素提取率的影響Fig.7 Effects of the interaction with HCL concentration and processing time within NaOH solution on chitin yield rate
2.2.2 響應面的曲面分析
響應面曲面分析見下圖5至圖10。
由圖5至圖10可以看出,HCl溶液處理時間對鯉魚魚鱗中甲殼素的提取率影響最為顯著,曲線幅度變化最為明顯;余下的3個因素,由于曲線相對平緩,且與響應面方差結論相一致。因此,可通過有形狀的等高線來呈現其相互作用的強和弱。提取率變化明顯的用橢圓來表示,變化不明顯的用圓形來表示。從圖6中可以看出HCl溶液濃度與NaOH溶液濃度交互作用顯示橢圓形,交互作用顯著。從圖8中可以看出HCl溶液處理時間與NaOH溶液濃度交互作用顯示為圓形,交互作用不顯著。
根據響應面軟件優化結果得出,鯉魚魚鱗最佳提取工藝條件為HCl溶液濃度1 mol/L,HCl溶液浸泡時間30 min,NaOH溶液濃度1 mol/L,NaOH溶液處理時間8 min,此時甲殼素提取率為11.72%。
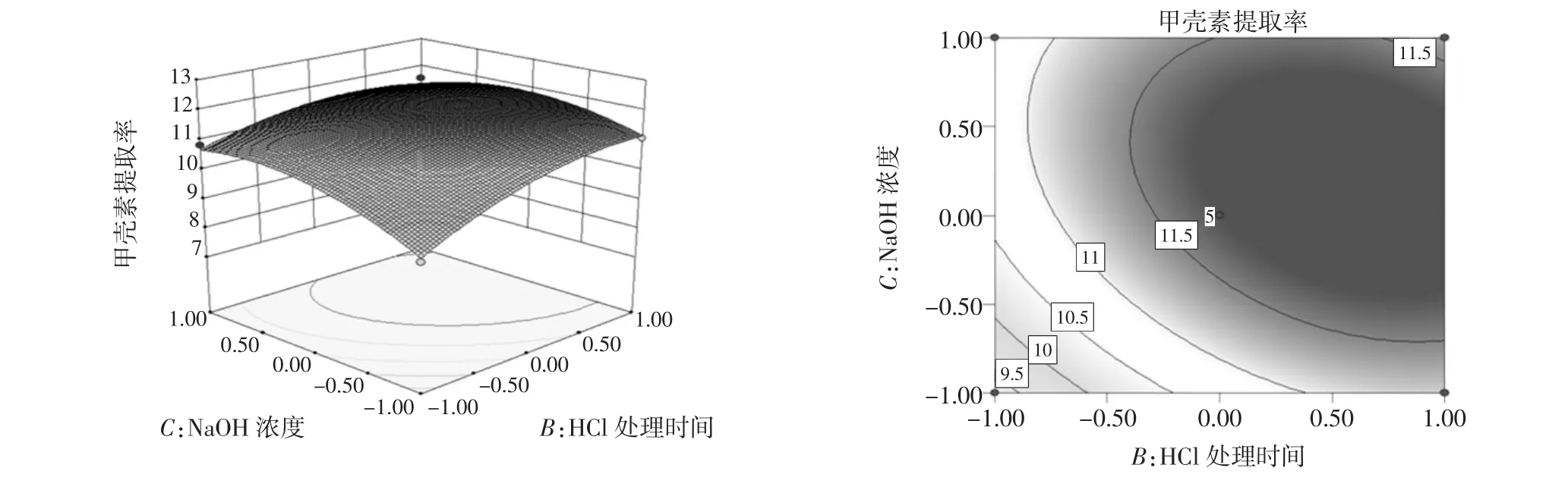
圖8 HCl溶液處理時間與NaOH溶液濃度交互作用對甲殼素提取率的影響Fig.8 Effects of the interaction with processing time within HCL solution and NaOH concentration on chitin yield rate
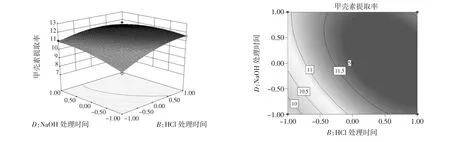
圖9 HCl溶液處理時間與NaOH溶液處理時間交互作用對甲殼素提取率的影響Fig.9 Effects of the interaction with processing time within HCL solution and processing time within NaOH solution on chitin yield rate

圖10 NaOH溶液濃度與NaOH溶液處理時間交互作用對甲殼素提取率的影響Fig.10 Effects of the interaction with NaOH concentration and processing time within NaOH solution on chitin yield rate
2.3 甲殼素灰分測定的結果
甲殼素灰分測定的結果見表4。
2.4 甲殼素脂肪含量測定的結果
甲殼素脂肪含量測定的結果見表5。

表4 灰分測定結果Table 4 Ash determination results
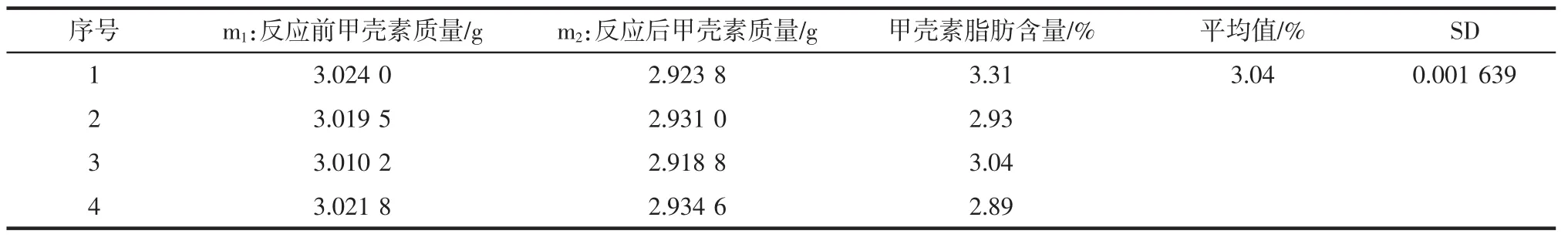
表5 脂肪含量測定結果Table 5 Fat content determination results
2.5 殼聚糖的制備結果
將殼聚糖從恒溫鼓風干燥箱中取出,黃色,細絲狀。
3 結論
本次試驗以鯉魚魚鱗為主要原料提取甲殼素,通過不同的單因素試驗來確定最佳工藝條件:HCl溶液濃度1 mol/L,HCl溶液浸泡時間30 min,NaOH溶液濃度1 mol/L,NaOH溶液處理時間8 min,提取率為11.72%,與文獻[12]比較,甲殼素提取率基本相同,可以有效解決目前國內加工甲殼素存在的原料來源有限的問題,加大鯉魚魚鱗資源的有效利用。根據響應面方差分析和響應面軟件優化結果得出影響提取率因素的大小:HCl溶液處理時間>HCl溶液濃度>NaOH溶液濃度>NaOH溶液處理時間。殼聚糖是由甲殼素在1 mol/L NaOH溶液中通過80℃水浴中加熱10 min,制得的黃色絲狀固體。
[1] 張文博,陳盛.甲殼素/殼聚糖的提取及其應用研究新進展[J].福建師大福清分校學報,2008(2):18-25
[2] 唐家林,吳成業,鐘建業,等.甲殼素、殼聚糖生產工藝研究[J].福建水產,2010,6(2):38-42
[3] 唐振榮,謝志榮,寧方堯,等.甲殼素及其衍生物在食品工業清凈的應用綜述[J].輕工科技,2015,12(2):28-31
[4] 鄧海萍,陳奇,李向紅,等.不同電荷多糖添加物對鰱魚魚糜凝膠結構的影響[J].食品與機械,2014(3):39-41
[5] 王南平,何蘭,曹俊,等.魚鱗綜合開發利用工藝與設備綜述[J].漁業現代化,2014,2(9):421-430
[6] 蘇廣宇,劉四新,李從發.甲殼素/殼聚糖的研究與應用概況[J].廣東農業科學,2008,5(8):78-83
[7] 李川,姚俊杰,姜海波,等.甌江彩鯉魚鱗的生化成分分析[J].西南農業學報,2010,23(4):1303-1307
[8] 顧楊娟,李杰,李富威,等.魚鱗有效成分的研究進展[J].食品工業科技,2012(10):415-419
[9] 石維煥,許永安.魚鱗利用的研究進展[J].漁業研究,2011,33(4):67-72
[10]張志紅,張國華,王菊華,等.甲殼素及其衍生物在水產動物養殖上的應用現狀[J].江西科學,2016,1(2):19-23
[11]王岸娜,王璋,許時嬰.不同粒度甲殼素對所制備殼聚糖脫乙酰度和相對分子質量影響的研究[J].食品與機械,2007,23(3):28-31
[12]蔚鑫鑫,劉艷,吳光旭.小龍蝦殼中甲殼素的提取及殼聚糖的制備[J].湖北農業科學.2013,52(13):3120-3123
[13]肖冰梅,劉義芳,劉彩虹,等.不同產地夏枯草果穗水分、灰分含量測定[J].中國民族民間醫藥,2015,24(4):26-27
[14]趙亮,柴平海.魚肉制品中脂肪的測定[J].安徽農業科學,2015(20):285-287
[15]喬德亮.低聚糖的制備及其在功能食品中的應用[J].食品工業科技,2007,4(5):21-23
[16]廖戎.甲殼素制備殼聚糖脫乙酰度可控性的研究[J].四川化工,2007,10(2):14-17

