半胱氨酸/納米金修飾電極差分脈沖伏安法測定蘆丁
黃玉斌,嚴春榮,王齊
(1.玉溪市質量技術監督綜合檢測中心,云南玉溪653100;2.昆明理工大學分析測試研究中心,云南昆明650000;3.云南省分析測試中心,云南昆明650000)
蘆丁(Rutin)又名蕓香苷,普遍存在于植物的根、莖、葉、花、果實、種子中,是一種具有生物活性的重要黃酮類物質[1]。其分子中的α、β不飽和吡喃酮是各種生物活性的關鍵基團,而A、B、C三環的各種取代基則決定了其特定的藥效作用,從而決定了其不同生物活性。經過大量的研究表明,蘆丁具有抗炎、抗病毒、鎮痛、抗氧化、抗癌抗腫瘤、抑制醛糖還原酶活性和治療毛細血管通透性增高引起的出血癥等功效,并且對器官缺血損傷也有保護與修復作用[2]。蘆丁的以上性質,使其成為許多中成藥試劑或保健食品的重要性指標組分,因此研究簡便、快捷、高效、準確的檢測方法具有實際意義。蘆丁分子結構式見圖1。
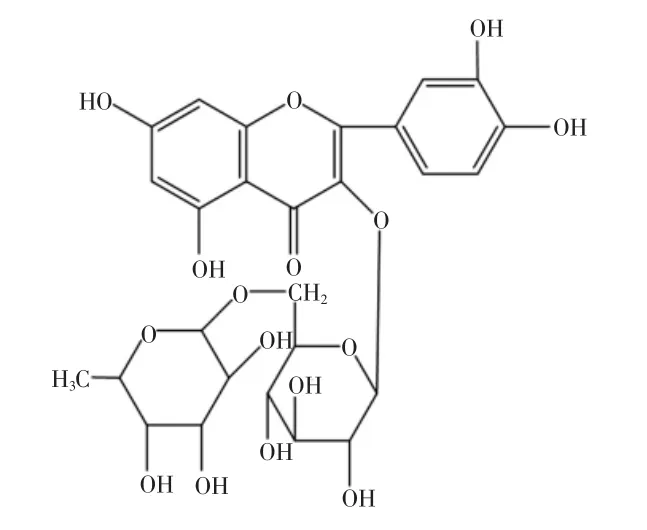
圖1 蘆丁分子結構式Fig.1 Chemical structure of rutin
目前蘆丁的檢測方法主要是高效液相色譜法和分光光度法,其中高效液相色譜法是一種比較準確的分離、定量測定方法[3-4],但是其具有龐大的色譜分離系統、較高儀器與試劑成本的缺點;而紫外分光光度法在實際樣品測定中,經常會受到共存還原性組分或樣品自身空白的影響,使測定結果比實際含量偏高30%~100%以上[5]。如何簡便、高效地對復雜體系中蘆丁含量進行定量分析,成為分析工作者的難題。近十年來,電化學分析法利用物質在特定電極上氧化還原電位的不同,建立起了多種測定微、痕量物質的方法,如循環伏安法、差分脈沖伏安法、溶出伏安法等[6-10],在未對物質進行預分離的情況下,這些方法對復雜體系中某一組分的定量測定有很好的效果。
本研究利用半胱氨酸分子在金表面和金納米的自組裝性質,制備了一種多層結構的修飾電極,研究了蘆丁分子在修飾電極上的電化學性質,并利用蘆丁分子在修飾電極上的差分脈沖伏安響應信號,建立了一種高靈敏度測定蘆丁含量的方法。
1 材料與方法
1.1 儀器與試劑
CHI660C電化學工作站、電化學測量采用三電極體系、金圓盤電極(φ=2mm)、飽和甘汞參比電極、鉑絲輔助電極:美國CHI公司;Milli-Q Element超純水系統:美國Millipore公司;SK3300H超聲波清洗儀:中國科導公司。
L-半胱氨酸(>98.5%)、氯金酸(HAuCl4,99%):Aldrich公司;甲醇、檸檬酸、磷酸、濃硫酸(均為分析純):Aladdin公司。
1.2 Au納米微粒的制備
Au納米微粒的制備采用簡單的Frens法[11-13],即在100 mL沸水中加入30 mg檸檬酸,在攪拌加熱下緩慢滴加入2 mL 0.5 mg/mL HAuCl4,反應30 min后立即用冰水浴冷卻至室溫后4℃保存。
1.3 修飾電極的制備
電極的預處理:將金圓盤電極在金相砂紙上打磨,再依次用 0.3、0.1、0.05 μm Al2O3粉拋光,用水超聲清洗數分鐘后取出清洗;再置于0.5 mol/L稀H2SO4溶液中以10 V/s掃描速度在-0.5 V~2.0 V的電位范圍內進行循環伏安掃描10 min,即為裸金電極(NAu)。
修飾電極的自組裝過程:將預處理好的NAu電極置于0.01 mol/L L-半胱氨酸水溶液中進行自組裝6 h后取出、用水超聲清洗5 min,為L-半胱氨酸修飾電極(NAu/C);制備好的NAu/C電極再次放入Au納米微粒溶液中自組裝6 h后取出、用水清洗,為金納米微粒修飾電極(NAu/C/Au);將NAu/C/Au電極再次放入0.01 mol/L L-半胱氨酸水溶液中進行自組裝6 h后取出用水清洗,為二次L-半胱氨酸修飾電極(NAu/C/Au/C)。制備的修飾電極浸泡在水中4℃保存。
1.4 標準溶液和樣品的制備
準確稱取蘆丁標準品10.0 mg,用適量甲醇及pH 6.8的磷酸緩沖溶液溶解定容至50 mL,得200.0 μg/mL蘆丁標準儲備液,再分別吸取若干用pH 6.8的磷酸緩沖溶液定容至 50mL,得到濃度分別為 6.0、8.0、10.0、12.0、14.0、16.0、18.0、20.0 μg/mL 的蘆丁標準工作溶液。
準確稱取約0.10 g精制苦蕎茶用適量甲醇及pH 6.8的磷酸緩沖溶液超聲溶解,經濾紙過濾定容于250 mL容量瓶中,待測。
1.5 試驗方法
以修飾電極為工作電極,記錄-0.2 V~0.6 V范圍內的差分脈沖伏安(Differential Pulse Voltammetry,DPV)信號,其試驗參數為:脈沖幅度50mV、脈沖寬度0.05 s、采樣寬度0.016 s、脈沖周期0.2 s、靜置時間為2 s。
2 結果與討論
2.1 修飾電極的自組裝過程
本試驗所制備的Au納米微粒為酒紅色膠體溶液,其紫外可見吸收見圖2,吸收峰波長約為530 nm,與文獻報道相一致[11];經高分辨TEM(圖2)表征發現,Au納米微粒為球型微粒,納米微粒半徑為(8±2)nm,且能觀察到清晰的晶格線條紋,說明本試驗所制備的Au納米微粒晶體生長較完整。
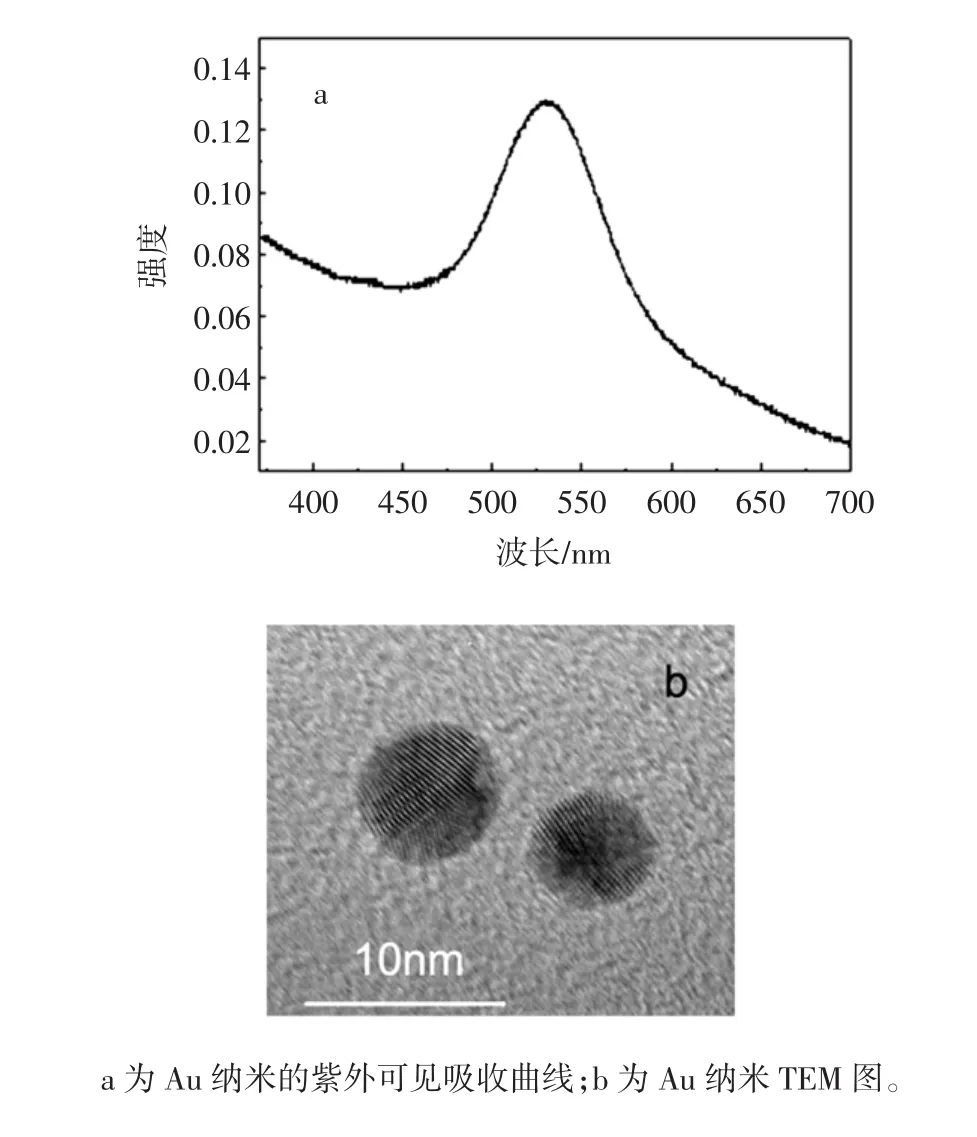
圖2 Au納米微粒的光學與形貌表征Fig.2 The optical characteristic and morphology of Au nanoparticles
在電極的自組裝過程中,半胱氨酸分子首先通過巰基與裸Au電極表面的相互作用,定向自組裝在裸Au電極的表面;半胱氨酸分子的氨基再通過靜電作用力與表面帶負電荷的Au納米微粒相互作用,使Au納米微粒自組裝在半胱氨酸分子表面;最終半胱氨酸分子再通過巰基自組裝于Au納米微粒表面,形成一種典型的多層結構修飾電極,其組裝示意圖見圖3。
2.2 蘆丁在修飾電極上的電化學行為
圖4為蘆丁分子在NAu/C修飾電極上的循環伏安曲線圖。
在0.1 V~0.4 V之間出現一對明顯的氧化還原峰。蘆丁是一種重要的黃酮類物質,其抗氧化活性成分主要來源于蘆丁分子結構上苯環羥基。在pH 6.8的磷酸緩沖溶液中,掃描循環伏安過程時,蘆丁分子B環上的3’,4’-取代羥基發生兩電子兩質子氧化還原反應,進一步發生電子重排[9-10,13],此氧化還原反應對應于循環伏安曲線中的0.21 V還原電位峰和0.26 V氧化電位峰。
然而,蘆丁分子在NAu/C修飾電極上的循環伏安氧化還原電位峰很弱,對蘆丁的信號響應靈敏度很低。為了提高響應靈敏度,繼續考察了蘆丁分子在修飾電極上的差分脈沖伏安(DPV)信號響應,結果見圖5。
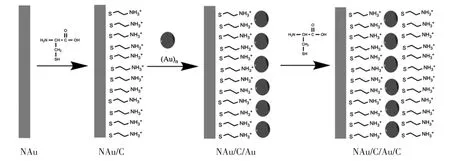
圖3 修飾電極的自組裝示意圖Fig.3 Schematic illustration of the modified electrode fabrication process
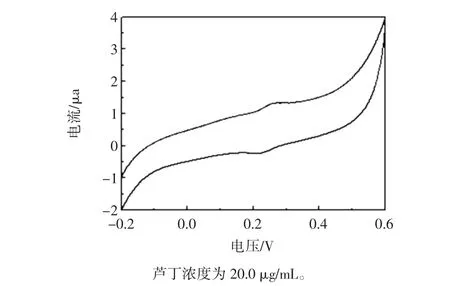
圖4 蘆丁分子在NAu/C修飾電極上的循環伏安曲線圖Fig.4 Cyclic vohammograms of rutin on the NAu/C modified electrode
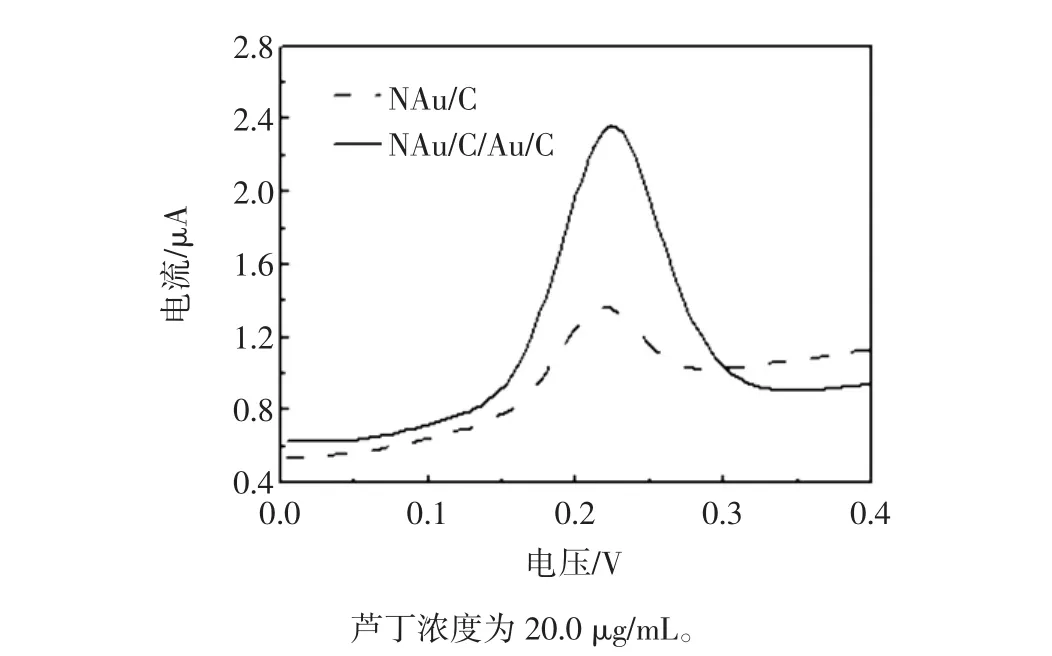
圖5 蘆丁分子在NAu/C和NAu/C/Au/C修飾電極上的差分脈沖伏安圖Fig.5 DPV of the NAu/C and NAu/C/Au/C modified electrode
在pH 6.8的磷酸緩沖溶液中,蘆丁分子在NAu/C修飾電極上通過差分脈沖伏安掃描出現了位于0.23 V處的氧化峰,并且隨著電極的進一步修飾,在NAu/C/Au/C多層修飾電極上,0.23 V處的氧化峰信號進一步增強。這是由于具有大比表面積Au納米微粒對電極的多層修飾,增加了氧化還原反應位點,提高了修飾電極對蘆丁分子響應靈敏度。
2.3 差分脈沖伏安法對蘆丁的定量測定
在pH 6.8的磷酸緩沖溶液中,對不同濃度的蘆丁采集了DPV電化學信號如圖6所示。
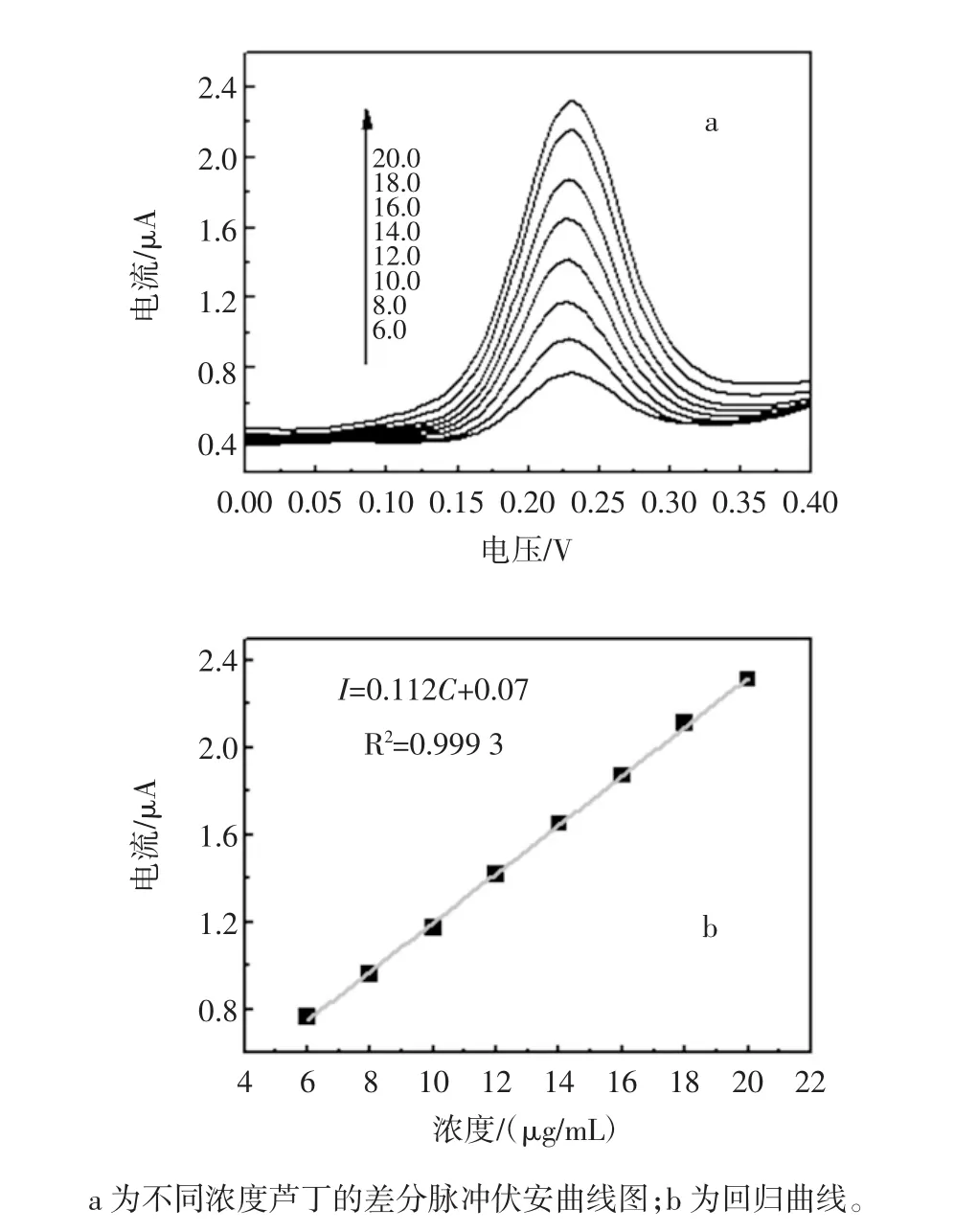
圖6 蘆丁差分脈沖伏安測定信號的線性關系Fig.6 The linear relationship of DPV signals on rutin
隨著蘆丁濃度的增加,DPV在0.23V處的信號峰也隨之增加,其峰電流與蘆丁的濃度呈線性變化關系,線性回歸方程為 I(μA)=0.112C(μg/mL)+0.07,相關系數 R2=0.999 3,儀器檢出限(3S/N)為 0.024 μg/mL,結果見表1。
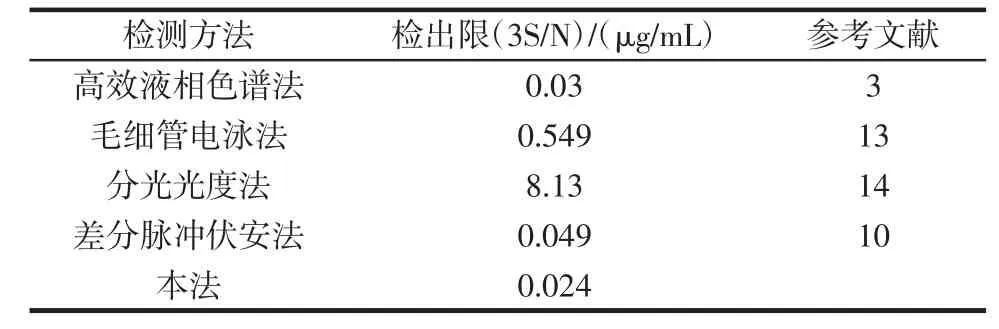
表1 不同儀器方法測定蘆丁的靈敏度比較Table 1 Different methods of determination of rutin
分析方法檢出限為6.0 mg/100 g。重復10次測定蘆丁,其RSD為1.70%,方法重復性滿足定量測定要求。
2.4 實際樣品中蘆丁的測定
用差分脈沖伏安法對精制苦蕎茶樣液中的蘆丁含量進行了測定,并且用紫外可見分光光度法[14]和高效液相色譜法[3]對樣品做了方法比對試驗,測定結果如表2所示。
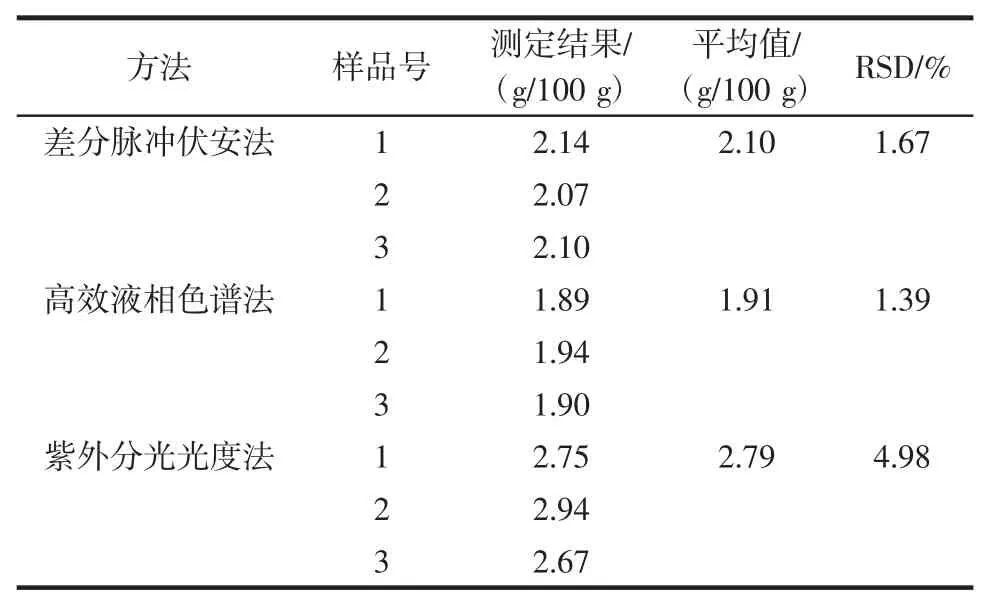
表2 不同方法測定苦蕎茶樣品中蘆丁的結果比較Table 2 Measurement result of rutin in Buckwheat tea with different methods
從表2中可以看出,本方法對實際樣品中的蘆丁含量測定的3次平行性結果為2.10 g/100 g(RSD值小于5.0%),與高效液相色譜法結果相比略高7.3%,而相比紫外分光光度法而言,結果低了近30%。結果表明,本法可以通過DPV測定電位的不同將其他具有類似酚羥基結構分子的雜質物質對蘆丁組分的測定干擾進行有效的降低,但是仍然有約7%的干擾,但此結果在可接受范圍之內。
同時,試驗了實際樣品的回收率,以1號樣品溶液20 mL 為母液(10.91 μg/mL),分別加入 0.2、0.5、0.7 mL 200.0 μg/mL的標準儲備液,制得3組標準加入樣品,分別測定回收率,結果如表3所示。
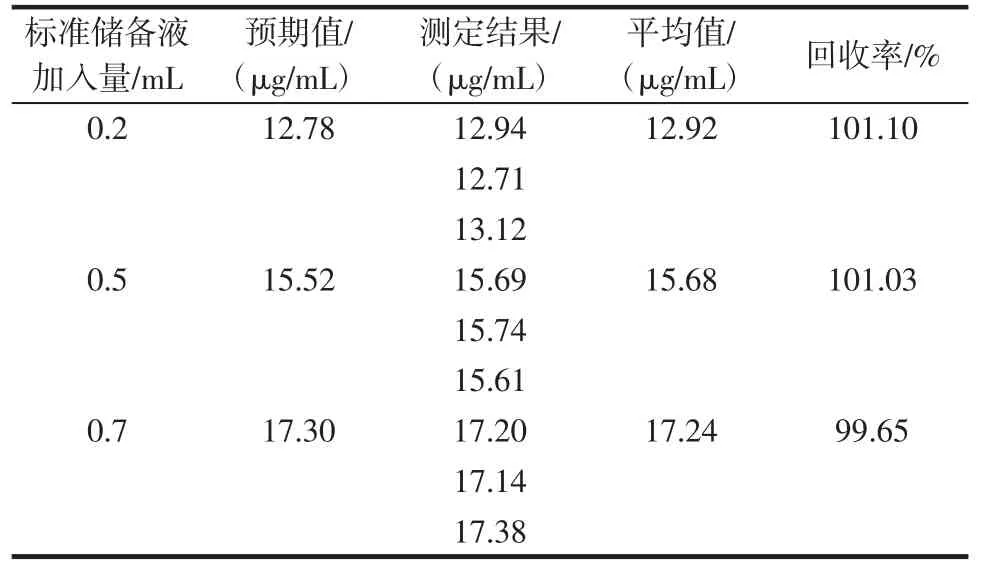
表3 苦蕎茶樣品中蘆丁加標回收試驗結果Table 3 Measurement result of Recovery experiments in Buckwheat tea
回收率在99.65%~101.10%之間,表明此方法用于試劑樣品中蘆丁含量的測定具有較高的準確性。
3 結論
本文以半胱氨酸與Au的靜電吸附自組裝原理,制備了一種多層結構的半胱氨酸/納米金修飾電極。在此修飾電極上研究了蘆丁分子的電化學行為,利用蘆丁分子在修飾電極上的兩電子兩質子氧化還原反應所產生的位于0.23 V處差分脈沖伏安信號,建立了一種蘆丁定量分析方法。該方法線性回歸方程為I(μA)=0.112C(μg/mL)+0.07,相關系數 R2=0.999 3,且具有較低的檢出限,重復10次測定蘆丁,其RSD為1.70%,方法重復性滿足定量測定要求,與高效液相方法和紫外分光光度法比較,該方法能夠簡便、快速、高效地適應于復雜體系中蘆丁含量的測定。
[1] 龍全江,楊韜.蘆丁的研究概況及展望[J].中國中醫藥信息雜志,2002,9(4):39-42
[2] 牛小花,陳洪源,曹曉鋼,等.蘆丁的研究新進展[J].天然產物研究與開發,2008(b5):156-159
[3] 黃興富,黎其萬,劉宏程,等.高效液相色譜法同時測定苦蕎中蘆丁、槲皮素和山柰酚的含量[J].中成藥,2011,33(2):345-347
[4] Court W A.High-performance reversed-phase liquid chromatography of naturally occurring phenolic compounds[J].Journal of Chromatography A,1977,130:287-291
[5] 文平,陳進紅.蕎麥蘆丁的研究進展[J].中國糧油學報,2006,21(3):107-111
[6] Barthus R C,Mazo L H,Poppi R J.Simultaneous determination of vitamins C,B6 and PP in pharmaceutics using differential pulse voltammetry with a glassy carbon electrode and multivariate calibration tools[J].Journal of Pharmaceutical&Biomedical Analysis,2005,38(1):94-99
[7] Ozkan S A,Kauffmann J M,Zuman P.Electrochemical Biosensors for Drug Analysis[M].Berlin Heidelberg:Springer-Verlag,2015:141-186
[8]Kang Jing-wan,Lu Xiao-quan,Zeng Hongjuan,et al.INVESTIGATION ON THE ELECTROCHEMISTRY OF RUTIN AND ITS ANALYTICAL APPLICATION[J].Analytical Letters,2002,35(4):677-686
[9] Ghica M E,Brett A.Electrochemical Oxidation of Rutin[J].Electroanalysis,2010,17(4):313-318
[10]徐青,王榮,陸秋艷,等.氨基乙硫醇修飾金電極直接測定蘆丁含量的研究[J].分析化學,2006,34(7):971-974
[11]蔣治良,馮忠偉,李廷盛,等.金納米粒子的共振散射光譜[J].中國科學:化學,2001,31(2):183-188
[12]Hendrickson H P,Sahafayen M,Bell M A,et al.Relationship of flavonoid oxidation potential and effect on rat hepatic microsomal metabolism of benzene and phenol[J].Journal of Pharmaceutical&Biomedical Analysis,1994,12(3):335-41
[13]鄧光輝,王士偉,王輝,等.毛細管電泳安培法測定田基黃中的蘆丁與槲皮素[J].分析試驗室,2014(4):424-427
[14]張宏志,管正學.分光光度法測定蕎麥中蘆丁含量[J].光譜實驗室,1996(3):24-27

