熱變性乳清濃縮蛋白與高甲氧基果膠混合體系相分離行為的研究
曹傳愛,吳鑫本,賈惜文,趙神彳,張帥,劉騫,*
(1.東北農業大學食品學院,黑龍江哈爾濱150030;2.虎林出入境檢驗檢疫局,黑龍江虎林158400)
天然高分子包括蛋白質、多糖等親水性膠體,由于良好的乳化性、穩定性、持水性等性能,廣泛應用在食品工業、制藥行業以及生物技術行業。但是由于種類有限、化學結構相對單一,在食品物性設計中可利用的選擇較少,無法滿足對食品精細結構、質地多樣、口感獨特以及功能性的需求[1],因此出現多種天然高分子物質復合使用的方法。當兩種或多種天然高分子物質混合后,由于熱力學不相容性使體系發生相分離成為一種較為普遍的現象[2]。在食品的加工和儲藏過程中,相分離行為造成食品體系不穩定。但是有些研究需要利用相分離行為制備特殊的質地和結構,達到豐富食品微結構和物性的目的。因此研究高分子混合體系的復雜相分離行為具有重要的理論和應用前景。在適當條件下兩種及以上天然高分子物質混合可產生不同類型的相分離行為[3],分為隔離型相分離和結合型相分離兩種。隔離型相分離的兩相中分別富含一種高分子物質,由攜帶相同電荷的高分子間的靜電排斥作用或是不帶電荷的高分子之間的熱力學不平衡而引起[4-5]。結合型相分離是由于高分子攜帶相反電荷形成的,主要的推動力是靜電庫侖力,使得一相中富含兩種高分子物質,另一相中幾乎為溶劑[5-6]。
研究發現,蛋白與多糖混合體系之間存在明顯相分離行為。Grinberg等[7]研究了不同類型的多糖與蛋白質的熱力學不相容性,不同類型多糖熱力學不相容性的大小順序為:羧基多糖>中性多糖>硫酸基多糖,線性多糖與支鏈多糖相比,易發生相分離行為。Tuinier等[8]研究發現,當酪蛋白/果膠混合體系的pH<5時,因果膠與酪蛋白帶相同電荷產生靜電相互作用,使果膠在酪蛋白膠粒表面發生多層吸附;當體系pH>5時,果膠與酪蛋白由于熱力學不相容性出現相分離現象。乳清蛋白是以球蛋白的形式存在于乳中,約占總蛋白的20%,具有凝膠性、乳化性、起泡性等特點[9]。乳清濃縮蛋白(Whey Protein Concentrate,WPC)是從巴氏殺菌的乳清中盡量去除非蛋白質成分得到的,蛋白質含量約占34%~82%[10]。研究發現,加熱處理乳清蛋白會使球狀蛋白部分地展開,暴露出更多埋藏在分子內的疏水基團和巰基,然而加熱過程中蛋白容易變性導致蛋白聚集,使其功能性質受到限制,影響其在食品工業中的應用[11]。果膠是一種天然陰離子多糖,存在于植物的初生細胞壁和中間層中。通常將酯化度(Degree of Esterification,DE)高于50%的果膠稱之為高甲氧基果膠(High-methoxylPectin,HM-P),反之低于 50%的為低甲氧基果膠。因果膠具有良好的膠凝、增稠性能,已被廣泛應用于食品工業中。目前關于蛋白/多糖混合體系相行為的研究已有不少報道,大多數研究提出利用相分離行為進行新型食品微結構的設計,如填充水凝膠的制備[12]、保護不穩定功能因子的多層乳液的制備[13]和緩釋技術[14]等,然而關于熱變性乳清蛋白(HeatDenaturedWheyProteinConcentrate,HD-WPC)與果膠混合體系相分離行為研究較少。另外影響相分離的因素包括混合比例、溫度、濃度、離子強度、pH值等,通過改善各種因素對混合體系復雜的相行為的影響,可以幫助我們得到理想的產品微結構和物性。
因此,本實驗主要研究熱變性乳清濃縮蛋白與高甲氧基果膠以不同質量比(1∶1、2∶1、3∶1、4∶1、5∶1)混合后整個混合體系的相分離行為。分析探討混合體系中上相與下相中的蛋白和多糖含量、混合體系表觀黏度以及外觀的變化趨勢,為后續在水凝膠中的研究奠定一定的理論基礎。
1 材料與方法
1.1 材料與試劑
乳清濃縮蛋白(WPC,80%):北京銀河路商貿有限責任公司;高甲氧基果膠:上海源葉生物科技有限公司;磷酸二氫鈉、磷酸氫二鈉:天津市巴斯夫化工有限公司;鹽酸磷酸濃硫酸:哈爾濱市萬太生物藥品公司;疊氮鈉、羅丹明B、考馬斯亮藍G-250、苯酚均為分析純;試驗中所用的水均為超純水。
1.2 儀器與設備
JD500-2電子天平:沈陽龍騰電子稱量儀器有限公司;AL-104型精密電子天平、FE20K型pH計上海梅特勒-托利多儀器設備有限公司;DK-8B電熱恒溫水浴鍋:上海驚宏實驗設備有限公司;GL-21M冷凍離心機:湖南湘儀實驗室儀器開發有限公司;TU-1800紫外可見光分光光度計:北京普析通用儀器有限公司;TA流變儀Discovery DHR-1:美國TA儀器公司。
1.3 試驗方法
1.3.1 溶液的制備
HD-WPC溶液的制備:稱取一定量的乳清濃縮蛋白粉末分散于pH=7.0的0.01 mol/L磷酸鹽緩沖液中,于室溫下用磁力攪拌器1 000 r/min下攪拌1 h使其充分溶解,用4 mol/L NaOH調至pH=7.0,配制成30 mg/mL的蛋白分散液。將制得的蛋白分散液在85℃下水浴加熱30 min,熱處理后,立刻冰浴冷卻到室溫。然后在7 500 r/min下離心2 h,去除不溶物。4℃下貯藏。同時加入0.02%的疊氮鈉。
HM-P溶液的制備:稱取一定量的HM-P粉末溶解于pH=7.0的0.01 mol/L磷酸鹽緩沖液中,室溫下1 000 r/min下攪拌1 h,用4 mol/L NaOH調至pH=7.0,制得濃度為30 mg/mL HM-P溶液,4℃下貯藏過夜水合。同時加入0.02%的疊氮鈉。
1.3.2 相分離體系的制備
將初始濃度30 mg/mL HD-WPC溶液和初始濃度 30 mg/mL HM-P 溶液按照 1 ∶1、2 ∶1、3 ∶1、4 ∶1、5∶1質量比混合,用1 mol/L HCI或1 mol/L NaOH調至pH=7.0,于室溫下用磁力攪拌器1 000 r/min下攪拌30 min。將樣品等體積分為兩份。其中一份加入濃度為0.05%羅丹明B溶液,加入量為5 μg/g混合物,混合均勻。未加羅丹明B的樣品和加羅丹明B的樣品在20℃,7 500 r/min下離心2 h。混合物分為明顯的兩相。
1.3.3 樣品蛋白量的測定
參照Bradford等[15]的方法測定樣品蛋白含量。采用考馬斯亮藍的方法進行測定,用牛血清白蛋白進行蛋白標準曲線的測定,在595 nm處測量吸光度。以蛋白質含量(mg)為橫坐標、A595為縱坐標,繪制單邊標準曲線。最后進行樣品蛋白的測定,對樣品進行稀釋樣品,按上述方法測定吸光度,計算樣品溶液的蛋白含量。
1.3.4 樣品多糖含量的測定
參照Dubois等[16]的方法測定樣品多糖含量。用葡萄糖標準溶液進行多糖標準曲線的制備,于490nm處測定吸光度,以葡萄糖含量為橫坐標,以吸光值為縱坐標,繪制多糖標準曲線。然后進行樣品多糖含量的測定,將樣品進行適度稀釋,按照上述方法測定吸光值,計算樣品多糖含量。
1.3.5 表觀黏度的測定
使用動態剪切流變儀測定上相、下相以及混合樣品的表觀黏度。在0.1 s-1~100 s-1的剪切速率范圍內進行穩態剪切流變試驗。受控應力范圍:0.1 Pa~10 Pa,測量溫度:25℃,平板直徑:40 mm,間隙:0.5 mm。
1.3.6 樣品外觀觀察
將不同質量比的HD-WPC/HM-P樣品離心結束后觀察相分離現象,拍照。
1.4 數據統計分析
每個試驗重復3次,結果表示為平均數±SD。數據統計分析采用Statistix 8.1(分析軟件,St Paul,MN)軟件包中Linear Models程序進行,差異顯著性(P<0.05)分析使用Tukey HSD程序。采用sigmaplot 12.5軟件作圖。
2 結果與分析
2.1 相分離體系中上相組分分析
這組實驗的目的是表征不同質量比(1∶1、2∶1、3∶1、4∶1、5∶1) 的 HD-WPC 與 HM-P 形成的相分離體系(pH=7.0)中上、下相的相組成性質。不同質量比的混合溶液經過離心后出現明顯的相分離行為。Laneuville等[17]研究發現樣品在混合后立即形成渾濁的分散體,其在所研究的所有條件下不平衡并且相分離。發生相分離的速率主要取決于混合體系的黏度。因此,為了加速平衡相分離,將混合體系經過離心處理,得到含有頂層相和生物聚合物沉淀。蛋白/多糖相分離體系可以視為水包水(water in water,W/W)乳液。W/W乳液是一種分散體系,其中一種不混溶的水溶液的液滴分散在另一種生物聚合物水溶液中[18]。其特征在于生物聚合物在共存階段的共溶性[19]。
圖1所示的是不同質量比的HD-WPC/HM-P混合體系中上相蛋白、多糖濃度分析。
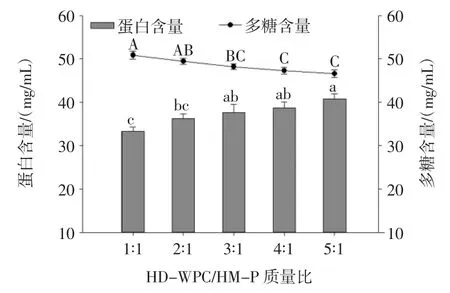
圖1 不同質量比的HD-WPC/HM-P相分離體系中上相蛋白、多糖濃度Fig.1 Concentration of proteins and polysaccharides in upper phases of HD-WPC/HM-P phase separation system with different quality ratios
從圖1中我們可以看出,不同質量比的相分離系統中上相都含有蛋白和多糖,且多糖含量總高于蛋白含量,證明上相為多糖(HM-P)富集相。從圖1中還可以發現,上相多糖含量隨著HD-WPC/HM-P混合質量比的增加而顯著降低(P<0.05)。HD-WPC/HM-P質量比由1∶1增加到5∶1時,多糖含量從50.83 mg/mL降低到46.59 mg/mL,質量比為5∶1時達到最小值,這可能是由于隨著混合比例增加,HM-P含量逐漸降低,使得HD-WPC與HM-P之間的排斥力降低。隨著比例的增加,蛋白含量逐漸增加,但是低于多糖含量,說明上相中仍然含有大量的蛋白。Jara等[20]研究發現初始羥丙基甲基纖維素(Hydroxypropylmethylcellulose,HPMC)濃度降低,在恒定的WPC濃度下,會降低分離的驅動力,使上相中更多的蛋白質與HPMC共存。因此,初始濃度較低的HPMC可以在上相中含有更多的蛋白質。
2.2 相分離體系中下相組分分析
不同質量比的HD-WPC/HM-P相分離混合體系中下相蛋白、多糖濃度分析如圖2所示。
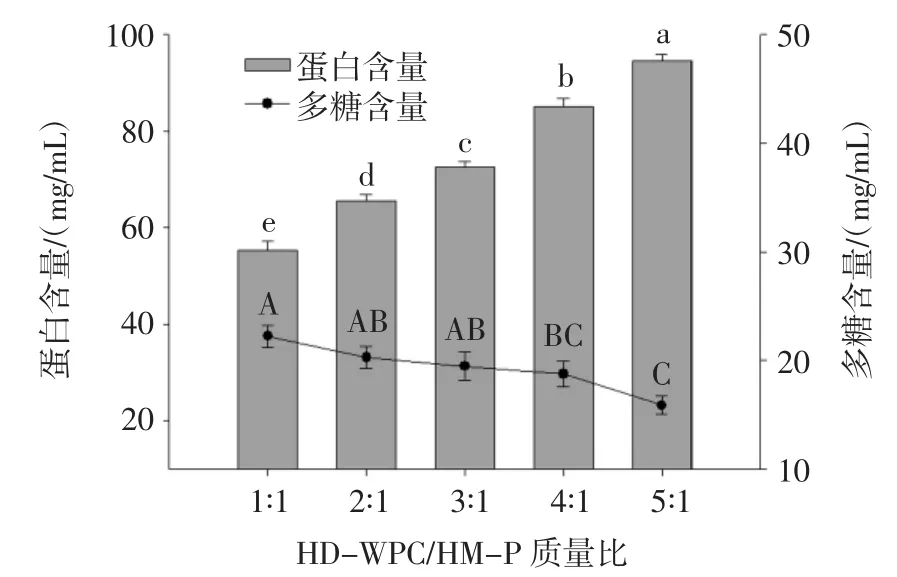
圖2 不同質量比的HD-WPC/HM-P相分離體系中下相蛋白、多糖濃度Fig.2 Concentration of proteins and polysaccharides in lower phases of HD-WPC/HM-P phase separation system with different quality ratios
從圖2中我們可以看出,不同質量比的HDWPC/HM-P相分離混合體系的下相中,均含有蛋白和多糖,這與上相分析結果相同,然而下相蛋白含量高于多糖含量,蛋白含量隨著混合質量比的增加顯著增加(P<0.05),證明下相為蛋白(HD-WPC)富集相。HD-WPC/HM-P混合質量比為1∶1的相分離體系下相中,蛋白含量約為多糖含量的250%。隨著混合質量比的增加,比例為5∶1時蛋白含量達到最大值,下相中含有多糖含量較低。這是由于隨著混合質量比增加,果膠含量逐漸降低,比例為5∶1時,多糖參與復合物形成的量減少,蛋白質聚集體形成量增加。此外,蛋白質濃度較高使得蛋白相互接近而容易發生碰撞和聚集[17]。
通過分析不同HD-WPC與HM-P質量比形成的相分離體系(pH=7.0)中上、下相分析可知,上相為多糖富集相,下相為蛋白富集相,組成分析結果與其他研究結果一致,發生相分離的體系形成兩個富集相,每一相中富含一種高分子物質[12,21]。蛋白/多糖混合體系相分離行為的發生是由于熱力學不相容性,這種不相容性是由于耗竭-絮凝相互作用引起的[22]。當HD-WPC和HM-P兩種不相容的生物大分子在系統中共同存在時,由于它們之間的不相容性形成耗竭層,這是由于HM-P粒子周圍的HDWPC負吸附,使HM-P周圍HD-WPC濃度較低。由于布朗運動,耗竭層包圍的HM-P之間發生耗竭層重疊,導致HM-P粒子間與分散介質形成溶劑(HD-WPC)濃度梯度,滲透壓力促使HD-WPC從HM-P粒子間擴散到分散介質中,使HM-P粒子克服彼此之間的靜電斥力而聚集,由于分子之間的熱力學不穩定性導致相分離的產生,具體過程如圖3所示。
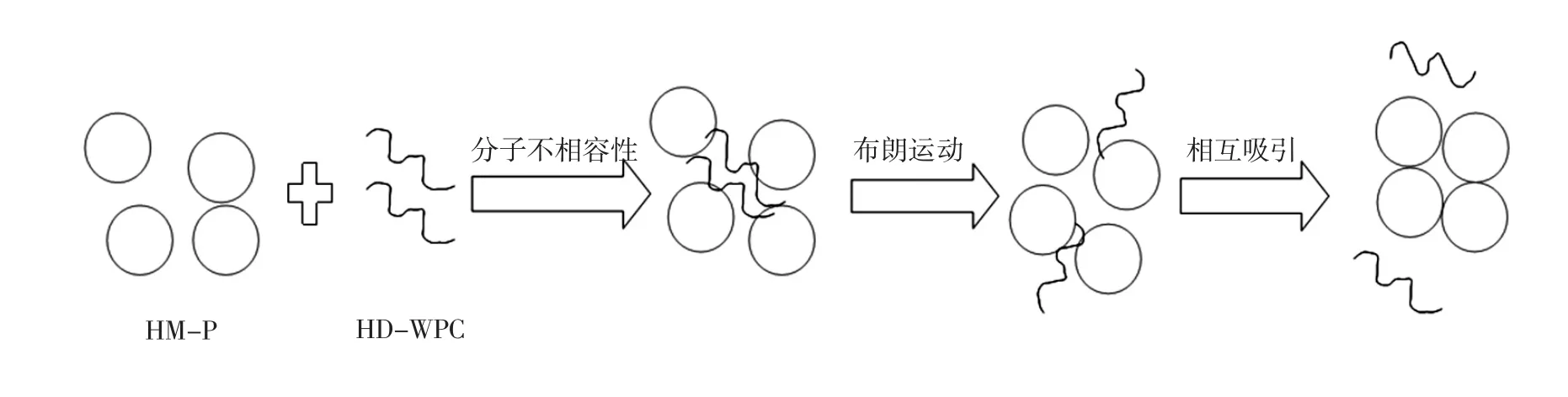
圖3 耗竭-絮凝作用機理Fig.3 The mechanism of depletion-flocculation
HD-WPC,是一種兩性聚電解質,Syrbe等[23]研究發現在溶液pH值為5~7時,一些中性多糖如葡聚糖與天然乳清蛋白之間發生相分離現象;而一些陰離子多糖如高甲氧基果膠會與變性乳清蛋白發生相分離。Kim等[21]報道未經處理的乳清分離蛋白未出現相分離的現象,這可能是由于沒有鹽離子條件下,乳清蛋白分子在pH7.0,溫度高于熱變性溫度時,易形成長絲狀結構。這些細絲是由球狀蛋白質部分展開并暴露在表面上的非極性基團形成,然后作為蛋白質分子之間的疏水交聯,一旦蛋白質分子聚合成這些相對較高分子量的結構,通常有利于整個系統中兩種不同生物聚合物均勻分布的混合熵被大大降低,所以與天然乳清蛋白相比,熱處理乳清蛋白更利于相分離的發生。
2.3 相分離混合體系的流變行為
在分子分級現象的影響下,高分子物質的性質在相分離前后通常會發生明顯變化,因此利用流變方法測定混合樣品以及相分離樣品上、下相的表觀黏度隨剪切速率的變化趨勢。圖4所示的是不同HD-WPC/HM-P質量比的相分離混合體系的表觀黏度隨著剪切速率的變化。
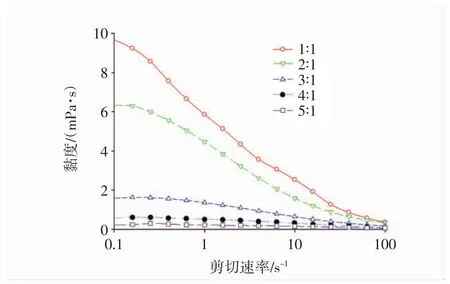
圖4 不同質量比的HD-WPC/HM-P相分離體系表觀黏度分析Fig.4 Apparent viscosity analysis of HD-WPC/HM-P phase seperation system with different quality proportions
從圖4中可以發現,HD-WPC/HM-P質量比不超過3∶1時,混合體系的表觀黏度隨著剪切速率的增加而逐漸降低,表現出明顯的剪切變稀行為,為假塑性流體,且質量比為1∶1時表觀黏度最大。說明隨著剪切速率的增加可能破壞了熱變性乳清蛋白和果膠形成的微弱的結構,顆粒可能變性和破碎,使顆粒之間的摩擦作用變小,從而降低了黏度值[24]。當 HD-WPC/HM-P 質量比為 4∶1、5∶1時,表觀黏度并未受到剪切速率的較大影響,在0.1 s-1~100 s-1剪切速率范圍內趨勢比較平緩,接近于0,表現出近似牛頓流體的性質。這可能是因為HM-P的濃度過低,分子鏈較短,陰性多糖與陽性蛋白之間發生相互作用極弱,使體系表現出近似牛頓流體的性質。Bourriot等[18]研究黏度對相分離特性的影響時指出低黏度的多糖因占據較小的膠粒空間使得排阻效應降低,使得乳蛋白(尤其是酪蛋白)膠粒間的凝聚作用大大降低。
2.4 相分離混合體系中上相、下相流變行為
相分離的動力學取決于生物聚合物相的流變性質,因此我們還測定上、下相的表觀黏度變化趨勢。圖 5(a)、(b)分別為上相、下相表觀黏度隨著剪切速率的變化趨勢。
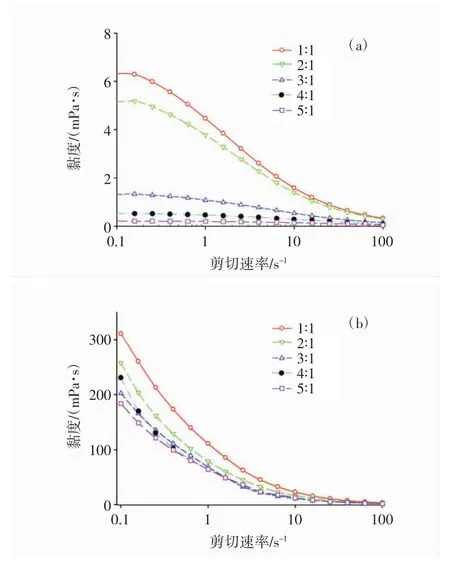
圖5 不同質量比的HD-WPC/HM-P相分離體系中上相(a)、下相(b)表觀黏度分析Fig.5 Apparent viscosity analysis of upper(a)and lower(b)phases in different quality ratios of HD-WPC/HM-P phase separation system
從圖5(a)中可以看到,上相表觀黏度在質量比不超過3∶1時,表觀黏度隨著剪切速率的增加而降低,特別剪切速率超過1 s-1時表現出明顯的剪切稀釋行為,為假塑性流體。當質量比為4∶1、5∶1時,表觀黏度隨剪切速率變化不大,趨勢比較平緩,接近于0,表現出近似牛頓流體的性質,這與混合體系觀察到的相似。圖5(b)所示的是下相表觀黏度的變化。我們可以觀察到不同HD-WPC/HM-P質量比的混合體系的表觀黏度隨著剪切速率的增加均呈現降低的趨勢,表現出剪切變稀行為。而且隨著混合質量比的增加,表觀黏度逐漸降低。從圖5中還可以觀察到,在0.1 s-1~100 s-1剪切速率范圍內,下相的表觀黏度遠高于上相。可以假設,下相蛋白濃度高導致該相表觀黏度高[12]。
相分離混合體系的表觀黏度與上相表觀黏度相似,但是略高于上相。膠態分散體的總粘度由連續相的黏度以及有效顆粒濃度決定[25-26]。McClements等[27]研究發現由于膠體分散體的黏度應始終大于連續相的黏度,因此可以知道構成系統連續相的是上相還是下相。由2.3分析可知上相表觀黏度明顯低于下相,表明富含多糖的上相在這個系統中形成連續相,而富含蛋白的下相為分散相。
2.5 相分離混合體系外觀變化
圖6所示的是不同質量比的HD-WPC/HM-P相分離混合體系離心2 h后外觀的變化。

圖6 不同質量比的HD-WPC/HM-P混合體系外觀分析Fig.6 Appearance analysis of differen qualityt ratio HD-WPC/HM-P phase separation systems
從圖6中可以發現,不同比例的混合體系均發生相分離現象。下相體積隨著蛋白濃度的增加而增加,上相體積隨著多糖濃度增加而增加,由此也可以推斷出下相可能為蛋白富集相,上相為多糖富集相,這與前面研究上、下相蛋白多糖含量的結果一致。
3 結論
本試驗主要探討了不同質量比(1∶1、2∶1、3∶1、4∶1、5∶1)的熱變性乳清濃縮蛋白與高甲氧基果膠對整個混合體系相分離行為的影響,通過分析相分離混合體系中蛋白、多糖濃度、表觀黏度以及外觀可知,不同質量比的混合體系均發生相分離行為,上相為多糖富集相,下相為蛋白富集相。混合溶液的表觀黏度隨著剪切速率的增加而降低,且隨著混合HD-WPC/HM-P質量比的增加,表觀黏度逐漸降低。結果表明,不同比例的混合體系均發生相分離行為,且上相為連續相,下相為分散相,這為我們后續在水凝膠中的研究奠定一定的理論基礎。
[1]Nunes M C,Batista P,Raymundo A,et al.Vegetable proteins and milk puddings[J].Colloids and Surfaces B:Biointerfaces,2003,31(1):21-29
[2]Fang Y,Li L,Inoue C,et al.Associative and segregative phase separations of gelatin/kappa-carrageenan aqueous mixtures[J].Langmuir,2006,22(23):9532-9537
[3]Antonov Y A,Moldenaers P.Structure formation and phase-separation behaviour of aqueous casein-alginate emulsions in the presence of strong polyelectrolyte[J].Food Hydrocolloids,2011,25(3):350-360
[4]Bergfeldt K,Lennart Piculell A,Linse P.Segregation and Association in Mixed Polymer Solutions from Flory Huggins Model Calculations[J].Journal of Physical Chemistry,1996,100(9):3680-3687
[5]Doublier J L,Garnier C,Renard D,et al.Protein-polysaccharide interactions[J].Current Opinion in Colloid&Interface Science,2000,5:202-214
[6]Kruif C G D,Weinbreck F,Vries R D.Complex coacervation of proteins and anionic polysaccharides[J].Current Opinion in Colloid&Interface Science,2005,9(5):340-349
[7]Grinberg V Y,Tolstoguzov V B.Thermodynamic incompatibility of proteins and polysaccharides in solutions[J].Food Hydrocolloids,1997,11(2):145-158
[8]Tuinier R,Rolin C,de Kruif C G.Electrosorption of pectin onto casein micelles[J].Biomacromolecules,2002,3(3):632-638
[9]韓雪,孫冰.乳清蛋白的功能特性及應用[J].中國乳品工業,2003,31(3):28-30
[10]張丹鳳.乳清蛋白的特性及其在乳制品生產中的應用[J].中國乳業,2007(3):27-28
[11]Setiowatia A D,Vermeira L,Martinsb J,et al.Improved heat stability of protein solutions and O/W emulsions upon dry heat treatment of whey protein isolate in the presence of low-methoxyl pectin[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2016,510:93-103
[12]Matalanis A,Lesmes U,Decker E A,et al.Fabrication and characterization of filled hydrogel particles based on sequential segregative and aggregative biopolymer phase separation[J].Food Hydrocolloids,2010,24(8):689-701
[13]Perrechil F A,Cunha R L.Development of multiple emulsions based on the repulsive interaction between sodium caseinate and LBG[J].Food Hydrocolloids,2012,26(1):126-134
[14]Bosnea L A,Moschakis T,Biliaderis C G.Complex Coacervation as a Novel Microencapsulation Technique to Improve Viability of Probiotics Under Different Stresses[J].Food&Bioprocess Technology,2014,7(10):2767-2781
[15]Bradford M M.A rapid and sensitive method for quantitation of microgram quantities of proteins utilizing the principle of protein dyebinding[J].Biochemistry,1976,72:248-258
[16]Dubois M,Gilles K A,Hamilton J K,et al.Colorimetric Method for Determination of Sugars and Related Substances[J].Analytical Chemistry,1956,28(3):350-356
[17]Laneuville S I,Paquin P,Turgeon S L.Effect of preparation conditions on the characteristics of whey protein-xanthan gum complexes.[J].Food Hydrocolloids,2000,14(4):305-314
[18]Bourriot S,Garnier C,Doublier J L.Phase separation,rheology and microstructure of micellar casein-guar gum mixtures[J].Food Hydrocolloids,1999,13(1):43-49
[19]Turgeon S L,Beaulieu M,Schmitt C,et al.Protein-polysaccharide interactions:phase-ordering kinetics,thermodynamic and structural aspects[J].Current Opinion in Colloid&Interface Science,2003,8(4):401-414
[20]Jara F,Pilosof AMR.Partitioning of α -lactalbumin and β -lactoglobulin in whey protein concentrate/hydroxypropylmethylcellulose aqueous two-phase systems[J].Food Hydrocolloids,2011,25(3):374-380
[21]Kim H J,Decker E A,Mcclements D J.Preparation of multiple emulsions based on thermodynamic incompatibility of heat-denatured whey protein and pectin solutions[J].Food Hydrocolloids,2006,20(5):586-595
[22]李向紅,裘愛泳,華欲飛,等.蛋白質-多糖相分離性質及其研究進展[J].糧食與油脂,2006(9):14-15
[23]Syrbe A,Bauer W J,Klostermeyer H.Polymer science concepts in dairy systems--an overview of milk protein and food hydrocolloid interaction[J].International Dairy Journal,1998,8(3):179-193
[24]王翠娜.聚合乳清蛋白與多糖相互作用對其凝膠特性影響及應用[D].長春:吉林大學,2015.
[25]Genovese D B,Lozano J E,Rao M A.The rheology of colloidal and noncolloidal food dispersions[J].Journal of Food Science,2007,72(2):R11-R20
[26]Mcclements D J,Decker E A,Weiss J.Emulsion-Based Delivery Systems for Lipophilic Bioactive Components[J].Journal of Food Science,2007,72(8):109-24
[27]Mcclements D J.Food emulsions:principles,practices,and techniques[J].International Journal of Food Science&Technology,1999,36(2):223-224

