電場對三疣梭子蟹微凍貯藏過程中品質的影響
李苑,王麗平,余海霞,楊水兵,胡亞芹,*
(1.浙江大學生物系統工程與食品科學學院,馥莉食品研究院,浙江省食品加工技術與裝備工程中心,浙江省農產品加工技術研究重點實驗室,浙江杭州310058;2.浙江大學舟山海洋研究中心,浙江舟山316021)
三疣梭子蟹是一種肉質細嫩的甲殼類生物[1],具有高蛋白、低脂肪的特點,是一種被人們廣泛喜愛的水產品[2]。然而由于其肌肉結構組織松散,梭子蟹死后發生復雜的物理、化學及生化變化,體內蛋白質、脂肪等被內源和外源的酶或微生物分解成小分子的產物,并且被腐敗微生物利用,在質構、營養上都發生巨大的變化,并產生揮發性物質等,影響其風味及食用價值[3-4]。因此,選擇合適的方法對三疣梭子蟹進行保藏,延長其貨架期,具有重要的意義。
目前水產品的保鮮技術主要有低溫保鮮技術[5-6]、生化保鮮技術[7-8]、高壓保鮮技術[9-10]、氣調保鮮技術等[11]。隨著科技的發展和人們對于水產品品質要求的提高,新的保鮮方法例如冰溫保鮮[12]、輻照保鮮[13]、臭氧保鮮[14]、微凍保鮮等也被研究和逐步應用。
微凍保鮮是將貯藏溫度控制在低于被凍結生物體冰點1℃~2℃的一種保鮮技術,與傳統的冷藏技術相比,微凍保鮮使得微生物的生長得到更好的抑制,從而起到延長貨架期的作用[15];與傳統的冷凍技術相比,微凍過程中水產品部分結冰,通過抑制冰晶的生成,控制了冰晶對肌肉組織的損害,控制水分的流失[16]。但是微凍對于環境溫度的要求較高,很小的溫度波動都會使得肌肉中的冰晶大量生長[17]。
冰晶的形成分為晶核形成和晶體生長兩步。在水分凍結的過程中,電場對水分子施加力矩,破壞其平衡狀態,從而使得晶核的形成受到抑制[18]。同時,電場的引入可以造成水與酶結合狀態的變化,使得酶失活[19]。電場同時具有一定的殺菌作用,電穿孔模型是其中廣為接受的理論。電場也可以通過增大細胞的跨膜電位,使得細胞膜通透性增強,細胞質流出而造成細胞的死亡[20]。
目前對于電場保鮮已經有一些研究。Ko等[21]對羅非魚在高壓靜電場中進行處理,殺菌效果比較明顯。Ko等[22]研究也發現高壓靜電場可以有效的抑制羅非魚的鹽溶性蛋白含量下降。陳建榮等[23]研究發現電場處理的魚貯藏期得到了延長。然而在微凍過程中引入電場的研究還很少。在微凍過程中加入電場,可以起到抑制冰晶生成的作用,在一定程度上減少微凍過程中冰晶對水產品造成的損傷。本研究采用三疣梭子蟹為原料,將其分別進行有電場參與和無電場參與的微凍保鮮,通過對其貯藏過程中各項指標進行測定,包括與蛋白相關的揮發性鹽基氮(total volatile basic nitrogen,TVB-N)、SDS-PAGE電泳,與脂肪氧化相關的硫代巴比妥酸(thiobarbituric acid,TBA)、與微生物生長相關的菌落總數(total viable count,TVC)以及微觀組織成分觀察,比較有無電場參與對于微凍過程的影響,為電場與微凍結合對水產品的保鮮提供依據。
1 材料與方法
1.1 材料與試劑
新鮮舟山三疣梭子蟹:浙江省舟山市國際水產城,選取重量約100.0 g~150.0 g的新鮮三疣梭子蟹,放入裝有碎冰的泡沫盒中40 min內運回實驗室。
三 氯 乙 酸 、 氧 化 鎂 、CuSO4、NaOH、HCl、NaCl、NaH2PO4、Na2HPO4、甘氨酸、十二烷基硫酸鈉、2-硫代巴比妥酸(均為分析純):國藥集團化學試劑有限公司。三羥甲基氨基甲烷、四乙基乙二胺、過硫酸銨、丙烯酰胺/甲叉雙丙烯酰胺溶液:生工生物工程(上海)股份有限公司。
1.2 儀器與設備
L93-2L溫度記錄儀:杭州路格科技有限公司;YD202A石蠟切片機、D-A智能型生物組織攤片機、YD-B智能型生物組織烤片機:浙江省金華益迪醫療設備廠;DKS-12電熱恒溫水浴鍋:嘉興市中新醫療儀器有限公司;TGL-16G高速臺式離心機:上海安亨科學儀器廠;FLY-YS-108L恒溫保存箱:北京福意電器有限公司;UV-1800PC紫外-可見分光光度計:上海美普達有限公司;XBLL-23A絞肉機:上海帥佳電子科技有限公司;AR124CN分析天平:美國 Ohaus公司;Tanon EPS 300垂直電泳儀:上海天能科技有限公司。
1.3 樣品處理
將活的三疣梭子蟹流水清洗5 min后,瀝干水分用自封袋包裝,分別置于-3℃普通微凍冰箱(P組)和-3℃電場微凍冰箱(D組)進行保鮮。
電場微凍冰箱內部左右兩側置有電場,其發射電源為220 V,經變頻器輸出為3 000 V。
1.4 凍結曲線的測定
將溫度記儀設置為30 s記錄一次溫度后,將溫度探頭插入三疣梭子蟹腹部肌肉中,將三疣梭子蟹放入-18℃冰箱中,溫度隨時間變化的曲線即為凍結曲線。試驗測定3次。根據凍結曲線得到三疣梭子蟹的凍結點,并確定其微凍溫度。
1.5 TVB-N的測定
參照GB 5009.228-2016《食品安全國家標準食品中揮發性鹽基氮的測定》中半微量定氮法進行TVB-N的測定。
1.6 肌原纖維蛋白的提取
肌原纖維蛋白的提取按照Lefever等[24]的方法來進行。取約20 g樣品,加入10倍體積的緩沖液A(100 mmol/L NaCl-1 mmol/L EDTA-20 mmol/L磷酸緩沖液,pH7.0),勻漿30min后在4℃下1000g(3000r/min)離心15 min。向離心所得的沉淀中加入5倍體積的緩沖液A,按上述條件再次離心。棄去上清液后,向沉淀中加入5倍體積的緩沖液A進行過濾,然后將沉淀用5倍體積的緩沖液A進行沖洗,得到的濾液再在相同條件下進行離心,得到沉淀。該過濾離心的過程重復2遍~3遍,最后得到的沉淀用5倍體積的緩沖液B(1 mol/L NaCl-50 mmol/L磷酸緩沖液,pH7.0)溶解,勻漿離心后的上清液,即為肌原纖維蛋白溶液。
1.7 SDS-PAGE電泳
SDS-PAGE電泳過程按照劉文娟[25]的方法進行并稍加改動。將按照1.6提取的5 mL肌原纖維蛋白溶液樣品和5 mL雙縮脲試劑混合后,在25℃下水浴1.5 h。用可見光紫外分光光度計于540 nm處測定吸光值,與牛血清蛋白標準蛋白曲線對照得到蛋白濃度,并用緩沖液B調整濃度至4 mg/mL。按樣品∶蛋白上樣緩沖液為1∶4(體積比)的比例處理樣品,樣品在95℃加熱5 min后冷卻,然后上樣10 μL。電泳分離膠為12%,濃縮膠為5%。恒壓100 V下進行電泳。染色使用考馬斯亮藍溶液進行。脫色后觀察蛋白條帶的變化。
1.8 TBA的測定
TBA的測定參照Siu等[26]的方法進行并稍加改動。將5.0 g樣品攪碎后,加入25 mL含有0.1%的EDTA溶液,振搖30 min后,混合物用雙層濾紙過濾,取5 mL上清液加入0.02mol/L的TBA溶液5mL,沸水浴40min后流水冷卻,5 000 r/min離心20 min,取上清液加入5 mL氯仿搖勻,靜置后取上清液,分別在532 nm和600 nm處測定吸光值,按以下公式計算TBA值:
TBA/(mg/100 g)=(A532-A600)/155×(1/10)×(1/10)×72.6×100
1.9 TVC的測定
TVC的測定參照Wu等[27]的方法進行,并加以改動。向無菌袋中加入10.0 g樣品和90 mL0.9%的無菌生理鹽水,均質5 min后,使用無菌生理鹽水對懸浮液進行體積比為1∶10的連續稀釋。再分別吸取1 mL不同濃度稀釋液于滅菌培養皿內(每個稀釋濃度兩個平行,兩個空白),將冷卻至46℃左右的營養瓊脂培養基注入培養皿,混合均勻,在瓊脂冷卻至凝固后,將接種好的平板在30℃恒溫培養箱中培養72 h,計數方法采用平板計數法。試驗結果以lg(CFU/g)表示。
1.10 肌肉組織微觀結構形態觀察
參照胡玥等[28]的方法,三疣梭子蟹從腹部肌肉取樣,大小為5 mm×5 mm×10 mm,進行垂直于肌原纖維方向的橫切,肌肉的微觀組織結構在400×的光學顯微鏡下進行觀察。
1.11 統計方法
所有試驗至少重復3次,數據以平均值及方差表示。使用Excel 2007、SPSS 16.0軟件以及方差分析(ANOVA)進行數據處理。
2 結果與分析
2.1 三疣梭子蟹凍結曲線分析及微凍溫度的確定
三疣梭子蟹的凍結曲線如圖1所示。
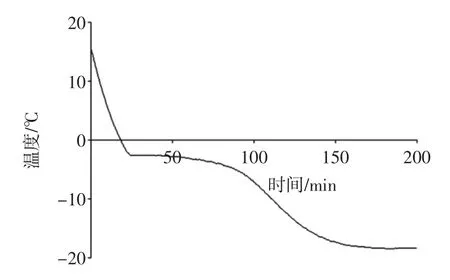
圖1 三疣梭子蟹凍結曲線Fig.1 Freezing curve of Pseudosciaena polyactis
隨著時間的延長,三疣梭子蟹的中心溫度首先迅速降低,在第24 min左右到達第一個拐點,溫度為-2.6℃。凍結曲線中出現的第一個拐點為物料的凍結點。到達第一個拐點之后,隨著凍結過程的繼續進行,三疣梭子蟹的溫度沒有顯著下降,即通過最大冰晶生成帶。在該過程中,肌肉中大部分水分形成冰晶。在通過最大冰晶生成帶后,繼續凍結,三疣梭子蟹溫度繼續下降,直到達到環境溫度(-18℃)并保持穩定。根據微凍溫度在凍結點1℃~2℃的定義,綜合考慮儀器實際情況及三疣梭子蟹的凍結點,選擇-4℃對三疣梭子蟹進行貯藏。
2.2 兩種條件貯藏過程中三疣梭子蟹TVB-N變化
揮發性鹽基氮(TVB-N)是水產品體內由于酶和微生物的作用而使蛋白質等分解產生堿性物質的總稱,一般用于反映水產品的新鮮程度[29]。普通微凍和電場微凍貯藏過程中三疣梭子蟹的TVB-N值的變化如圖2所示。
隨著貯藏時間的延長,兩組的TVB-N值都呈現了上升的趨勢,代表著三疣梭子蟹在貯藏過程中品質的下降。電場微凍組表現出比普通微凍組緩慢的上升趨勢,這與Ko等[21]的研究結果一致。在貯藏第25天時,普通微凍組(P)和電場微凍組(D)的TVB-N值分別為26.1 mg/100 g和22.3 mg/100 g,根據GB 2733-2015《食品安全國家標準鮮、凍動物性水產品》的要求,海蟹中的TVB-N值應≤25 mg/100 g,普通微凍組在貯藏第25天已超過海蟹TVB-N值應≤25 mg/100 g的標準,為不可食狀態。在貯藏第31天,電場微凍組的TVB-N值達到25.2 mg/100 g,達到不可食用狀態。電場的添加可能通過抑制酶和微生物的活力達到了減緩三疣梭子蟹腐敗,從而達到延緩體內揮發性鹽基氮增加的作用[30]。
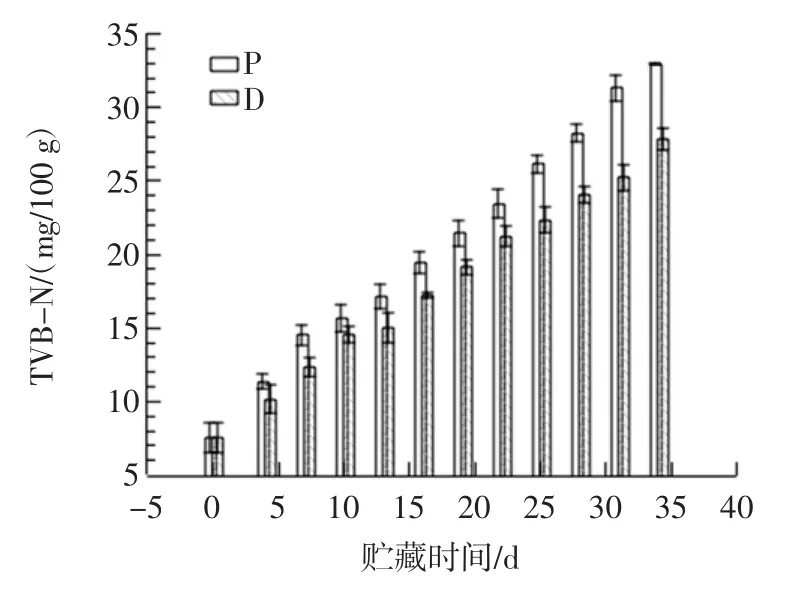
圖2 普通微凍及電場微凍條件下三疣梭子蟹TVB-N變化Fig.2 Changes of TVB-N in Pseudosciaena polyactis during storage of regular superchilling and electric field superimposed superchilling
2.3 兩種條件貯藏過程中三疣梭子蟹SDS-PAGE電泳分析
普通微凍及電場微凍條件下,貯藏第7、16、28天時三疣梭子蟹的肌原纖維SDS-PAGE電泳圖譜如圖3所示。
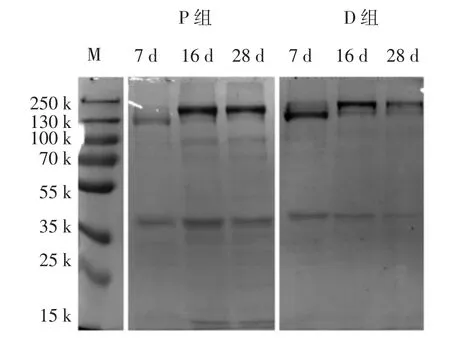
圖3 普通微凍及電場微凍條件下三疣梭子蟹肌原纖維SDSPAGE電泳圖譜Fig.3 Electrophoresis of Pseudosciaena polyactis during storage of regular superchilling and electric field superimposed superchilling
在圖3P組三疣梭子蟹的電泳圖譜中,肌球蛋白的條帶(130 k左右)隨著貯藏時間延長逐漸溶解,而250 k左右的蛋白條帶明顯加粗,這可能是由于肌原纖維中二硫鍵和二酪氨酸的形成導致的蛋白聚集[31]。與普通微凍組相比,電場微凍組250 k處的蛋白質聚集顯示出了較慢的聚集,一方面,這可能與電場的殺菌作用導致三疣梭子蟹的腐敗進程減緩,蛋白質分解速度較普通微凍慢;另一方面,電場對冰晶的形成具有抑制作用,冰晶形成的減少減弱了冰晶對于組織細胞的擠壓,從而延緩了蛋白質的變性。
2.4 兩種條件貯藏過程中三疣梭子蟹TBA變化
水產品中的脂肪,尤其是不飽和脂肪酸容易氧化變質或者因受到微生物等的影響而腐敗,TBA值為判定脂肪氧化程度的一個指標。普通微凍和電場微凍過程中三疣梭子蟹的TBA值變化如圖4所示。
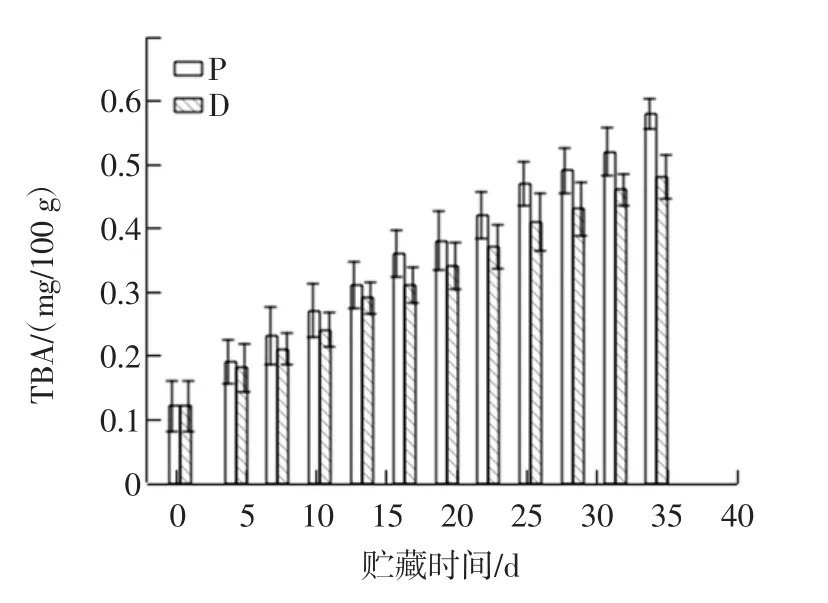
圖4 普通微凍及電場微凍條件下三疣梭子蟹TBA變化Fig.4 Changes of TBA in Pseudosciaena polyactis during storage of regular superchilling and electric field superimposed superchilling
隨著貯藏時間的延長,兩組的TBA值都呈現上升趨勢。電場微凍組相對普通微凍組顯示出了較慢的TBA值增長趨勢,在貯藏第35天,普通微凍組和電場微凍組TBA值分別達到了0.48 mg/100 g和0.58 mg/100 g。Ko等[21]認為,這可能與電場的加入有關,電場會使得電荷在水產品表現形成,從而隔絕了氧氣的進入,減緩了脂肪氧化的發生。另一方面,電場通過抑制冰晶形成,減緩了冰晶對細胞的破壞,減緩了水產品腐敗進程,因此電場微凍組TBA值的增加減慢。
2.5 兩種條件貯藏過程中三疣梭子蟹TVC變化
菌落總數(TVC)是反映水產品新鮮程度的重要指標。梭子蟹營養豐富,水分含量高,外界微生物也容易侵染。圖5反映了普通微凍和電場微凍條件下三疣梭子蟹肌肉內TVC的變化情況。隨著貯藏時間的延長,普通微凍和電場微凍的菌落總數都是不斷增加,貯藏后期TVC的增加較前期快。電場微凍組菌落總數增加較普通微凍組慢。在貯藏第34天,電場微凍組和普通微凍組的TVC值分別達到6.40 lg(CFU/g)和7.53 lg(CFU/g)。這很可能是由于電場所具有的殺菌作用。
2.6 三疣梭子蟹肌肉組織微觀結構形態觀察
圖6表示了貯藏第10天和第31天時普通微凍及電場微凍條件下三疣梭子蟹微觀結構的變化。
如圖6所示,在貯藏第10天,三疣梭子蟹肌肉細胞之間出現了比較小的縫隙,其中電場保鮮組的縫隙比較均勻,而普通微凍組存在一些不均勻的縫隙。隨著貯藏的進行,電場微凍組(D)在第31天依然表現為較為均勻的肌肉組織間隙,而普通微凍組(P)則有明顯的冰晶聚集和肌肉纖維造成的粗細不一的空隙。這可能與電場抑制了冰晶的生長有關。Kaale等[32]認為,在有外部電場作用的情況下,由于平行于電場方向的水分子需要克服的位能低,容易克服固液界面阻力,完成從水到冰晶的轉變。因此除平行于電場方向的冰晶形成都受到抑制。
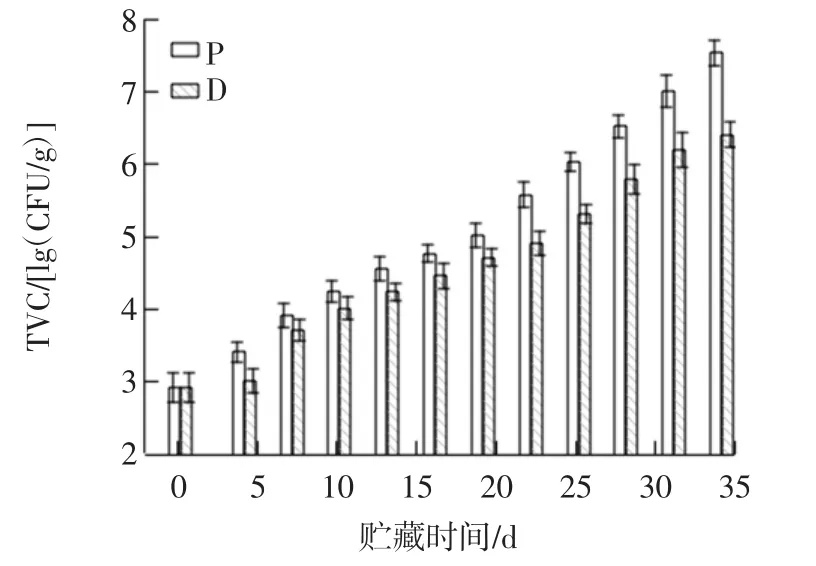
圖5 普通微凍及電場微凍條件下三疣梭子蟹TVC變化Fig.5 Changes of TVC in Pseudosciaena polyactis during storage of regular superchilling and electric field superimposed superchilling
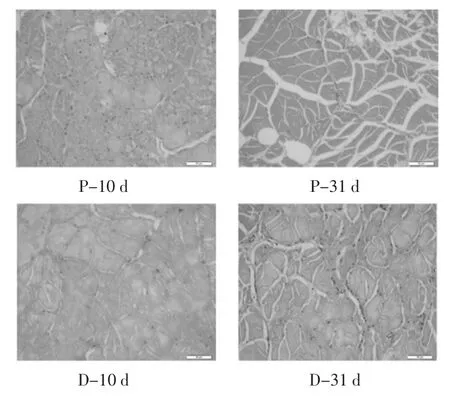
圖6 普通微凍及電場微凍條件下三疣梭子蟹肌肉微觀組織變化Fig.6 Changes of microstructure in Pseudosciaena polyactis during storage of regular superchilling and electric field superimposed superchilling
3 結論
以三疣梭子蟹為對象,對比研究普通微凍和電場微凍兩種方法下其在貯藏過程中理化性質和肌肉微觀結構的影響。電場微凍相對普通微凍,更好地維持了三疣梭子蟹在貯藏過程中的品質,延緩了酶和微生物對肌肉的破壞,脂肪氧化速度減慢,肌肉微觀組織破壞程度也相對較低。電場微凍減緩了三疣梭子蟹的變質,延長了其貨架期。本研究將電場與微凍技術結合,為水產品保鮮提供了新的思路。
[1]鄭丹,段青源,朱勵華,等.三疣梭子蟹不同包裝方式保鮮效果的比較[J].農業工程學報,2009(12):357-360
[2]Hamasaki K,Fukunaga K,Kitada S.Batch fecundity of the swimming crab Portunus trituberculatus(Brachyura:Portunidae)[J].Aquaculture,2006,253(1):359-365
[3]苗鈺湘,湯海青,歐昌榮,等.基于電子鼻的三疣梭子蟹鮮度評價方法研究[J].核農學報,2016,30(4):748-754
[4]Sarnoski P J,O’Keefe S F,Jahncke M L,et al.Analysis of crab meat volatiles as possible spoilage indicators for blue crab(Callinectes sapidus)meat by gas chromatography-mass spectrometry[J].Food chemistry,2010,122(3):930-935
[5]楊文鴿,薛長湖,徐大倫,等.大黃魚冰藏期間ATP關聯物含量變化及其鮮度評價[J].農業工程學報,2007,23(6):217-222
[6]Vanesa L.Sensory,microbial and chemical effects of a slurry ice system on horse mackerel(Trachurus trachurus)[J].Journal of the Science of Food and Agriculture,2005,85(2):235-242
[7]廖列文,崔英德,朱文淵,等.高吸水性樹脂在魚類保鮮中的應用研究[J].食品科學,2002,23(8):241-243
[8]Kim J.Determination of chorate and chlorite and mutagenicity of seafood treated with aqueous chlorine dioxide[J].Journal of Agriculture and Food Chemistry,1999,47(9):3586-3591
[9]Zahra Z.High peressure processing of fresh tuna fish and its effects on shelf life[D].Montreal:Department of Food Science and Agriculture Chemistry Macdonald Campus of McGill University,2004:59-61
[10]Juan C R,Michael T M.Effect of high pressure processing on shelf life of albacore tuna minced muscle[J].Innovative Food Science and Emerging Technologies,2006,7(1/2):19-27
[11]Hobbs G.Fish:microbiological spoilage and safety[J].Food Science and Technology,1991,5(3):166-173
[12]楊華,張建斌,吳曉,等.冰溫貯藏對鰱,草,鯉魚糜制品品質的影響[J].食品科學,2016,37(12):273-278
[13]鞠健,胡建中,廖李,等.Nisin結合輻照處理對冷藏鱸魚品質的影響[J].食品工業科技,2016(21):280-284
[14]趙永強,李來好,楊賢慶,等.臭氧在水產品加工中應用綜述[J].南方水產科學,2013,9(5):149-154
[15]蔡青文,謝晶.微凍保鮮技術研究進展[J].食品與機械,2013,29(6):248-252
[16]李苑,王麗平,李鈺金,等.水產品凍結貯藏中冰晶的形成及控制研究進展[J].食品科學,2016,37(19):277-282
[17]DINCER I.Heat transfer in food cooling applications[M].Washington:CRC Press,1997:42-48
[18]陳程,陶樂仁,華澤釗.靜電場對紅細胞與冰晶間相互機械性作用的影響[J].低溫工程,2004(5):45-49
[19]CHAPMAN D.The role of water in biomembrane structures[J].Journal of Food Engineering,1994(22):367-380
[20]Barba F J,Grimi N,Vorobiev E.New Approaches for the Use of Non-conventional Cell Disruption Technologies to Extract Potential Food Additives and Nutraceuticals from Microalgae[J].Food Engineering Reviews,2014,7(1):45-62
[21]KO W,YANG S,CHANG C,et al.Effects of adjustable parallel high voltage electrostatic field on the freshness of tilapia(Orechromis niloticus)during refrigeration[J].LWT-Food Science and Technology,2016,66:151-157
[22]Ko W,Shi H,Chang C,et al.Effect of adjustable parallel high voltage on biochemical indicators and actomyosin Ca2+-ATPase from tilapia(Orechromis niloticus)[J].LWT-Food Science and Technology,2016,69:417-423
[23]陳建榮.高壓靜電場對魚的保鮮研究[J].現代食品科技,2012(5):499-501,498
[24]Lefevre F,Fauconneau B,Thompson J W,et al.Thermal denaturation and aggregation properties of Atlantic salmon myofibrils and myosin from white and red muscles[J].Journal of agricultural and food chemistry,2007,55(12):4761-4770
[25]劉文娟.凝膠增強劑對帶魚肌肉蛋白質熱凝膠形成的影響及機理研究[D].杭州:浙江大學,2015:23
[26]Siu G M,Draper H H.A SURVEY OF THE MALONALDEHYDE CONTENT OF RETAIL MEATS AND FISH[J].Journal of Food Science,1978,43(4):1147-1149
[27]Wu C,Li Y,Wang L,et al.Efficacy of chitosan-gallic acid coating on shelf life extension of refrigerated pacific mackerel fillets[J].Food and bioprocess technology,2016,4(9):675-685
[28]胡玥,楊水兵,余海霞,等.微凍保鮮方法對帶魚品質及組織結構的影響[J].食品科學,2016,37(18):290-297
[29]范凱,廖李,程薇,等.茶多酚結合輻照對鱸魚冷藏品質的影響[J].核農學報,2016,30(9):1780-1785
[30]He X,Liu R,Nirasawa S,et al.Effect of high voltage electrostatic field treatment on thawing characteristics and post-thawing quality of frozen pork tenderloin meat[J].Journal of Food Engineering,2013,115(2):245-250
[31]姜晴晴,邵世奇,陳士國,等.凍融循環對帶魚蛋白性質及肌肉品質的影響[J].中國食品學報,2016(4):122-129
[32]Kaale L D,Eikevik T M,Kolsaker K,et al.Modeling and simulation of food products in superchilling technology[J].Journal of aquatic food product technology,2014,23(4):409-420

