基于生活的問題導學在高中化學復習課中的實踐
沈婷


摘要:基于生活的問題導學策略就是以學生活動和經歷為基礎,以問題作為驅動教學過程的核心,將問題貫穿于課堂始末。作者以“氧化還原”復習課為例,介紹了該教學模式的實踐過程,并進行了教學反思。
關鍵詞:氧化還原;問題導學;生活
文章編號:1008—0546(2017)11—0058—03 中圖分類號:G633.8 文獻標識碼:B
doi:10.3969/j.issn.1008—0546.2017.11.019
復習課是化學教學的重要課型之一,學生掌握知識往往需要經過領會、理解和應用三個環節。由于學生存在個體差異,在學習過程中對知識掌握程度不同,如果復習課只是炒冷飯,將原本的知識進行抽象的重復與堆積,往往導致會的學生沒興趣,不會的學生又不想聽的兩難境地。因此,復習課同樣需要將知識與生產生活相聯系,使學科知識更“接地氣”。
一、核心概念解讀
基于生活的問題導學策略就是以學生的日常活動和經歷為基礎,以問題作為驅動教學過程的核心,以問題引入,以問題歸結,將問題貫穿于課堂始末。教師依據課程標準和教學內容,通過創設生活情景,引導學生發現問題并探尋解決途徑,使概念、規律具有生命力,使學生更易理解知識的內涵,也使學生學會學習,形成正確的學科觀、社會觀和價值觀。
二、教學設計模型
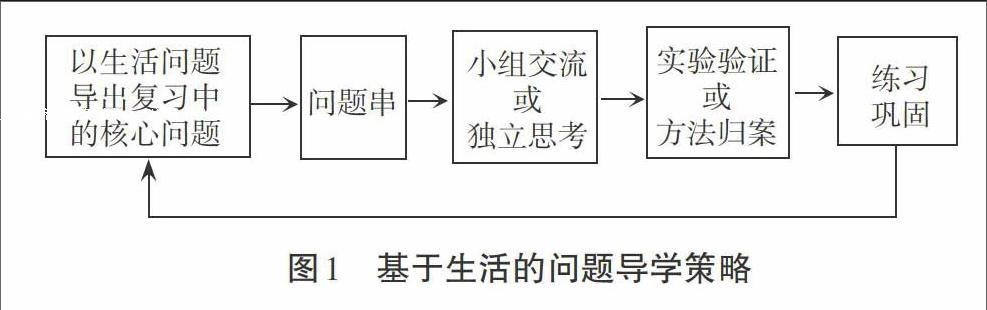
實施基于生活的問題導學策略,需要教師根據教學目標和學生的認知特點,復習時圍繞核心知識,用生活問題進行導學,提出核心問題以及圍繞核心問題的問題串,再采用小組討論、實驗驗證、獨立思考和方法歸納等環節突破復習中的難點,最終回歸與復習知識點相關的化學生活問題,達到應用知識的高度。當然核心問題可能不止一個,核心問題之間具有一定的內在聯系,設計時按螺旋上升的形式,形成多層次的問題鏈分層提問、逐層解答。
三、教學案例
以學業水平測試“氧化還原”復習課為例。根據學業水平測試考試要求,以及對近幾年真題的研究,確立了本節課的兩個核心知識點:一、氧化還原反應方程式中幾組相對概念的判斷;二、氧化還原離子反應方程式的書寫方法。
1.氧化還原相關概念
①創設生活情境,呈現核心問題
教師播放一小段新聞視頻,這則新聞講述的是一位小伙在清潔廁所時,同時使用了84消毒液和潔廁靈而發生中毒,險些喪命的事件。
②問題串
問題一:為什么這位小伙會中毒?
問題二:發生了什么化學反應?請寫出反應方程式。
問題三:該反應中的氧化劑、還原劑、氧化產物和還原產物分別是什么?
問題四:該反應中電子是如何轉移的?
③小組交流
學生從84消毒液和潔廁靈的使用說明信息中找到了關于其成分和注意事項的線索,并順藤摸瓜寫出相應的反應原理:NaCIO+2HCl=NaCl+Cl2↑+H2O根據已掌握的化學知識,不難推測出是氯氣使新聞中的小伙中毒。
以此反應分析氧化還原的幾組相對概念,學生通過回憶氧化還原反應的特征和本質,標出化合價的升降變化,判斷出氧化劑為NaClO,還原劑為HCl,氧化劑發生還原反應,還原劑發生氧化反應,生成的Cl2既是氧化產物又是還原產物。NaClO中的氯元素在反應中化合價降低,得到電子;HCl中的氯元素化合價升高,失去電子。若用單線橋表示電子的轉移數目和方向,可表示為:
④實驗驗證
實驗是檢驗化學原理的可靠途徑。在課堂上,現場驗證上述實驗,同學們觀察實驗現象。
實驗器材:84消毒液、潔廁靈、試管、針筒、淀粉KT試紙、橡膠塞
實驗過程:向試管中倒入1mL潔廁靈,將淀粉-KI試紙潤濕后貼在試管內壁,并塞上橡膠塞,用針筒吸入1mL 84消毒液,穿過橡膠塞,注入試管中,振蕩試管,觀察到淀粉-KI試紙由無色變為藍色。
⑤練習鞏固
上述實驗中淀粉KI-試紙為什么會變藍?請大家寫出此反應原理,并分析該反應中的氧化劑、還原劑、氧化產物和還原產物,并用雙線橋標出電子轉移的方向和數目。
2.氧化還原離子反應方程式的書寫方法
氧化還原離子反應方程式的書寫是近年來高考和學業水平測試中經常出現的一種題型,能綜合考查學生氧化還原概念以及運用信息分析、解決問題的能力。
①創設生活情境,呈現核心問題
剛才演示圖4實驗時,我們觀察到試紙由無色變為藍色,現在我們再來觀察一下當前的實驗現象,驚奇地發現此時試紙是無色的,剛才的藍色已經褪去了。在剛剛過去的幾分鐘內,試管中又發生了什么新的反應呢?
②問題串
問題一:氧化劑、還原劑分別是什么?(根據實驗信息進行推測)
問題二:氧化產物、還原產物分別是什么?(根據化合價升降進行推測)
問題三:該反應在什么樣的環境中發生?
③獨立思考
④方法歸納:
a.找——找出氧化劑、還原劑、氧化產物、還原產物;
b.配——根據電子得失守恒,配平氧化劑、還原劑、氧化產物、還原產物;
c.補——從電荷守恒角度,結合反應的酸堿環境,在方程兩邊補充相應離子或物質;
d.查——檢查方程式中元素和電荷是否守恒。
⑤練習鞏固
例1:用H2O2和H2SO4的混合溶液可溶出印刷電路板金屬粉末中的銅,生成Cu2+和H2O。其離子方程式為____________。endprint
例2:高鐵酸鉀(K2FeO4)是一種強氧化劑,可作為水處理劑和高容量電池材料。FeCl3與KClO在強堿性條件下反應可制取K2FeO4,其反應的離子方程式為
四、生活問題導學復習課教學反思
1.設計生活問題和情境使復習更有效
化學課堂教學的核心目標是促進學生發展,學生是學習的主體,因此高效的化學課堂必須符合學生心理特點和認知規律。高中生抽象邏輯思維雖占優勢,但同樣需要感性經驗的直接支持,生活問題拉近了理論和實踐的距離,在復習中更能激發學生積極思維,引導他們去發現問題,解決問題,從而提高復習的有效性。
本節復習課中,選擇學生感興趣的生活化學問題創設情境,引起學生對氧化還原相關知識的回憶和檢索,通過兩個核心問題、一系列問題串來診斷認知缺陷,將無意注意轉化為有意注意,創造了良好的學習氛圍。書本上的方塊字變成了有血有肉的鮮活的化學,提高了學習的主動性,也提高了課堂的效率。
2.設計核心問題和問題串使知識更系統
導學問題的設計要呈現螺旋而上、層層推進的狀態,問題串中的每個問題都應有其對應的地位和作用。核心問題是指能整合教材中的學習重點內容,能與學生生活實際和思維水平密切相關的,能貫穿整節課的問題或者任務。設計核心問題,能夠使學生在有限的學習時間里,有效地把握核心知識點,在復習課中,這些核心問題就是核心考點。
本課設計了兩個核心問題,正是氧化還原這部分教學中最核心的兩個考點。兩個核心問題都來源于生活,且具有螺旋而上的遞進關系。問題串也緊緊圍繞核心問題提出,起到了鋪設臺階,引導學生解釋或解決核心問題的作用。整個問題鏈具有一條鮮明的主線,能夠將課堂的核心內容、核心目標與學生的發展高度地整合起來。
3.設計活動與交流使學習更主動
傳統的復習課習慣于通過溫故知識點以及練習、講解習題來達到鞏固知識的目的,很少關注學生能力的發展,化學復習課上的“實驗”變得很奢侈,在復習過程中學生沒有了“再現”、“再探”的機會,從而阻礙了學生能力的發展。
本課精心設計了一個看似簡單的實驗——84消毒液與潔廁靈的反應,將這個實驗充分地運用起來,貫穿了氧化還原的兩個核心考點。學生通過對實驗現象的觀察,來驗證第一個核心問題,從而復習了氧化還原的幾對基本概念以及電子轉移的數量與方向;而后,從實驗現象發生的新變化,引導學生探究發生的新反應,再歸納氧化還原離子反應方程式書寫的步驟“找、配、補、查”。這一源于生活的實驗得到了充分的挖掘,學生也進行了充分的探究,使學生對氧化還原這部分知識的內在聯系更加清晰,思維層次也得到了提升。endprint

