由“蛋的奇妙變化”引出的酸堿主題復習課的教學反思
游梅

摘要:文章是基5-“雞蛋中的化學”主題的酸堿性質復習課的教學反思。教師用“酸蛋”實驗讓學生分析了反應物的幾種可能,酸性廢液的處理方法等。從制做皮蛋的配料之間的反應,到料液中氫氧化鈉濃度的測定,再到皮蛋的酸堿性檢驗、皮蛋的最佳吃法等方面討論“堿蛋”知識。整節課主題新穎,科學、技術、社會三者巧妙結合,融知識、情境一體,實驗、計算一體。
關鍵詞:酸蛋;堿蛋;實驗;計算;中性;細節
文章編號:1008—0546(2017)11—0067—03 中圖分類號:G633.8 文獻標識碼:B
doi:10.3969/j.issn.1008—0546.2017.11.022
一、教學思路
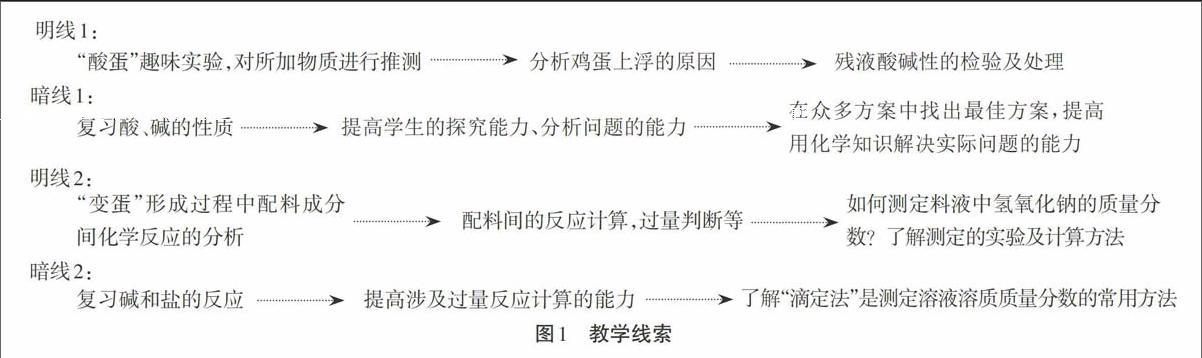
本堂課有“酸蛋”和“堿蛋”兩個版塊的內容,每個版塊又有明線、暗線兩條線索。課堂的每條線索、每個環節都是緊緊圍繞酸、堿的性質展開,將化學知識靈活運用到實驗和實際生產、生活中,把化學、技術、社會三者巧妙地結合在一起,還在新授課基礎上進行了深度的挖掘,在復習課中體現出“新、深、活”的特點。
二、主題式復習,將化學知識置于實驗、生活情境中
主題化復習是以某一主題為中心,調動有關的化學知識、能力得以發展。主題化復習有效地契合學生的直接經驗和間接經驗,有利于學生對所學內容的意義構建,有利于化學學科觀念的形成。
1.融知識、情境、實驗一體
本堂課酸堿鹽的性質內容比較枯燥、繁瑣,怎樣讓學生用積極的態度參與學習呢?這就涉及到激發學生學習興趣的問題了。初三學生的心智很不成熟,他們的認知特點有其特殊性:注意力不能持久集中,而且只有對感興趣的事物才產生深層次學習的要求,因此不能用成人學習的態度和方式要求他們。針對學生這樣的認知特點,課堂沒有采取機械炒冷飯的方式復習酸的5條性質、堿的4條性質,而是在“把雞蛋泡在酸溶液中”“分析皮蛋制作的配料”等情境中展開復習。教師先設計了一個“酸蛋”趣味實驗:在燒杯中倒一種無色溶液,放入一只雞蛋,雞蛋沉在溶液底部沒有明顯現象,再倒另一種無色溶液,觀察到溶液先變紅,再褪色,雞蛋表面逐漸產生大量氣泡,最終雞蛋上浮。這個實驗吸引了學生的目光,激發他們思考:趣味實驗中先后倒的兩種溶液分別是什么?同學們想到起初蛋殼表面沒有氣泡,而最終蛋殼表面產生大量氣泡,因為蛋殼的主要成分是碳酸鈣,那么后倒的一定是酸性溶液,先倒的是堿性溶液如氫氧化鈉溶液,且之后倒的酸性溶液中一定含有酚酞,課堂討論第一次達到高潮。
接下來,從“酸蛋”到“堿蛋”,情境貼近學生生活實際,在“堿蛋”中給出制作皮蛋的配料,分析配料中可能的化學反應,料液中氫氧化鈉溶液濃度的測定計算,皮蛋酸堿性的檢測,皮蛋的最佳吃法等。在生活素材中用化學,不僅體現了化學學科的有用性,學了化學能更好地生活,也避免了復習的枯燥,提高了復習效率。在討論酸液會不會是稀硫酸時,有學生說不行,有學生說可以,在大家相持不下時,教師把雞蛋放人盛大量稀硫酸的燒杯中,讓學生觀察實驗現象:開始雞蛋表面產生氣泡,一會兒就停止了,雞蛋沒有上浮!從這個現象學生聯系到實驗室制取二氧化碳不用稀硫酸的原因,有了實驗佐證,教師不需要太多的言語,學生自然會領悟其中的道理!還有在討論廢酸液如何處理時,教師拿來了幾個久置石灰水的細口瓶,瓶內壁上有較多白色固體,分析了白色固體的成分后,教師倒入廢酸液,輕輕振蕩幾下,瓶壁變干凈透明了!白色固體被“洗”掉了。一個簡單的實驗,詮釋了變廢為寶,循環利用,節約藥品的理念,處理既合理又巧妙!
2.融實驗與真實計算一體
受知識水平和實驗儀器的限制,初中化學定量實驗不多,大多數是定性實驗。試題常常會出現“恰好完全反應”的說法,而在真實的實驗和生產實際中,恰好完全反應的情況并不多。新課程強調:化學計算必須是真實的計算,是基于真實實驗情境和實踐運用的計算,因此,化學計算和純數學計算是有很大不同的。
課堂中皮蛋問題的情境:制作皮蛋時要用到堿性物質,因此皮蛋也稱為“堿蛋”。某地制作皮蛋的配料:生雞蛋800枚,生石灰10kg(純度80%),純堿3.5kg,食鹽4kg,花椒250g,松柏枝300g,紅茶末50g,水100kg,鋸末稻殼、黃泥適量。(生石灰480元/t,純堿1700元/t)
問題1:配料表中的10kg生石灰與水反應得到的熟石灰與3.5kg純堿最多能產生多少千克氫氧化鈉?
思路:先算一算10kg含氧化鈣80%的生石灰與水反應,最多得到熟石灰多少千克?再算:多少千克的氫氧化鈣與3.Skg純堿恰好完全反應?最后算:最多能產生多少千克氫氧化鈉?
該題中熟石灰和純堿的配比,氫氧化鈣大大過量,主要是為了更好地利用價格更高的純堿。這個實例說明在實際生產生活中的化學反應,反應物之間不一定會恰好完全反應,一種反應物過量的情況往往會更多。那么,有沒有恰好完全反應的情況呢?接下來的問題2便是恰好完全反應的應用實例。
問題2:為保證松花蛋的質量,需要對料液中氫氧化鈉進行定量分析。一般濃度大于6%或者小于4.5%時,都需要調整原料的投入量。某禽蛋加工廠用燒堿代替石灰、純堿配制料液加工皮蛋。現取某待測料液樣品10g加蒸餾水到250mL,搖勻后過濾。取濾液25mL注入錐形瓶,滴入1-2滴酚酞,溶液呈粉紅色,用0.365%的鹽酸標準液滴定至溶液的粉紅色恰好消失,共消耗鹽酸12mL,標準液的密度以1g/mL計。計算說明該料液中氫氧化鈉的質量分數是否在正常范圍。
這里的滴定法用到鹽酸和氫氧化鈉恰好完全反應的定量實驗,這樣的設計在深層次上進行挖掘,將初三學生的實驗和計算能力提高到一個新的高度,而這種高度是新授課無法企及的。這也是我們上復習課的一個重要目的:在復習中接觸新實驗、學習新方法,加深對新授課內容的理解。
三、兩點反思
本節課開始的趣味實驗,實驗結束后,請學生用廣泛pH試紙測廢液的pH,測定結果為0。我又提出:如何將廢液處理至中性?endprint
學生思考后,提出了很多方案,說到鎂、鋅、生石灰、熟石灰、氫氧化鈉、大理石等可以與酸反應的物質都可以處理該廢液至中性。我對學生的方案表示非常肯定,說考慮到試劑價格的因素,一般選用熟石灰或大理石。
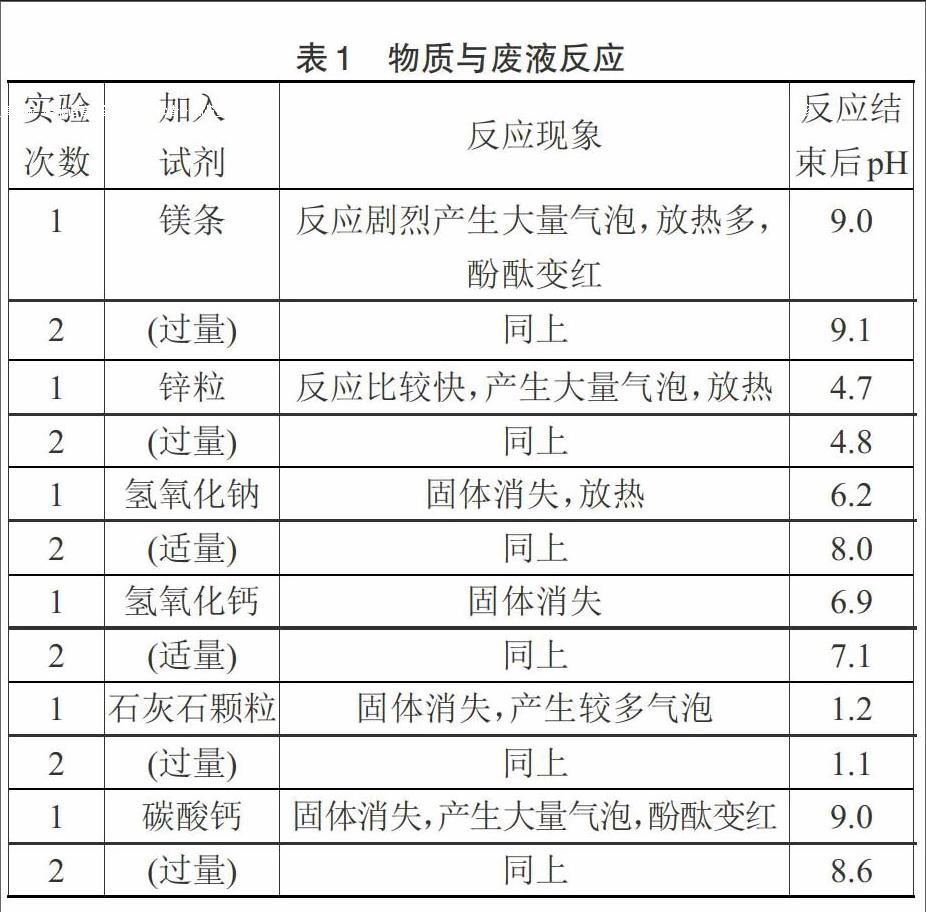
這些物質真能將廢液反應至中性嗎?筆者用鎂、鋅、氫氧化鈉、氫氧化鈣、石灰石顆粒、碳酸鈣等6種固體試劑分別與廢液反應,每種試劑做2次實驗,實驗現象、結果見表1。
廢液的pH=0.1(精密pH計測定)
一般廢液排放的標準是pH=6~9,從實驗過程和結果分析:
①鎂條與鹽酸反應放熱且在氣溫較高的夏天實驗時,過量的鎂與水反應產生了氫氧化鎂,溶液顯弱堿性。鎂價格較高,且與廢液產生大量氫氣,不適合用來處理廢液。
②鋅粒不能將廢液反應至中性,鹽酸的濃度小到一定程度時反應幾乎停止,應是氯化鋅溶液呈酸性的緣故。
③氫氧化鈉能將廢液反應至中性,但氫氧化鈉堿性、腐蝕性太強,價格較高,一般也不用于廢液的處理。
④氫氧化鈣能將廢液處理至中性,反應的終點(pH=7.0)容易把握,氫氧化鈣的價格也不高,一般可用于廢液的處理。
⑤石灰石顆粒不能將廢液反應至中性,可能鹽酸的濃度小到一定量反應就幾乎停止,最終溶液呈酸性。
⑥碳酸鈣粉末能將廢液處理成中性,碳酸鈣過量后溶液呈弱堿性,碳酸鈣粉末可用于處理廢液。
綜上分析:處理酸性廢液合適的物質是氫氧化鈣或碳酸鈣。
我們可以在實驗之前作出合理的假設、推測,但不宜輕易下結論,因為化學反應有其復雜性,有時一個看似很簡單的問題,也需要在實驗之后才能下結論。那么,如何更好地處理該廢液呢?廢物利用、以廢治廢是最佳的處理、利用廢液的方法。實驗室中盛放石灰水的試劑瓶壁上的一層白膜、廁所便池中的污垢、校園鐵質車棚、鐵質運動器材上的鐵銹等等都可以用該廢酸處理。
還有一個反思是課堂教學要關注細節,比如,皮蛋計算題的問題2中數據的有效數字位數不統一,有1位、2位還有3位,很不規范。“細節決定成敗”,“勿以惡小而為之,勿以善小而不為”,追究細節不是強調細枝末節,而是一種嚴謹的態度和科學的精神。我們教育的對象是模仿性極強的未成年人,我們不經意的一句話、一個操作細節,他們就記住了。提高教師的專業素養,細節很重要!
本堂是基于“雞蛋中的化學”的復習課,即以雞蛋在酸性溶液中的變化和皮蛋制作知識為主題的酸堿性質的復習課,題材新穎、線索清晰,值得反思、品味。真正完美的課堂幾乎是不存在的,卻是我們追求的。不斷追求,不斷超越,一輩子做化學教師,一輩子學做化學教師。endprint

