基于網絡藥理學探討桃仁-紅花藥對活血化瘀的分子機制*
楊凱麟,曾柳庭,葛安琪,葛金文,龍治勇,鮑婷婷,蔣 燕
(1.湖南中醫藥大學醫學院 長沙 410208;2.湖南中醫藥大學中西醫結合學院 長沙 410208;3湖南中醫藥大學第一附屬醫院 長沙 410007;4.北京中醫藥大學 北京 100029;5.南華大學附屬第一醫院 衡陽 421001)
藥對是連接單味中藥與方劑的橋梁,兼具方劑的基本主治功效,其以四氣五味、升降沉浮、歸經、有毒無毒等中藥藥性理論和相輔相成或相反相成的組合原理為配伍基礎[1]。桃仁-紅花是活血化瘀的經典藥對。桃仁(Persicae Semen)具有活血化瘀,潤腸通便,止咳平喘之功效,用于經閉痛經,癥瘕痞塊,肺癰腸癰,跌撲損傷,腸燥便秘,咳嗽氣喘[2],而紅花(Carthami Flos)能活血通經,散瘀止痛,用于經閉,痛經,惡露不行,癥瘕痞塊,胸痹心痛,瘀滯腹痛,胸脅刺痛,跌撲損傷,瘡瘍腫痛[2]。二藥均系活血化瘀之品,前者質重沉降,偏入里走下,破瘀力強;后者質輕升浮,善走外達上,行血力勝。二者相互配對,破瘀而利血行,行血而利瘀去,從而使活血化瘀之力倍增[3]。因此本研究基于網絡藥理學的方法,對桃仁-紅花藥對活血化瘀的分子機制進行分析,為傳統藥對作用機制研究提供新的范式。
1 材料與方法
1.1 目標化合物的選取
本研究中的中草藥植物中所含化合物從TCM@Taiwan 數 據 庫[4]、Traditional Chinese Medicine Systems Pharmacology(TCMSP)數據庫[5]和TCMID數據庫 (https://academic.oup.com/nar/article/41/D1/D1089/1057998)中選取。由于中藥發揮藥效作用的物質基礎是化學成分的組合,中藥中雖有眾多成分,但只有被吸收入血的成分才能產生作用。因此,基于絕大多數藥物在動物體內起作用必須被吸收進入血液這一原理,采用了口服生物利用度(OB)和Caco-2滲透性兩個參數來對中草藥化合物進行篩選[5-7]。此外,由于中草藥成分眾多,而且結構具有多樣性,因此需要利用類藥性(DL)來對成分進行進一步篩選[7]。以上三種參數可在TCMSP數據庫中查詢,根據該數據庫所提供的標準,OB>30%,Caco-2>-0.4和DL>0.18可被認為是符合規定的、可口服吸收的、具有藥理活性的化合物,將會成為目標化合物[5-7]。
1.2 已知靶點的搜集
將目標化合物的名稱輸入SciFinder,選擇Categorize選項并選擇Genetics&protein chemistry最后選擇其下級菜單Proteins&peptides獲得蛋白質和肽類的已知靶點信息。
1.3 潛在作用靶點反向預測
從SciFinder、TCMSP數據庫上獲得目標化合物的化學結構的模式圖,利用ChemBioDraw 14.0按照模式圖進行構建,將其以mol2格式導入PharmMapper進行靶點預測,該數據庫采用“反向藥效團匹配方法”,以活性小分子為探針通過對Targetbank、Drugbank、Binding DB和PDTD四大數據庫[8,9]進行快速檢索而獲得化合物的靶點信息,并根據匹配結果的相似度進行打分和排序。由于檢索到的藥物靶點存在命名不規范等問題,本實驗用UniProtKB搜索功能,通過輸入蛋白名稱并限定“物種(Specie)”為“智人(Homo Sapiens)”,將檢索得到的所有蛋白校正為其官方名稱(Official Symbol),經上述數據庫檢索和轉化操作,獲取與活性成分相關的蛋白信息[10]。
1.4 靶點通路注釋分析
將靶點導入DAVID數據庫以進行信號通路富集,即進行KEGG通路注釋。桃仁-紅花藥對對應的靶蛋白(基因)直接映射到通路上,藥物靶點富集的通路被認為是藥物調控的通路[10,11]。
1.5 相關網絡構建
根據上述桃仁-紅花藥對的已知靶點搜集、潛在靶點預測以及富集分析的結果,采用網絡的可視化軟件Cytoscape 3.4.0構建活性成分-預測靶點網絡模型和成分-靶點-通路網絡模型[12]。網絡中的節點(node)表示活性成分、靶點或者作用通路等。節點之間則以邊(edge)相連,根據所構建網絡的不同,邊代表的意義也不同[11,12]。
2 結果
2.1 桃仁-紅花藥對的成分
通過TCM@Taiwan數據庫和TCMSP數據庫檢索,結合文獻[13],的本次研究共獲取了17個成分,其中紅花4個,桃仁13個。紅花的成分為紅花素(醌式紅花苷)(Carthamone)、6-羥基山奈酚(6-Hydroxykaempferol)、山奈酚(Kaempferol)、槲皮素(Quercetin);而桃仁的成分為α1-谷甾醇(Sitosterol α1)、2,3-二脫氫GA70(2,3-didehydro GA70)、GA119、GA120、GA121-isolactone、GA122、GA122-isolactone、赤 霉 素 A44(Gibberellin A44)、赤霉素7(Gibberellin 7)、楊屬靈(Populoside)、常春藤苷元(Hederagenin)、β-谷甾醇(β-sitosterol)、菜油甾醇(Campesterol)。
2.2 桃仁-紅花藥對成分-靶點網絡
通過對桃仁-紅花藥對成分的已知靶點收集并對靶點的主要作用進行分類,主要可分為:改善血流動力學、抗凝血、抗炎、調控細胞凋亡和細胞增殖四個方面發揮活血化瘀的作用。通過以下的對比和分析,單個的細胞因子可能作用介導于多個生物過程,并組成和連同其他多條信號通路作用于一個生物過程,從表1中可以初步看出桃仁-紅花的已知靶點可以歸納為四個與活血化瘀作用相關的模塊(表1,圖1)。
根據分析,發現在改善血流動力學方面,LDL、LDLR、COX1、HDL、AngII、VEGFR2等受到較多成分的作用,這些生物活性物質介導了血管的動脈粥樣硬化、血管重構;在凝血-抗凝血作用中,F2、Hemagglutinins受到較多的成分調控;在炎癥-抗炎作用中CRP、CYP450、IL1β、IL6、TNFα、ICAM1、IL1、NF-κB受到較多成分的調節,其中IL1、IL6、TNFα、NF-κB是炎癥通路中的核心因子;在腫瘤細胞的增殖和死亡作用方面,P53、BCL2、CASP3、BAX、TGFβ等受到較多成分的作用,其中經典的抑癌基因P53和相關抗凋亡因子。每一個單一成分均可調控較多靶點,不同成分所側重調控的分子靶點群有所不同,例如山奈酚和槲皮素均善于調控改善血流動力學、抗凝血、抗炎和腫瘤細胞的增殖和死亡相關的分子靶點群,而常春藤苷元擅長于調節抗炎和腫瘤細胞的增殖和死亡相關的分子靶點群等。這些側面反映出了中藥多成分-多靶點的特性(圖1,表1)。
2.3 桃仁-紅花藥對成分-靶點網絡點圖
由于桃仁-紅花藥對中有些化學成分的現代藥理研究較少或已有藥理作用的化學成分現代藥理研究報道的不深入,有必要利用預測的潛在靶點來進行進一步的網絡關聯性分析與研究。

圖1 桃仁-紅花藥對的中藥-成分-靶點網絡
通過PharmMapper的預測,17個成分一共反饋回317個靶點。結合所有數據構建“成分-靶點網絡”。該網絡由334個節點和2227條邊構成。在這一圖中,靠近圓心的節點相對靠外的節點受到更多藥對成分的作用。這表明,大部分靶點可以通過多種化合物來調節,而非僅僅通過一個來調節。例如CA2、CDK2、PDPK1、GSTP1、BACE1等可由所有17個成分來調節,除了最外圍的Nodes,內部的Nodes均可由一個以上的有效成分來調節(圖2)。
2.4 桃仁-紅花藥對通路富集
通過KEGG分析探討桃仁-紅花藥化瘀作用預測靶點的通路分布,返回128條信號通路。根據所獲取的靶點、信號通路等數據,構建“單味藥-潛在靶點-信號通路”網絡,將單味藥、多個靶點及多條通路間的關聯關系(圖3,表2)。
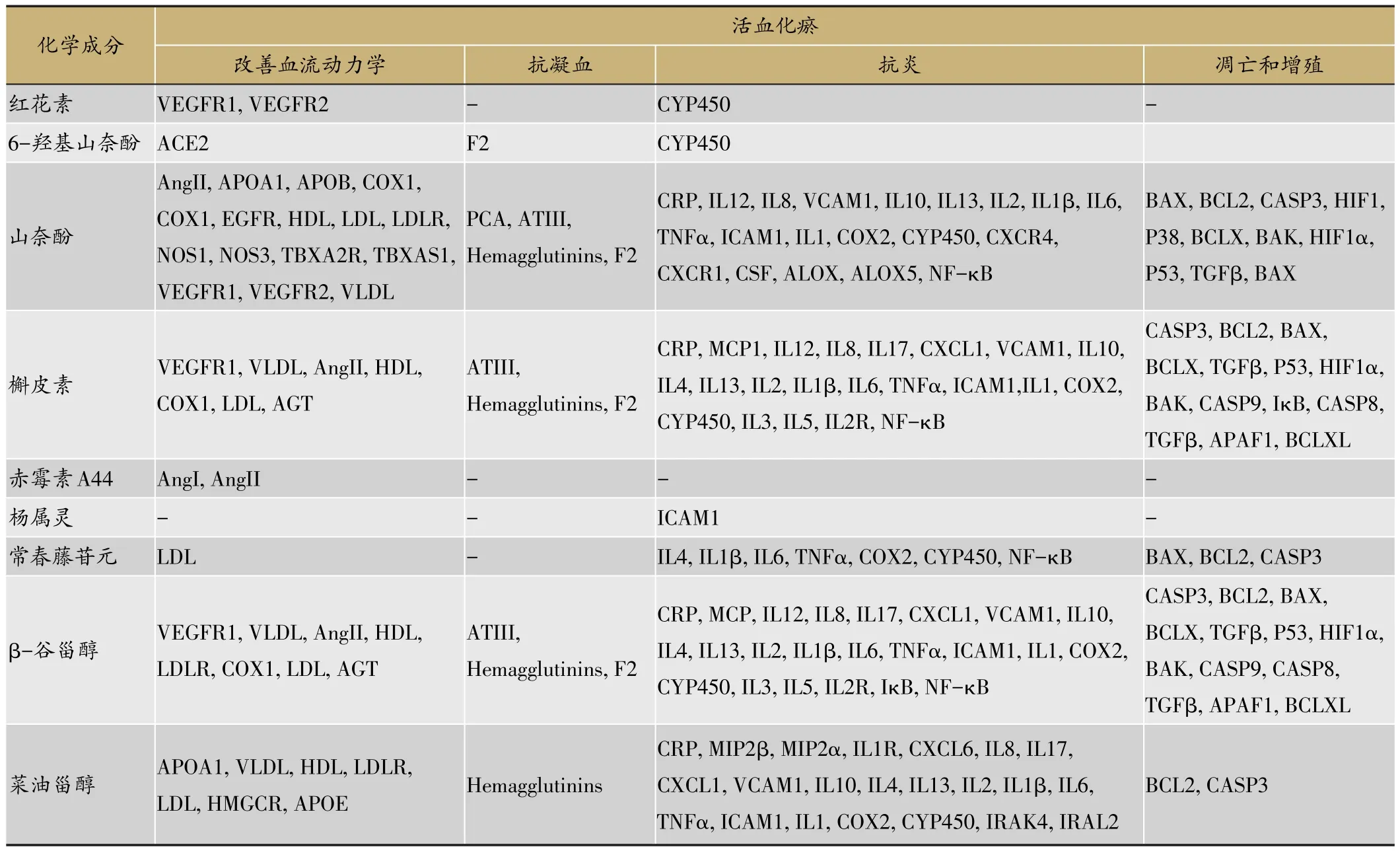
表1 桃仁-紅花活血化瘀的已知靶點歸納
總之,在這些相關的通路中,涉及了血瘀證中對應的大部分疾病的主要病理機制,如心血管疾病中的代謝紊亂,炎癥介質的介導發展,免疫系統的調節以及腫瘤的發生發展機制。
3 討論
瘀血是傳統醫學多種疾病共同存在的病因及病理產物,而炎癥反應是現代醫學多系統疾病研究中的熱點環節。兩者相互之間在病理、病機及治療方面存在密切的關系。基礎和臨床研究的結果顯示血瘀與炎癥具有很大的相關性,主要集中在血瘀證與炎癥、血流動力學、微循環、血小板功能、凝血與抗凝血、纖溶與抗纖溶等方面,結合現代藥理的研究顯示造成瘀血的病理因素主要集中在三個方面:①體外生物性因素和理化因素所致的病理狀態;②體內臟器衰竭引起炎癥因子的瀑布性級聯反應;③體外因素所致的炎癥因子與體內臟器炎癥因子的相互促進[14]。血瘀的現代病理研究表明各種致病因子所造成的全身或局部組織器官缺血、缺氧、血瘀、血液循環障礙以及血液流變性和粘滯性異常等一系列的病理變化[15]。因此,根據目前對血瘀的現代病理研究,炎癥反應在血瘀證的發生發展中發揮了重要的作用。目前血瘀證的病理基礎研究支持血瘀證伴有全血黏度、血漿黏度、紅細胞壓積升高,血小板聚集性增強,電泳時間延長,體外血栓形成的干濕量及長度增加,纖維蛋白原增高等病理變化[14]。另有部分研究認為,瘀血證除與上述病理異常有關外,還與血管內皮細胞的損傷、動脈粥樣硬化、局部缺血缺氧、血栓形成、微循環障,炎癥病理過程、免疫功能障礙、結締組織代謝異常、細胞增殖性病變、內臟病理腫大、內臟及肢體血流量分布異常等病理變化過程有關[16]。近年來,大量實驗研究發現以上許多不同疾病過程中都與血瘀證有著密切的關系,而炎癥反應從一個側面揭示了血瘀證的實質,大量血瘀證與炎癥相關性研究顯示,血瘀證在活性因子、臨床治療及動物模型方面與炎癥存在著密不可分的關系,炎癥、免疫反應與腫瘤等病理機制在一定程度上介導了血瘀證的發生發展,并且相互作用促進[15,17-19]。此外,在目前大量的臨床及實驗研究中發現,在腫瘤的發病過程中,與血液循環有關的許多因素的檢測指標的異常,如外周循環障礙,血液流變學的改變以及抗凝血機制的減弱等都與腫瘤血瘀證的形成密切相關[20,21]。

圖2 桃仁-紅花藥對成分-靶點網絡

表2 信號通路一覽表
綜上,血瘀證主要與血流動力學異常、凝血異常、炎癥反應和細胞惡性增殖性有關。在桃仁-紅花藥對的中藥-成分-靶點網絡(圖1)中,根據已知靶點的作用特征歸納總結為四個分子靶點群,稱為“模塊”:改善血流動力學、抗凝血、抗炎、腫瘤細胞的增殖和死亡相關方面,這與傳統血瘀證四個特征:血流動力學異常、凝血異常、炎癥反應和腫瘤形成相對應。通過網絡分析發現在改善血流動力學方面,LDL(6個邊)、LDLR(5個邊)、COX1(5個邊)、HDL(5個邊)、AngII(4個邊)、VEGFR2(3個邊)等受到較多成分的作用;在凝血-抗凝血作用中,F2(6個邊)、Hemagglutinins(4個邊)受到較多的成分調控;在炎癥-抗炎作用中CYP450(10個邊)、IL1β(6個邊)、IL6(6個邊)、TNFα(6個邊)、ICAM1(6個邊)、IL1(6個邊)、CRP(5個邊)、NF-κB(5個邊)受到較多成分的調節;在腫瘤細胞的增殖和死亡作用方面,BCL2(6個邊)、CASP3(6個邊)、BAX(5個邊)、TGFβ(4個邊)等受到較多成分的作用。這些模塊中的靶點可能分別是桃仁-紅花藥對改善血流動力學、凝血-抗凝血、炎癥-抗炎、影響腫瘤細胞的增殖和死亡的核心靶點。我們的研究顯示山奈酚、槲皮素、菜油甾醇、β-谷甾醇均能改善血流動力學、抗凝血、抗炎和腫瘤,同時常春藤苷元則主要集中于抗炎和腫瘤細胞的增殖和死亡,赤霉素A44主要集中于改善血流動力學.同時,現代實驗研究顯示,桃仁-紅花藥對的提取物能通過影響血流動力學、血漿凝血和血小板聚集來促進血液循環[22];山奈酚能抑制血栓形成和血小板活化[23,24],槲皮素能抑制凝血酶的活性,抑制纖維蛋白凝塊的形成和血液凝固[25,26],間接驗證了桃仁-紅花藥對活血化瘀是通過其化學成分的改善血流動力學、凝血-抗凝血等作用實現的。而其它成分由于收集到的靶點較少,不足以觀察其主要作用。基于現有的桃仁-紅花藥對多組分藥理學研究從側面也反應了桃仁-紅花藥對多組分-多靶點干預血瘀證各個信號途徑與生物過程的特性。
化學成分-潛在靶點網絡的結果分析顯示,大部分靶點多通過多組分化合物來調節,而非僅僅通過一個來調節,其中CDK2、MMP3、F2、METAP2、HSP90AA1(熱休克蛋白90-α)、ALB(血清白蛋白)、MMP12(巨噬細胞彈性蛋白酶)、F10(凝血因子10)等靶點是頻率最高的靶點之一(可被幾乎所有化學成分所調控),其中ALB等靶點主要與改善血液流變性有關,F2、F10等靶點與抗凝血有關,MMP3等靶點與抗炎有關,CDK2、METAP2、HSP90AA1、MMP12等靶點與腫瘤形成相關的基因有關。與此同時,各組分化合物中紅花素(154個邊)、槲皮素(145個邊)、山奈酚(143個邊)、楊屬靈(141個邊)成分連接的潛在靶點最多,可能是桃仁-紅花藥對活血化瘀的主要成分或者核心成分。從化合物分子結構預測其原理作用和活性靶點的角度也反應了該藥對多組分-多靶點協同干預血瘀證不同途徑以及上下游不同信使和基因靶點的特性。這些預測靶點集合與已知靶點集合有存在重疊之處;例如預測靶點集合和已知靶點集合均含有F2、ANG、IL2等,這些重疊的部分間接體現了預測靶點網絡的可靠性。部分出現在已知靶點網絡中的靶點未出現在預測靶點網絡中(例如CYP450、ATIII、COX2等),這可能是由于有效成分通過預測靶點間接作用于這些未出現在預測網絡中的已知靶點。此外,預測靶點存在一些未出現于驗證靶點網絡中的靶點,這些新的靶點可能是未來實驗驗證的方向。
從單味藥-潛在靶點-信號通路網絡的構建來看,我們可以發現桃仁-紅花藥對構建的通路主要與腫瘤相關通路、代謝相關的通路、免疫相關的通路主要集、內分泌相關的通路、細胞過程相關通路、信號轉導相關通路等有關。其中,與內分泌相關通路,如胰島素信號通路[27]、雌激素信號通路[28-30]、催乳素信號通路[31-33]等通路,間接影響了血流動力學。與信號轉導相關的通路則幾乎涵蓋了大部分的在腫瘤、炎癥與免疫方面的通路,如PI3K-Akt信號通路[34-38]、VEGF信號通路[38,39]、MAPK信號通路[40-42]、mTOR信號通路[38]、NF-kappa B信號通路[35]等。
綜上所述,槲皮素、山奈酚、菜油甾醇、β-谷甾醇可能是桃仁-紅花藥對干預血瘀證的主要活性成分,結合預測靶點數據來看,紅花素、楊屬靈等可能是潛在的活性成分。從靶點的層面看CDK2、MMP3、F2、METAP2、HSP90AA1、ALB、MMP12、F10等一系列由多化學成分調控的靶點可能是其對干預血瘀證中的主要活性靶點。從預測的有效成分靶點來看未來桃仁-紅花藥對在血瘀證方面的研究主要可以從TNF信號通路、TRP通道的炎癥介質調節、FcγR-介導的吞噬作用、NOD樣受體信號通路、PI3K-Akt信號通路、VEGF信號通路、MAPK信號通路、HIF-1信號傳導途徑、cAMP信號通路、AMPK信號通路、mTOR信號通路、NF-kappa B信號通路、cGMP-PKG信號通路等相關信號通路入手,進行新的進一步的探索探索。
中藥作為中醫藥臨床實踐過程中的最重要一環成為中藥發展和走向臨床應用的最終瓶頸,盡管其功效已為幾千年的歷史和現代臨床療效所肯定但其現代化如今已經成為中醫藥發展的共識,其現代化過程之路從最初的中藥系統整理文獻,揭示蘊含在文獻中的辯證、用藥的一般規律,到現在運用定量科學模型的數字化方法和生物生化分子學的發展以及生物計算機學的工具對中藥重新進行傳統理論的闡述。本文通過對桃仁-紅花藥對化學成分的獲取與篩選,利用數據庫收集其已知靶點并用分子反向對接的方法獲取其潛在靶點,利用DAVID進行KEGG通路注釋分析,最后利用cytoscape 3.4.0軟件對已知靶點網絡、化學成分-潛在靶點網絡和單味藥-潛在靶點-信號通路網絡進行分析,從而對該藥對的化學成分、作用靶點、作用通路三個層次,整體、組織、細胞、分子四個藥理水平所獲得的多有效成分、多指標數據進一步挖掘與分析桃仁-紅花的物質基礎和作用機理。
4 結論
通過網絡藥理學方法,發現了已知靶點所分成的四個模塊與血瘀證的四個特性相對應,發現潛在作用靶點及其信號通路的富集所獲得的128個信號通路涉及血瘀證的多種病理生理過程,體現了桃仁-紅花藥對干預血瘀證的分子機制。這體現了桃仁-紅花藥在“藥物-疾病-細胞-分子”方面對血瘀證的影響,不僅為桃仁-紅花藥對的活血化瘀作用提供了理論依據及為未來的相關研究提供了基礎,同時對桃仁-紅花藥對等傳統藥對作用機制研究提供新的范式。

