兩種術前活檢方案用于早期胃癌患者行內鏡黏膜下剝離術的臨床價值比較
王巖,孫成剛,黃麗
(1.山東省濟南市濟鋼醫院 消化內科,山東 濟南 250101;2.山東省立醫院 消化內科,山東 濟南 250021;3.山東省淄博市中心醫院 消化內科,山東 淄博 255000)
目前胃癌早發現早診斷主要依賴內鏡活檢術病理檢查,其中以多點多塊活檢和靶向活檢術最為常用[1]。以往對于胃癌患者篩查常規行白光成像內鏡引導下多點多塊活檢術,并被廣泛用于胃癌癌前病變內鏡隨訪[2]。近年來放大窄帶成像內鏡技術逐漸發展成熟,可清晰顯示胃黏膜腺管和異型血管形態,避免傳統取材盲目性和有效提高診斷準確度,亦減輕患者檢查痛苦,提高治療依從性[3];但對于該活檢方案能否較多點多塊活檢方案增加患者臨床收益,國內尚缺乏相關比較研究證實。本文以本院2013年6月-2016年6月行ESD術治療早期胃癌患者共60例作為研究對象,分別在術前行多次多點活檢術和靶向活檢術,探討術前活檢方案差異對行內鏡黏膜下剝離術(endoscopic submucosal dissection,ESD)早期胃癌患者取材量及手術用時的影響。現報道如下:
1 資料與方法
1.1 一般資料
研究對象選取本院2013年6月-2016年6月行內鏡黏膜下剝離術(endoscopic submucosal dissection,ESD)治療早期胃癌患者共60例,根據活檢方案不同分為A組和B組,每組各30例。A組患者中男17例,女13例,年齡35~82歲,平均(57.40±6.82)歲,病變直徑3.0~6.5 cm,平均(4.72±1.63)cm;B組患者中男19例,女11例,年齡34~84歲,平均(57.61±6.87)歲,病變直徑3.2~6.7cm,平均(4.81±1.66)cm。兩組患者一般資料比較差異無統計學意義(P>0.05),具有可比性。見表1。
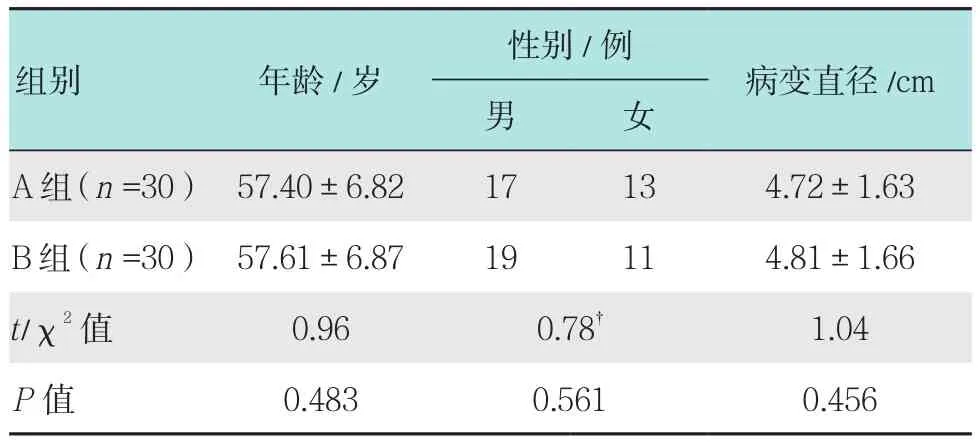
表1 兩組基本資料比較Table 1 Comparison of general information between the two groups
1.1.1 納入標準①符合日本《胃癌治療指南》(2014年)ESD手術指證[4];②年齡18~70歲;③病理活檢確診胃竇部早期胃癌或上皮內瘤變;④方案經醫院倫理委員會批準,且患者及家屬簽署知情同意書。
1.1.2 排除標準①病變累及黏膜下層;②感染性或家族性腸道疾病;③合并淋巴結或遠處轉移;④既往ESD手術史;⑤長期服用非甾體抗炎藥;⑥其他系統惡性腫瘤;⑦凝血功能障礙;⑧精神系統疾病;⑨心腦肝腎功能障礙;⑩臨床資料不全。
1.2 方法
1.2.1 取材方法A組患者術前行多次多點活檢術,白光成像內鏡引導下進行取材;常規鉗取2塊,潰瘍者圍繞周邊4個方位各取1塊,息肉于頂部及基底部多點取材;可疑癌變者則取材≥5塊;B組患者術前行靶向活檢術,放大窄帶成像內鏡引導下進行取材,即在白光成像內鏡發現病變位置后改為放大窄帶成像模式,靠近病灶處行黏膜淺層、黏膜下血管、胃黏膜腺管微結構識別,于異型微血管處定向取材。
1.2.2 ESD手術方法于距病灶邊緣5 mm處行氬離子凝固術(argon plasma coagulation,APC)凝固標記,標記點外5 mm處進行多點注射,順序為遠側、兩側及近側;注射液成分為5 ml生理鹽水+10%甘油+5%果糖+亞甲藍+去甲腎上腺素,保證病灶充分抬舉;采用Dual刀沿標記外緣切開黏膜層及黏膜下層,在病變部位全周切開后自基底部逐步剝離黏膜下層;電凝止血,對于可疑穿孔處采用金屬鈦夾夾閉,觀察創面無出血后退鏡。
1.3 觀察指標
①記錄患者活檢次數和取材總標本數,計算平均值;②記錄患者術后病理活檢診斷結果,包括早期胃癌、高級別瘤變及低級別瘤變例數,計算符合率;符合例數=早期胃癌例數+高級別瘤變例數;③記錄患者確定切除范圍時間、標記時間、黏膜下注射時間、黏膜剝離時間、止血時間、創面處理時間及切除標本處理時間,計算平均值。
1.4 統計學方法
采用SPSS 20.0軟件進行數據分析,其中計量資料以均數±標準差(±s)表示,采用t檢驗;計數資料以百分比(%)表示,采用χ2檢驗;檢驗水準為α=0.05。
2 結果
2.1 兩組患者活檢次數和取材總標本數比較
B組患者活檢次數和取材總標本數均明顯少于A組,差異有統計學意義(P<0.05)。見表2。
2.2 兩組患者術后病理符合率比較
B組患者術后病理符合率明顯高于A組,差異有統計學意義(P<0.05)。見表3。
2.3 兩組患者ESD手術過程用時比較
兩組患者確定切除范圍時間、標記時間、黏膜下注射時間及切除標本處理時間比較差異無統計學意義(P>0.05);B組患者黏膜剝離時間、止血時間及創面處理時間均明顯短于A組,差異有統計學意義(P<0.05)。見表4。
表2 兩組患者活檢次數和取材總標本數比較 (±s)Table 2 Comparison of number of biopsy and the total number of specimens between the two groups (±s)
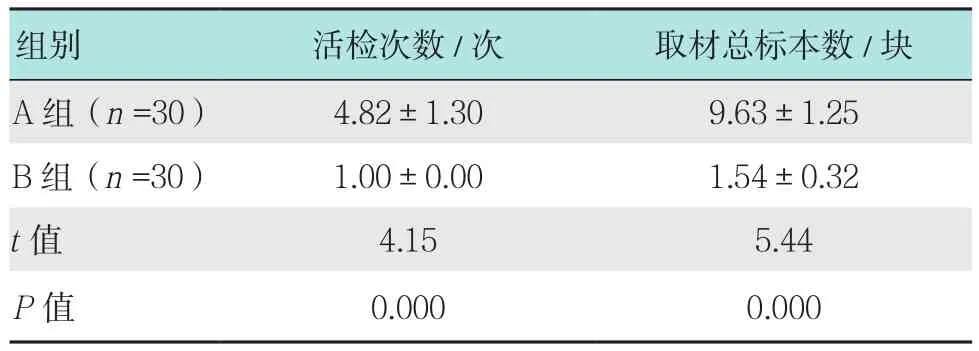
表2 兩組患者活檢次數和取材總標本數比較 (±s)Table 2 Comparison of number of biopsy and the total number of specimens between the two groups (±s)
組別 活檢次數/次 取材總標本數/塊A組(n =30) 4.82±1.30 9.63±1.25 B 組(n =30) 1.00±0.00 1.54±0.32 t值 4.15 5.44 P值 0.000 0.000
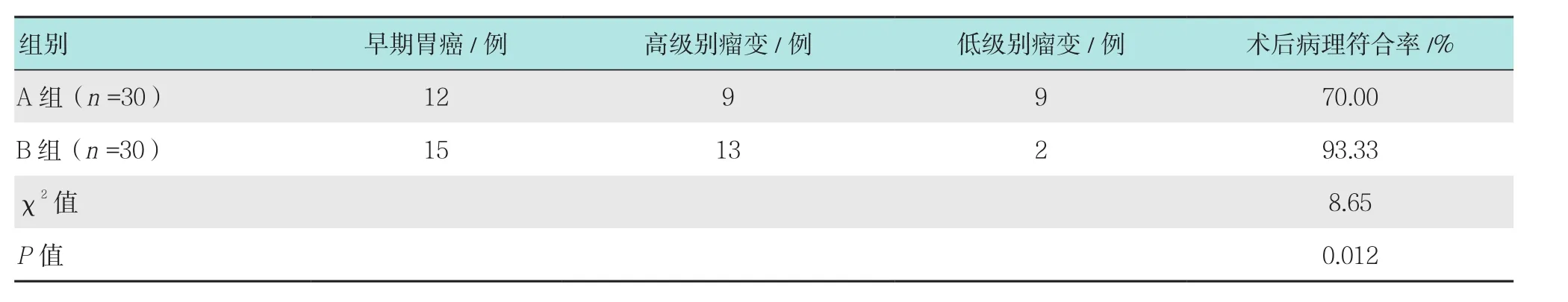
表3 兩組患者術后病理符合率比較Table 3 Comparison of postoperative pathological coincidence rate between the two groups
表4 兩組患者ESD手術過程用時比較 (min,±s)Table 4 Comparison of ESD operation time between the two group (min,±s)
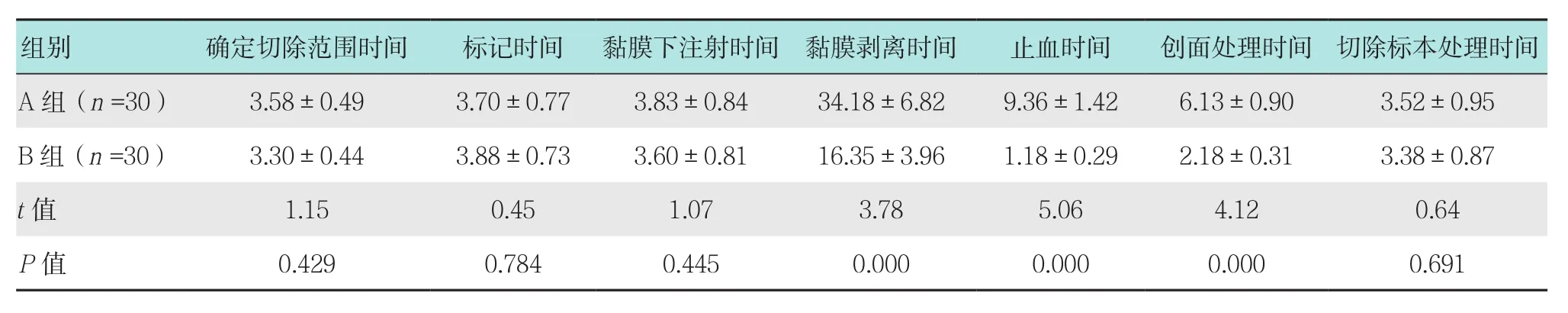
表4 兩組患者ESD手術過程用時比較 (min,±s)Table 4 Comparison of ESD operation time between the two group (min,±s)
?
3 討論
白光成像內鏡引導下多塊多次活檢術鉗取胃黏膜要求具有代表性,在保證病變部位準確基礎上,應盡量鉗取達黏膜肌層大塊組織,以對胃黏膜全層進行清晰觀察[5];但已有研究顯示,盡管該活檢術采用專用鉗取材多量黏膜組織,但病理診斷特異度較低,造成較多假陰性病例出現[6]。國外多中心回顧性報道證實,行多點多塊活檢術患者術后病理結果較術前病變程度加重比例可達33.80%,而減輕比例亦接近10.00%[7];同時白光內鏡診斷過程因鉗取組織過多,在多次內鏡隨訪活檢后,可出現胃黏膜纖維粘連甚至瘢痕,對診療效果產生不利影響,嚴重者甚至出現穿孔,威脅生命安全[8]。
放大窄帶成像是一種新型內鏡成像技術,相較于白光成像,其能夠觀察胃黏膜腺管和間質內微血管增生程度,鑒別分化型與非分化型惡性腫瘤[9];其中分化型腫瘤細胞自腺管內形成、間質內可見微血管增生,且密度較正常黏膜微血管增加,部分可見不規則微血管;而未分化型腫瘤細胞則自黏膜肌層內形成,無正常微血管和黏膜結構,部分可見皺襞樣改變[10]。由放大窄帶成像內鏡引導下進行活檢取材能夠更精確判斷病變位置和范圍,提高良惡性凹陷性病變檢出效能,在較小取材量下即可進行準確診斷[11];同時借助放大窄帶成像技術在觀察胃黏膜細微結構方面的優勢,臨床醫師還能夠將病變特點和病理活檢結果進行評價,更早確定治療方案;此外該方案對于病變位置和范圍更為精確定位亦有助于避免過度治療發生[12-13]。
本次研究結果中,B組患者活檢次數和取材總標本數均明顯少于A組(P<0.05);B組患者術后病理符合率明顯高于A組(P<0.05),證實術前靶向活檢術應用有助于提高早期胃癌患者診斷準確性,減少有創取材所致胃黏膜損傷,而活檢次數減少亦能夠降低檢查費用,提高患者依從性;同時兩組患者確定切除范圍時間、標記時間、黏膜下注射時間及切除標本處理時間比較差異無統計學意義(P>0.05);B組患者黏膜剝離時間、止血時間及創面處理時間均明顯短于A組(P<0.05),則表明行ESD術早期胃癌患者術前采用靶向活檢術進行取材在縮短手術操作用時和提高檢查效率方面具有優勢;常規多塊多次活檢術取材組織深度可達黏膜肌層,故ESD術中黏膜下注射后難以充分隆起;而潰瘍瘢痕、取材部位瘢痕粘連及黏膜下豐富血管叢導致手術操作需更加謹慎,且需要花費大量時間進行瘢痕剝離松解,進一步增加手術難度和風險[14];而放大窄帶成像引導下靶向活檢術取材后,患者病變黏膜下注射抬舉征(+)比例可達96.0%以上,且液體墊持續時間易顯著延長,這對于降低操作難度、減少術中出血及縮短手術用時具有重要意義[15]。
對于ESD術后切緣病理診斷陽性問題,筆者認為主要與病變位置染色和白光成像下邊界判斷不足有關,推薦采用聯合色素染色或改為放大窄帶成像模式下判斷;本次研究中,A組患者中1例術后病理活檢提示為進展期胃癌,并行胃癌根治切除+淋巴結清掃術治療;這可能與該患者之前多次活檢造成胃黏膜粘連、無法均勻剝離基底部有關;同時提醒臨床醫師對于基底切緣陽性者再行ESD術治療時因黏膜下層往往形成大量瘢痕和纖維化組織,注射后難以有效抬舉,故剝離深度應以緊貼并暴露固有肌層為宜,范圍包括殘留病變組織和外擴1.0 cm正常黏膜組織[16]。
綜上所述,術前靶向活檢術用于行ESD手術患者可有效減少取材創傷,提高活檢準確率,并有助于縮短手術用時,價值優于多次多點活檢術。
[1]ABE S, ODA I, NAKAJIMA T, et al.A case of local recurrence and distant metastasis following curative endoscopic submucosal dissection of early gastric cancer[J].Gastric Cancer, 2015, 18(1):188-192.
[2]ONO H, YAO K, FUJISHIRO M, et al.Guidelines for endoscopic submucosal dissection and endoscopic mucosal resection for early gastric cancer[J].Dig Endosc, 2016, 28(1): 3-15.
[3]REN G, CAI R, ZHANG W J, et al.Prediction of risk factors for lymph node metastasis in early gastric cancer[J].World J Gastroenterol, 2013, 19(20): 3096-3107.
[4]胡祥.2014年第4版日本《胃癌治療指南》更新要旨[J].中國實用外科雜志, 2015, 35(1): 16-19.
[4]HU X.The fourth edition Japan’s 《Guidebook for the treatment of gastric cancer》update keystone in 2014[J].Chin J Prac Surg,2015, 35(1): 16-19.Chinese
[5]KANG S H, LEE K, LEE H W.Delayed perforation occurring after endoscopic submucosal dissection for early gastric cancer[J].Clin Endosc, 2015, 48(3): 251-255.
[6]TANABE S, ISHIDO K, HIGUCHI K, et al.Long-term outcomes of endoscopic submucosal dissection for early gastric cancer: a retrospective comparison with conventional endoscopic resection in a single center[J].Gastric Cancer, 2014, 17(1): 130-136.
[7]KIM Y D, LEE J, CHO J Y, et al.Efficacy and safety of 0.4 percent sodium hyaluronate for endoscopic submucosal dissection of gastric neoplasms[J].World J Gastroenterol, 2013, 19(20): 3069-3076.
[8]SCHMIDT A, FUCHS KH, CACA K, et al.The endoscopic treatment of iatrogenic gastrointestinal perforation[J].Deuts Arztebl Int, 2016, 113(8): 121-128.
[9]TAHARA T, YAMAZAKI J, TAHARA S, et al.Magnifying narrowband imaging of gastric mucosal morphology predicts the H.pylori-related epigenetic fi eld defect[J].Sci Rep, 2017, 7(1): 3090-3097.
[10]VESPER I, SCHMIEGEL W, BRECHMANN T.Equal detection rate of cervical heterotopic gastric mucosa in standard white light, high de fi nition and narrow band imaging endoscopy[J].Z Gastroenterol, 2015, 53(11): 1247-1254.
[11]NOZAKI I, HATO S, KOBATAKE T, et al.Incidence of metachronous gastric cancer in the remnant stomach after synchronous multiple cancer surgery[J].Gastric Cancer, 2014,17(1): 61-66.
[12]NODA H, OGASAWARA N, IZAWA S, et al.Risk factors for bleeding evaluated using the Forrest classification in Japanese patients after endoscopic submucosal dissection for early gastric neoplasm[J].Eur Gastroenterol Hepatol, 2015, 27(9): 1022-1029.
[13]DINC S, CAYDERE M, AKGUL G, et al.Methylene Blue inhibits the in fl ammatory process of the acetic acid-induced colitis in the rat colonic mucosa[J].Int Surg, 2015, 5(10): 57-65.
[14]BANG C S, BAIK G H, SHIN I S, et al.Endoscopic submucosal dissection for early gastric cancer with undifferentiated-type histology: a meta-analysis[J].World J Gastroenterol, 2015,21(19): 6032-6043.
[15]MILHOMEM L M, CARDOSO D M, MOTA E D, et al.Frequency and predictive factors related to lymphatic metastasis in early gastric cancer[J].Arq Bras Cir Dig, 2012, 25(4): 235-239.
[16]AKINTOYE E, OBAITAN I, MUTHUSAMY A, et al.Endoscopic submucosal dissection of gastric tumors: A systematic review and meta-analysis[J].World J Gastrointest Endosc, 2016, 8(15): 517-532.

