三個稀土-主族三金屬Lnバ-Srギ-Kガ配合物的結構與發光性質
王宏勝 李公春 吳艷超 張萬強 陳新華
0 引 言
近年來,設計合成含有稀土元素的配位聚合物成為配位化學研究領域的一大熱點。特別是具有良好發光性質的稀土配合物,由于在熒光探針、激光材料、光致發光及電致發光等領域的潛在應用價值而受到極大關注[1-5]。含稀土的異金屬配合物特別是3d~4f配位聚合物,由于其新穎的結構和良好的性質成為相關研究的重要內容之一[6-10]。而稀土與主族元素的配位聚合物的合成與性質研究相對比較少,一些研究者合成并研究了稀土-堿金屬和稀土-堿土金屬的雙金屬配位聚合物的性質[11-13]。根據文獻報道,少數含稀土元素的三金屬配位聚合物被合成并報道,其中配體均為多元羧酸或氰根離子[14-18],而這些配合物中只有Euバ-Srギ-Kガ和Tbバ-Srギ)-Kガ與2,4,6-吡啶三甲酸的配合物具有較好的光致發光性質[18]。研究表明,有機配體在配位聚合物的結構和性質方面有著重要的作用,對于含稀土異金屬配位聚合物的性質,非稀土元素可能對稀土元素有不同的影響,比如在發光配合物中,部分元素可能會對稀土離子的熒光產生敏化作用,也可能產生淬滅作用。在此基礎上,我們使用2,4,6-吡啶三甲酸(H3ptc)為有機配體,在水熱條件下和稀土釤、釓或鏑的三價離子的高氯酸鹽水溶液、碳酸鉀及碳酸鍶反應,成功合成出3個含有3種金屬離子的三維配位聚合物[LnSrK(ptc)2(H2O)]n(Ln=Sm(1)、Gd(2)、Dy(3)), 其 中Smバ-Srギ-Kガ和Dyバ-Srギ-Kガ的配合物在紫外光照射下發射Smバ和Dyバ的特征熒光,Gdバ-Srギ-Kガ配合物在紫外光照射下發射由配體向金屬離子發生核移躍遷產生的綠色熒光。
1 實驗部分
1.1 試劑與儀器
Sm(ClO4)3、Dy(ClO4)3和 Gd(ClO4)3水溶液分別用Sm2O3、Dy2O3和 Gd2O3與高氯酸反應制得,3種稀土氧化物純度均大于99.95%;2,4,6-吡啶三甲酸用氧化法合成;實驗中所使用的其它化學試劑均為分析純。
C、H、N元素含量用VarioELⅢ元素分析儀 (德國Elementar公司)測定;紅外光譜用FTIR-650型紅外光譜儀(天津港東科技發展股份有限公司)(4 000~400 cm-1,KBr壓片法)測定;熔點儀用 WRS-1B數字熔點儀(上海申光儀器儀表有限公司)測定;熒光激發光譜、發射光譜和絕對量子產率用FLS980穩態瞬態熒光光譜儀(英國Edinburgh儀器公司)測定。
1.2 配體的合成
2,4,6-吡啶三甲酸 (H3ptc)用高錳酸鉀氧化2,4,6-三甲基吡啶制備[19],對產品進行了元素分析和紅外光譜測試,結果如下。元素分析按C8H5NO6計算值(%):C,45.51;H,2.39;N,6.63。 測定值(%):C,45.74;H,2.08;N,6.49。 IR(KBr pellet,cm-1):3 544,3 421,1 719,1 591s,1555,1431,1402,1 280,1 197,1088,926,722,758,706,685,626,563。
1.3 [LnSr K(ptc)2(H 2O)]n(Ln=Sm(1)、Dy(2)、Gd(3))的合成
配合物[SmSrK(ptc)2(H2O)]n(1)的單晶體用0.040 mol·L-1的 Sm(ClO4)3水 溶 液 (0.2 mmol,5.00 mL),SrCO3(0.2 mmol,0.029 6 g),K2CO3(0.1 mmol,0.013 8 g)和 H3ptc(0.4 mmol,0.084 4 g)在 180 ℃水熱條件下反應制備,產率55%(基于Sm3+計算)。配位聚合物[DySrK(ptc)2(H2O)]n(2)和[GdSrK(ptc)2(H2O)]n(3)的單晶體制備方法與配合物1的制備方法相同,只是將使用的Sm(ClO4)3水溶液改變為Dy(ClO4)3或Gd(ClO4)3水溶液,產率63%和58%。對配合物1(C16H6N2O13SmSrK)的元素分析理論值(%):C,27.02;H,0.85;N,3.94。 測 定 值 (%):C,26.65;H,1.24;N,4.15。 配合物 2(C16H6N2O13DySrK)的理論值(%):C,26.56;H,0.84;N,3.87。測定值(%):C,26.21;H,1.13;N,3.91。 配合物 3(C16H6N2O13GdSrK)的理論值(%):C,26.76;H,0.84;N,3.90;測定值(%):C,26.42;H,1.08;N,3.77。熔點測試表明,3個配合物的熔點均大于300℃。
1.4 配合物的結構表征
選取適合結構分析的3種配合物的單晶體,配合物1在Bruker SMART1000 CCD X射線單晶衍射儀上,采用經石墨單色器單色化的Mo Kα射線(λ=0.071 073 nm),以φ-ω掃描方式在一定的θ范圍內收集衍射數據,利用SADABS程序對數據進行吸收校正,晶體結構用 SHELXS-97[20]和 SHELXL-97[21]軟件進行解析和精修。配合物2和3在Bruker APEX-ⅡCCD型X射線單晶衍射儀上收集數據,同樣用SHELXS-97和SHELXL-97軟件進行解析和精修。3個配合物的主要晶體學數據和結構精修參數列于表1。3種金屬離子和氧原子或氮原子的鍵長值列于表2中。
CCDC:1566176,1;1566177,2;1566178,3。
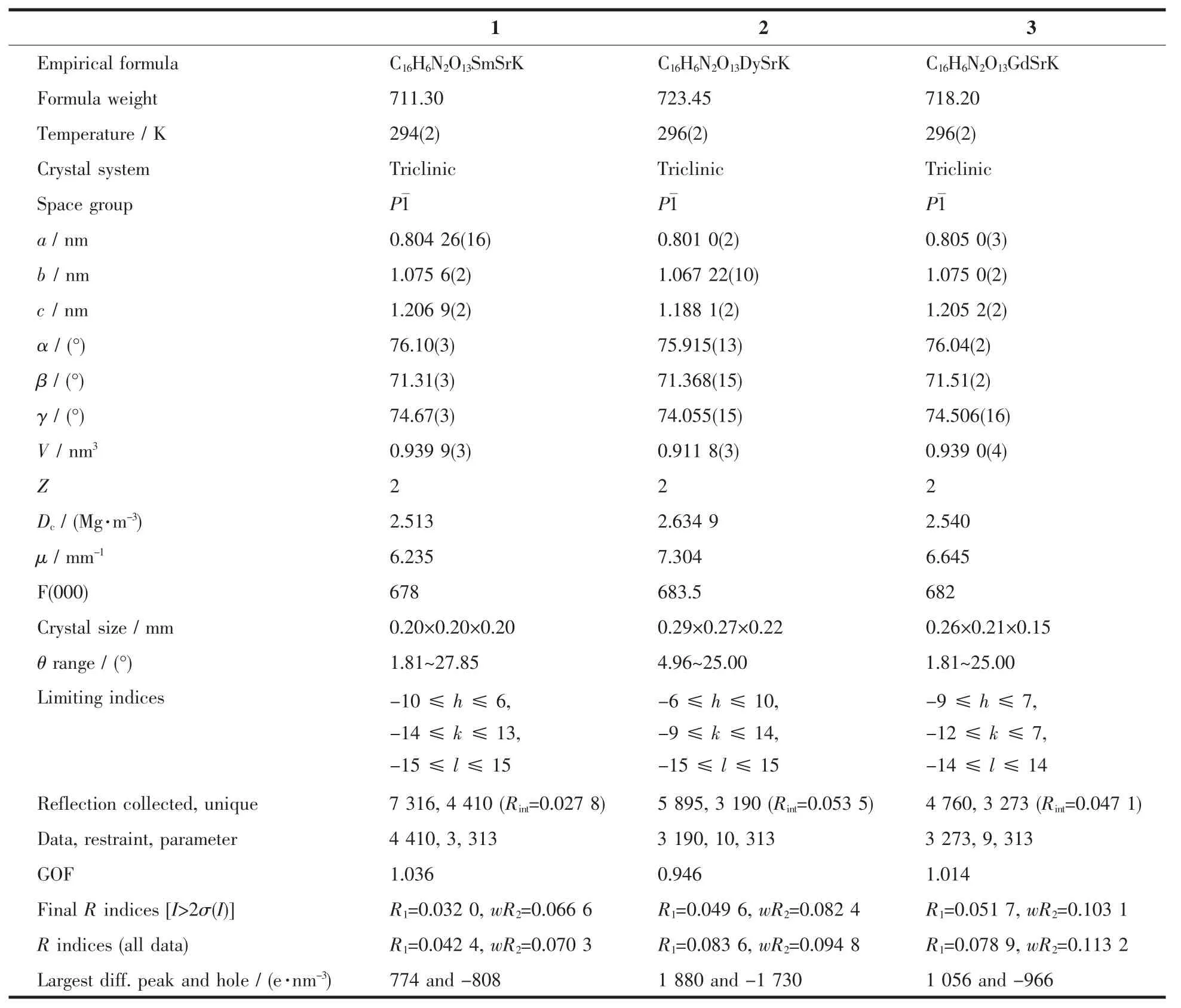
表1 三個配合物的晶體和結構精修數據Table 1 Crystal data and structure refinement for the three complexes
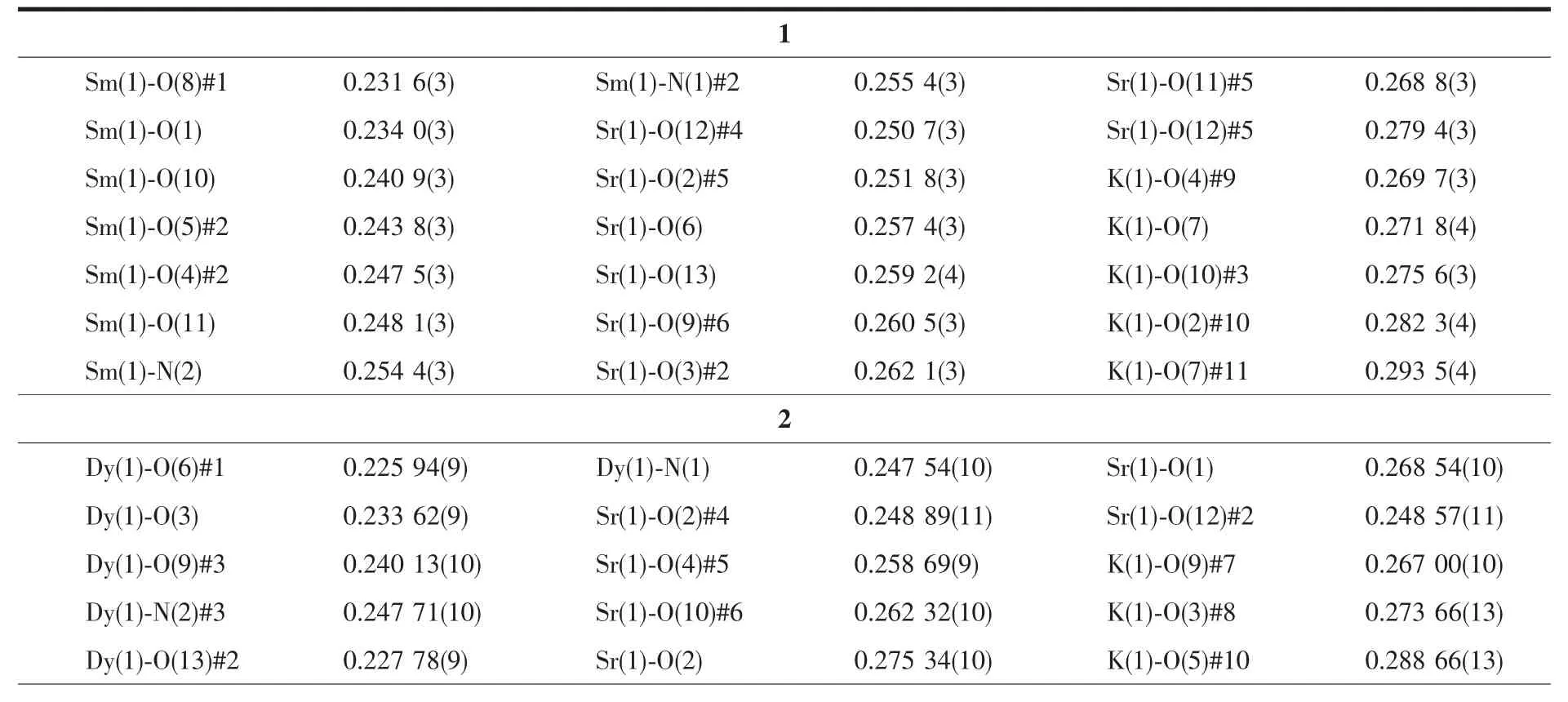
表2 三個配合物的部分鍵長(nm)Table 2 Selected bond lengths(nm)for three complexes
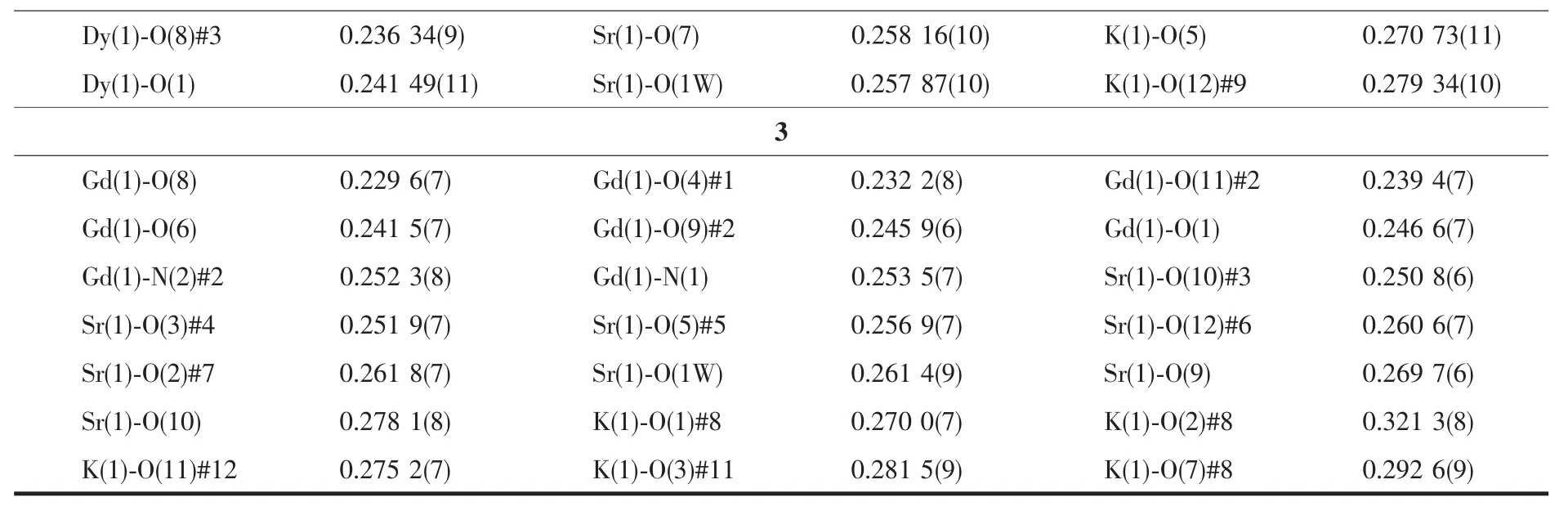
續表2
2 結果與討論
2.1 配合物的結構
三個配合物為同構化合物,以配合物2為例對三者的結構進行說明。如圖1所示,稀土Dy3+離子在配合物中為八配位,配位原子為6個氧原子和2個氮原子,配位氧原子均為配體羧基氧原子,每個Dy3+離子與2個ptc陰離子配體的2-、6-位羧基上一個氧原子及吡啶環上氮原子螯合配位;Sr2+離子也是八配位,配位原子都是氧原子,其中1個氧原子來自配位水分子,其余7個來自配體羧基氧原子。Dy3+離子和Sr2+離子都處于由8個配位原子形成的變形四方反棱柱多面體中。K+離子與5個羧基氧原子配位,形成了變形四方錐結構。通過配體與金屬離子的連接,形成了三維網狀結構的配位聚合物,如圖2所示。配體ptc在配合物中有2種配位方式,一種方式中同時連接了2個Dy3+、3個Sr2+及2個K+共7個金屬離子,另一方式中連接了2個Dy3+、3個Sr2+及3個K+共8個金屬離子(圖3)。
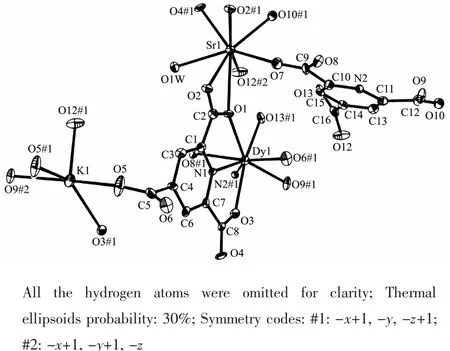
圖1 配合物2中Dyバ、Srギ、Kガ離子的配位環境Fig.1 ORTEPrepresentation of 2 showing the coordination environment of Dyバ,Srギand Kガ
2.2 配合物的紅外光譜
三個配合物的紅外譜圖如圖4所示。從圖中可以看出,羧酸配體在1 700 cm-1附近的-COOH的紅外吸收峰消失,在1 625 cm-1處出現了-COO-的反對稱伸縮振動吸收峰,而在1 370 cm-1附近出現了-COO-的對稱伸縮振動吸收峰。表明H3ptc形成陰離子配體與金屬離子配位,而且3個配合物的紅外圖非常相近,表明ptc陰離子以相同的配位方式與稀土離子形成配合物,這也與結構解析的結果一致。
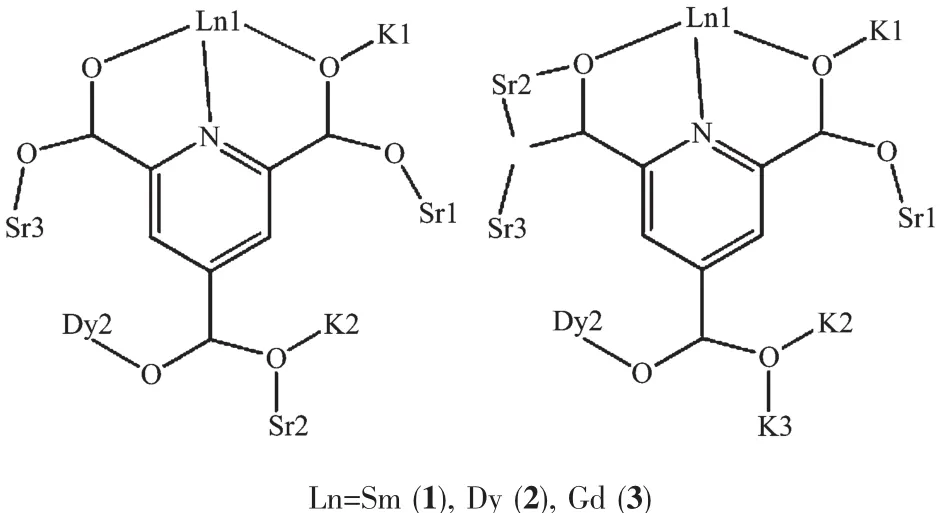
圖3 配體ptc在配合物中的2種配位方式Fig.3 Coordination modes of ptc ligands in the complexes
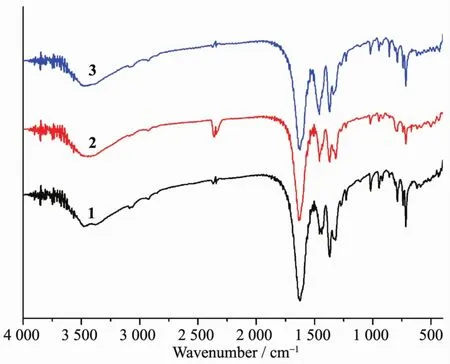
圖4 三個配合物的紅外光譜Fig.4 IR spectra of three complexes
2.3 配合物的光致發光性質
在室溫下,測試了3個配合物的激發和發射光譜及光致發光的量子產率。
2.3.1 配合物1的熒光光譜及量子產率
以600 nm作為發射波長,激發狹縫為2.0 nm,發射狹縫為0.5 nm,測試了配合物1粉末樣品的激發光譜,如圖5a所示。從圖中可以看出其最佳激發波長在306 nm。用306 nm作激發波長,激發狹縫為2.0 nm,發射狹縫為0.5 nm,測試了配合物的發射光譜, 如圖 5b所示,在 562、601、645、709和 788 nm等5處出現了熒光發射峰,分別對應于Smバ4G5/2→6HJ(J=5/2、7/2、9/2、11/2、13/2)的躍遷。 通常釤配合物的發射光譜中可以看到在可見區4G5/2→6HJ(J=5/2、7/2、9/2)躍遷的3個發射峰,在此配合物中,還可以看到在可見區的4G5/2→6H11/2躍遷峰及在近紅外區的4G5/2→6H13/2的躍遷發射峰。在室溫下測試該配合物粉末樣品光致發光的絕對量子產率為0.5%。
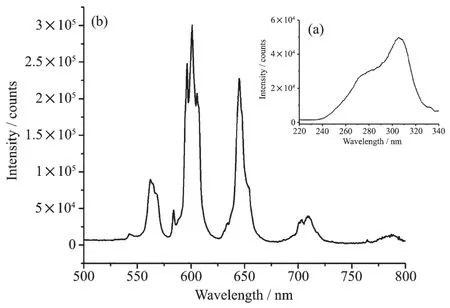
圖5 配合物1的激發光譜(a)和發射光譜(b)Fig.5 Excitation(a)and emission(b)spectra of complex 1
2.3.2 配合物2的熒光光譜及量子產率
以575 nm作為發射波長,激發狹縫為1.0 nm,發射狹縫為0.5 nm測試了配合物2粉末樣品的激發光譜,如圖6a所示。從圖中可以看出其最佳激發波長在304 nm。用304 nm作激發波長,激發狹縫為1.0 nm,發射狹縫為0.5 nm,測試了配合物的發射光譜,如圖6b所示,在486、575、663和753 nm等4處出現了熒光發射峰,分別對應于Dyバ的4F5/2→6HJ(J=15/2、13/2、11/2、9/2)躍遷。 通常鏑配合物的發射光譜中可以看到4F5/2→6HJ(J=15/2、13/2)躍遷的2個發射峰,在此配合物中,也可以看到4F5/2→6H11/2和4F5/2→6H9/2躍遷產生的2個較弱發射峰。在室溫下測試該配合物粉末樣品光致發光的絕對量子產率為2.0%。
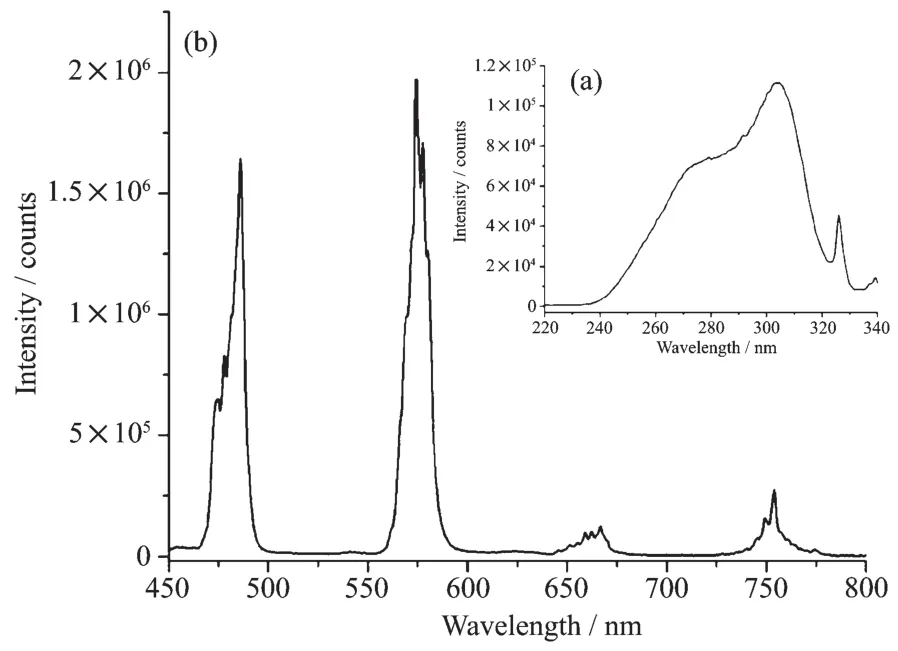
圖6 配合物2的激發光譜(a)和發射光譜(b)Fig.6 Excitation(a)and emission(b)spectra of complex 2
2.3.3 配合物3的熒光光譜及量子產率
以515 nm作為發射波長,激發狹縫和發射狹縫分別為1和0.5 nm測試了配合物3的粉末樣品的激發光譜,如圖7所示。從圖中可以看出其最佳激發波長在352 nm。用352 nm作激發波長,激發狹縫為1.0 nm,發射狹縫為0.5 nm,測試了配合物的發射光譜,如圖8所示,在450~650 nm范圍內出現了一個寬的熒光發射峰,其中最強峰在515 nm處,該發射峰是由于配體向金屬離子發生荷移躍遷產生。從該配合物的最佳激發波長和發射波長可以看出,該配合物對紫外光的Stokes位移比較大,達到了~170 nm。另外,該配合物發射光譜范圍比較寬,在450~650 nm均有發射,覆蓋了可見光的大部分區域。在室溫下測試該配合物粉末樣品光致發光的絕對量子產率為12.8%。另外從該配合物的色度坐標圖(圖9)可以看出,該配合物在波長為350 nm左右的紫外光激發下,發射綠色熒光。
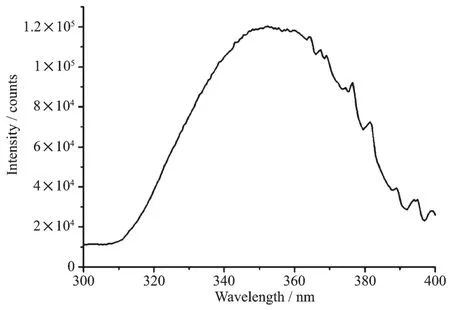
圖7 配合物3的激發光譜Fig.7 Excitation spectrum of complex 3
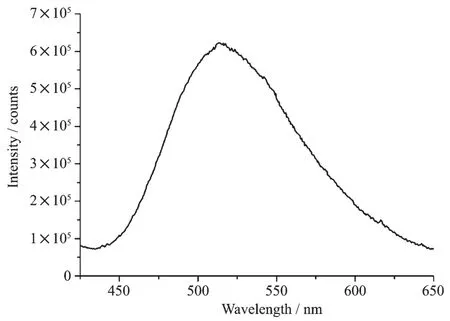
圖8 配合物3的發射光譜Fig.8 Emission spectrum of complex 3
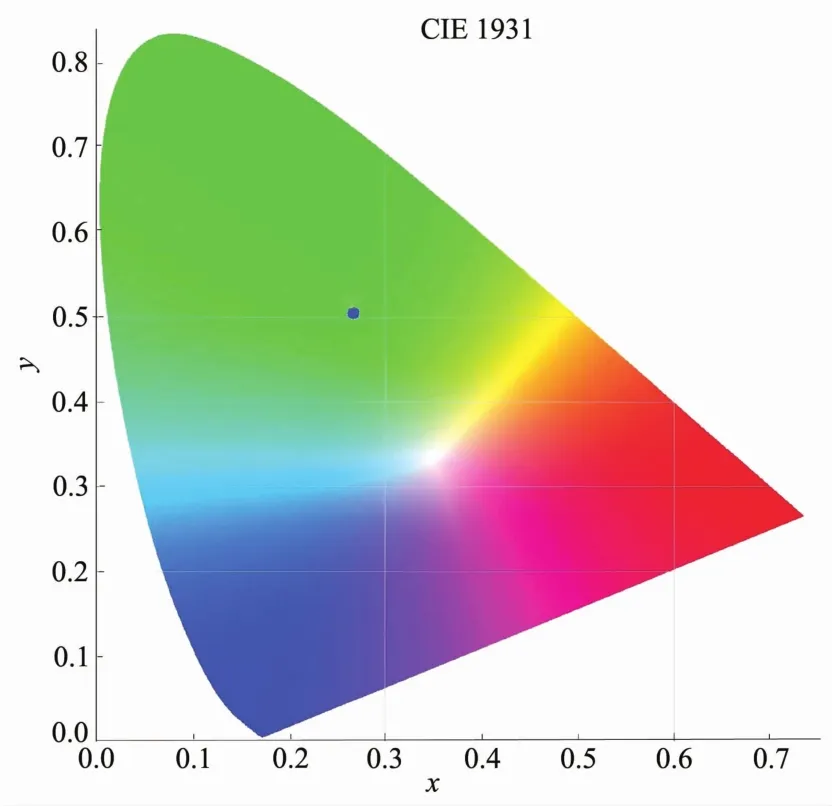
圖9 配合物3的色度坐標Fig.9 Chromaticity diagram of complex 3
對比3個配合物的熒光激發光譜,可以看出1、2兩個配合物的最佳激發波長很相近,而且激發峰形也相似,它們和3的激發峰峰形及最佳激發波長相差很大,由此可知,盡管3種配合物的配體和結構相同,且均為三金屬配合物,但是在光致發光的機理上有著本質的區別,配合物1和2是按照稀土配合物發光機理中的“天線效應”產生熒光,即在紫外光激發時,配體被首先激發,然后經過系間竄越到配體三重激發態,再將能量傳遞給稀土離子使其被激發產生熒光,而配合物3是由于發生配體向金屬離子的核移躍遷產生熒光。
3 結 論
采用水熱合成法制備了3個含稀土和主族元素的三金屬配位聚合物,測定了3種化合物的晶體結構。對配合物進行了元素分析、紅外光譜、熔點等表征。對3種配合物的光致發光性質進行了測試,結果表明,Smバ-Srギ-Kガ和 Dyバ-Srギ-Kガ與配體 ptc生成的配合物在紫外光照射下發射Smバ和Dyバ的特征熒光;Gdバ-Srギ-Kガ配合物在紫外光照射下發綠色熒光,該發光是由于配體向金屬離子發生核移躍遷產生。這為利用稀土釓元素合成發光配合物提供了新的思路。
參考文獻:
[1]Liu Q Y,Wang W F,Wang Y L,et al.Inorg.Chem.,2012,51:2381-2392
[2]QUAN Jing-Miao(全靜苗),LEI Hai-Rui(雷海瑞),LIU Feng-Yi(劉峰毅),et al.Scientia Sinica Chimica(中國科學:化學),2017,47(7):876-881
[3]Cui Y J,Xu H,Yue Y F,et al.J.Am.Chem.Soc.,2012,134:3979-3982
[4]ZHAO Peng-Fei(趙朋飛),SHE Jiang-Bo(佘江波),LI Dong-Dong(李冬冬),et al.Acta Photonica Sinica(光子學報),2014,43(2):0216001
[5]ZHOULiang(周亮),DENGRui-Ping(鄧瑞平),ZHANGHong-Jie(張洪杰).Chinese J.Inorg.Chem.(無機化學學報),2014,30(1):113-120
[6]Zhao B,Cheng P,Dai Y,et al.Angew.Chem.Int.Ed.,2003,42:934-936
[7]Zhao B,Cheng P,Chen X Y,et al.J.Am.Chem.Soc.,2004,126:3012-3013
[8]Zhao X Q,Zhao B,Ma Y,et al.Inorg.Chem.,2007,46:5832-5834
[9]Gao H L,Zhao B,Zhao X,et al.Inorg.Chem.,2008,47:11057-11061
[10]Cui Y J,Yue Y F,Qian G D,et al.Chem.Rev.,2012,112:1126-1162
[11]Huang Y G,Jiang FL,Hong M C.Coord.Chem.Rev.,2009,253:2814-2834
[12]Mishra S,Ledoux G,Jeanneau E,et al.Dalton Trans.,2012,41:1490-1502
[13]Zhao X Q,Zuo Y,Gao D L,et al.Cryst.Growth Des.,2009,9:3948-3957
[14]Gao H L,Yi L,Ding B,et al.Inorg.Chem.,2006,45:481-483
[15]Kou H Z,Zhou B C,Gao S,et al.Angew.Chem.Int.Ed.,2003,42:3288-3291
[16]Kou H Z,Zhou B C,Wang R J.Inorg.Chem.,2003,42:7658-7665
[17]Zhang W Z,Lv T Y,Wei D Z,et al.Inorg.Chem.Commun.,2011,14:1245-1249
[18]Wang H S,Xia J,Zhai B,et al.J.Coord.Chem.,2014,67:3234-3242
[19]Syper L,Kloc K,Mlochowski J.Tetrahedron,1980,36:123-129
[20]Sheldrick G M.SHELXS 97,Program for the Solution of Crystal Structures,University of G?ttingen,Germany,1997.
[21]Sheldrick G M.SHELXL 97,Program for the Refinement of Crystal Structures,University of G?ttingen,Germany,1997.

