草魚日糧中添加飼料桑粉對其生長性能及非特異性免疫的影響
劉家星,陳霞,曹英偉,李良玉,張小麗,魏文燕,楊馬,唐洪,陳健
(成都市農林科學院水產研究所,四川 成都 611130)
隨著糧食耕地的減少以及農作勞動力的減少,在滿足人類消費的情況下,剩余用來加工成畜禽、水生動物飼料的糧食越來越短缺,人和動物的糧食競爭矛盾日益突出。因此,為有效緩解飼料原料緊缺的情況,開發和尋找新的、優質的飼料原料迫在眉睫[1]。
飼料桑[2]是我國科研人員通過努力培育出的具有超大潛力的桑樹新品系,具有較強的抗逆性,很強的耐貧瘠和耐嚴寒能力[3]。生長非常迅速,在條件良好的情況下當年桑苗可達2.5~3.0 m,單株鮮重達1.5 kg,干重0.3 kg。鮮葉重每1hm2每年可達40 t,干物質10 t,可飼用部分干物質合計13 t[2]。飼料桑的營養價值豐富,含有大量的粗蛋白,其平均含氮量高達3.574%[3],有研究表明飼料桑葉的總干物質中蛋白質的比例為23%,氨基酸種類有18種之多。此外,飼料桑中還含有大量的纖維素、維生素和礦物質元素等營養成分,其營養組成和比例適宜動物的生長發育需要[4-6]。
目前飼料桑已在肉雞、蛋雞、豬、肉牛、奶牛、肉羊等動物上得到了廣泛應用。一方面可以提高動物的生長性能,動物產品的質量[7-8];另一方面還可以提高動物的免疫能力,改善動物的生長狀態[7]。桑葉屬天然植物,含有黃酮類、多糖類、植物甾醇等多種天然活性物質,能提高動物免疫力,有利于動物抗病和保健。英國最新研究成果表明桑葉中還含有一種叫做“達菲”的物質,對防治H5N1型禽流感有效[9]。關于飼料桑在淡水魚養殖的應用中,目前僅見2002年中國工程院三峽工程評估項目組將飼料桑應用于庫區養殖魚中,并取得了不錯的效果[10]。但是,目前相關資料的研究相對較少,對于其是否能夠提高魚體的免疫能力相關的研究更是匱乏。因此,本試驗選取傳統養殖品種草魚(Ctenopharyngodon idellus)作為試驗對象,探究在草魚日糧中添加飼料桑對草魚生長性能及非特異性免疫的影響,以期能夠為飼料桑在淡水魚飼料中的開發應用奠定基礎。
1 材料和方法
1.1 材料及試劑
草魚魚種 1 200 尾,體質量(55±4.5)g;飼料桑原粉200 kg,飼料桑鮮葉若干;規格為直徑115 cm、高45 cm的玻鋼纖維盆24個;血清總補體測試試劑盒、總超氧化物岐化酶測試試劑盒購自南京建成生物工程研究所;其他試劑購自上海生工生物科技有限公司。所有試劑均為分析純。
1.2 試驗方法
1.2.1 試驗動物分組 試驗用玻鋼纖維盆使用0.1%高錳酸鉀盛滿浸泡2 h,再反復刷洗消毒后方可用于試驗。試驗用草魚購買回來后以3%的食鹽水浸泡魚體15 min,然后在池塘暫養15 d后進行試驗分組。試驗分為6個組,其中添加飼料桑原粉共5組,添加比例為0%、3%、6%、9%、12%,另單獨1組投喂飼料桑鮮葉。隨機挑選規格一致、體質健壯、體質量50 g左右的草魚,每組飼養草魚100尾,設兩個平行。
1.2.2 飼料制備及投喂 試驗用飼料配方營養需求參照草魚NRC 1993,各組添加飼料桑分別為0%(A0)、3%(A1)、6%(A2)、9%(A3)、12%(A4),配制成5種等氮(蛋白水平為 30.8%~30.9%)、等能(能值為13 kJ/g)的試驗飼料。各原料經粉碎機粉碎過60目篩,按配方準確稱重,逐級放大混合,加水拌勻,用飼料顆粒機制成粒徑1.0 mm顆粒飼料,于40~45℃下烘干至水分含量10%以下,保存在-20℃冰箱中備用。飼料桑鮮葉組(A5),在飼喂基礎日糧基礎上每日采摘飼料桑鮮葉投喂。試驗從草魚分組后第 5 天開始投喂,每日早、中、晚(8:00,12:00,18:00)投喂3次,嚴格按投喂“四定”(定時、定點、定量、定質)原則進行。日投餌率5%左右,以20 min內食完為宜。玻鋼纖維盆施以微流水,水體交換量0.1 m3/h。每日巡視做好防逃防敵害工作,對投喂、吃食等情況做好記錄。試驗飼料組成及營養成分見表1和表2。
1.2.3 生長性能測定 分別于試驗開始前記錄各組的初始體質量,飼養90 d后記錄末體質量,記錄投飼量。每次稱重前魚體饑餓24 h。每組隨機選取4尾魚,測定其體長、體質量,用于計算魚體增重率、飼料系數、特定生長率。計算公式如下:
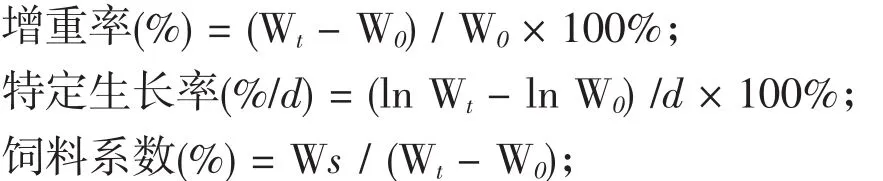
式中,Wt表示試驗末均重,W0表示試驗初均重,Ws表示試驗均投飼量,d表示試驗天數。
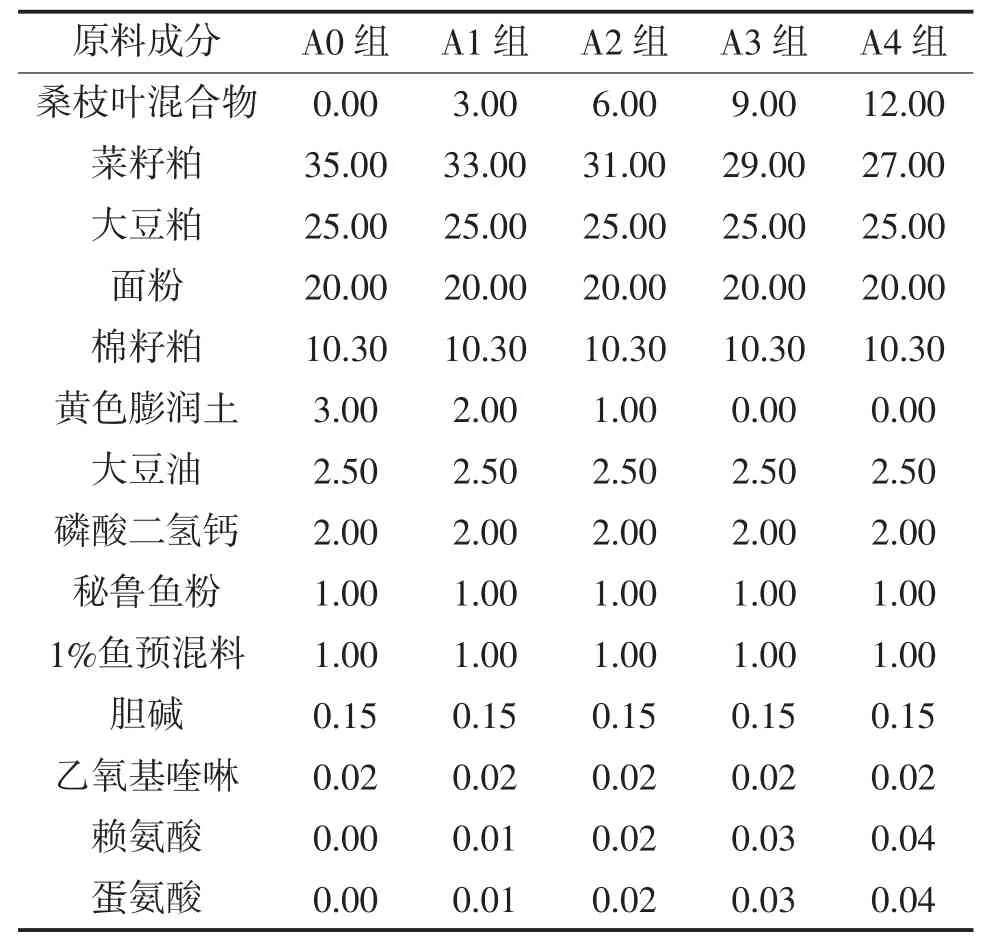
表1試驗分組飼料配方表 %
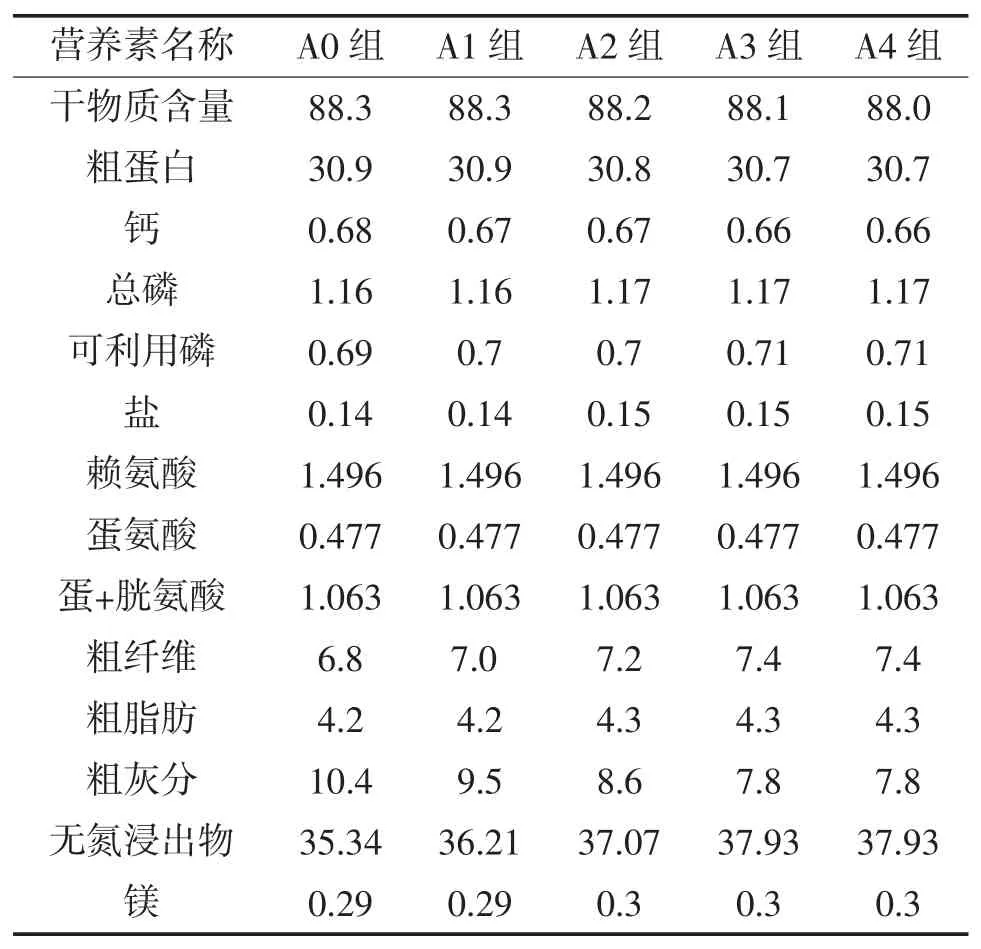
表2草魚飼料營養成分表 %
1.2.4 非特異性免疫指標測定 分別于投喂飼料0、15、30、45、60、75、90 d 對草魚非特異性免疫指標進行測定(總超氧化物歧化酶、溶菌酶活性、血清殺菌活性,血清補體C3),每組隨機挑選4尾魚進行尾靜脈采血,收集血液置于1.5 mL的PE管中,于4℃靜置12 h,4 000 r/min離心l0 min,取上層血清置于-80°C超低溫冰箱保存備用。總超氧化物歧化酶、血清補體C3測定方法參照南京建成生物工程研究所試劑盒說明書進行;溶菌酶測定參照Swain P和Behera T等[11-12]文獻方法進行;血清殺菌活性參照Sun Y等[13]文獻方法進行。
1.2.5 數據統計 使用 SPSS 22.0軟件進行統計學分析,對各組試驗重復數據作方差同質性檢測后進行單因素方差分析,使用LSD法進行事后多重比較,結果以“平均數±標準差(mean±SD)”表示。分別在0.01和0.05差異水平上進行檢驗,當P<0.01表示差異極具統計學意義,P<0.05表示差異具統計學意義,P>0.05表示差異不具統計學意義。
2 試驗結果
2.1 草魚生長性能
按照1.2.3種所述方法,用添加不同含量的飼料桑粉飼料投喂90 d,各組草魚在試驗結束后計算各組的增重率、特定生長率、飼料系數,結果見表3。從表中可知,添加量為6%的試驗組(A2)和飼喂鮮葉組(A5)的草魚其增重率極顯著(P<0.01)高于其他試驗組和對照組;添加量為3%的試驗組(A1)特定生長率極顯著(P<0.01)低于其他試驗組而與對照組(A0)相比差異不具統計學意義(P>0.05);添加量為6%的試驗組飼料系數極顯著(P<0.01)低于對照組,且顯著(P<0.05)低于添加量為3%、12%(A4)的試驗組。

表3草魚生長性能測定
2.2 非特異性免疫指標
2.2.1 總超氧化物歧化酶活力 投喂不同時間后采集各組草魚血清后測得血清總超氧化物歧化酶活力變化情況見圖1。在投喂后15 d開始,添加不同比例飼料桑的試驗組以及投喂飼料桑鮮葉組(A5)血清的總超氧化物歧化酶活性呈上升趨勢,除與對照組(A0)差異極具統計學意義(P<0.01)外,其余各組差異不顯著(P>0.05);第30天,添加量為12%的試驗組(A4)與其他組具統計學意義(P<0.05);到第60天,各個試驗組均達到較高的酶活力,添加量為9%的試驗組(A3)酶活力水平為整個試驗周期最大值,達到(23.14±0.03)U/mL;隨后各試驗組酶活力開始下降,但在試驗周期內與對照組仍保持極具統計學意義(P<0.01)。對照組在整個試驗周期中酶活力水平維持在16.4~16.9 U/mL范圍內。添加量為9%的試驗組在整個試驗周期中,能夠持續較好地刺激草魚魚體的抗氧化系統。
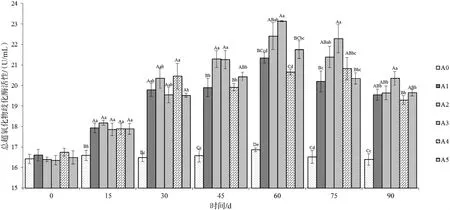
圖1血清總超氧化物歧化酶(T-SOD)活力變化
2.2.2 血清溶菌酶活性 參考Swain P等[11-12]方法,在測定試驗開始前使用凍干的雞蛋白溶菌酶做標準曲線(酶活分別為 50 U、40 U、30 U、20 U、10 U、5 U、1 U)。溶菌水平以U/mL表示,0.001 U/mL表示一個單位U。投喂不同時間后采集各組草魚血清后測得血清溶菌酶變化情況見圖2。在投喂后15 d開始,添加不同比例飼料桑的試驗組以及投喂飼料桑鮮葉組(A5)血清溶菌酶活性呈上升趨勢,除與對照組(A0)和添加量為9%(A3)的試驗組差異極具統計學意義(P<0.01)外,其余各組差異不具統計學意義(P>0.05);第30天,各試驗組血清溶菌酶活性均有上升,差異顯著性與15 d相似;第45天,添加量為3%的試驗組酶活性上升較為緩慢,與其他試驗組差異極具統計學意義(P<0.01);到第60天,添加量為3%和9%的試驗組酶活性與其他試驗組差異極具統計學意義(P<0.01);到第75天添加量為6%的試驗組血清溶菌酶活性達到整個試驗周期最大值,為(637±10)U/mL;隨后各試驗組血清溶菌酶活性開始下降,但添加量為3%以及鮮葉組下降的速率相對緩慢,與其他試驗組仍差異極顯著(P<0.01)。對照組在整個試驗周期中酶活力水平維持在230~260 U/mL范圍內。整個試驗周期中,不同添加量的試驗組均能較好地刺激魚體溶菌酶系統的發生,以添加量為6%的試驗組以及飼喂鮮葉的試驗組能持續更長的時間。
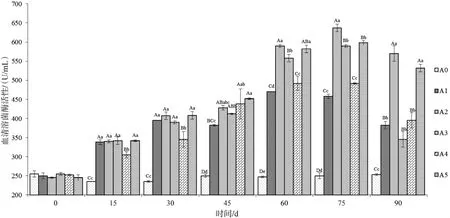
圖2血清溶菌酶活性變化
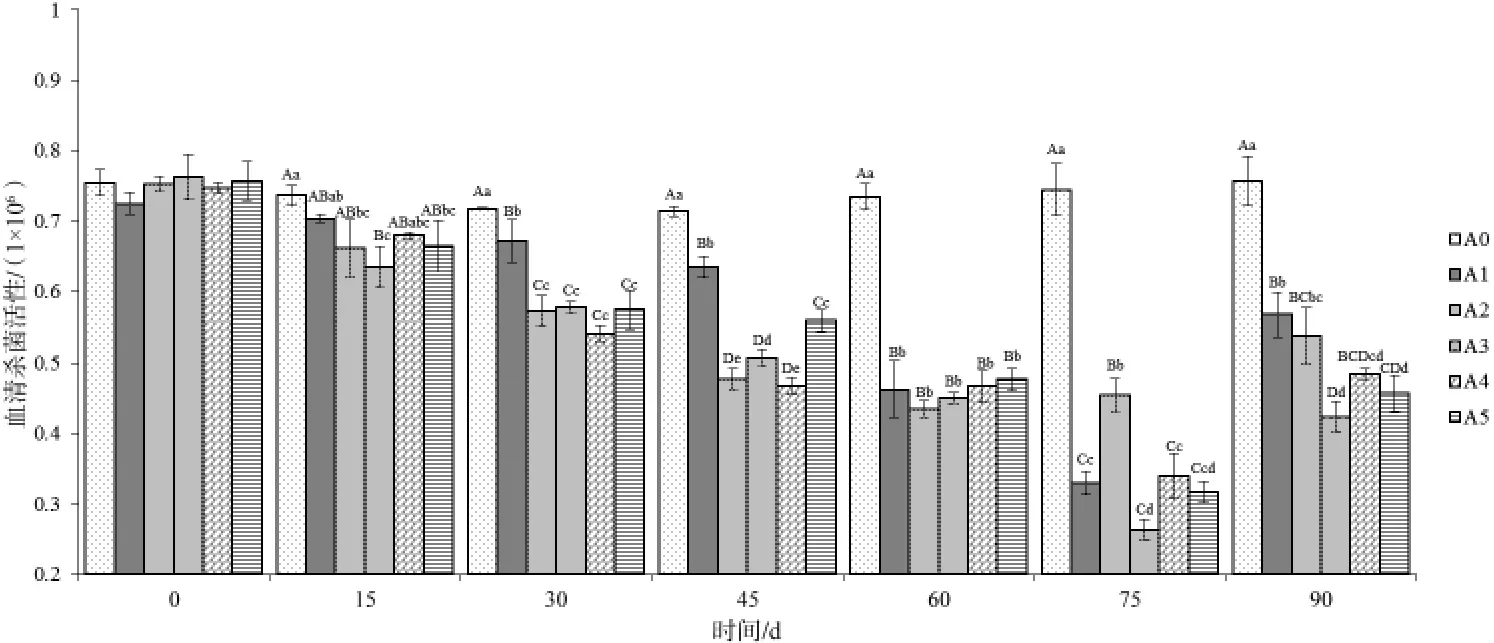
圖3血清殺菌活性變化
2.2.3 血清殺菌活性 參考Sun Y等[13]方法,采用平板計數法反映各試驗組不同時間點的血清殺菌活性,活菌數少的樣本血清殺菌活性高。投喂不同時間后采集各組草魚血清測得血清殺菌活性變化情況見圖3。在投喂后15 d開始,添加不同比例飼料桑的試驗組以及投喂飼料桑鮮葉組(A5)血清殺菌活性開始上升,除添加量為9%(A3)的試驗組與其他試驗組及對照組差異極具統計學意義(P<0.01)外,其余各組變化幅度較小;第30天,各試驗組血清殺菌活性均有上升,但添加量為3%(A1)的試驗組上升較慢,與其他試驗組差異極具統計學意義(P < 0.01);第75天,添加量為9%的試驗組(A3)血清殺菌活性達到整個試驗周期最大值,平板計數活菌數僅為(0.263±0.015)×106CFU/mL;隨后各試驗組血清殺菌活性開始下降,但添加量為9%以及鮮葉組下降的速率相對緩慢,與其他試驗組仍差異極具統計學意義(P<0.01)。對照組在整個試驗周期中平板計數活菌數維持在 0.71×106~0.76×106CFU/mL。
2.2.4 血清補體C3 按照試劑盒說明書,建立標準曲線,根據測得吸光度值對應標準曲線即可得到血清補體C3含量。投喂不同時間后采集各組草魚血清測得血清補體C3含量變化情況見圖4。從結果可知,各試驗組血清補體C3含量變化均呈現先升高后降低的趨勢,與測定的其他指標變化趨勢類似。添加量為9%的試驗組(A3)血清補體C3含量在75 d達到整個試驗周期最大值,為(48.91±1.21)mg/mL。對照組在整個試驗周期中血清補體C3含量維持在12.3~12.7 mg/mL之間。
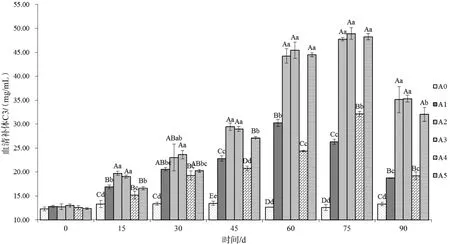
圖4血清補體C3含量變化
3 討論
3.1 添加飼料桑粉對生長性能的影響
在本試驗中,在草魚日糧中添加飼料桑粉或投喂飼料桑鮮葉均呈現較好的促生長作用。目前關于飼料桑在淡水漁業中的應用相關報道較少,僅在陸生動物中有相關研究。在草魚日糧中添加飼料桑粉一方面可促進草魚生長,降低餌料系數;另一方面,可減少糧食的投入降低人與動物之間的糧食競爭。同時提高飼料的利用率,減少飼料的投喂以及對環境的污染。
3.2 添加飼料桑粉對非特異性免疫的影響
血清超氧化物歧化酶(SOD)是重要的抗氧化酶之一,廣泛存在于生物體內,它的主要功能是清除氧自由基,保護機體免受氧化傷害的一種關鍵酶。在調節機體氧化與抗氧化之間的平衡中扮演重要角色。在正常機體內氧自由基的形成和清除處于動態平衡,一旦平衡被打破,那么機體產生的氧自由基就會在體內堆積,造成疾病和衰老。此外血清超氧化物歧化酶還關乎生物體的免疫水平,它能夠提高巨噬細胞的防御能力以及對整個機體的免疫功能都有一定的影響,它通常作為機體非特異性免疫的一個指標[14]。在本試驗中,在草魚日糧中添加飼料桑粉在一定程度上能刺激魚體抗氧化系統的發生,通過對不同時間點草魚血清SOD活性進行檢測,結果發現不同添加量的試驗組以及飼喂鮮葉的草魚血清SOD活性呈現先升高后降低的趨勢,且以添加量為9%的試驗組最好,添加量為6%的試驗組和飼喂鮮葉組次之。結果說明在草魚日糧中添加飼料桑粉能夠激發草魚機體產生抗氧化酶,但相對于免疫增強劑來說,其激發程度相對弱一些,不會對機體產生過氧化損傷。
血清溶菌酶主要在肝臟總合成,廣泛存在于魚類血清、皮膚黏液、巨噬細胞和嗜中性粒細胞[15],是一種能水解致病菌中黏多糖的堿性酶,在防御病原入侵時起到溶解細菌的作用。在本試驗中,對飼喂飼料桑粉后的草魚血清溶菌酶含量進行檢測,結果發現飼喂含飼料桑粉的飼料或飼料桑鮮葉后的草魚血清溶菌酶含量都呈現先升高后降低的趨勢,在投喂后的75 d各試驗組溶菌酶含量水平較高。這表明飼料桑能夠有效提高草魚的非特異性免疫,刺激肝臟產生溶菌酶。整個試驗周期中,添加量為6%的試驗組產生的溶菌酶水平最好,添加量為9%的試驗組和飼喂鮮葉組次之。
血清補體C3在魚類上,可以作為抗體和吞噬細胞間連接的中介,是能夠增強體液和細胞介導的特異性免疫的關鍵成分[16];血清殺菌活性反映了血清中殺菌成分抗菌力大小的指標,綜合反映了多種血清非特異性免疫物質綜合作用的抗菌能力。在本試驗中,對這兩種非特異性免疫指標檢測結果發現,飼喂飼料桑粉和鮮葉均可提高魚體的抗菌能力,有助于魚體抵抗病原微生物的入侵,能夠綜合提高魚體的抗病能力。
3.3 草魚日糧中飼料桑粉添加量探討
在整個試驗周期中,在草魚日糧中添加飼料桑粉含量為6%和9%的試驗組能夠較好地促進草魚生長,提高草魚的增重率,降低餌料系數。同時還可以刺激魚體非特異性免疫,產生一系列體液因子,有助于提高草魚的抗病能力。由此可見,飼料桑粉作為新的飼料原料添加在草魚日糧中具有非常大的價值,根據本試驗研究結果可知添加量為9%可作為實際生產中的添加含量。
參考文獻:
[1]李有業,耿鳳琴.桑葉桑枝在雞飼料中的應用效果[J].當代畜牧,2009(1):30-31.
[2]孫雙印,侯向陽,盧欣石.二十一世紀的綠色神奇功能飼料植物——飼料桑[J].中國奶牛,2007(2):53-54.
[3]孫雙印,侯向陽,盧欣石.飼料桑特性研究與加工利用分析[J].草原與草坪,2008(1):63-69.
[4]劉紅,葉志毅.桑葉為畜禽飼料的利用價值評價[J].飼料研究,2001(9):13-14.
[5]蘇海涯,吳躍明,劉建新.桑葉中的營養物質和生物活性物質[J].飼料研究,2001(9):1-3.
[6]黃自然,楊軍,呂雪娟.桑樹作為動物飼料的應用價值與研究進展[J].蠶業科學,2006,32(3):377-385.
[7]楊靜.飼料桑粉的營養價值評定及在生長育肥豬日糧中的應用研究[D].河北:河北農業大學,2014.
[8]李鋼.新的功能性飼料原料——飼用桑葉粉在我國問世[J].畜牧市場,2006(11):31-31.
[9]蔡晶晶,盧玉飛,李軍,等.桑葉在飼料資源開發中的研究與利用[J].廣東飼料,2011(6):31-33.
[10]許勤.利用飼料桑發展畜禽淡水魚產業生態經濟社會效益顯著[J].林業經濟,2014(2):128-128.
[11]Swain P,Dash S,Sahoo P K,et al.Non-specific immune parameters of brood Indian major carp Labeo rohita,and their seasonal variations[J].Fish&Shellfish Immunology,2007,22(1-2):38-43.
[12]Behera T,Swain P.Alginate-chitosan-PLGA composite microspheres induce both innate and adaptive immune response through parenteral immunization in fish[J].Fish&Shellfish Immunology,2013,35(3):785-91.
[13]Sun Y,Hu Y H,Liu C S,et al.Construction and comparative study of monovalent and multivalent DNA vaccines against Streptococcus iniae.[J].Fish&Shellfish Immunology,2012,33(6):1303-1310.
[14]艾春香,陳立僑,高露姣,等.Vc對河蟹血清和組織中超氧化物歧化酶及磷酸酶活性的影響[J].應用海洋學學報,2002,21(4):431-438.
[15]楊先樂.魚類免疫學研究的進展[J].水產學報,1989,13(3):271-284.
[16]Sakai D K.Repertoire of complement in immunological defense mechanisms of fish[J].Annual Review of Fish Diseases,1992,2(2):223-247.

