不同品種藍莓發酵酒的抗氧化性研究
李 碩
(上海食品科技學校,上海201599)
藍莓(Blueberry)屬越桔科越桔屬(Vacinium)灌木,原產北美[1]。近20年,在美國、加拿大、日本和歐洲的很多國家藍莓都倍受人們青睞。近年來,我國開始種植藍莓,并對藍莓開展研究。近年美國農業部(USDA)和美國國家醫學研究院(NIH)著重對藍莓的營養與保健作用進行了深入研究,結果表明,藍莓富含抗氧化劑、細菌生長抑制劑、葉酸、花色素苷、類黃酮等化合物,而這些化合物對于人體內自由基的清除、抑制及逆轉人體衰老有密切關系[2-3]。隨著人們對健康生活的需求越來越高,富含多酚類等抗氧化物質成分的藍莓成為保健品市場的新寵,藍莓的生產和深加工引起了生產者和消費者的廣泛關注[4]。
在眾多的藍莓加工產品中,藍莓酒既保留藍莓果實的營養價值,提高附加值,又作為時尚飲品滿足市場的需要。藍莓酒發酵后具有抗氧化能力,具有較高的營養價值,將逐漸成為藍莓深加工中的主導產品[5]。Rupasinghe等[6]研究顯示,藍莓酒的總抗氧化能力和總酚含量具有較高水平,酚類物質中的黃酮和酚酸類能夠清除人體自由基,賦予了藍莓酒較強的抗氧化能力。隨著藍莓酒抗氧化性的深入研究,引起了生產者和消費者的廣泛關注,研究不同品種藍莓酒中酚類物質及其抗氧化活性對藍莓酒的實際生產有著積極的推動作用。因此本文對上海市金山地區種植的6種藍莓進行發酵,對生產的藍莓酒的抗氧化能力及其總酚、總黃酮等抗氧化物質含量進行了檢測分析,科學評價藍莓酒的抗氧化活性,為深入開發利用藍莓酒資源提供理論依據,為金山地區的果酒發展提供借鑒。

表1 藍莓品種
1 材料與方法
1.1 實驗材料
藍莓由上海市藍莓研究所提供,見表1。
抗氧化能力(T-AOC)測定試劑盒,南京建成生物工程研究所。其他試劑均購于國藥集團化學試劑有限公司,分析純。
1.2 實驗方法
1.2.1 藍莓酒釀造工藝
鮮果清洗?榨汁?酶解?調整?接種活化好的酵母液?主發酵(23℃)?后發酵?陳釀?澄清?過濾?殺菌?灌裝?成品
操作要點:調整初始糖度至180 g/L;接種量按照果醪量的0.151‰加入活性干酵母,用藍莓醪液活化,活化條件為30℃下3 h;發酵至殘糖不再明顯降低時去除酒腳,下罐。
1.2.2 總抗氧化能力(T-AOC)測定試劑盒法
定義:在37℃時,每分鐘每毫升酒樣使反應體系的吸光度(OD)值每增加0.01時,為一個總抗氧化能力單位。
計算公式:

其中:30為37℃反應30 min,0.1為取樣0.1 mL。1.2.3 總酚測試
總酚測試采用福林酚法[7],以對羥基苯甲酸作為標準品,每個樣品平行測定3次。標準曲線方程為 y=0.0672+0.0011x,r2=0.9804。
1.2.4 總黃酮測試
總黃酮測試,以蘆丁作為標準品,采用硝酸-亞硝酸鈉比色法[8],每個樣品平行測定3次。標準曲線方程為 y=0.03986+5.7910×10-4x,r2=0.9983。
1.2.5 總三萜皂苷測試
準確稱取20.0 mg熊果酸,加入95%vol乙醇溶解并定容至100 mL,配成標準溶液。準確移取標準溶液0.00 mL、0.50 mL、1.00 mL、1.50 mL、2.00 mL、2.50 mL和3.00 mL于10 mL比色管中,氮吹干。各加入5%的香草醛-冰醋酸溶液0.5 mL,搖勻,再各加高氯酸1.0 mL,搖勻,60℃水浴15 min,取出冷卻,加入冰醋酸5.0 mL,搖勻,于548 nm波長處測定吸光度。以熊果酸濃度(或質量)為橫坐標(x),吸光度作為縱坐標(y),繪制標準曲線。各取一定體積的待測樣品上清液,按上述方法操作。每個樣品平行測定3次。標準曲線方程為y=0.04957+5.61145×10-4x,r2=0.9923。
1.2.6 清除DPPH能力測定
參照Brand-William等建立的方法[9],準確配制濃度為1×10-4mol/L的溶液。移取上述樣品提取液0.2 mL,DPPH溶液3.8 mL,以0.2 mL 50%vol乙醇與DPPH反應液為空白。避光反應1 h,517 nm測定吸光度。
因此,各酒樣的清除率(%)=(1-A1/A0)×100%。
其中:A1為測試液吸光度,A0為空白對照組的吸光度。
1.2.7 清除ABTS·+能力測定
將7 mmol/L的ABTS溶液和140 mmol/L的過硫酸鉀溶液,以500∶88比例混合,避光靜止12~16 h,形成墨綠色穩定化合物,作為儲備液。將儲備液用乙醇稀釋至734 nm吸光度0.70±0.02。移取上述提取液0.1 mL,加入3.9 mL ABTS·+工作液3.9 mL,混勻后,靜止避光反應6 min,測試734 nm波長吸光度。以0.1 mL 50%vol乙醇和3.9 mLABTS·+工作液吸光度為空白對照A0。
得到各樣品的ABTS·+清除率(%)=(1-A1/A0)×100%。
1.2.8 亞鐵離子還原能力測定(FRAP)[10-11]
以10∶1∶1混合0.3 mol/L(pH 3.6)的醋酸緩沖溶液,10 mmol/L TPTZ溶液和20 mmol/L氯化鐵溶液。
準確吸取0.1mL系列濃度為0.2 mmol/L、0.4 mmol/L、0.6 mmol/L、0.8 mmol/L和1 mmol/L的硫酸亞鐵溶液,與0.3 mL去離子水混合,再加入3.9 mL FRAP溶液,混勻,37℃反應4 min。593 nm測吸光度,繪制硫酸亞鐵-吸光度標準曲線。標準曲線方程為y=0.0618+0.000288x,r2=0.9926。
準確吸取0.1 mL上述樣品提取液,與0.3 mL去離子水混合,再加入3.9 mL FRAP溶液,混勻,37℃反應4 min,593 nm測吸光度。以硫酸亞鐵標準曲線計算出相應的FeSO4濃度,定義為當量濃度(FRAP值)。最終結果表示為每FRAP值越大,表示抗氧化活性越強。
2 結果與分析
2.1 藍莓酒總抗氧化能力的比較
總抗氧化能力實際上是測定鐵離子的還原能力,即將體系中的Fe3+還原成Fe2+,后者可與菲啉類物質形成穩固的絡合物,通過分光光度計比色測出其抗氧化能力的高低,光吸收值變化越大,總抗氧化能力越強。測試結果見表2。
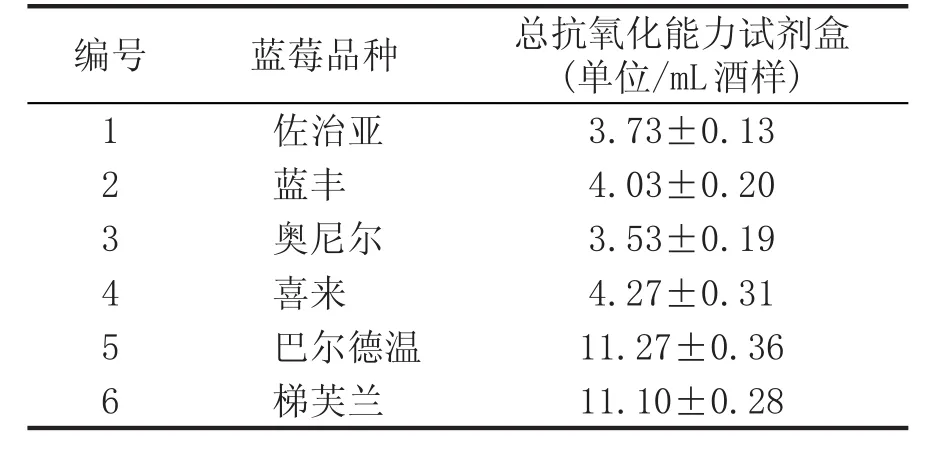
表2 總抗氧化指標測試結果
從表2可看出,巴爾德溫和梯芙蘭品種的藍莓酒總抗氧化能力明顯高于其他品種。
2.2 藍莓酒總酚含量的比較(圖1)
近年來很多實驗都證實紅葡萄酒具有抗氧化性,而其抗氧化性主要來源于其自身所含的酚類物質,總酚含量越高,抗氧化性則越強[12]。酚類物質是強體外抗氧化劑,許多研究證實其有預防心血管疾病、預防癌癥等功能,酚類物質的這些功能和其清除自由基金屬螯合能力等有直接的關系[13]。

圖1 6種品種藍莓酒總酚含量
圖1表明,6種品種藍莓酒均具有一定量的總酚,其中巴爾德溫和梯芙蘭藍莓酒含量較高,分別為1.234 mg/mL±0.026 mg/mL和1.160 mg/mL±0.022 mg/mL,喜來藍莓酒含量最少,為0.406 mg/mL±0.004 mg/mL。對應的紅酒、白葡萄酒、黃酒,其酚類物質的含量分別是1~4 mg/mL、0.2~0.4 mg/mL、0.249 g/mL[14]。藍莓酒總酚含量接近于紅葡萄酒,高于白葡萄酒和黃酒。
2.3 藍莓酒總黃酮含量的比較(圖2)
黃酮類化合物是多酚的主要成分之一,具有清除氧自由基等多種生理活性,在抗氧化、保護視力、延緩衰老、增強免疫力、保護人體免受自由基的損傷等方面起到很好的作用[15]。

圖2 6種品種藍莓酒總黃酮含量
如圖2所示,6種品種藍莓酒均具有一定量的總黃酮,其中巴爾德溫藍莓酒含量最高,含量為1.232 mg/mL±0.025 mg/mL,其次是梯芙蘭藍莓酒,含量為1.010 mg/mL±0.021 mg/mL,喜來藍莓酒含量最少,為0.216 mg/mL±0.001 mg/mL。
大量實驗表明,一些類黃酮物質具有較強的抗氧化性,能抗微生物、螯合金屬離子、抑制低密度脂蛋白氧化和腫瘤細胞生長等作用。因此,食物類黃酮物質生物學作用及其機制已成為當今營養與食品科學研究領域的熱點之一[16]。因此,研究藍莓酒中總黃酮的含量,對藍莓酒的開發具有指導意義。
2.4 藍莓酒總三萜皂苷含量的比較
三萜皂苷廣泛分布于多種植物的根、莖、葉、樹皮及花中,資源豐富,具有抗腫瘤、抗衰老及增強免疫力等生理活性,可預防和治療多種疾病,對開發利用天然資源具有廣闊的發展前景[17]。本實驗采用比色法測定6種品種藍莓酒總三萜皂苷含量(圖3)。

圖3 6種品種藍莓酒總三萜皂苷含量
如圖3所示,6種品種藍莓酒總三萜皂苷含量最低1.618mg/mL±0.011mg/mL,最高15.229mg/mL±1.003 mg/mL,表明藍莓酒含有一定量總三萜皂苷,具有抗衰老、增強免疫力等功能。奧尼爾品種藍莓酒具有較高的總三萜皂苷含量。
2.5 藍莓酒清除DPPH自由基能力的比較
DPPH自由基在517 nm處有最大吸光值,它能夠從釋放質子的物質處得到質子,形成一種穩定的反磁性分子[18]。研究表明[19],釋放質子是物質抗氧化能力的機理之一,通過測定物質對自由基的清除能力,可以較迅速地評價物質的抗氧化能力。所以,在517 nm處吸光值會變小,原先穩定的紫色會變淺或成為黃色。吸光值越低表示清除自由基的能力越強。結果見圖4。

圖4 6種品種藍莓酒清除DPPH自由基的能力
如圖4所示,6種品種藍莓酒對自由基的清除能力最低為36.78%±3.04%,最高為74.02%±4.87%,這表明藍莓酒有明顯的清除自由基的能力。巴爾德溫和梯芙蘭藍莓酒具有較強的清除自由基能力。在體內,若自由基的形成超過人體機能自身保護能力時,就會誘發如動脈粥狀硬化等慢性病。藍莓酒作為一種自由基抑制劑,可以降低自由基在人體中產生的危害。
2.6 藍莓酒清除ABTS·+能力的比較(圖5)
1993年,Miller等[20]首次介紹了用ABTS·+法來測定一些化合物的抗氧化活性。在734 nm處,ABTS·+有特征吸收,利用待測化合物清除ABTS·+引起吸光度變化來評價抗氧化活性[21]。此后,在飲料、一些植物提取物,尤其是葡萄酒中廣泛采用ABTS·+法來判斷其抗氧化活性[22-23]。

圖5 6種品種藍莓酒清除ABTS·+的能力
如圖5所示,6種品種藍莓酒對ABTS·+的清除能力最低為45.78%±3.28%,最高為83.91%±5.51%,這表明藍莓酒有明顯的清除ABTS·+能力。巴爾德溫和梯芙蘭藍莓酒具有較強的清除ABTS·+能力。
2.7 藍莓酒亞鐵離子還原能力的比較
測定藍莓酒還原力,實質上是檢驗藍莓酒中是否含有良好的電子供應體,通過自身的還原作用給出電子而清除自由基的。還原力越強,則抗氧化性越強。因此可通過測定還原力來說明抗氧化活性的強弱。本試驗吸光度越大,FRAP值越大,還原力越強,表示抗氧化活性越強。結果見圖6。
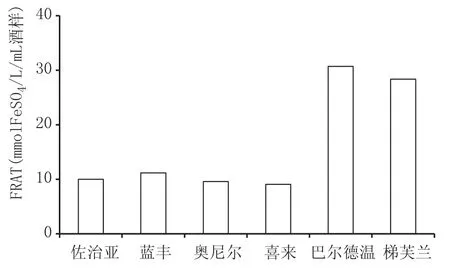
圖6 6種品種藍莓酒的亞鐵離子還原能力
如圖6所示,亞鐵離子還原能力:巴爾德溫>梯芙蘭>藍豐>佐治亞>奧尼爾>喜來。其中,巴爾德溫品種的藍莓酒亞鐵離子還原能力為30.72 mmol±2.38 mmol Fe2SO4L/mL酒樣。
3 總結
3.1 建立了一個以總抗氧化能力、清除DPPH自由基能力、清除ABTS·+能力、離子還原能力為指標的抗氧化檢測體系。根據此體系,對不同品種藍莓采用相同工藝釀造的藍莓酒的抗氧化能力進行了初步檢測。
3.2 藍莓酒具有一定的抗氧化能力,不同品種藍莓酒差異較大,其中巴爾德溫和梯芙蘭品種抗氧化能力最強。
3.3 藍莓酒總酚含量:巴德爾溫>梯芙蘭>奧尼爾>藍豐、佐治亞>喜來,其總酚含量范圍為0.406~1.234 mg/mL,接近于紅葡萄酒,高于白葡萄酒和黃酒。
3.4 藍莓酒總黃酮含量:巴德爾溫>梯芙蘭>藍豐>佐治亞>奧尼爾>喜來,其總黃酮含量范圍為0.216~1.232 mg/mL,接近于紅葡萄酒,高于白葡萄酒和黃酒。
3.5 藍莓酒的總酚、總黃酮對其抗氧化能力有正相關性,也進一步說明藍莓酒中的多酚物質是藍莓酒抗氧化作用的重要物質基礎。
3.6 藍莓酒含有一定量總三萜皂苷,具有抗衰老、增強免疫力功能。其中奧尼爾品種含量最高,為15.229 mg/mL。
參考文獻:
[1]PRITTS M,HANCOCK J.Highbush Blueberry Production Guide[M].Northeast Regional Agricultural Engineering Service,1992:4-7.
[2]JOSEPH J A,SHUKITT-HALE B,DENISOVA N A,et al.Reversals of age-related declines in the neuronal signal transduction,cognitive,and motor behavioral deficits with blueberry,spinach,or strawberry dietary supplementation[J].Journal of neuroscience,1999,19(18):8114-8121.
[3]苑兆和.世界藍莓生產歷史與發展趨勢[J].落葉果樹,2003(1):49-52.
[4]ZAFRA-STONE S,YASMIN T,BAGCHI M,et al.Berry anthocyanins as novel antioxidants in human health and disease prevention[J].Mol nutr food res,2007,51(6):675-683.
[5]梁晨,張倩雯,盛啟明,等.不同品種藍莓酒抗氧化能力及其多酚含量分析[J].中國釀造,2013(8):46-49.
[6]RUPASINGHE H P V,CLEGG S.Total antioxidant capacity,total phenolic content,mineral elements,and histamine concentrations in wines of different fruit sources[J].Journal of food composition and analysis,2007,20(2):133-137.
[7]SLINKARD K,SINGLETON V L.Total phenol analyses:automation and comparison with manual methods[J].American journal of enology and viticulture,1977,28:40-55.
[8]朱友春,田世龍,王東暉.比色法測定苦蕎中黃酮含量的方法改進[J].甘肅科技,2003(2):13-14.
[9]BRAND-WILLIAM W,CUVELIER M E,BERSET C.Use of a free radical methods to evaluate antioxidant activity[J].LWT-Food science and Technology,1995,28:25-30.
[10]SHON M Y,LEE J,CHOI J H,et al.Antioxidant and free radical scavenging activity of methanol extract of chungkukjang[J].Journal of Food composition and analysis,2007,20(2):113-118.
[11]PRIOR R L,WU X,SCHAICH K.Standardized methods for the determination of antioxidant capacity and phenolics in foods and dietary supplements[J].Journal of agricultural and food chemistry,2005,53(10):4290-4302.
[12]胡博然,聞雯,陰淑貞,等.電子順磁共振波譜儀分析干紅葡萄酒DPPH清除能力及其與總酚含量的關系[J].中國農業科學,2012,45(1):135-141.
[13]LODOVICI M,GUGLIELMI F,CASALINI M,et al.Antioxidant and radical scavenging properties in vitro of polyphenolic extracts from red wine[J].European journal of nutrition,2001,40:74-77.
[14]鄭校先,李燕,徐維菲,等.黃酒的抗氧化活性研究[J].釀酒科技,2009(10):57-64.
[15]黃曉杰,柴哲,楊鐘燕,等.藍莓酒發酵過程中抗氧化物質變化規律研究[J].食品工業科技,2013(17):103-109.
[16]金紅,段輝,何亞敦,等.保健酒中總黃酮測定方法的比選[J].釀酒科技,2009(2):79-81.
[17]陳穎,董孝剛,孟麗,等.天花粉中總三萜皂苷的含量分析[J].中國野生植物資源,2010(8):61-63.
[18]SOARES J R,DINS T C P,CUNHAA P,et al.Antioxidant activity of some extracts ofThymus zygis[J].Free radical research,1997,26:469-478.
[19]勾明玥,劉梁,張春枝.采用DPPH法測定26種植物的抗氧化活性[J].食品與發酵工業,2016,36(3):148-150.
[20]MILLER N J,RICE-EVANS C A,DAVIES M J,et al.A novel method for measuring antioxidant capacity and its application to monitoring the antioxidant status in premature neonates[J].Clinical science,1993,84:407-412.
[21]KIRSCHBAUM B.Total urine antioxidant capacity[J].Clinica chimica acta,2001,305:167-173.
[22]MAZZA G,KAY C D,COTTRELL T,et al.Absorption of anthocyanins from blueberries and serum antioxidant status in human subjects[J].Agric food chem,2002,50:7731-7737.
[23]DEBEER D,JOUBERT E,GELDERBLOM W C A,et al.Antioxidant activity of South African red and white cultivar wines:free radical scavenging[J].Agric food chem,2003,51:902-909.

