離子色譜法同時測定葡萄酒中26種有機酸和陰離子
宋衛得,李兆杰,劉 冰,姜維珍,葉佳宇,李林杰,李 健
(1.日照出入境檢驗檢疫局,山東日照276826; 2.威海出入境檢驗檢疫局,山東威海264200)
有機酸是酒中重要的風味物質,葡萄酒中主要有機酸有乳酸、琥珀酸、酒石酸、草酸、檸檬酸、甲酸、丁酸等[1],有機酸的種類和含量影響著葡萄酒的色澤、口感、生物穩定性;葡萄酒中有毒有害陰離子超標時,就會危害人體健康;有機酸含量測定還可監控生產、識別質量、辨別摻假等[2]。因此,建立葡萄酒中多種有機酸和陰離子同時檢測的方法,對于葡萄酒釀制過程質量控制和產品質量監控具有重要的實用價值。
離子色譜法具有高效、快速、靈敏、準確等優點[3-8],是同時測定有機酸和陰離子的理想方法。潘丙珍等[9]采用離子色譜法測定了酒中16種有機酸,但是存在基線不平穩、檢測組分較少等不足;吳飛燕等[10]采用離子色譜法建立了酒中17種有機酸同時檢測的方法,靈敏度高,但僅分析了有機酸類物質,需52 min后才能全部出峰。目前離子色譜法測定葡萄酒中多種有機酸和陰離子的方法研究較少,且存在分析組分少、影響因素考察不全、檢測時間較長等不足。本研究采用多級梯度淋洗離子色譜法,分析實驗影響因素,優化色譜分離條件,建立了同時測定葡萄酒中26種有機酸和陰離子的方法,26種組分在32 min內即可全部出峰,實現了快速分析、綠色分析、多組分同時分析的目標。
1 材料與方法
1.1 材料、儀器和試劑
酒樣:國產、進口的紅白葡萄酒,市售。
儀器:離子色譜儀(Dionex ICS2100),配備電導檢測器和自動進樣器(AS-DV);自動再生抑制器(ASRS 300);Milli-Q超純水儀(美國Millipore公司)。
試劑:超純水(電阻率18.2 MΩ·cm);8種陰離子標準溶液(濟南眾標科技有限公司),質量濃度為1000 mg/L;18種有機酸均為優級純以上級別試劑,使用時配成所需的質量濃度。
1.2 離子色譜條件
陰離子分離柱:Dionex IonPacTMAS11-HC;保護柱:Dionex IonPacTMAG11-HC;抑制器再生模式:外加水電導抑制,電導檢測器檢測;流動相:KOH梯度淋洗液;流速:1.00 mL/min;柱溫:30℃;進樣量:50 μL。
1.3 前處理步驟
采用濃度為2.0 mol/L的KOH溶液,調節pH值至5.3~6.0,取10 mL樣品放入50 mL離心管中,移取上清液樣品1.0 mL,用超純水定容至100 mL容量瓶中,搖勻、靜置10 min,取10.0 mL溶液,過0.22 μm水相濾膜,棄去前面3 mL,收集后面清液,待上機檢測。
2 結果與討論
2.1 色譜條件的選擇
2.1.1 色譜柱的選擇
在相同實驗條件下,先后進行了AS11-HC、AS11、AS19共3種色譜柱的分析對比實驗。實驗結果表明,使用AS11-HC色譜柱時多數組分峰型較尖銳、靈敏度較好。這是因為AS11-HC是一種高容量、強親水性色譜柱,尤其適用于食品中多種有機酸和陰離子同時測定。因此,選擇AS11-HC色譜柱進行實驗分析。
2.1.2 流速的選擇
分別進行了0.50 mL/min、0.75 mL/min、1.00 mL/min、1.25 mL/min、1.50 mL/min 5個流速條件下的實驗對比。在0.50 mL/min和0.75 mL/min流速時,因流速低,壓力小,峰寬較大,總出峰時間較長,靈敏度不高。1.25 mL/min和1.50 mL/min流速時系統壓力不斷升高,壓力過大易損害色譜柱的固定相,從而極大影響色譜柱使用壽命。在1.00 mL/min時,壓力大小適中,靈敏度高,總出峰時間縮至32 min。綜合考慮各種影響因素,實驗流速選擇1.00 mL/min。
2.1.3 pH值的選擇
首先進行了0.01~10.0 mg/L濃度混合標準溶液的pH值測定實驗,實驗發現,當標準混合溶液中組分濃度由0.01增至10.0 mg/L時,溶液中H+濃度增大,溶液酸性逐漸增大,pH值由5.47降為3.52。
本實驗所測組分中,存在一些不穩定的弱酸和有機酸,如ClO2-和NO2-離子,受到溶液pH值影響較大,pH值小于4.0時,ClO2-和NO2-離子檢測濃度低于理論濃度的80%,這正是與溶液中高濃度的H+發生反應而產生的損失。本實驗使用KOH溶液來調節一系列不同pH值的去離子水溶液為溶劑,而后配制不同pH值的同一理論濃度混合標準溶液,進而測定26種組分在不同pH值時測定含量的變化。結果表明,弱酸和不穩定有機酸在強酸性條件下受影響較大,而在pH5.5~7.0時,多數組分檢測含量穩定、變化小。這是因為多數有機酸的解離常數pKa值在4.2~6.9,當pH值與pKa值相等時,溶液中的離子型分子和中性分子的濃度相同,組分處于相對穩定的狀態,便于定量分析。
考慮到葡萄酒的pH值一般在2.7~4.0范圍,而pH值大小又直接影響著某些弱酸和不穩定有機酸的電離程度,實驗發現,稀釋100倍后酒類樣品的pH值處于4.5~6.0,考慮到中性或弱酸性環境下,標準溶液和測定樣品中多數組分處于含量穩定狀態,因此,本次實驗選取標準溶液配制至pH值為5.3~6.0之間。
2.1.4 梯度淋洗條件的選擇
本試驗一次性測定多種組分,而個別組分結構性能類似、分子量相近,普通淋洗濃度梯度條件,難以保證26種組分的有效分離。根據實驗結果和各種組分的色譜柱保留特性,將26種組分分為3類:弱保留組分(1~13)、中等保留組分(14~21)、強保留組分(22~26)。首先,0~6 min為初始淋洗濃度時間段,分別進行了0.80 mmol/L、1.00 mmol/L、1.25 mmol/L初始濃度時的實驗對比,發現在0.80 mmol/L初始濃度下,各組分出峰時間拖后,總出峰時間延長,且前3種弱保留組分的分離度不理想;1.25 mmol/L初始濃度時,前10種弱保留組分分離效果不好;初始濃度1.00 mmol/L時,多數組分色譜峰的分離狀況較理想。因此,選擇1.00 mmol/L為初始淋洗濃度。
6~22 min時,出峰組分有21種,在實驗時最初選擇使用了2次淋洗濃度變化,但此時難以確保21種組分的有效分離。前后進行了30多次實驗分析對比,最終選擇了使用3次淋洗濃度和淋洗斜率的變化,首先,在6~13 min時,淋洗濃度由1.0 mmol/L增至14.0 mmol/L,淋洗斜率為1.857 mmol/L·min;在13~17 min時,淋洗濃度由14.0 mmol/L增至14.5 mmol/L,此時基本是一個等度淋洗濃度,斜率只有0.125 mmol/L·min;在17~22 min時,選取淋洗斜率為0.700mmol/L·min,淋洗濃度由14.5mmol/L增至18.0 mmol/L。在此梯度淋洗條件下,21種組分靈敏度較高,分離效果理想。
在22~33 min時,進行了最高淋洗濃度分別為50 mmol/L、60 mmol/L、70 mmol/L條件下對比分析實驗。實驗結果證實,最高淋洗濃度為50 mmol/L時,淋洗濃度較低,5種強保留組分出峰時間拖后,且靈敏度不高;最高淋洗濃度為70 mmol/L時,5種組分出峰速度快,靈敏度較高,但分離度不高,且組分峰有重疊情況;最高淋洗濃度為60 mmol/L時,5種強保留組分靈敏度和分離度較好,因此,選擇60 mmol/L為最高淋洗濃度。
總之,初始濃度的選擇、淋洗斜率大小、最高淋洗濃度的選擇及時間段的劃分都是影響多組分分離測定效果的重要因素。通過科學系統的研究,綜合分析各種實驗影響因素,實現了32 min內快速準確測定葡萄酒中26種有機酸和陰離子的目標。淋洗條件見表1,離子色譜圖見圖1。
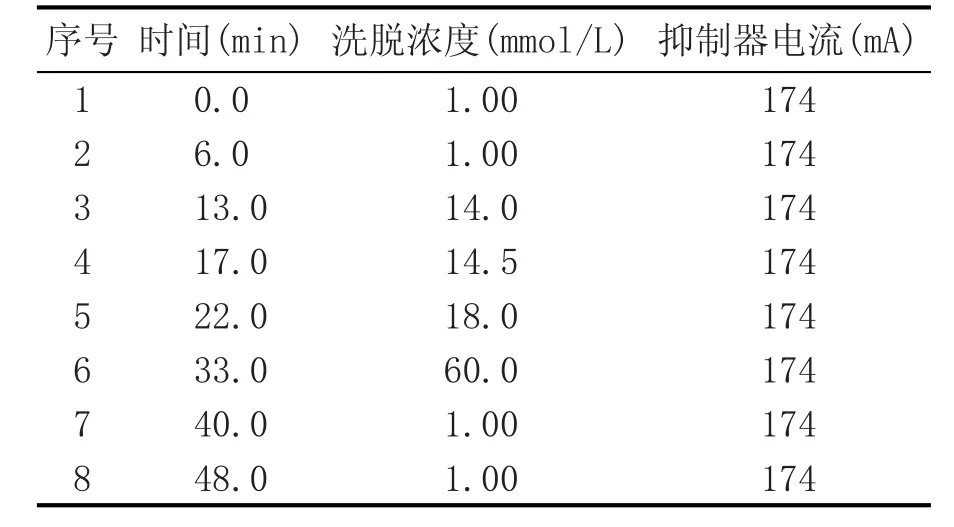
表1 離子色譜多級梯度淋洗條件
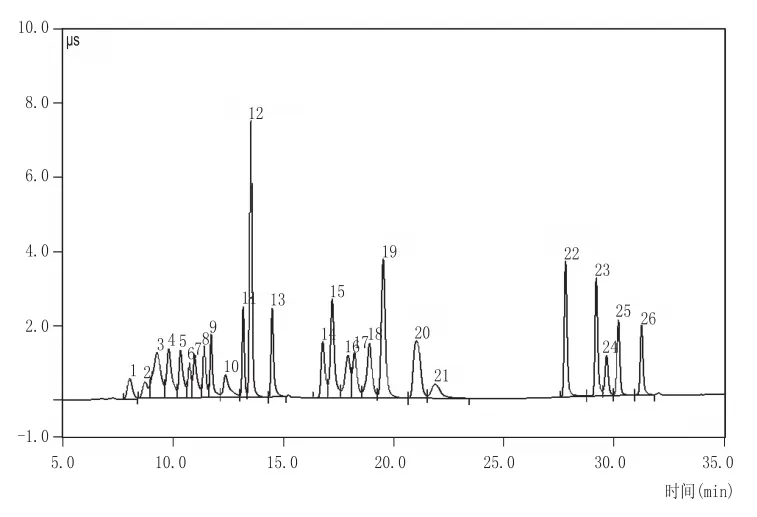
圖1 26種組分混合標準溶液的離子色譜圖
2.2 方法學考察
2.2.1 線性范圍與檢出限(表2)
進行了26種有機酸和陰離子的混合標準溶液測定實驗,進行校準曲線擬合。通過色譜峰信噪比來計算待測組分的檢出限(S/N=3),在0.01~1.00 mg/L濃度范圍內,進行了7個不同濃度水平(0.01mg/L、0.02mg/L、0.05mg/L、0.10mg/L、0.20mg/L、0.50 mg/L、1.00 mg/L)標準工作液的檢測和線性擬合。實驗證實,26種組分線性相關系數均大于0.99,除了F-外,其他7種無機陰離子相關系數均大于0.995,線性較好;個別有機酸由于分離度不夠或自身不穩定,線性相關性不理想;總體來說,26種組分線性均已達到食品理化定量技術要求。25種組分檢出限在0.00009~0.0783 mg/L之間,僅有苯甲酸檢出限為0.201 mg/L,本次實驗的檢出限較前期研究時有所增大,主要是實驗時色譜柱使用時間較長,基線噪音有所增大的原因。

表2 測定組分的線性范圍、線性方程、相關系數及檢出限(S/N=3)
2.2.2 回收率與精密度
選取3種葡萄酒樣品,依次向3種樣品中添加濃度級別水平分別為0.10 mg/L、0.20 mg/L、1.00 mg/L的混合標準溶液,每個濃度水平進行6次平行測定實驗,來驗證方法的回收率和精密度。方法回收率和RSD數據見表3。
由表3可看出,在0.10 mg/L添加濃度水平下,回收率在75.97%~109.80%之間,RSD在0.22%~8.38%范圍內;在0.20 mg/L添加濃度水平下,回收率在78.24%~107.25%之間,RSD在0.71%~8.06%范圍內;在1.00 mg/L添加濃度水平下,回收率在80.59%~105.84%,RSD在0.78%~5.66%范圍。實驗數據表明,隨著添加濃度的增大,回收率和RSD數據范圍逐漸變小,準確度和精密度漸趨穩定。3個濃度水平下,苯甲酸的回收率在78.24%~81.30%之間,其中兩個濃度下RSD數據大于8.0%,主要因為苯甲酸是離子半徑較大、疏水性較強的有機酸,且自身不穩定,因此色譜峰型不對稱。順烏頭酸在0.10 mg/L和0.20 mg/L添加濃度水平下,回收率分別為75.97%和83.58%,這是因為順烏頭酸不夠穩定,在一定條件下,有小部分轉化成反烏頭酸,表3中反烏頭酸回收率偏大也證實了這一點,但小部分的轉化并不影響定性定量分析,回收率和精密度依然滿足食品理化檢驗技術要求。從總體上來看,3個濃度水平、6次平行檢測回收率數據結果比較理想,說明葡萄酒中26種組分同時檢測的方法精密度高、穩定性好。
2.2.3 準確度
選取一種葡萄酒,添加0.50 mg/L濃度水平標準溶液,進行3 d 9次平行測定實驗。理論真值以基質濃度和添加濃度相加來計,計算出9次測定值和理論真值的相對偏差。實驗數據表明,葡萄酒(0.50 mg/L)中26組分的9次平行實驗結果與理論真值的相對偏差在-15.09%~9.57%范圍內,滿足食品理化準確度技術要求,充分驗證了檢測方法的準確性。

表3 測定組分的回收率及精密度(RSD)(n=6)
2.3 實際樣品測定
選取5種代表性葡萄酒樣品(國產紅葡萄酒2種、進口紅葡萄酒2種、進口白葡萄酒1種),根據所選前處理方法和離子色譜條件,檢測了葡萄酒實際樣品中有機酸和陰離子含量。
由圖2可看出,葡萄酒中主要的有機酸有乳酸、乙酸、戊酸、戊二酸、琥珀酸、酒石酸、草酸、檸檬酸、順烏頭酸、富馬酸、甲酸、丁酸等,無機陰離子有Cl-、NO3-、PO43-。僅有一個紅葡萄酒樣品中檢出微量 NO2-,有毒有害的 ClO2-、BrO3-、CrO42-陰離子均未檢出,說明這些葡萄酒釀造所用原料質量和水質較好。從色譜圖中看出,除乳酸和乙酸組分濃度較高,分離度不理想,其他各種組分色譜峰尖銳,分離度較好,說明方法的靈敏度好、穩定性高。
從紅葡萄酒和白葡萄酒圖譜對比來看,紅葡萄酒中乳酸、戊酸、草酸的含量較高,而白葡萄酒中的琥珀酸、酒石酸、檸檬酸、Cl-、NO3-、PO43-比紅葡萄酒中高,這主要因為白葡萄酒是用白葡萄或者紅葡萄去皮和去核后壓榨、發酵而成,而紅葡萄酒卻是用紅葡萄連帶葡萄皮和果核釀制而成,原料和釀制方法的不同是白葡萄酒和紅葡萄酒的有機酸和陰離子含量不同的主要原因。
3 結論
通過對色譜柱、流速、溶液pH值、初始梯度濃度等多種實驗影響因素的分析,探索出適合葡萄酒中26種組分分離的梯度淋洗條件,建立了多級梯度淋洗-離子色譜法同時測定葡萄酒中26種有機酸和陰離子的方法。實驗結果證實,流速為1.00 mL/min,柱溫為30℃,pH值在5.3~6.0之間時,26種組分的分離效果理想。對比發現,本方法主要優點有:(1)一次性同時檢測26種組分,實現了有機酸、陰離子、防腐劑等多種類組分同時檢測;(2)多因素多角度考察分析實驗影響因素,有效提高了多組分檢測方法的穩定性和準確性;(3)操作快速便捷、靈敏度高、適用性強,經簡單前處理后上機測定,32 min內26種組分全部出峰。由此可見,該方法快速、簡便、靈敏、準確,完全適于葡萄酒中26種有機酸和陰離子的分析測定。
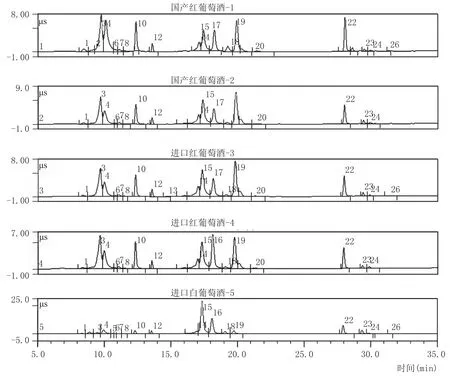
圖2 5種葡萄酒樣品的離子色譜圖
參考文獻:
[1]ZERAVIK J,FOHLEROVA Z,MILOVANOVIC M,et al.Various instrumental approaches for determination of organic acids in wines[J].Food chemistry,2016,194(1):432-440.
[2]向進樂,杜琳,郭香鳳,等.離子抑制反相高效液相色譜法測定菠蘿果酒中10種有機酸[J].中國食品學報,2014,14(6):229.
[3]GENG X M,ZHANG S F,WANG Q,et al.Determination of organic acids in the presence of inorganic anions by ion chromatography with suppressed conductivity detection[J].Journal of chromatography A,2008,1192(1):187-190.
[4]邵宏宏,周秀錦,周向陽,等.抑制型離子色譜法測定海產品中的有機酸類鮮味物質[J].中國調味品,2014,39(3):94-97.
[5]LUO X M,CHEN L,ZHAO Y Q.Simultaneous determination of three chloroacetic acids,three herbicides,and 12 anions in water by ionchromatography[J].Journal of separation science,2015,38(17):3096-3102.
[6]GUO B,ZHAO Y,LIU J Y.Simultaneous determination of seven carbohydrates in tobacco by ultrasonic extraction-ion chromatography[J].Asian journal of chemistry,2014,26(16):5149-5155.
[7]施超歐,姚寶龍,胡咪,等.離子轉換色譜-紫外檢測法測定啤酒中的無機陰離子和有機酸[J].色譜,2016,34(10):951-955.
[8]DOLGONOSOV A M,KOLOTILINA N K.Ion-exchange sample preparation for the determination of anions in highly alkaline solutions by ion chromatography[J].Journal of analytical chemistry,2015,70(11):1322-1324.
[9]潘丙珍,劉青,龐世琦,等.離子色譜法測定酒中的有機酸和無機陰離子[J].現代食品科技,2013,29(4):876-877.
[10]吳飛燕,賈之慎,朱巖.離子色譜電導檢測法測定酒中的有機酸和無機陰離子[J].浙江大學學報,2006,33(3):312-313.

