綠河頁巖干酪根分步瞬時熱解演化特征及機理研究
侯孝歡,吳應琴,王作棟,劉艷紅
1.甘肅省油氣資源研究重點實驗室/中國科學院油氣資源研究重點實驗室,蘭州 730000
2.中國科學院大學,北京 100049
0 引言
一直以來,對有機質的物質組成、結構類型和成烴機制等一系列的認識評價是油氣地球化學發展前進中研究的重中之重。在前人研究過程中元素分析和生油巖評價(Rock-Eval)技術常常被認為是簡潔快速評價烴源巖宏觀特性(有機質豐度、類型及總生烴能力等信息)的有效方法,如Rock-Eval技術能反映烴源巖中游離烴(S1)和熱解烴(S2)的總量,但卻無法認識其中的任何單體烴的組成特征信息,更無法提供不同演化階段的詳細生烴產物的變化特征[1-4],而這些對于定性評價烴源巖及其成烴機理更顯得至關重要。隨著熱解技術和色譜質譜技術的全面發展,熱解色譜質譜聯用儀為有機質進行在線分析研究提供了十分契合的方案。
熱解氣相色譜質譜聯用儀(Py-GC-MS)作為研究有機質生烴特征的重要技術方法和手段之一,可以揭示這一轉化過程中各種組分產出特征及變化規律并幫助探討產物之間的相互關系。有機質是多種有機組分通過橋鍵和不同基團聯結而成的復雜三維大分子,由于連接鍵的強弱不同,其受熱分解或加氫分解時可依次產生相對小的烴類化合物。因此,高溫瞬時熱解實驗可以提供與有機質大分子支鏈結構相關的大量信息。一方面,由于有機質熱解瞬時完成,盡量避免了二次反應的發生,其裂解產物基本代表了各種鍵合于干酪根大分子上的側鏈經高溫自鍵能較弱的部位斷裂的小分子組分[5-6]。低溫瞬時熱解產物則主要是以游離態或其他賦存狀態(弱的化學鍵、氫鍵等作用力)吸附于干酪根表面或空隙的吸附烴。另一方面,分步熱解可以模擬樣品的演化過程,有助于了解其各個生烴階段的熱解產物特征,并對不同演化階段的產物變化進行對比,可以提供干酪根、烴源巖等有機質從未熟、低熟到高熟的演變過程,探討干酪根隨熱解溫度升高的變化規律,認識其生烴機制[7]。本文以萊尼段綠河頁巖干酪根為研究對象,運用Py-GC-MS熱解色譜質譜聯用儀,采用瞬時分步熱解法對干酪根樣品進行分析研究。本次研究所用的萊尼段綠河頁巖沉積物顯示出了界限分明的洪泛和干燥的準層序,不是單一的有機相,而是沉積于不同條件下的層段和沉積相的一個集合體,準層序具有不同的生物標志化合物特征[8]。這些層段的烴源巖干酪根類型相似,大多由藻類體構成,因此極具有研究價值。
1 熱模擬實驗條件和樣品
1.1 實驗條件與方法
1.1.1 熱解實驗方法
本次熱模擬實驗是應用熱解氣相色譜質譜儀(Py-GC-MS)對干酪根樣品進行開放體系下的分階段在線分析。實驗儀器為Frontier(日本)多功能熱裂解器EGA/PY-3030D(熱解裝置溫度范圍為40 ℃~1 050 ℃)連接Agilent(美國)7890-7000B型氣相色譜三重四級桿聯用儀,組裝成完整的熱模擬分析系統。色譜柱為Ultra Alloy Plus-5毛細管柱(Frontier-LAB,30 m × 0.25 mm × 0.25 μm,日本)。熱解裝置預升溫至100 ℃時將載著干酪根樣品(1.80 mg)的熱解杯推進熱解器,以200 ℃/min的速率程序升至300 ℃恒溫6 min,熱解產物進入色譜柱被冷凍富集,熱解結束后,冷阱快速加熱,產物被采集進行色譜質譜分析。待色譜質譜分析結束后,對殘余的熱解樣品以同樣的升溫速率繼續升溫至350 ℃恒溫6 min,生成一系列新的熱解產物,每次熱解的溫度區間都是50 ℃,依次升溫至600 ℃。在每個溫度的熱解實驗之前都進行一次空白樣實驗確保前后不被干擾。
色譜條件:初始溫度40 ℃,恒溫1 min,以3 ℃/min升至290 ℃,恒溫40 min。氦氣作為載氣,離子源(EI)電離能為70 eV,離子源溫度為230 ℃,采用全掃描模式(m/z10-650),分流比為10∶1,譜庫為NIST 11。
1.1.2 Rock-Eval
Rock-Eval分析采用法國VINCI公司生產的Rock-Eval 6;總有機碳(TOC)分析采用美國LECO公司生產的CS-344型碳硫分析儀。
1.1.3 紅外光譜
紅外光譜分析采用美國Nicolet公司生產的NEXUS670型傅里葉變換紅外光譜儀,波數范圍為11 000~50 cm-1,分辨率是0.06 cm-1,波數精度≤±0.01 cm-1。
1.2 樣品特征
實驗樣品為采自美國綠河盆地古近系萊尼段的綠河頁巖經處理所得的干酪根。綠河頁巖干酪根樣品的基本地球化學特征及顯微組分特征見表1。綠河頁巖干酪根的制備如下:將綠河頁巖樣品粉碎進行索氏抽提72 h之后加入濃鹽酸于60 ℃充分反應6 h除去碳酸鹽巖,用蒸餾水洗至弱酸性除去清液;再加入40%的氫氟酸于60 ℃攪拌反應6 h除去硅酸鹽礦物,用蒸餾水洗至弱酸性除去清液。上述步驟分別重復處理兩次后,加入氯化鋅重液超聲離心除去黃鐵礦及其他礦物浮選出干酪根。最后在室溫下風干,充分研磨至200目以便在熱模擬實驗中能夠充分熱解。
2 實驗結果與討論
2.1 干酪根顯微組分、結構及各溫度點熱解產物組成特征
2.1.1 顯微組分特征
綠河頁巖有機質來源主要有以下兩部分:1)水體內豐富的細菌及水生生物;2)湖盆四周補給的水源或風等介質帶來的部分陸生植物[9]。但綠河頁巖干酪根中主要組分是腐泥組,含量為93%(表1),表明其有機質的主要來源為細菌和藻類等低等水生生物。總體上綠河頁巖干酪根屬于典型的低成熟樣品,其母質類型為I型,具有良好的生烴潛力,可以很好的用于熱模擬實驗,研究其生烴產物的詳細特征。
2.1.2 紅外光譜結構特征
對綠河頁巖干酪根樣品進行了紅外光譜分析,其譜圖如圖1所示,其中4 000~1 300 cm-1為官能團區,在3 600~3 200 cm-1范圍出現強的羥基(OH)峰,脂肪族CHx的伸縮、變形振動吸收峰主要出現在2 925 cm-1、2 852 cm-1、1 460 cm-1、1 376 cm-1;1 725~1 600 cm-1出現強的羰基(C=O)峰。在指紋區(1 300~600 cm-1),1 300~1 000 cm-1主要反映酚,醚的C-O伸縮振動;631 cm-1出現C-H的強峰。因此綠河頁巖干酪根樣品主要是含有甲基、亞甲基等脂肪族結構,含氧官能團如羰基、羥基等系列化合物或基團的混合物。

表1 樣品基本地球化學參數及顯微組分特征Table 1 Bulk organic geochemical and petrographic information for kerogen of Green River shale
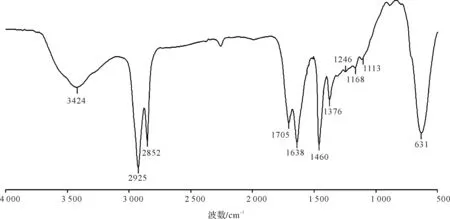
圖1 綠河頁巖干酪根的紅外譜圖Fig.1 FTIR spectra of Green River shale kerogen
2.1.3 各溫度點熱解產物組成特征
在每個溫度段生成的熱解產物具有很大的豐度差異。通過樣品熱解產物的色譜圖峰面積得到的豐度值曲線如圖2所示。低溫瞬時熱解產物主要是烴源巖中解析的吸附烴,所以本研究中干酪根樣品在300 ℃時熱解基本檢測不到產物。之后溫度升高連接在干酪根結構上的大分子裂解成小分子導致熱解產物逐漸增多,到450 ℃時達到高峰,在400 ℃、450 ℃、500 ℃三個溫度點上有著豐富的烷烴、烯烴成對出現(圖2,3)。在550 ℃時出現了一系列的長鏈烷烴及烯烴,且C29以后烷烴烯烴開始共流。600 ℃時熱解結束,和300 ℃時類似,基本無熱解產物。
(1) 300 ℃和350 ℃
對于烴源巖樣品而言,在300 ℃~350 ℃之前的熱解產物對應于Rock-Eval中S1,即代表源巖樣品在早期演化階段生成的游離烴。本次實驗采用的干酪根樣品在300 ℃時沒有熱解產物出現。溫度達到350 ℃時,有機質開始裂解生成一系列的熱解產物。少量的直鏈烯烴-1開始出現,并在高碳數時(C25~C28)與正構烷烴共流(圖3c)。在該溫度點的熱解產物與綠河頁巖樣品直接進行柱色層分離得到的飽和烴色譜圖分布類似但是也有明顯差異。這表明350 ℃的熱解產物是殘留的吸附烴與裂解烴混合的產物。在350 ℃熱解條件下生成了豐富的類異戊二烯烷烴如姥鮫烯-1等。
(2) 400 ℃
與350 ℃相比,熱解溫度為400 ℃時總的生烴量迅速增加,烯烴相對于烷烴含量也開始增加,干酪根開始大量裂解。碳數分布范圍為C4~C28(圖3d)。類異戊二烯烷烴含量也迅速增加。姥鮫烯-1的特征與350 ℃基本一致,并且依然是熱解產物中的最高峰。另外,一系列的碳鏈分布范圍為C7~C23的脂肪2-酮開始出現,并有微弱的奇偶優勢(圖4b),而且經鑒定2-酮比相鄰的正構烷烴少兩個碳。
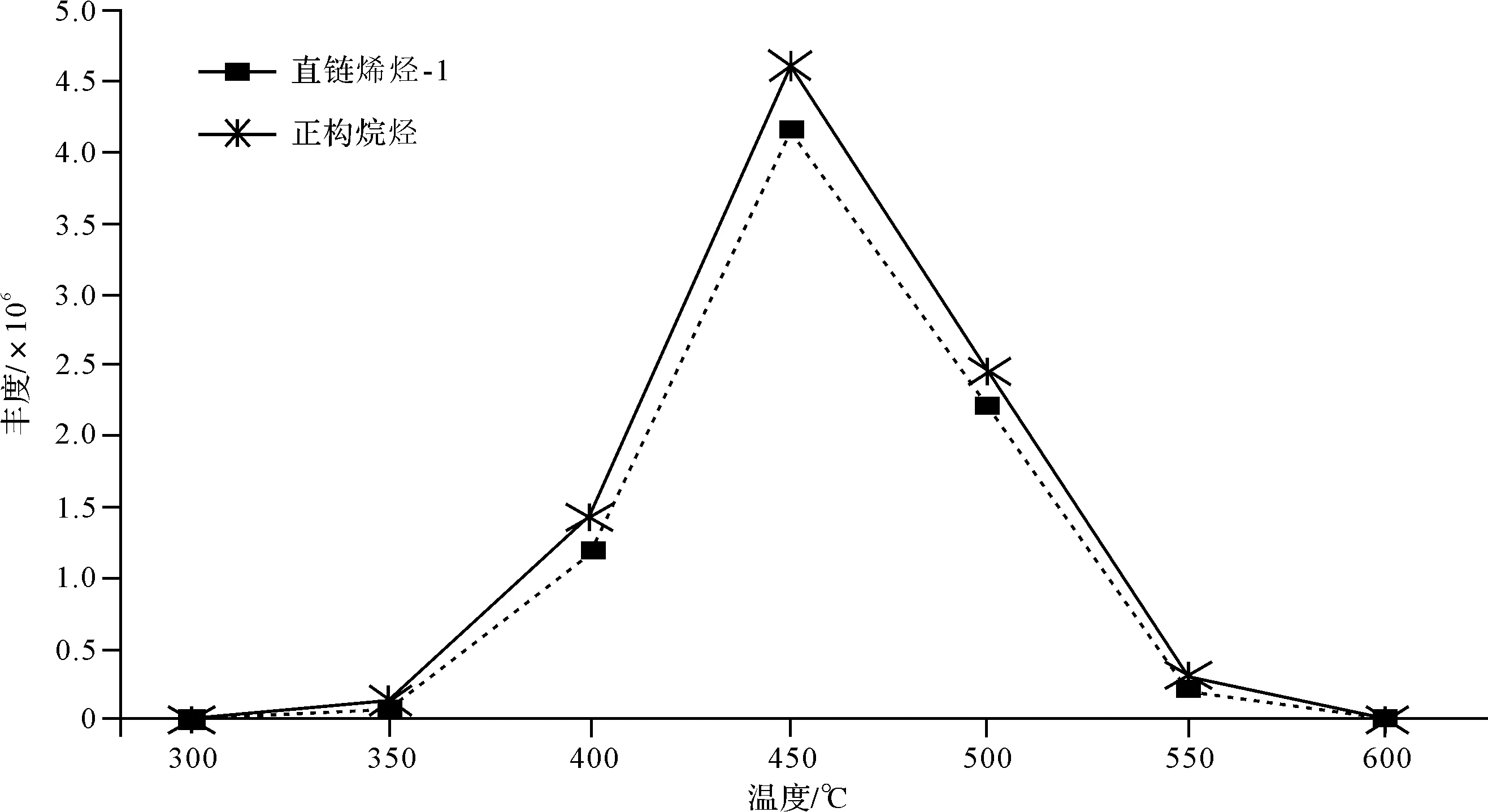
圖2 不同熱解溫度點正構烷烴和直鏈烯烴-1的相對豐度Fig.2 Relative amounts of n-alkanes and n-alkenes which were calculated from peak areas in the m/z 83+85 mass fragmentograms

圖3 不同溫度點熱解產物烷烴、烯烴分布圖(m/z 83 + 85)Fig.3 Mass fragmentograms for m/z 83 + 85 showing distributions of n-alkanes and n-alkenes doublets in pyrolyzates at different temperatures

圖4 綠河頁巖干酪根抽提產物及400 ℃、450 ℃時熱解產物中的脂肪酮(2-酮)分布質量色譜圖Fig.4 Mass fragmentograms for m/z 59 showing the distributions of n-alkan-2-ones in the extracts and pyrolysates at 400 ℃, 450 ℃ of kerogen of Green River shale
(3) 450 ℃和500 ℃
450℃是產烴高峰期(圖2,3),該階段主要是C8~C25成對出現的正構烷烴和直鏈烯烴,也含有豐富的類異戊二烯烴,但是姥鮫烷、植烷含量很低。隨著溫度的升高,產物的奇偶優勢逐漸消失,姥鮫烯-1的相對含量減少,脂肪酮亦被檢測到(圖4c),碳數分布范圍與400 ℃基本一致,但奇碳優勢基本消失。500 ℃熱解產物的分布和450 ℃時類似(圖3e,f)。主要組分為正構烷烴、烯烴。類異戊二烯烷烴的含量極低。
(4) 550 ℃和600 ℃
在550 ℃時熱解產物驟減,僅包含少量烴類。特別的是在該溫度點烴類主要為C27~C32高碳數烴類,最高峰為C29(圖3g)。而在600 ℃時基本沒有熱解產物產生(圖3h),表明在低于600 ℃條件下,有機質已經大量熱解。
2.2 討論
2.2.1 正構烷烴、直鏈烯烴-1
成對出現的正構烷烴和直鏈烯烴-1是典型低熟烴源巖的熱解產物。400 ℃、450 ℃、500 ℃三個溫度點中成對的烷烴、烯烴都是主要的熱解產物,且這三個溫度點中二者的分布趨勢相似,這表明在該溫度范圍附近,烷烴與烯烴的形成機理相似,綠河頁巖干酪根上含有豐富的烷基結構(圖1)在高溫、高強度能量下逐漸斷裂。從300 ℃到600 ℃六個溫度點生烴量先增加后降低,在450 ℃達到生烴高峰。明顯地,溫度升高至500 ℃時,碳鏈長度范圍略有縮短,低碳數烴類比例大幅增加(圖3),這主要是由于干酪根上連接的長鏈脂族結構的斷裂脫落形成的[10]。其中脂肪族酸經α或β脫羧生成正構烷烴,酯中一級醇經脫水形成直鏈烯烴[11]。隨著溫度的升高,在熱作用下長的烷基鏈逐漸斷裂形成短鏈烴類。550 ℃時熱解產物比較特別,僅檢測到豐富的C27~C31系列長鏈脂肪烴類化合物(圖3g),這些長鏈脂肪烴類化合物可能是綠河頁巖干酪根中類似綠藻的相關組分通過C-C、C-O共價鍵連接的組分經熱解所形成的產物[7,10,12]。
綠河頁巖干酪根熱解產物在低溫條件下具有微弱的奇偶優勢,隨著溫度升高到500 ℃基本消失。通常認為,OEP值介于1.2~1.4時,有機質處于低熟階段;介于1.0~1.2時,有機質處于成熟階段[8],在本次研究中350 ℃時OEP值為1.34印證了綠河頁巖干酪根處于低熟階段,溫度升高至400 ℃、450 ℃和500 ℃過程中OEP值依次降低分別為:1.31、1.29、1.11(表2),表明有機質成熟度隨著熱解溫度的升高逐漸增加。550 ℃時,因該溫度點熱解產物為C27~C32的長鏈烷烴,跟前面四個溫度點的碳數峰不一致,故未計算其OEP值。
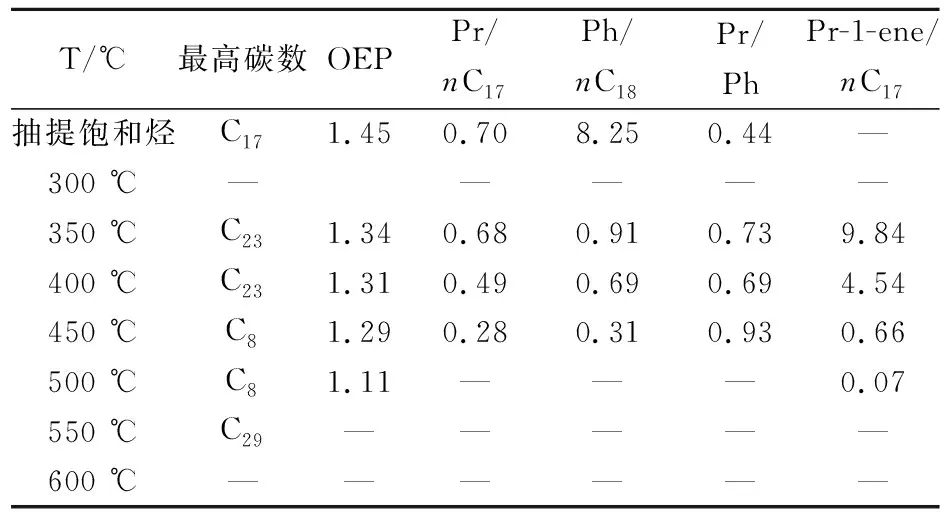
表2 不同條件下綠河頁巖(干酪根)熱解烴地球化學參數Table 2 Basic parameters ofkerogen of Green Rivershale produced at different conditions
正構烷烴/直鏈烯烴-1比值是研究該類物質特征的重要參數。圖5是400 ℃、450 ℃、500 ℃三個不同溫度點的烯烴/烷烴比率曲線,可以發現其比值變化的總體趨勢是一致的,從C8~C11先是降低,接著保持平穩的上升趨勢,且均在C21時開始出現比值突變點。尤其在高碳數(C21~C28)間其比率出現明顯的奇碳優勢。蔣啟貴等[2]認為突變點很有可能與熱解條件、烴源巖類型及所處的演化階段有關。在C11~C21之間,400 ℃、450 ℃、500 ℃各溫度點的平均比率依次為:1.11、1.01、0.98,隨著溫度升高,比值逐漸降低。這說明瞬時熱解溫度升高的過程中,烯烴的產率相對于烷烴逐漸增加,即短暫的高溫條件下可能更容易形成烯烴,而不同于長時間高溫熱解,有充足的能量和時間獲取氫發生加成反應而形成烷烴。
2.2.2 類異戊二烯烴
類異戊二烯烴也是熱解產物中的主要成分,除去低溫條件下殘留的吸附烴之外,隨著溫度的升高(400 ℃~550 ℃),類異戊二烯烴所占的比例逐漸減少,到500 ℃時基本消失(圖3)。異構烷烴類的產出主要是由于類異戊二烯結構的酯基斷裂[11]。姥鮫烯-1是瞬時熱解的特征產物,主要出現在350 ℃和400 ℃,并伴隨著少量的姥鮫烯-2出現,兩者通常認為是來源于葉綠素的植醇側鏈,最初通過醚鍵連接到干酪根的大分子結構上,在高溫情況下斷裂形成,這與姥鮫烷等產物的來源一致[8,13]。Larteretal.[14]通過標準物質熱解模型研究發現姥鮫烯-1的前驅物很可能是C-C及C-O鍵合的部分,其在地質過程中產生姥鮫烷,而在熱解過程中可能生成姥鮫烯。表2顯示了隨著溫度的變化姥鮫烯-1/nC17比值(Pr-1/nC17)明顯降低,姥鮫烯-1以較易斷裂的醚鍵與干酪根核連接,裂解所需活化能低,所以較弱的熱作用下即可形成。
在350 ℃、400 ℃、450 ℃溫度條件下檢測出了姥鮫烷和植烷。在地質條件下,它們主要是光合生物中葉綠素a及細菌葉綠素a和b的植基側鏈經過氧化作用或還原作用形成的[8]。但是本研究過程中出現了豐富的姥鮫烯-1,表明上述過程并不是姥鮫烷和植烷在熱解模擬過程中形成的主要途徑,而很大程度上是由綠河頁巖干酪根基質中非水解C-C或C-O鍵連接的類異戊二烯部分熱解形成[6,14]。一般而言,姥植比(Pr/Ph)是有機地化研究中常用來判識有機質古環境的氧化還原程度有意義的參數[8]。Pr/Ph>1時,表明其沉積環境偏氧化性,古環境水體較淺;Pr/Ph<1時,主要為還原性的膏鹽沉積環境。本研究中綠河頁巖Pr/Ph值明顯小于1,說明綠河頁巖主要形成于還原性沉積環境中。此外,通常,隨著熱成熟度的增加,姥植比會增大,而Ph/nC18則減小[15],可從表中發現Pr/Ph總體趨勢是變大,但在400 ℃時降低,而后再增加,經重復試驗結果一致。這一方面說明姥植比受熱成熟度的影響,所以使用該參數來辨識烴源巖氧化還原條件的專屬性不高;另一方面,姥植比隨成熟度增加而變大并不具有系統性[8]。
2.2.3 脂肪酮
脂肪酮是許多油頁巖、原油以及深海沉積物、湖泊沉積物等中常見的但含量極少的重要組分[16-23]。在綠河頁巖干酪根的熱解產物中也檢測到了部分酮類(脂肪2-酮和降姥鮫酮等),這與紅外光譜中顯示的該樣品中強的羰基峰相對應(圖1)。本研究中,400 ℃和450 ℃兩個溫度點都含有豐富的降姥鮫酮,400 ℃時相對豐度更高。降姥鮫酮主要是連接在烴類上的長的側鏈降解衍生物[20]。相比之下綠河頁巖經抽提分離并用于GC-MS分析也發現有降姥鮫酮,且占據最主要地位,另外,抽提物中還含有少量的2-酮(圖4a)。國內外許多研究人員發現正構脂肪酮多是與微生物的氧化作用或者脂肪酸的氧化和隨后的脫羧反應有關[17,20-23],在此次熱解過程中400 ℃后脂肪酮的出現,表明熱作用也是其產生的一個主要因素。相比于400 ℃,450 ℃時長鏈脂肪酮豐度明顯低于短鏈脂肪酮含量,這也說明其含量變化類似于正構烷烴,隨著溫度升高,長鏈烴類共價鍵斷裂形成低碳數熱解產物。前人在熱解產物中也曾檢測到豐富的3-酮,9-酮,10-酮等多種不飽和的異構體[9,23],而在本研究中則沒有發現其他碳位數上的脂肪酮。
2.2.4 萜烷
綠河油頁巖中含有豐富的五環三萜烷、三環萜烷及少量的四環萜烷,還有豐富的γ-蠟烷(圖6a)。圖6b~f經鑒定除部分萜類產物可明顯辨認之外,其他都屬于非常規的系列化合物。這些化合物應屬于熱解過程中形成的中間產物。由圖6b~f這一系列不同溫度萜類產物可以發現,在350 ℃時藿烷有產出,而400 ℃時卻沒有,表明在350 ℃干酪根中仍然殘存有少量的吸附熱解烴,但同時在該溫度點條件下干酪根已經開始裂解。另外,由圖6b~e明顯看出,產出時間在藿烷之前的一系列化合物異常豐富,并且隨著溫度的升高低碳數烴類的豐度逐漸增加;藿烷系列在550 ℃高溫下依然很豐富,且在除400 ℃之外的幾個溫度點中都檢測到了藿烯。對比不同溫度的熱解產物變化,可以看到不同溫度狀態下產物的變化趨勢,為詳細認證地質體演化過程中生物標志化合物的中間產物及其形成機理的研究提供了重要依據。

圖5 不同溫度點同碳數正構烷烴與直鏈烯烴-1的比值Fig.5 Ratios of n-alkanes/n-alkenes at different temperatures
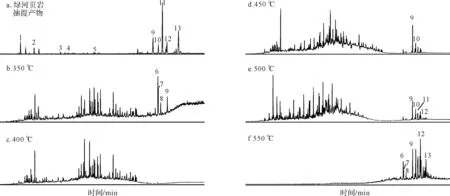
圖6 綠河頁巖抽提產物和其干酪根熱解產物中萜烷質量色譜圖(m/z 191)Fig.6 m/z 191 mass chromatograms of extracts and pyrolyzates of Green River shale kerogen
此次干酪根分步熱解模擬實驗中甾烷的豐度極低,說明綠河頁巖干酪根中甾骨架相比于萜類含量更少。在先前綠河頁巖樣品的熱模擬實驗研究中檢測到了一定含量的甾烷系列,但其相對豐度與抽提物相比也是低數個量級,目前主要認為造成這種差別的原因是受熱溫度,時間不同,實驗室采用的高溫快速裂解法,而自然界則是低溫慢速度的裂解[6]。
2.2.5 綠河頁巖600 ℃一步熱解
圖7展示了利用Py-GC-MS由100 ℃按200 ℃/min的升溫速率直接升到600 ℃高溫情況下,綠河頁巖干酪根樣品熱解得到的正構烷烴、烯烴、脂肪酮及萜烷等產物的質量色譜分布圖。由圖7a可以明顯看出直接升到600 ℃熱解產物中正構烷烴、烯烴的分布特征與分步熱解法中450 ℃和500 ℃分布特征類似(圖2e,f),但類異戊二烯烴大量缺失;圖7c萜烷分布與圖6f相近。而瞬時分步熱解過程中產生了較一步熱解更多的組分,它提供了一種快捷有效地研究干酪根或者是其他類似聚合物的方法。不同溫度條件下正構烷烴、烯烴、脂肪酮、甾萜烷等產物的分布變化相比直接高溫度熱解產物要直觀清晰。因此分步熱解對于研究烴類演化終端產物的前驅物具有一定的指導意義,并有很大機會發現并研究一些新的生物標志化合物。
3 結論
(1) 在300 ℃~600 ℃設定的七個分步熱解溫度點中,干酪根的生烴量基本符合正態分布。在低溫階段,產烴量較少,450 ℃達到生烴高峰,之后再逐漸減少,直至600 ℃生烴結束。在350 ℃之前,熱解產物主要是干酪根中殘存的游離態吸附烴,350 ℃以后為熱解烴,350 ℃到500 ℃之間生烴機制基本一致,但在550 ℃生烴機理(烴類來源)明顯發生變化。
(2) 隨著熱解溫度的升高,干酪根經熱解產生的不同有機組分特征呈現出明顯的規律性。熱解產物中短鏈烴類的比例逐漸增加,類異戊二烯烴的含量逐漸降低,且姥植比這一傳統的評價烴源巖沉積氧化還原環境的生標參數有一定的局限性。
(3) 綠河頁巖干酪根熱解過程中檢測到了豐富的脂肪2-酮,其來源可能是在熱力作用下由烷烴等相近組分轉變而形成;而且脂肪2-酮僅出現在450 ℃以下,說明高溫度條件下脂肪酮不易存在。
(4) 分步瞬時熱解法與氣相色譜質譜聯用提供了一種有效研究烴源巖等樣品演化過程及產物組分變化的方便快捷的方法。

圖7 綠河頁巖干酪根直接一步熱解到600 ℃時產物質量色譜圖(化合物6-13見圖6)Fig.7 The distributions of n-alkanes/alkenes, n-alkan-2-ones and terpanes produced by direct pyrolysis of Green River shale kerogen at 600 ℃(compound 6-13 has been identified in Fig.6)
參考文獻(References)
[1] 鄭倫舉,馬中良,何生. 海相烴源巖二次生烴潛力定量評價新方法[J]. 沉積學報,2012,30(3):594-602. [Zheng Lunju, Ma Zhongliang, He Sheng. The new method for quantitative evaluation secondary hydrocarbon generation potential of marine source rocks[J]. Acta Sedimentologica Sinica, 2012, 30(3): 594-602.]
[2] 蔣啟貴,馬媛媛,李欣. 單冷阱熱解色譜儀在烴源巖評價中的應用[J]. 石油實驗地質,2011,33(5):546-551,558. [Jiang Qigui, Ma Yuanyuan, Li Xin. Application of single cold trap pyrolysis chromatography in source rock evaluation[J]. Petroleum Geology & Experiment, 2011, 33(5): 546-551, 558.]
記者了解到,今年10月份以來,民營企業的經營情況和融資狀況受到各方關注,財政部、人民銀行、銀保監會等多個部門密集出臺扶持政策,金融業加大對民企有效的金融支持,解決民企融資難融資貴問題,幫助民企紓困解難,一些企業也切身感受到變化。
[3] 孫永革,楊中威,謝柳娟,等. 基于裂解色譜質譜技術的瓊東南盆地漸新統源巖生烴潛力評價[J]. 石油學報,2010,31(4):579-585. [Sun Yongge, Yang Zhongwei, Xie Liujuan, et al. Pyrolysis-gas chromatography-mass spectrography as a method to evaluate hydrocarbon generation potential of Oligocene source rocks from Qiongdongnan Basin, offshore South China Sea[J]. Acta Petrolei Sinca, 2010, 31(4): 579-585.]
[4] 孫永革,盛國英,傅家謨. 我國主要含煤油氣盆地煤系源巖PY-GC熱解產物組成及意義[J]. 沉積學報,1995,13(2):120-127. [Sun Yongge, Sheng Guoying, Fu Jiamo. Pyrolysate compositions of source beds from major Chinese coal-bearing petroliferous basins and their geochemical significance[J]. Acta Sedimentologica Sinica, 1995, 13(2): 120-127.]
[5] 劉大永,彭平安. 鏡質組與其混合溶劑抽余物瞬時熱解產物分布特征及其油氣地質意義[J]. 科學通報,2006,51(14):1696-1701. [Liu Dayong, Peng Ping’an. Pyrolysates of raw vitrinites and their residues after CS2-NMP solvent extraction and its significance for petroleum geology[J]. Chinese Science Bulletin, 2006, 51(14): 1696-1701.]
[6] 傅家謨,秦匡宗. 干酪根地球化學[M]. 廣州:廣東科技出版社,1995. [Fu Jiamo, Qin Kuangzong. Kerogen geochemistry[M]. Guangzhou: Guangdong Science and Technology Press, 1995.]
[7] Larter S R. Application of analytical pyrolysis techniques to kerogen characterization and fossil fuel exploration/exploitation[M]//Voorhees K J. Analytical pyrolysis. Amsterdam: Elsevier, 1984: 212-275.
[8] Peters K E, Walters C C, Moldowan J M. The biomarker guide: interpreting molecular fossils in petroleum and ancient sediments[M]. 2nd ed. Cambridge, UK: Cambridge University Press, 2005.
[9] Robinson W E. Origin and characteristics of Green River oil shale[J]. Developments in Petroleum Science, 1976, 5: 61-79.
[10] Zhang Z R, Volkman J K, Xie X M, et al. Stepwise pyrolysis of the kerogen from the Huadian oil shale, NE China: Algaenan-derived hydrocarbons and mid-chain ketones[J]. Organic Geochemistry, 2016, 91: 89-99.
[11] 尚慧云,李晉超,郭舜玲. 有機地球化學和熒光顯微鏡技術[M]. 北京:石油工業出版社,1990:90. [Shang Huiyun, Li Jinchao, Guo Shunling. Organic geochemistry and fluorescence microscopy[M]. Beijing: Petroleum Industry Press, 1990: 90.]
[12] Derenne S, Largeau C, Behar F. Low polarity pyrolysis products of Permian to recentBotryococcus-rich sediments: First evidence for the contribution of an isoprenoid algaenan to kerogen formation[J]. Geochimica et Cosmochimica Acta, 1994, 58(17): 3703-3711.
[13] Larter S R, Solli H, Douglas A G, et al. Occurrence and significance of prist-1-ene in kerogen pyrolysates[J]. Nature, 1979, 279(5712): 405-408.
[14] Larter S R, Horsfield B. Determination of structural components of kerogens by the use of analytical pyrolysis methods[M]//Engel M H, Macko S A. Organic geochemistry. Boston, MA: Springer, 1993: 271-287.
[15] ten Haven H L, de Leeuw J W, Rullk?tter J, et al. Restricted utility of the pristane/phytane ratio as a palaeoenvironmental indicator[J]. Nature, 1987, 330(6149): 641-643.
[16] George S C, Jardine D R. Ketones in a Proterozoic dolerite sill[J]. Organic Geochemistry, 1994, 21(8/9): 829-839.
[17] 謝樹成,梁斌,顧延生,等. 脂肪酮分子在第四紀古土壤中的分布及其古氣候意義[J]. 古生物學報,2008,47(3):273-278. [Xie Shucheng, Liang Bin, Gu Yansheng, et al. Distributions ofn-alkan-2-ones in quaternary paleosols indicative of paleoclimate changes[J]. Acta Palaeontologica Sinica, 2008, 47(3): 273-278.]
[18] 康晏,王萬春,任軍虎,等. 柴達木盆地第四系生物氣氣源巖中脂肪酮的檢出及其成因探討[J]. 天然氣地球科學,2005,16(6):804-808. [Kang Yan, Wang Wanchun, Ren Junhu, et al. Identification of aliphatic ketones in biogeneic gas source rock in quaternary of Qaidam Basin and approach to their sources[J]. Natural Gas Geoscience, 2005, 16(6): 804-808.]
[19] Ortiz J E, Díaz-Bautista A, Aldasoro J J, et al.N-Alkan-2-ones in peat-forming plants from the Roanzas ombrotrophic bog (Asturias, northern Spain)[J]. Organic Geochemistry, 2011, 42(6): 586-592.
[20] Rzama A, Benharref A, Arreguy B, et al. Volatile compounds of green microalgae grown on reused waste water[J]. Phytochemistry, 1995, 38(6): 1375-1379.
[21] WuY Q, Wang Y L, Lei T Z, et al. Possible origin of high molecular weightn-alkan-2-ones in jurassic bitumens from the Sichuan Basin in Southwest China[J]. Chemistry and Technology of Fuels and Oils, 2012, 48(3): 195-201.
[22] Gatellier J P L A, de Leeuw J W, Sinninghe Damsté J S, et al. A comparative study of macromolecular substances of a Coorongite and cell walls of the extant algaBotryococcusbraunii[J]. Geochimica et Cosmochimica Acta, 1993, 57(9): 2053-2068.
[23] Derenne S, Largeau C, Hetényi M, et al. Chemical structure of the organic matter in a Pliocene maar-type shale: ImplicatedBotryococcusrace strains and formation pathways[J]. Geochimica et Cosmochimica Acta, 1997, 61(9): 1879-1889.

