非小細胞肺癌患者電視輔助胸腔鏡肺葉切除術中轉開胸的影響因素分析
李 海,徐 剛,宋永祥,蔡慶勇,李 劍,陳 成
研究[1]報道電視輔助胸腔鏡手術(video-assisted thoracic surgery,VATS)的中轉開胸率約為2.5%~11.8%。若鏡下損傷重要血管,短時間內可致患者大量失血,危及生命。因此,術前了解中轉開胸的影響因素,術中結合患者情況判斷中轉開胸的時機,必要時果斷中轉開胸,可降低手術風險,保證患者安全[2]。該研究以行VATS中轉開胸及同期未中轉開胸的非小細胞肺癌(non-small-cell lung cancer,NSCLC)患者為研究對象,探討中轉開胸的影響因素。
1 材料與方法
1.1病例資料以2014年1月~2017年6月遵義醫學院附屬醫院胸外科行VATS治療的NSCLC患者為研究對象。入選標準:① 術后病理證實為NSCLC;② 手術為三孔胸腔鏡下根治性肺葉切除。排除標準:① 多肺葉腫瘤;② 既往肺部手術史;③ 手術為全肺切除;④ 病例資料不完整。基于以上標準,分為兩組共182例患者納入最終分析:中轉開胸65例(中轉組)、同期腔鏡手術117例(腔鏡組)。兩組患者一般情況及比較見表1。

表1 兩組患者一般情況比較
1.2手術方法手術均于全麻下行雙腔氣管插管,術中單肺通氣。手術通過三個腔鏡孔完成,鏡下操作順序與傳統開胸肺葉切除基本相同,對原發肺癌患者均行淋巴結清掃。術中因胸膜粘連,縱隔、肺門淋巴結腫大、粘連或鈣化等,鏡下處理困難,存在損傷或可能損傷血管引起大出血時,將操作孔向肩胛下角延長,逐層開胸,撐開器撐開肋骨,直視下行肺葉切除及淋巴結清掃,術后安置引流管并常規關胸。
1.3比較指標比較中轉開胸組與腔鏡組患者的性別、年齡、吸煙史、肺結核病史、腫瘤類型、手術組別。根據術前胸部螺旋CT掃描確定腫瘤所在部位并測量腫瘤最大直徑。胸膜粘連程度參考Oncel et al[3]建立的動物模型及舒敬奎 等[4]分級方法分為0~5級,具體判別為:無胸膜粘連為0級;經牽拉即可分離的疏松胸膜粘連為1級;需鈍性分離的胸膜粘連為2級;需銳性分離的胸膜粘連為3級;胸膜粘連分離時出現胸膜損傷為4級;胸膜粘連分離時出現胸膜下組織損傷為5級。術中建立第一個腔鏡孔后腔鏡探查整個術側胸膜腔,不同部位胸膜粘連不同時以最嚴重的級別記錄。

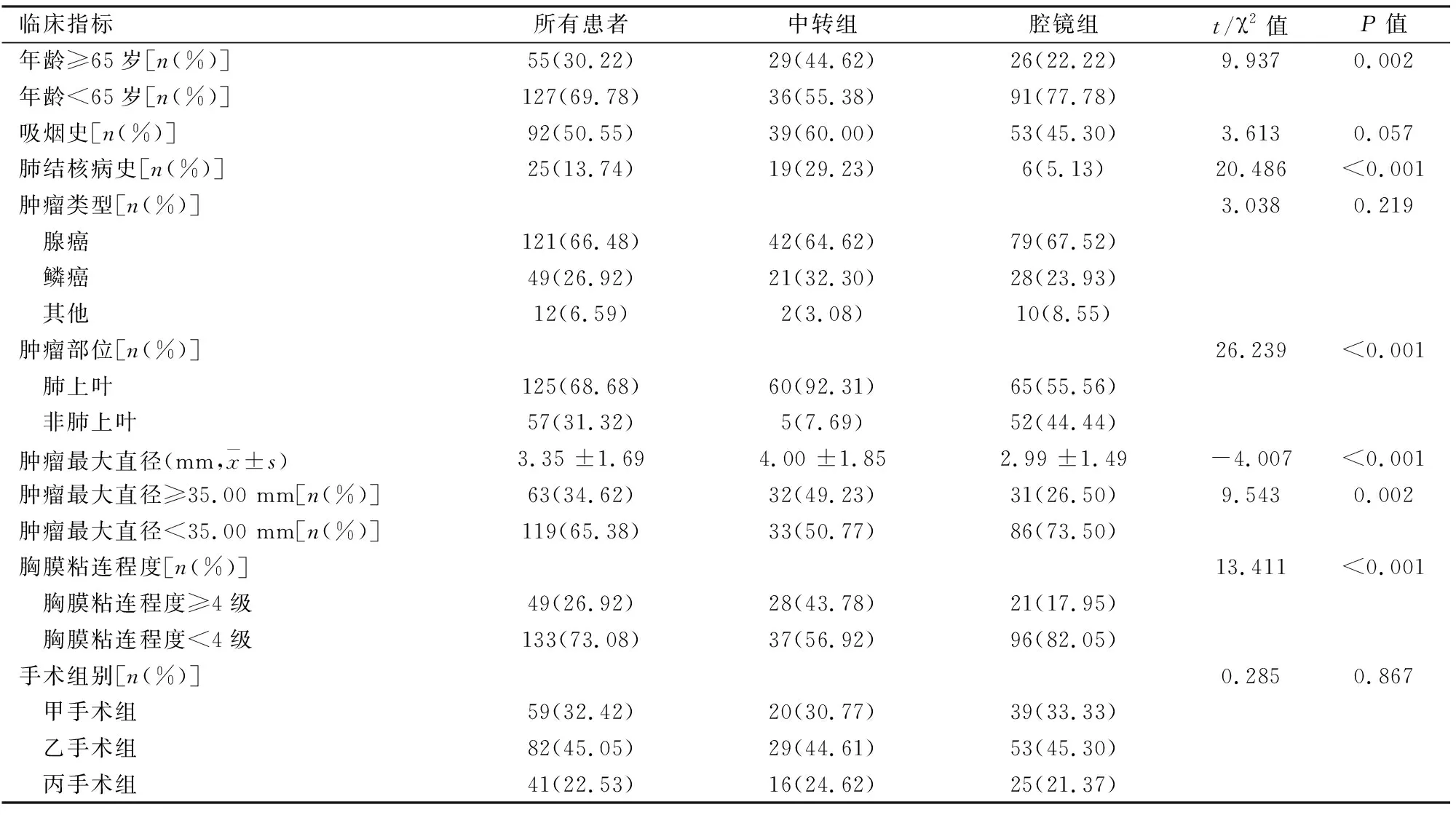
表2 非小細胞肺癌患者行電視輔助腔鏡肺葉切除術中轉開胸的單因素分析

表3 非小細胞肺癌患者行電視輔助腔鏡肺葉切除術中轉開胸的多因素Logistic回歸分析結果
2 結果
單因素分析結果顯示:男性患者、年齡≥65歲、肺結核病史、腫瘤位于上肺、腫瘤直徑≥35.00 mm、胸膜粘連程度≥4級與中轉開胸有關(P<0.05)。見表2。
多因素Logistic回歸分析結果顯示:肺結核病史、腫瘤位于上肺、胸膜粘連程度≥4級為NSCLC患者VATS中轉開胸的獨立影響因素(P<0.05)。見表3。
3 討論
VATS在臨床上應用甚廣,中轉開胸的情況亦多見[5-8]。既往研究根據淋巴結鈣化粘連、術中出血、腫瘤浸潤程度等[9]術中情況判斷是否中轉開胸,本研究從患者術前相關臨床資料及術中建立腔鏡孔后探查胸膜粘連程度來分析中轉開胸的影響因素。
肺結核與肺癌均為我國常見呼吸系統疾病,近年兩者并發病例數明顯增多[10]。肺結核發病隱匿,臨床癥狀不典型,同時受經濟及教育水平影響,部分患者患病而不自知。該類患者肺結核病史長且未及時診治,術中常見淋巴結鈣化粘連明顯,局部解剖結構不清,術區血管難以辨別。肺結核好發于雙肺上葉,切除位于肺上葉的腫瘤時更易受結核病變所致的淋巴結粘連或鈣化影響,從而中轉開胸。
肺上葉動脈分支多,血管粗,可顯露長度短,易損傷。其中,左肺上葉動脈分支短且多,右肺上葉肺動脈第一支在所有肺動脈分支中距肺門最近,術中易損傷出血。同時,肺血管變異率較高且血管壁較其他部位薄而脆[11],易受縱隔、肺門淋巴結粘連或轉移的影響, 鏡下游離時易受損傷。本研究中腫瘤位于上肺占69%(125/182),上葉腫瘤中轉開胸占92%(60/65),結果同李運 等[12]相近。術中大多因淋巴結鈣化粘連嚴重或腫瘤包繞縱隔、肺門,鏡下分離可能損傷血管,為避免大出血轉而開胸。
胸膜的炎癥反應及炎癥恢復過程均可導致胸膜粘連。對胸膜粘連程度的判斷臨床尚未見統一標準,本研究將胸膜粘連分為0~5級。彌漫疏松的條索狀或膜狀粘連可于鏡下處理,粘連疏松時經鈍銳結合的方法亦可于VATS下游離胸腔,且整個過程中出血量較少,大多無需中轉開胸。而分離粘連時損傷胸膜或胸膜下組織時,即胸膜粘連程度≥4級時中轉開胸情況增多。胸腔粘連致密且范圍較大時,鏡下處理存在一定難度,操作時間長且因損傷胸膜或胸膜下組織往往滲血明顯,常需中轉開胸。
術前了解中轉開胸的影響因素,術中結合患者具體情況,必要時果斷中轉開胸,保證患者安全。
參考文獻

