藥品質量投訴調查實例及對策分析
周華琴
(上海上藥新亞藥業有限公司,上海201203)
0 引言
作為藥品生產企業的QA人員,在日常工作中會收到各種涉及本公司產品信息、質量投訴、咨詢等方面的反饋,通常將這些反饋歸納為3種情況:
(1)藥品的不良反應,如皮疹、腹瀉等,需按《藥品不良反應報告和監測管理辦法》進行處理,并按需上報;
(2)不合理用藥,如藥品因配伍禁忌產生的沉淀渾濁,溶液放置時間過長導致的顏色異常等;
(3)由質量缺陷引起的投訴,如包裝破損、瓶內異物、顏色發黃等。
對于收到的藥品質量投訴及不良反應信息,均應記錄在冊;分析調查由產品質量缺陷引起的投訴,采取必要的糾正與預防措施,避免同一質量問題反復發生。
抗生素粉針劑作為處方藥,在藥品的生產和流通環節可能會出現各種問題,最終影響醫護人員和患者的使用,因此,對于由質量缺陷引起的用戶質量投訴,應通過對藥品生產各工序和藥品檢驗環節進行分析調查,查找出引發質量問題的原因,采取必要的糾正與預防措施,確保產品質量和用藥安全。
本文以某抗生素粉針劑產品的質量投訴為例,梳理和分析導致出現質量缺陷的原因,并探討相應的對策。
1 藥品質量投訴調查及對策流程
1.1 樣品的確認
根據用戶提供的相應照片或實樣,對收到的投訴產品進行包裝形式、外觀的確認,可與同品種、同批次產品的留樣進行比對,以確認其是否為我公司生產的產品,并對產品包裝的完整性進行確認。
1.2 原因分析
各部門相互配合,對被投訴產品的生產、檢驗相關環節進行調查分析及確認,查找引起質量缺陷的原因,必要時對原因進行模擬驗證。
1.2.1 生產方面
對被投訴產品的生產過程進行追溯。追溯被投訴產品的批生產記錄、崗位記錄,復核生產時所使用的原輔料、生產設備性能、生產工藝過程參數控制、生產環境以及人員的操作等環節是否有異常情況發生;追溯相關設備的檢修、運行情況;追溯空氣凈化、水處理等公用系統的運行情況。必要時,對相關的其他批次的生產過程進行追溯。
1.2.2 檢驗方面
對被投訴產品的批檢驗記錄進行復核,并復核檢驗時所用的原輔料、包裝材料以及成品檢驗過程是否有異常情況發生。
如需對被投訴產品內在質量進行進一步確認的,可對被投訴樣品或留樣產品進行檢驗。
1.2.3 儲存方面
對被投訴產品的儲存過程進行復核,檢查其是否有異常情況發生,調取溫濕度監控記錄等。
1.2.4 運輸方面
對于有特殊儲存條件的被投訴產品(對溫濕度、光照比較敏感的產品),可追溯其運輸過程的貯藏記錄等。
1.3 對策的制定、實施及效果確認
對于由質量問題引起的投訴,制定相關糾正與預防措施,并對糾正與預防措施的實施效果進行跟蹤確認。
2 投訴調查實例分析
在某用戶反饋的一批抗生素粉針劑產品中,發現有一瓶瓶內有異物,經溝通收到投訴樣品后,立即展開調查,并進行產品確認、原因分析、對策制定以及對策的實施和效果確認,以保證我公司產品的質量。
2.1 產品確認
將投訴樣品與我公司同一批號、同一規格的留樣產品進行比對,發現包裝形式和外觀完全一致,確認為我公司產品,且產品包裝完整性良好。
對投訴樣品中的藥粉進行成分分析,發現成分與標簽一致,異物取出后不溶于水,為6mm左右的白色塑料材質異物,初步分析該異物可能是在生產環節中帶入。
2.2 原因分析
結合該產品的生產工藝,確認白色異物的成分和帶入原因。
抗生素粉針劑產品的生產工藝如圖1所示。由于膠塞與抗生素模制瓶都是與藥品直接接觸的包裝材料,且產品分裝崗位是高污染風險崗位,因此在產品中帶入上述塑料材質異物的環節和崗位可能是玻璃瓶的清洗滅菌、膠塞的清洗滅菌和分裝崗位。
2.2.1 抗生素瓶的清洗滅菌
抗生素瓶拆除內層塑料包裝袋后推入洗瓶機前端的過渡輸送帶,經軌道進入超聲波洗瓶機;瓶體經超聲波預洗后,再用注射用水、潔凈壓縮空氣依次進行“三水三氣”的噴淋、清洗、吹干;完成清洗的抗生素瓶再經隧道滅菌烘箱進行滅菌干燥并冷卻;最后在RABS保護下出瓶,傳入分裝機分裝崗位。
在日常生產中,洗瓶崗位未出現過設備維修及其他異常情況,洗瓶機運行情況良好,人員和環境亦無類似異物帶入,此工序可能帶入異物的環節為玻璃瓶內本身帶入和拆除塑料包裝袋時帶入。若是上述兩種情況帶入異物,且經洗瓶工序未能沖洗去除,經過隧道烘箱高溫滅菌干燥后應呈現黃色或黑色的烤焦殘留物,與投訴的白色異物不符。因此,可以排除該異物在玻璃瓶清洗滅菌崗位帶入的可能性。
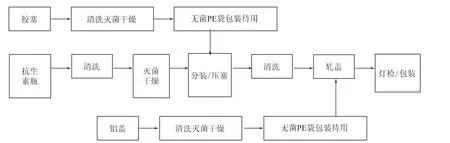
圖1 抗生素粉針劑產品的生產工藝流程圖
2.2.2 膠塞的清洗滅菌
膠塞拆除內層塑料包裝袋后,經真空吸料送入全自動膠塞清洗機內清洗,分別經過純化水清洗和注射用水清洗后,再經純蒸汽滅菌與真空干燥。干燥冷卻后,在膠塞清洗機出料,在RABS內裝入無菌PE袋中,隨后進行塑封備用。
在日常生產中,膠塞清洗滅菌工序未出現設備維修及其他異常情況,膠塞清洗機運行情況良好,人員和環境亦無類似異物帶入,此工序可能帶入異物的環節為膠塞本身帶入和拆除塑料包裝袋時帶入。在膠塞拆包時,需要用剪刀剪開包裝膠塞的塑料袋,可能會產生微小的塑料屑,如果塑料屑粘在膠塞上或塞芯內,則在清洗和濕熱滅菌過程中可能無法被去除。因此,膠塞清洗滅菌崗位存在帶入白色塑料異物的可能性。
2.2.3 分裝崗位
在分裝崗位中,原料粉經過螺桿分裝機完成定容量加粉及壓塞的過程。螺桿分裝機原理:電機帶動主動輪,通過同步帶帶動抗生素瓶間歇輸送,并間接帶動下粉連軸器,驅動螺桿旋轉,將原料粉定容量加至瓶內,再通過振蕩盤與軌道將膠塞定向輸送,并在軌道末端釋放膠塞,送入壓塞機構,完成膠塞的壓入。整個過程在RABS中完成。
現分析分裝崗位的人、機、料、環四個方面帶入異物的可能性。
2.2.3.1 人員
我公司生產的抗生素粉針劑通過螺桿分裝機進行分裝,原料桶在RABS中開啟,通過蝶閥與分裝機對接,原料粉經送粉管加入粉斗,通過攪拌后由螺桿和小嘴巴加入抗生素瓶中,壓塞后的產品通過傳送帶進入軋蓋間。整個過程的操作人員均不接觸原料桶內部,對分裝機的必要干預也是通過RABS上的隔離手套進行,且RABS在生產過程中始終處于A級層流的保護下。同時,在分裝崗位的操作人員都是經過培訓和有資質的人員。綜合分析認為,該異物不可能由分裝間的人員操作時帶入。
2.2.3.2 物料
原料是從合格供應商處采購,原料粉使用藥用鋁瓶包裝,入廠檢驗均符合法定標準及我公司內控標準。原料粉分裝前,車間質量員對每個鋁瓶的原料進行可見異物檢查,待檢查合格后方可進行分裝。若異物來自原料藥,原料粉是送入加料箱并通過攪拌后由小嘴巴處加入抗生素瓶中,而小嘴巴孔和螺桿都是配套的。以投訴中的異物體積而言,是不可能經過小嘴巴孔加入到抗生素瓶中的。
膠塞經清洗滅菌后,用無菌雙層PE袋密封待用,使用前的膠塞在RABS緩沖區拆包,拆包過程中可能會帶入塑料材質的異物。但是若由該工序帶入塑料異物,應該為暗透明色,這與投訴的白色異物不符。
2.2.3.3 設備、環境
通過查閱分裝崗位當天的空調系統及設備發現其運行狀況良好,并無異常情況出現,且環境及各設備中均無此類白色塑料材質物品,故該異物不可能由設備、環境中帶入。
2.3 模擬驗證
圖2為被投訴樣品(塑料屑)。為進一步確認白色異物是否為塑料袋屑和是否由膠塞清洗滅菌崗位帶入,我們進行了模擬實驗,將塑料袋屑放置于膠塞內芯中,然后按日常膠塞清洗滅菌程序進行操作,經清洗、滅菌、干燥與冷卻后,將放有塑料屑的膠塞取出,發現其塞芯內的塑料屑與被投訴產品中的異物外觀上基本相似,如圖3所示。因此,認為被投訴產品中的異物是膠塞清洗前的拆包過程中帶入的塑料包裝屑。

圖2 被投訴樣品(塑料屑)

圖3 驗證實驗中的塑料屑
3 對策制定與實施
通過上述原因分析可知,此類白色塑料材質異物可能是由于膠塞拆包時,開口處剪的不光滑,導致塑料屑掉進膠塞內。針對此類情況,我們立即進行了試驗,確定合適的拆包剪裁方式,確保剪口處光滑。
經過試驗,當縱向剪裁的時候,由于膠塞外包裝塑料袋的長度較長,無法一刀完成剪裁過程,導致剪口處不光滑;而橫向剪裁則能一刀完成剪裁過程,確保剪口處的光滑。因此,立即對相關操作人員進行培訓,統一膠塞拆包的剪裁方式,并加強抽查力度。
同時,對分裝間滅菌待用的膠塞和軋蓋間滅菌待用的鋁蓋PE袋拆除方式進行了規定。
4 結語
本文以某抗生素粉針劑產品的質量投訴為例,通過調查分析產品的生產工藝流程,確認引起質量投訴的原因,制定相應的對策,并跟蹤確認對策的實施效果,同時需要關注同批次產品的質量和使用情況。
若引起質量缺陷的原因并非偶然,且經評估確實影響產品質量或使用的,因予以召回,確保臨床用藥的安全。

