草魚呼腸孤病毒873株逆轉錄環介導等溫擴增(RT-LAMP)檢測方法研究
張 旻,王 娜,景宏麗,吳紹強
(中國檢驗檢疫科學研究院,北京 100029)
草魚呼腸孤病毒(grass carp reovirus,GCRV),又稱草魚出血病病毒(grass carp hemorrhagic virus,GCHV),屬呼腸孤病毒科(reoviridae)水生呼腸孤病毒屬[1]。目前已報道了GCRV的14種分離株,并在全基因測序的基礎上確立了2種基因型:以GCRV-873株為代表的Ⅰ型和以GCRV-108株為代表的Ⅱ型,二者核酸序列同源性只有50%左右[2]。GCRV-873株分離自湖南[3],該病毒為雙鏈RNA病毒,基因組由11條dsRNA片段組成[4],對草魚腎臟細胞系[5](grass carp kidney cell line,CIK)和草魚卵巢細胞系(grass carp ovarian cell line,CO)細胞系敏感[6,7]。已建立了針對GCRV-873株的病原分離[8]、ELISA[9]和RT-PCR檢測方法,并形成了技術規范[10],應用于疫病監測。
為提高檢測效率,建立了一種GCRV-873株特異性的逆轉錄環介導等溫擴增(reverse transcription loop-mediated isothermal amplification ,RT-LAMP)檢測方法。該方法檢測限可達10個拷貝數的目的基因,且不與鯉春病毒、傳染性造血器官壞死病病毒、傳染性胰臟壞死病毒和病毒性出血性敗血癥病毒RNA產生交叉反應。在反應體系中加入染料后,反應結果肉眼直接可見,不需電泳即可判斷結果,避免了LAMP技術常見的氣溶膠污染。該方法是一種便捷高效、安全可靠的檢測方法,適合大批量樣品的現場初篩和實驗室檢測。
1 材料與方法
1.1 病毒株及病毒RNA
GCRV-873株由中國科學院武漢病毒研究所提供。GCRV-873株接種于CIK細胞,25 ℃恒溫培養。待出現細胞病變效應(cytopathic effect,CPE),細胞大部分脫落后,反復凍融細胞液3次,再使用Trizol(Promega,USA)提取總RNA。
鯉春病毒(spring viraemia of carp virus,SVCV)RNA、傳染性造血器官壞死病毒(IHNV)RNA、傳染性胰臟壞死病毒(IPNV)RNA、病毒性出血性敗血癥病毒(viral haemorrhagic septicaemia virus,VHSV)RNA均由深圳出入境檢驗檢疫局水生動物病重點實驗室提供。
1.2 引物的設計
以GCRV VP5(Genbank No:AF239175.1)基因序列保守片段(218 bp)為模板,使用在線軟件http://primerexplorer.jp/elamp4.0.0/index.html和DNastar primer select 設計出2對引物(表1)。引物由上海生工有限公司合成。

表1 根據GCRV VP5基因片段設計的RT-LAMP引物Tab.1 RT-LAMP primers used to amplify GCRV VP5 gene
1.3 RT-LAMP反應體系
使用藍譜核糖核酸擴增試劑盒(Lanpu Bio-tech,China)中的試劑配置反應體系,體系為25 μL:RNA模板1 μL,2×反應緩沖液(含MgSQ416 mmol/L,和dNTPs 2.8 mmol/ L each)12.5 μL,引物GCRV-FIP和GCRV-BIP (20 pmol/μL)各2 μL,引物GCRV-F和GCRV-B (10 pmol/μL)各0.5 μL,酶溶液(Bst DNA聚合酶和AMV逆轉錄酶混合液)1 μL,去離子水5.5 μL。
1.4 RT-LAMP反應溫度的優化
以GCRV-873 RNA為模板,分別在58、60、62和65 ℃下進行RT-LAMP反應。使用濁度儀LA-320C(Lanpu Bio-tech,China)讀取擴展結果。
1.5 RT-LAMP反應產物的克隆及陽性對照制備
使用TIANgel Midi Purification Kit (TIANGEN,China)膠回收試劑盒,回收純化引物GCRV-F和GCRV-B的PCR擴增片段,再將片段連接入pGem-T-Esay 載體(Novigen),連接產物轉化入DH5α中進行藍白斑篩選。挑選白色菌落測序,若目的基因正確連接入重組質粒,則提取陽性重組質粒pGem-T-GCRV做為RT-LAMP檢測用陽性對照。使用微量紫外分光光度計對重組質粒溶液進行定量,并按照以下公式將重組質粒的質量濃度換算為拷貝數濃度:
(6.02×1023)×(濃度g/mL)/(MW g/moL)=copies/mL
1.6 RT-LAMP檢測方法的檢測限
根據測量和換算的濃度,將重組質粒pGem-T-GCRV溶液稀釋為1011copies/μL的溶液,再將該溶液以10倍梯度稀釋至100、101、102、103、104、106、107copies/μL,每稀釋度各取1 μL分別進行RT-LAMP反應,使用1.3的反應體系和1.4確認的反應溫度。
1.7 RT-LAMP檢測方法與RT-PCR檢測方法的檢測限對比
根據現行的出入境檢驗檢疫行業標準《草魚出血病檢疫技術規范》(SN/T 3584-2013),GCRV-873株RT-PCR檢測方法的目的基因為VP7基因片段,而本LAMP檢測VP5基因片段,因此無法使用同一種標準品進行檢測限比對,只能使用病毒RNA。將1.1提純的接種細胞總RNA(約100 ng/μL)10倍梯度稀釋,每個稀釋梯度各取1 μL作為模板,分別進行RT-LAMP(反應體系條件同1.6)和RT-PCR檢測(反應體系和條件參照標準SN/T 3584-2013),對比檢測限。
1.8 RT-LAMP檢測方法的交叉反應
以GCRV-873株、SVCV、IHNV、IPNV和VHSV RNA為模板,各取1 μL分別進行RT-LAMP檢測(反應體系和溫度同1.6)。
1.9 RT-LAMP檢測結果的可視化
在1.3反應體系的基礎上,加入0.5 μL calcein 染料,體系仍為25 μL。將PCR管放置于烘箱中,反應溫度為1.4確認的溫度,反應時間為60 min。
1.10 病毒樣品檢測
本實驗室根據《草魚出血病檢疫技術規范》(SN/T 3584-2013)推薦的病原分離和RT-PCR方法,檢測并保存了10份GCRV-873株陽性樣品和12份GCRV陰性樣品,利用建立的熒光RT-LAMP檢測方法進行檢測,統計符合率。
2 結果與分析
2.1 RT-LAMP反應溫度的優化
62 ℃和65 ℃組反應20 min出現擴增曲線,58 ℃和60 ℃組反應26 min出現擴增曲線,反應時間超過60 min,陰性對照會出現擴增曲線。為提高引物與模板結合的特異性,RT-LAMP的反應條件確定為65 ℃恒溫反應60 min(圖1)。
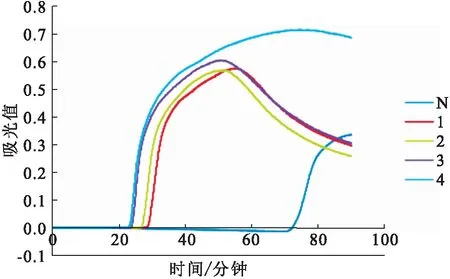
圖1 GCRV RT-LAMP反應條件優化Fig.1 The optimization of the reaction condition of RT-LAMP for GCRV N:陰性對照;1:58 ℃;2:60 ℃;3:62 ℃;4:65 ℃
2.2 RT-LAMP檢測方法的檢測限
反應條件為65 ℃恒溫反應60 min,隨著樣品模板量的遞減,RT-LAMP擴增曲線出現的時間也逐漸延長,模板稀釋到10個拷貝數,PCR 擴增結果仍為陽性,模板稀釋到100,即1拷貝數時擴增結果則為陰性。由此可得出RT-LAMP檢測限為10個拷貝數的目的基因核酸片段(圖2)。

圖2 RT-LAMP檢測限(拷貝數)Fig.2 The detection limit of RT-LAMP (copies)N:陰性對照;0~7:重組質粒標準品的模板量分別為100 ~107 copies
2.3 RT-LAMP與RT-PCR的檢測限對比
原液稀釋104倍,總RNA量約10 pg,RT-LAMP結果仍為陽性;相比之下,RT-PCR只能檢測到稀釋103倍,總RNA量約1 pg的3號樣品(圖4),而且條帶很淺。RT-LAMP檢測限比RT-PCR高10倍(圖3)。

圖3 RT-LAMP檢測限(RNA濃度)Fig.3 The detection limit of RT-LAMP (RNA concentration)

圖4 RT-PCR檢測限(RNA濃度)Fig.4 The detection limit of RT-PCR (RNA concentration)N:陰性對照;0:RNA原液;1~6:原液稀釋倍數分別為101~106 倍
2.4 RT-LAMP檢測方法的交叉反應
交叉反應只有 GCRV 873株呈陽性,而其他病毒則為陰性。建立的RT-LAMP檢測方法特異性良好(圖5)。

圖5 RT-LAMP交叉反應檢測結果Fig.5 Cross reaction results of RT-LAMPN:陰性對照;1:GCRV-873株;2:SVCV;3:IHNV;4:IPNV;5:VHSV
2.5 RT-LAMP檢測結果的可視化
檢測結果顯示GCRV-873株呈綠色,其他樣品未變色(圖6)。
2.6 病毒樣品檢測
利用建立的RT-LAMP檢測方法對本實驗室保存的10份GCRV陽性樣品和12份GCRV陰性樣品的檢測結果與按照《草魚出血病檢疫技術規范》(SN/T 3584-2013)檢測的結果一致,符合率100%。
3 討論
由于我國草魚養殖面積很大,在針對GCRV的檢測工作中,樣品量也非常大,有時一批樣品包括150尾魚。這導致檢測任務的工作量非常繁重。為減輕工作量、提高檢測效率,需要在保證檢測限和特異性的基礎上,建立比傳統的ELISA和RT-PCR方法更方便快捷的檢測方法。

圖6 熒光RT-LAMP檢測GCRV-873株Fig.6 Fluorescence RT-LAMP for detection of GCRV-873N:陰性對照;1:SVCV;2:IHNV;3:VHSV;4:GCRV-873株
LAMP技術的原理是針對靶基因的6個區域設計4條特異引物,利用Bst DNA polymerase在恒溫條件下完成核酸擴增反應[11]。LAMP技術的檢測限通常高于PCR方法,與熒光定量PCR方法相當[12]。作為新型核酸擴增技術,近年來國內外陸續建立了多種針對水產病毒的LAMP檢測方法,如皰疹病毒Ⅱ型[13]、傳染性造血組織壞死病毒[14]、真鯛虹彩病毒(RSIV)[15]等。
本研究建立的特異性檢測GCRV-873株的RT-LAMP檢測方法,將病原RNA的反轉錄與LAMP擴增反應集中于同一反應體系,恒溫條件下一次性完成擴增,相對于傳統的RT-PCR方法和ELISA方法,主要有以下兩點優勢:1.耗時短:RT-PCR方法檢測GCRV,需要3 h左右,ELISA方法也需要5 h左右,該RT-LAMP方法省去了制備瓊脂糖凝膠、電泳等過程,反應只需要60 min;2.檢測限比RT-PCR方法高10倍,因此該方法非常適合病原的臨床檢測。
目前國內外也建立了其他幾種針對GCRV的RT-LAMP檢測方法,與本研究建立的RT-LAMP檢測方法的區別如下:(1)2013年,建立了針對GCRV-HZ08株(GCRV Ⅱ型)的RT-LAMP檢測方法[16],而本研究建立的RT-LAMP方法是特異性檢測GCRV-873株(CCRV I型)的,兩種基因型的基因同源性只有50%,該方法能否檢測GCRV-873株的基因,尚未有報道;(2)2012年-2013年,先后報道了4種檢測GCRV VP6基因片段的RT-LAMP檢測方法,除其中1種未報道詳細數據外[17],其他3種檢測限分別達到7 copies[18]、10 copies[19]和33 pg[20]的病毒RNA。但這3種方法主要利用電泳檢測擴增產物,作為一種高效的核酸擴增技術,LAMP產物的目的基因含量極高,打開反應管取樣的過程中有一定氣溶膠污染風險[21],容易導致檢測結果出現假陽性。本研究建立的RT-LAMP檢測技術,不需要打開反應管,在封閉的環境中使用濁度儀或染料判斷檢測結果,極大降低了氣溶膠擴散的風險,可以有效避免核酸擴增結果出現假陽性[22]。
綜上所述,本研究建立的GCRV-873株RT-LAMP檢測方法,具備特異性強、檢測限高、耗時短、假陽性風險低等優點,適合大批量樣品的現場初篩和實驗室檢測。

