Wistar大鼠CBRH?3肝癌模型的構建*
楊煒,冉立峰,周崑,朱輝,王智彪(.重慶醫科大學生物醫學工程學院/省部共建國家重點實驗室培育基地/重慶市超聲醫學工程重點實驗室/重慶市生物醫學工程學重點實驗室/重慶市微無創醫學協同創新中心,重慶40006;.重慶醫科大學附屬第二醫院HIFU腫瘤治療中心,重慶40006)
肝癌是致死率僅次于胃癌、食道癌的第三大惡性腫瘤。隨著現代醫療科技的發展,肝癌的治療也有了很大的進展,且有多種治療方式,包括外科手術和非手術治療,非手術治療包括介入、射頻、微波、放療和高強度聚焦超聲(HIFU)[1-2],這些治療方式各有優勢和特點,但要治愈肝癌仍然是醫學界的難點。HIFU作為一種新型的無創治療手段,近年來發展迅速,被廣泛應用于各種非空腔臟器實體良惡性腫瘤、肝癌、腹膜后腫瘤、乳腺腫瘤、子宮肌瘤的治療中。隨著該技術的發展,還適應于多種非腫瘤良性疾病,能夠從體外無創地、適形地消融體內的腫瘤。目前,HIFU已經成為肝癌治療的重要手段之一[3-4]。但是HIFU治療肝癌的機制還有待進一步研究。因此,為了研究HIFU治療肝癌的機制,以期能使HIFU更好地應用于臨床,建立合適的肝癌模型就具有重要的臨床意義[5]。本文擬采用CBRH-3細胞株來構建大鼠肝癌模型,取得了比較令人滿意的模型效果,現報道如下。
1 材料與方法
1.1 材料
1.1.1 實驗動物 Wistar大鼠:雄性30只,鼠齡10周,體重60 g,由陸軍軍醫大學大坪醫院實驗動物中心提供;裸鼠:雄性20只,體重20 g,由重慶醫科大學實驗動物中心提供。
1.1.2 材料 CBRH-3(wistar大鼠肝癌細胞株,貼壁細胞),購于北京銀紫晶生物醫藥技術有限公司;胎牛血清由GIBCO公司生產。
1.2 方法
1.2.1 培養CBRH-3細胞株 將大鼠CBRH-3細胞株培養、擴增、傳代,從液氮罐里取出細胞凍存管,迅速放入38℃水浴中,并搖動,在1 min內使其完全融化,然后在無菌下取出細胞,在1 000 r/min速度下離心5 min,棄上層液,加入適量培養液(含胎牛血清10%的DMEM細胞培養液),然后接種于培養瓶中,置37℃恒溫CO2培養箱靜置培養,第2天更換1次培養液,繼續培養,觀察細胞生長情況,若細胞密度達到90%時給予傳代。倒出培養液,用磷酸鹽緩沖溶液(PBS)洗1次,倒入0.25%的胰酶約1 mL。在顯微鏡下觀察,如果細胞變圓,則加入DMEM培養液終止消化,巴氏管給予吹打使細胞脫落成細胞懸液,在1 000 r/min速度下離心5 min,棄去培養液,倒入新鮮的培養液,巴氏管吹打成細胞懸液,分入新的培養瓶中繼續培養,按1∶3傳代。
1.2.2 裸鼠皮下種植腫瘤細胞 將CBRH-3細胞株制成1×107mL-1的細胞懸液,注射入裸鼠背部兩側皮下,每側注射0.1 mL,2周后注射部位觀察長出直徑1~2 cm大小腫塊,用頸椎脫臼法處死裸鼠,無菌手術切下腫塊,放到生理鹽水中清洗,并把腫塊切成0.3~1.0 mm3組織大小的碎片備用。
1.2.3 Wistar大鼠肝癌模型的制備 用8%硫化鈉溶液將Wistar大鼠腹部脫毛,使其仰臥綁定于手術臺,用10%的水合氯醛按照0.3 mg/100 mg對大鼠進行腹腔注射麻醉,在腹正中自劍突往下切開約1.5 cm創口,進腹后暴露肝臟,在肉眼直視用小鑷子在肝臟上切一小口,長約5~10 mm,用紗布壓迫止血后取一瘤塊放入其內,縫合切口。必要時用吸收性明膠海綿顆粒進行填塞,如沒有發現活動性出血后關閉腹腔,為預防感染給予肌內注射青霉素8萬U。將大鼠交回飼養中心繼續飼養,繼續觀察2周,術前1周及術后1周每天給每只大鼠注射地塞米松2 mg,大鼠的飲食、大小便及精神狀態無明顯變化。
2 結 果
2.1 磁共振成像(MRI)觀察腫瘤的生長情況 在裸鼠腹腔移植傳代CBRH-3細胞株接種后2周,除2只死亡外,58只中有51只在彩色多普勒超聲和MRI(GE 1.5T)上顯示直徑大小約1~2 cm的腫瘤(2只出現2個腫塊),彩色多普勒超聲提示大多數腫塊為高回聲,只有少數呈低回聲的表現;MRI檢測采用FSE序列T2WI和T1WI脂肪抑制序列,發現51只均在相應部位出現圓形或類圓形腫塊影,T1WI呈均勻低信號、T2WI和T2WI脂肪抑制呈高信號,所有的腫塊均呈結節狀,信號均勻,邊界清楚,周圍未見明顯子灶,腫瘤無明顯纖維包裹、鈣化、凝固性壞死、出血、囊變和轉移征象。有部分大鼠伴有腹腔積液和腹膜后種植轉移灶。見圖1、2。
2.2 大體觀察及病理組織切片 腫瘤移植2周后,處死大鼠,肉眼觀察腫瘤組織生長、內部結構特點及與周圍正常肝組織的情況;取出肝臟腫瘤,放入10%甲醛中固定,并進行石蠟包埋切片以觀察腫瘤的組織病理學特征(圖3、4)。腫塊為魚肉狀灰白組織,無出血或者壞死改變,和周圍正常肝臟分界清楚,病理組織學:光學顯微鏡下檢查發現,腫瘤細胞呈巢狀或彌漫狀分布,胞核大濃染,異型性明顯,細胞大小不一,周邊伴行多支小血管,血供豐富,胞質量少,為肝癌腫瘤。

圖1 裸鼠腫瘤
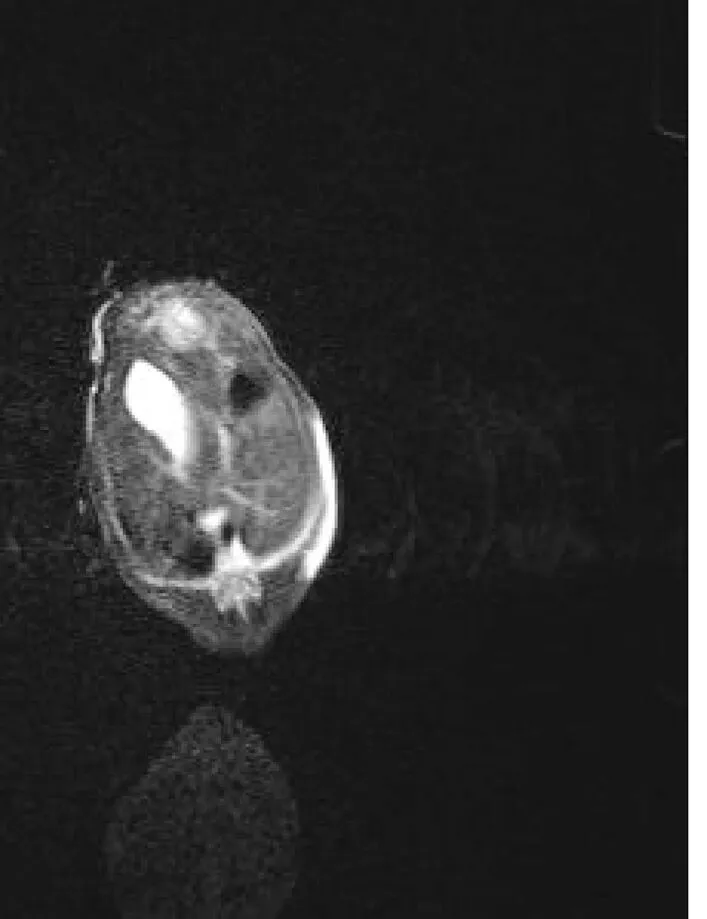
圖2 MRI檢查結果

圖3 Wistar大鼠肝移植瘤
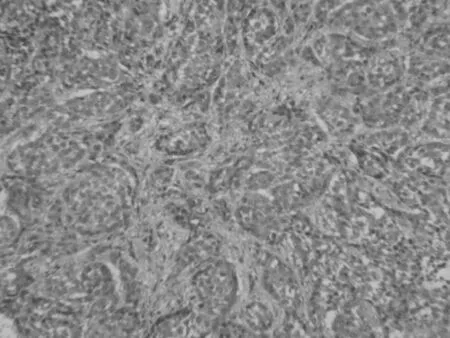
圖4 Wistar大鼠腫瘤顯微鏡下(HE,200×)
3 討 論
原發性肝癌是典型的富血供腫瘤[6-7],在中國是發病率最高的惡性腫瘤之一。其病變進展快,對患者危害大,病死率高,也是廣大科學工作者研究的重點。目前肝癌的治療方法主要為肝切除術和非手術治療。但肝癌的發病十分隱匿,臨床上僅有不到30%的患者就診時可獲得手術治療的機會,同時患者術后肝癌復發率很高,患者腫瘤復發后的處理也相對較為困難,大部分患者只能接受非手術治療,應用最廣泛的非手術治療方式是肝動脈化療栓塞術(TACE)[8-9],其作用機制主要是用碘化油加化學藥物栓塞腫瘤供血血管,使其缺血缺氧而發生壞死,并能夠提高腫瘤局部化療藥濃度及作用時間,近期療效確切,經過一段時間后栓塞劑會被清除,造成腫瘤復發,故其遠期效果并不確切。HIFU是一種非侵入性治療,具有創傷小,無放、化療不良反應,且可重復進行的治療手段。目前,在肝癌治療領域已開始被接受用于無創治療,取得了較好的臨床效果。HIFU治療腫瘤的機制是高溫效應和空化效應,對于HIFU治療腫瘤尤其是肝癌的研究還需要大量的動物實驗和臨床試驗進行相關的研究。因此必須快捷、高速、經濟地建立一種合適的肝癌動物模型,以利于促進HIFU治療肝癌的理論和實踐的發展。
近年來,大鼠肝癌模型分為3種,分別是誘發性模型[10]、自發性模型和移植性模型。誘發型常用二甲基亞硝胺(DENA)等化學物質誘發,建模周期較長,往往伴有肝硬化,腫瘤多為彌漫型或小結節型,無法滿足各種試驗性治療的需要和影像學診斷等方面的研究;自發性肝癌模型是動物自然發生的,未經任何人工誘導。這類模型的缺點是培育及觀察時間較長、耗費較大、發生率較低,難以滿足研究的要求,目前已很少被采用。而移植性肝癌模型多呈結節腫塊型,邊緣較清晰,在影像診斷學方面和正常肝實質易于分別,進行各類實驗研究,便于模擬各種實驗模型。作者在肝癌實驗中的動物常選用可移植Walker-256癌肉瘤的Wistar大鼠[11-12]和移植VX2鱗癌的新西蘭大白兔[13-15],Wistar大鼠移植性肝癌模型國內研究較多,因其腫瘤血供與人類原發性肝癌相似,該模型的腫瘤血供特點為在瘤體直徑小于3 mm時主要由門靜脈供血,直徑大于3 mm時主要由肝動脈供血。研究表明,其血供特點和生長行為與人類肝癌極相似。兔VX2肝癌模型是少數建立在大動物體內的肝臟富血供腫瘤模型,可以進行Seldinger法操作,從而最大限度地模擬臨床經TACE治療肝癌的操作過程,該模型也是供介入治療藥物代謝動力學研究較好的模型。但是這2種腫瘤模型的腫瘤細胞來源均不是肝癌細胞株,甲胎蛋白(AFP)陰性,故并不是真正意義上的肝細胞性肝癌模型。因此,本研究使用CBRH-3肝癌細胞株來構建肝癌模型。大鼠肝癌細胞株來源于用DNA誘發的大鼠原發性肝癌,病理鑒定為肝細胞性肝癌,細胞具有其起源的體內肝癌細胞的超微結構特點,且可分泌AFP,體外培養觀察,細胞保持惡性類上皮細胞的形態特點,單層細胞培養可見細胞重疊堆積的生長現象,是很好的大鼠肝細胞癌瘤株,擬高效建立可以完全模擬臨床肝癌的動物模型,有利于對HIFU治療腫瘤的機制的深入研究。
作者通過對Wistar大鼠的CBRH-3肝癌模型的病理及影像學綜合分析,認為該模型具有如下特點:(1)易于復制,移植成功率高,模型性能穩定,死亡率低;(2)腫瘤生長方式與臨床肝細胞癌生長方式相似,呈膨脹浸潤性生長結節狀;(3)MRI表現與人體腫瘤相似,易于影像學診斷;(4)可快捷設計選擇腫瘤移植生長部位。
總之,Wistar大鼠的CBRH-3肝癌模型的生物學特性與人類原發性肝癌相似,該方法簡單安全,制作簡單,造模周期短,適用于HIFU治療肝臟腫瘤的效應和機制的深入研究,為HIFU治療肝癌創造了良好的實驗基礎,值得推廣。

