乳清蛋白水解物結合吐溫對O/W型乳狀液穩定性的影響
王芳,李月,曹傳愛,商旭,劉騫,*
(1.黑龍江職業學院,黑龍江哈爾濱150080;2.東北農業大學食品學院,黑龍江哈爾濱150030)
水包油型(Oil-in-water,O/W)乳狀液是一種由分散在水相中的油滴組成的典型體系,存在于許多食品中,如沙拉醬、沙司、飲料、湯和嬰兒配方食品等[1]。不幸的是,這種乳狀液是一種高度不穩定的體系,因為它們由兩種不混溶的液體組成[2]。乳化劑必須在均質前使用,才能獲得動力學穩定的乳狀液[3]。因此,乳化劑的選擇對于食品乳液體系的高效設計至關重要。Ogawa等[4]研究表明食品乳化劑在均質過程中能粘附在新生成的液滴表面,在乳化液的貯存和利用過程中顯著地降低了界面張力,穩定了液滴[5]。大多數研究都采用低分子量合成表面活性劑制備食品乳狀液,主要是由于其界面擴散性能優于生物大分子,如蛋白質、多糖等[6-8]。Panya等[9]研究表明低分子量合成表面活性劑能提供更高的乳狀液的表面積,從而提高物理穩定性,因為這種反應經常發生在油水界面上[10]。然而,pH值仍然是蛋白質穩定乳狀液的最大缺點。此外,多糖用作乳化劑時,低濃度下很難制備出較為分散的乳狀液,高濃度下非吸附性的多糖又容易導致乳狀液絮凝,這對最終產品的質量有重大影響[11-13]。因此,需要找到可持續和生物相容的乳化劑用于食品乳狀液中。
蛋白質水解物和相關的分離肽由于其不同的生物活性,近年來受到越來越多的關注。然而,更廣泛的酶水解處理顯著降低了蛋白質的乳化性能,卻僅提高了溶解度[14]。Scherz等[15]表示盡管具有較高的水解度的蛋白水解產物具有增加溶解度和界面的擴散能力,但它們在常規乳化體系中也表現出較低的物理穩定性。Adjonu等[16]還建議通過研究更大的鏈蛋白水解物,可以提高多肽制備乳狀液的物理穩定性。此外,最近的研究表明,限制/控制酶水解的蛋白質可以顯著提高他們的乳化能力[17-18]。Lam等[19]表明高水解度的蛋白質水解物的乳化性能較弱主要是由于水相中殘留的肽比例較大,而不是吸附在油水界面上。Ye等[20]還宣布,廣泛地水解蛋白得到的水解產物由于短肽的大量生產而不利于O/W型乳狀液的穩定性。因此,限制性水解的蛋白在兩相乳化體系中能夠增加相關產品的質量參數的穩定作用。通過研究限制性水解的蛋白以及在乳化體系中的作用機理,能夠為生產健康、安全的食品提供理論基礎,具有生產加工的理論和實際意義。
本試驗研究了以Tween 20為乳化劑的大豆油水包油型(O/W型)乳狀液,并添加不同濃度的限制性水解乳清蛋白,通過測定濁度、ζ-電勢以及粒徑等指標來探討乳狀液乳化穩定性的變化,為限制性水解蛋白質在食品體系中的應用提供理論依據。
1 材料與方法
1.1 材料
乳清分離蛋白:北京銀河路商貿有限責任公司;中性蛋白酶(酶活為2.1 AU/g):丹麥Novozymes公司;大豆油:哈爾濱九三油脂;十二烷基磺酸鈉(sodium dodecyl sulfate,SDS):Sigma 公司;磷酸二氫鈉、磷酸氫二鈉:天津市巴斯夫化工有限公司;氫氧化鈉、鹽酸:哈爾濱市萬太生物藥品公司。
1.2 儀器與設備
JJD500-2電子天平:沈陽龍騰電子稱量儀器有限公司;AL-104型精密電子天平、FE20K型pH計:上海梅特勒-托利多儀器設備有限公司;DK-8B電熱恒溫水浴鍋:上海驚宏實驗設備有限公司;JB-2恒溫磁力攪拌器:上海雷磁新徑儀器有限公司;GL-21M冷凍離心機:湖南湘儀實驗室儀器開發有限公司;Bakeman離心機;TU-1800紫外可見光分光光度計:北京普析通用儀器有限公司;T18勻漿機:德國IKA公司。
1.3 試驗方法
1.3.1 乳清蛋白水解物的制備
根據 Liu等[19]的方法將加熱處理(95℃,5 min)的乳清蛋白水溶液(4%,pH 7.5)用中性蛋白酶在50℃下水解1 h,酶與底物濃度質量比為2∶100,反應過程中不斷加入1mol/L的NaOH,使pH值保持不變。水解結束后95℃水浴5 min進行滅酶,然后用1 mol/L HCl將水解液pH值調至7.0。水解物以9000g離心10min除去不溶顆粒。
1.3.2 乳狀液的制備
分別向不同乳化劑的水溶液中加入10%的大豆油,用高速均質機在13 500 r/min下乳化2 min后,35 Mpa下經高壓均質機均質兩次。加入疊代鈉(0.03%)進行抑菌。水相為10 mg/mL的Tween 20和不同濃度的WPH(0、1.25、2.5、5、7.5、10 mg/mL,終濃度)溶液的混合物。
1.3.3 乳清蛋白水解物水解度的測定
根據pH-Stat法[21]
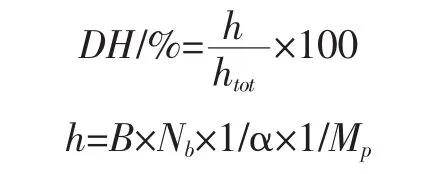
式中:h為單位質量蛋白質中被水解的肽鍵的量,mmol/g;htot為單位質量蛋白質中肽鍵的總量,mmol/g;B為水解過程中所消耗的堿量,mL;Nb為堿液的濃度,mol/l;Mp為水解液中蛋白質的質量,g;1/α 為校正系數。
1.3.4 乳清蛋白水解物乳化活性和乳化穩定性的測定
參照Pearce等[22]的方法,并略作修改。取8 mL的水解樣品(1 mg/mL),將其加入到2 mL的大豆油中,分散乳化1 min,其參數設定為20 000 r/min。在乳化0和10 min后,分別取50 μL乳狀液于裝有5 mL 0.1%SDS溶液的離心管中,混勻后,在波長500 nm處進行比色,計算公式如下:
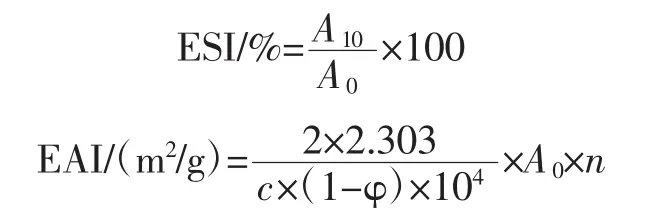
式中:A0為初始乳狀液的吸光值;A10為乳狀液靜置10 min后的吸光值;C為樣品溶液的蛋白濃度,g/mL;φ為乳狀液中油相的比例;n為稀釋倍數。
1.3.5 乳狀液濁度的測定
參照Cheng等[23]的方法。新制備的乳狀液立即加入離心管中,室溫放置0和10 h。從距離心管底0.5 cm處取乳狀液50 μL,加入裝有5 mL 0.1%SDS的離心管中振蕩混勻,在500 nm處測得的吸光度。濁度用500 nm下的吸光值A500表示。
1.3.6 乳化顆粒電位和粒徑的測定
將乳狀液 50 μL,加入到裝有 5 mL,0.1 mol/L,pH 7.0的磷酸鹽緩沖溶液中,混勻后注入到彎曲毛細管中,在常溫下使用Malvern激光粒度儀測定稀釋乳化顆粒的電位和粒徑。
1.4 統計分析
每個試驗重復3次,結果表示為平均值±標準差。數據統計分析采用Statistix 8.1(分析軟件,St Paul,MN)軟件包中Linear Models程序進行,差異顯著性(P<0.05)分析使用Tukey HSD程序,采用Sigmaplot 11.0軟件作圖。
2 結果與分析
2.1 乳清蛋白水解物的乳化性質
使用中性蛋白酶不同水解時間制備的乳清蛋白水解物的水解度(degree of hydrolysis,DH)、乳化活性(emulsifying activity index,EAI) 和乳化穩定性(emulsion stability index,ESI)見表1。
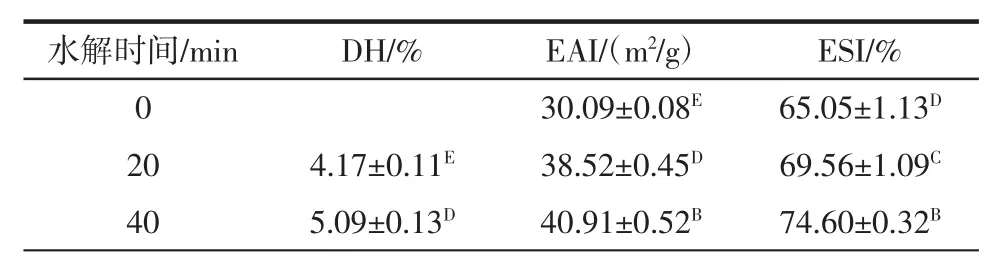
表1 使用中性蛋白酶不同水解時間制備的乳清蛋白水解物的水解度、乳化活性和乳化穩定性Table 1 Degree of hydrolysis(DH),emulsifying activity index(EAI)and emulsion stability index(ESI)of WPH prepared using neutral protease with different hydrolysis time
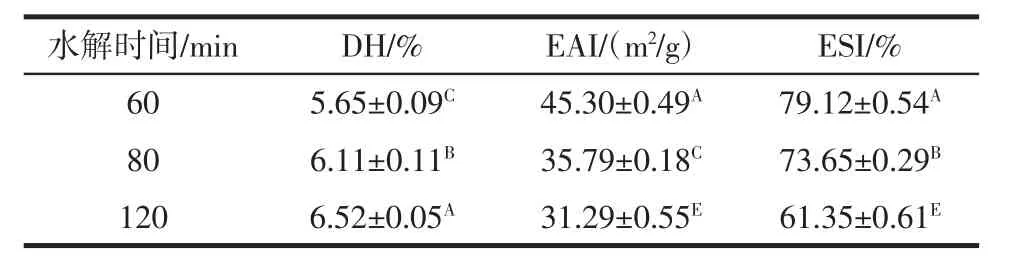
續表1 使用中性蛋白酶不同水解時間制備的乳清蛋白水解物的水解度、乳化活性和乳化穩定性Continue table 1 Degree of hydrolysis(DH),emulsifying activity index(EAI)and emulsion stability index(ESI)of WPH prepared using neutral protease with different hydrolysis time
隨著反應時間從20 min增加到120 min,水解度顯著增加(P<0.05),在乳清蛋白水解120 min時水解度達到6.52%。EAI代表蛋白質或蛋白質水解物形成和穩定乳狀液的能力,而ESI指的是蛋白質或蛋白質水解物對乳狀液施加強度以抵抗聚集和聚結的能力。通過乳化活性指數(EAI)和乳化穩定性指數(ESI)能夠進一步反應大分子蛋白質和水解后小肽的乳化性質[24]。由表1中可以觀察到隨著水解時間的不斷增加,EAI和ESI都呈現出先升后降的變化形勢,并在水解60 min時,EAI和ESI達到最高值,分別為45.30 m2/g和79.12%,而進一步延長水解時間EAI和ESI反而越低。Christiansen等[25]研究表明控制酶水解可以改變蛋白質的結構和部分暴露疏水核心,乳化活性得到改善。低水解度的肽或水解物在油水界面的擴散速率比未水解的蛋白要高。用來穩定新生成的乳狀液,能夠防止聚集和聚結現象的發生[26]。此外,Yust等[27]研究表明高的乳化性能是通過控制水解形成的,主要是促進親水和親脂域之間的適當平衡。已有研究發現對蛋白質過度水解會使蛋白質的疏水性和親水性殘基失衡,并使EAI和ESI降低[20]。這可以解釋為蛋白酶的水解使蛋白質的天然結構釋放使更多親水基團向外暴露,表面疏水性降低。初步試驗表明,平衡水解能提高乳清蛋白的乳化活性。綜上可知,中性蛋白酶水解乳清蛋白1 h具有最好的EAI和ESI。
2.2 乳清蛋白水解物對乳狀液乳化性質的影響
2.2.1 乳狀液的濁度
用不同濃度的WPH和Tween 20制備的乳狀液的濁度如圖2。
以WPH和Tween 20同時為乳化劑時,所有乳狀液樣品的濁度均較高,能夠更有效地分散大豆油。這表明WPH和Tween 20作為共乳化劑的乳化活性效果很好。并且,隨著WPH濃度的增加,乳狀液的濁度呈現先升高后降低的變化趨勢,當WPH的濃度為5 mg/mL時,乳狀液的濁度達到最大值為1.18。當WPH濃度較大時,乳狀液的濁度有所下降,這可以被解釋為這較高濃度的蛋白質或水解物與Tween 20之間形成了競爭吸附。蛋白濃度較高時,更多的多肽吸附在了界面上,增加了乳化顆粒間的相互作用,導致了濁度的降低。Cheng等[23]的研究也表明,較高濃度的馬鈴薯蛋白水解物和Tween 20制備的乳狀液的穩定性要低于低濃度條件下的。Dickinson和Golding[28]的研究發現蛋白的最適濃度能夠產生油滴飽和表面覆蓋率,達到較好的乳狀液穩定性。然而,過高的濃度使未被吸附的蛋白產生絮凝。此外,Dickinson等[29]表示含有蛋白和Tween 20的乳狀液具有明顯的物理穩定性,這主要是由于某種形式的橋聯作用。
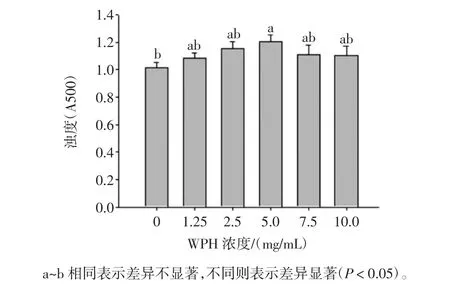
圖1 不同濃度WPH制備乳狀液的濁度的變化趨勢Fig.1 Stability of canola oil-in-water emulsions prepared with different concentrations of WPH and Tween 20
2.2.2 乳狀液的ζ-電勢
不同濃度的WPH和Tween 20制備的O/W乳狀液ζ-電勢的變化趨勢見表2。

表2 不同濃度的WPH和Tween 20制備的O/W乳狀液ζ-電勢的變化趨勢Table 2 Values of ζ-potential of the oil-in-water emulsions prepared with different concentrations of WPH and Tween 20
ζ-電勢是存在于乳狀液顆粒的一個關鍵物理性質,代表在粒子表面附近發生的靜電相互作用。高的ζ-電勢(絕對值)意味著更大的靜電斥力和更大的粒子間距離,這可以提高乳狀液體系的穩定性。Nattapol等人[30]也表明,潛在的ζ-電勢變化反映出液滴周圍界面的組成。從表2中乳狀液中WPH的濃度從1.25 mg/mL增加到10 mg/mL,ζ-電勢(絕對值)呈現先升高后降低的變化趨勢。在所有的樣品中,WPH的濃度為5 mg/mL時ζ-電勢值顯著高于其他處理組(P>0.05),第0天和第10天分別為7.78和6.45。由于較高WPH濃度下,水相中含有大量未被吸收的多肽,可以將它們從界面上去除,從而導致較低的ζ-電勢。Cheng等人[23]認為電荷減少可能是由于在界面處吸收的多肽數量較低。另一個可能的解釋是,高粘度與高的WPH濃度相關,會對多肽的擴散產生負面影響,從而降低蛋白質在界面上的含量。因此,當WPH與Tween 20同時作為乳化劑時,將會導致乳化液滴表面電勢的下降,液滴表面帶有較低的凈電荷,界面層多肽鏈間的靜電斥力變弱,有助于在液滴表面形成厚實且致密的界面膜。此外,Thaiphanit等人[31]發現適度水解椰子蛋白有助于提高乳狀液中液滴的負靜電荷。
2.2.3 乳狀液的粒徑大小
不同濃度的WPH和Tween 20制備的O/W乳狀液ζ-電勢的變化趨勢見表3。
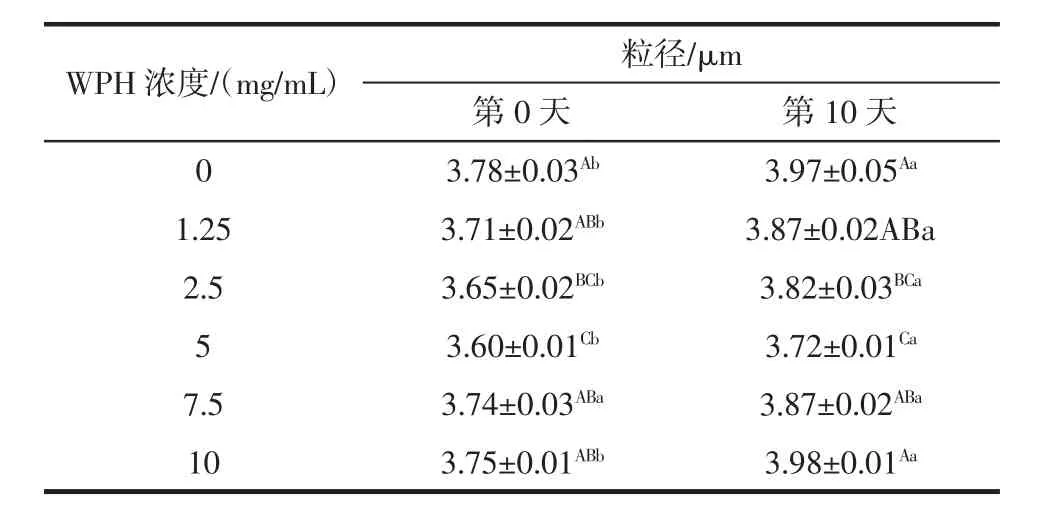
表3 不同濃度的WPH和Tween 20制備的O/W乳狀液ζ-電勢的變化趨勢Table 3 Values of droplet size of the oil-in-water emulsions prepared with different concentrations of WPH and Tween 20
動態光散射(dynamic light scattering,DLS)是評價乳狀液在貯存過程中凝結或絮凝變化的一種強有力的技術。從表3可以觀察到,在第0天和第10天時,乳狀液平均粒徑(d4,3)都隨著WPH的濃度從1.25 mg/mL增加到10 mg/mL而顯著增加(P<0.05)。乳狀液在貯藏10天后,含有不同濃度WPH的乳狀液粒徑都顯著增大。這種現象可能與乳狀液中液滴的聚集和凝結有關。WPH濃度為5 mg/mL時,乳狀液的粒徑達到最小值,濃度增加會引起粒徑的顯著增大。這可以解釋為高WPH濃度引起更高的粒徑可能是由于在這些液滴分散在連續相的密度差異,其次是相分離。乳狀液的穩定性隨液滴顆粒減小而增加,因為更多的乳化劑吸附到小顆粒表面。Thaiphanit等[32]還發現椰子蛋白水解物的表面有許多無定形的蛋白質大分子,而大量的這些大分子可能會使乳狀液不穩定。Dimitrova等[33]還發現,Tween 20能提高液滴由于高膠束凝聚在油水界面的排斥,增加乳狀液體系的穩定性。我們的研究結果發現,添加不同濃度WPH處理組的粒徑均低于未添加WPH的空白對照組,這可能與相同的油量下具有較高乳化活性的乳化劑有關。還可以解釋為是更多的表面活性物質吸附到液滴表面以及液滴間形成了更大的空間位阻,乳狀液的氧化穩定性隨液滴顆粒減小而增加,因為更多的乳化劑吸附到小顆粒表面。另外,乳化劑分子疏水部分更容易在小顆粒中抑制油脂分子和自由基的移動。因此,乳化液滴的粒徑分布降低有助于產生抗氧化效果。這與Li等的研究是一致的[34],總結了玉米醇溶蛋白水解物能夠顯著降低肌原纖維蛋白制備的O/W乳狀液的平均粒徑。Adjonu等[35]表明多肽的空間位阻穩定性差很容易導致多肽的聚集,加速油滴絮凝。非吸附肽的大小、形狀和數量對水解液穩定乳狀液的絮凝有著至關重要的影響。此外,Dimitrova等[33]研究表明,牛血清白蛋白添加到Tween 20制備的乳狀液中能夠通過重建蛋白質表面活性劑層或液滴周圍的絡合物將靜電斥力逐漸轉化為空間位阻。
3 結論
水解度是影響乳清蛋白乳化特性的主要因素,它通過有限的(60 min)中性蛋白酶水解得到WPH可以與Tween 20一起使用,能夠提高通過大豆油穩定的O/W乳狀液的穩定性,增加乳狀液的ζ-電勢(絕對值)并使其具有較小的粒徑,增強乳狀液的乳化穩定性。然而,較低濃度的WPH(5 mg/mL)與Tween 20共同制備的乳狀液最為穩定,這主要是由于WPH的濃度過高時在界面上存在競爭吸附。下一步我們將解決如何從粗水解物中制備具有較好界面性質的高分子量活性肽,為提高水包油型乳狀液滴的穩定性奠定基礎。

