乳清分離蛋白限制性脫酰胺及一些性質的表征
李丹,易偉民,范馨文,翟愛華,關琛
(黑龍江八一農墾大學食品學院,黑龍江大慶163319)
乳清分離蛋白(whey protein isolated,WPI)是一種優質的動物性蛋白資源,由于其具有營養價值高、易消化吸收、含有多種活性成分等特點,乳清分離蛋白日漸受到重視[1]。資料顯示,每年美國由制作干酪而產生的乳清達3 300萬噸,但僅有55%的乳清得到了進一步加工,其余未加工的乳清隨污水排放,既造成資源浪費又造成環境污染[2]。因此,生產一些高附加值產品使乳清蛋白被充分利用顯得尤為重要。近年來,與乳清分離蛋白有關的研究也有很多[3-4],然而幾乎沒有與脫酰胺有關的研究。
酶法脫酰胺主要使蛋白質分子側鏈的谷氨酰胺轉化為谷氨酸,使肽鏈內的負電荷有所增加,最終使得蛋白質的許多功能性質,如溶解性、表面疏水性、抗氧化性、與二價金屬離子螯合的能力等特性均受到不同程度的影響[5]。Matsudomi[6]、Hamada[7]等指出,脫酰胺作用基本不影響蛋白的一級與二級結構,食物蛋白的脫酰胺度達2%~6%時就能顯著提高食物中蛋白質的相關功能特性,尤其是溶解性。聶小華等[8]采用HCl對大米蛋白進行脫酰胺處理,結果表明,脫酰胺處理使大米蛋白功能性質均得到顯著提高,而且脫酰胺大米蛋白的表面疏水性也發生了明顯下降。
本研究采用谷氨酰胺酶(EC 3.2.1.5),對乳清分離蛋白進行限制性脫酰胺,從而制得具有較低脫酰胺度的蛋白產物,并對其產物的界面性質及Fe2+/Zn2+等二價金屬離子的螯合能力進行了評價和比較。研究結果可以為多功能食品的開發提供很好的基料,為乳清分離蛋白更好地應用于食品加工業提供理論基礎。
1 材料與方法
1.1 材料與儀器
乳清分離蛋白:天津銀河偉業進出口有限公司;3-(2-吡啶基)-5,6-雙(4-苯磺酸)-1,2,4-三嗪(Ferrozine)、谷氨酰胺酶(EC 3.2.1.5,酶活為 17.3 U/g):美國Sigma公司;大豆油:九三集團;其他試劑均為國產分析純。
UV-2401PC紫外-可見分光光度計:日本島津公司;Kjeltec TM 3200全自動凱氏定氮儀:瑞士Foss公司;AR224CN型電子天平:奧豪斯國際貿易(上海)有限公司;JJ-1型精密定時電動攪拌器:江蘇省金壇市榮華儀器制造有限公司;LD4-1.8型臺式離心機:北京京立離心機有限公司。
1.2 方法
1.2.1 乳清分離蛋白限制性脫酰胺
將一定量的乳清分離蛋白溶液與超純水、不同體積的谷氨酰胺酶溶液(濃度為0.1 g/mL)混合,配制成乳清分離蛋白濃度為5%、酶添加量分別為0.2、0.4、0.6、0.8、1.0 U/g乳清分離蛋白的反應體系。體系分別在 30、33、36、39、42 ℃下反應 1 h~20 h,按照以下方法分別測定產物的脫酰胺度。以未加谷氨酰胺酶溶液的乳清分離蛋白溶液為空白。
1.2.2 蛋白質含量測定
蛋白質含量測定采用凱氏定氮法GB/T 5009.5-2016《食品安全國家標準食品中蛋白質的測定》)[9]。
1.2.3 脫酰胺度測定
脫酰胺度測定采用苯酚-次氯酸鹽法[10]。
分別準確稱取5.0 g苯酚、25 mg亞硝基鐵氰化鈉,并加入雙蒸水定容至500 mL配制試劑A備用。準確稱取2.5 g NaOH并溶于雙蒸水中,移取4.2 mL次氯酸鈉溶液加入到NaOH溶液中,并容至500 mL配制試劑B。
準確移取5.0 mL試劑A于試管中,加入20 μL不同濃度的硫酸銨標準溶液(或待測樣品),充分振蕩、混勻。然后準確移取5.0 mL試劑B加入到上述混合溶液中,充分振蕩、混勻。迅速轉移至水浴鍋中,在37℃下水浴顯色20 min。然后冷卻至室溫,在625 nm處測定溶液吸光值。每個濃度做3個平行。
根據所測定的樣品游離氨含量及總酰胺含量,計算脫酰胺度,計算公式見式(1)。

1.2.4 Fe2+螯合能力測定
采用Ferrozine顯色法測定二價鐵螯合能力[11],略有改動。
準確吸取0.25 mL樣品溶液(1 mg/mL,終濃度0.10 mg/mL) 與0.15 mL 1 mmol/L的 FeSO4·7H2O 溶液(終濃度0.03 mmol/L,現用現配)混合。加入1.20 mL超純水,使反應體系終體積為1.50 mL。混勻后放置2 min,再加入1.00 mL 0.50 mmol/L的Ferrozine顯色劑水溶液(終濃度0.20 mmol/L),充分振蕩、混勻。室溫下靜置反應10 min,使Fe2+與Ferrozine充分結合,形成穩定的Fe2+-Ferrozine復合物,紫外分光光度法562 nm下測定吸光值。樣品對Fe2+的螯合效率計算公式見式(2):
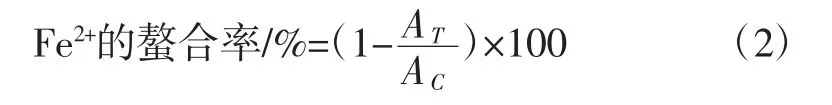
式中:AT為樣品吸光度;AC為對照樣吸光度。
1.2.5 Zn2+螯合能力測定
樣品鋅離子螯合能力的測定參照Wang等[12]的方法,計算方法略有改動。
鋅-肽螯合反應:分別取1.0 mL 0.05 mol/L ZnSO4(乙醇溶解)于4個25 mL離心管中,并分別緩慢滴入10 mL 2%的乳清分離蛋白和3份不同脫酰胺度的脫酰胺乳清分離蛋白樣品溶液(用體積分數為50%的乙醇溶解),室溫下攪拌反應1 h,直至有白色沉淀生成。
螯合鋅含量的測定:分別取上述反應液5 mL于4個燒杯中濃縮至近干,加入15 mL無水乙醇,混勻后5 000 r/min離心20 min,取沉淀并用蒸餾水定容至50 mL。用乙二胺四乙酸(elhylene diamine tetraacetic acid,EDTA)絡合滴定法測定螯合態鋅的含量。移取20 mL容量瓶中的溶液至錐形瓶中,加兩滴二甲酚橙指示劑(0.5%水溶液),滴加質量分數為20%的六亞甲基四胺-鹽酸緩沖液(pH 5.0)至溶液呈穩定的紫紅色后再加入4 mL緩沖液,用已標定的0.001 mol/L EDTA溶液滴定至溶液由紫紅色變成黃色,記錄EDTA的消耗量。樣品的Zn2+螯合能力計算公式見式(3):

式中:AP為沉淀中Zn2+含量,mg;P為樣品蛋白質含量,g。
1.2.6 界面性質測定
1.2.6.1 乳化性及乳化穩定性的測定
分別配置濃度為0.01%、0.02%、0.03%和0.04%的脫酰胺蛋白溶液。取150 mL蛋白溶液與50 mL大豆油混合,12 000 r/min均質 1 min,靜置,在 0 min和10 min時從容器底部取50μL乳狀液于試管中,加5mL 0.1%的十二烷基磺酸鈉(sodium dodecylsulphate,SDS),充分混勻,于500 nm處測定吸光度值(以0.1%的SDS調整儀器零點)[13]。乳化活性指數及乳化穩定性的計算方法見公式(4)、(5)。
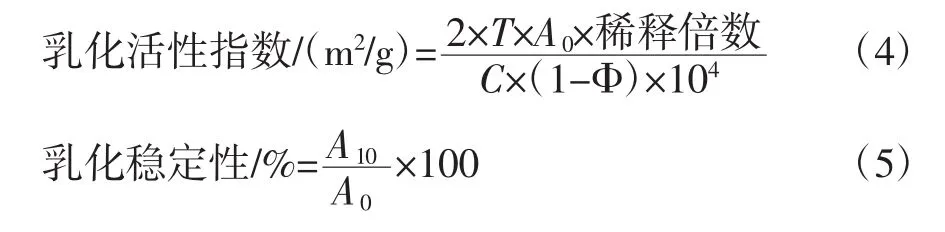
式中:T=2.303;A0為零時刻的吸光度值;C為蛋白質濃度,g/mL;Φ為溶液中油的體積分數;A10為靜置10 min后的吸光度值。
1.2.6.2 起泡性及泡沫穩定性的測定
準確稱取2 g乳清分離蛋白(脫酰胺乳清分離蛋白),加入100 mL水,置于裝料杯中,在高速組織搗碎機中攪打1 min,迅速倒入500 mL量筒中,記錄泡沫體積a;靜置10 min后,再次測量泡沫體積b[14]。起泡性與泡沫穩定性計算公式見公式(6)、(7)。

1.3 統計分析
采用SPSS16.0軟件中的單因素方差分析(Oneway ANOVA)和Duncan’s多重比較法進行數據統計分析,p<0.05為差異顯著,p<0.01為差異極顯著。所有指標的數據均以平均值±標準偏差表示。用Excel 2007軟件作圖。
2 結果與分析
2.1 乳清分離蛋白限制性脫酰胺反應條件
通過研究發現,酶添加量分別為 0.2、0.4、0.6、0.8、1.0 U/g乳清分離蛋白時,谷氨酰胺酶對乳清分離蛋白的脫酰胺作用隨酶添加量的增加而增大(如圖1),而酶添加量分別為0.8、1.0 U/g乳清分離蛋白時,脫酰胺度沒有大幅度變化,基本一致。
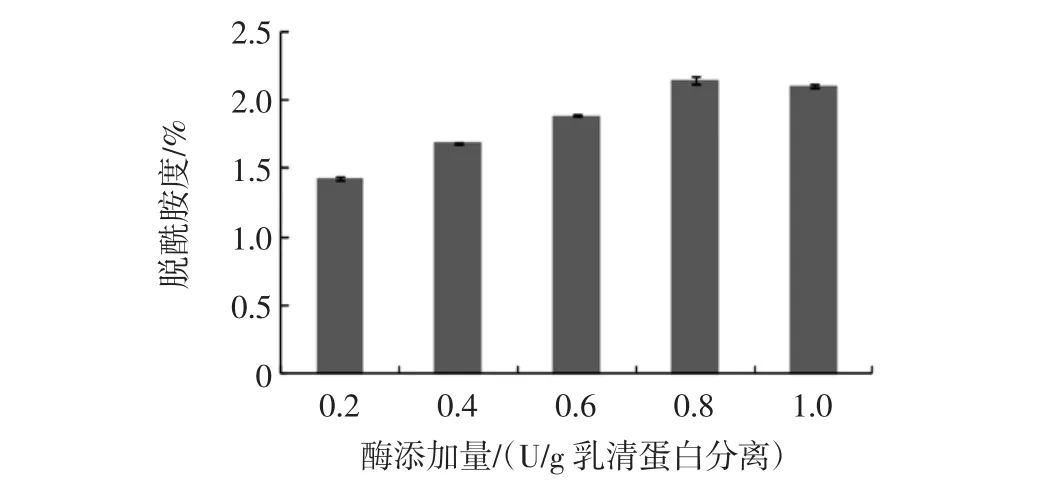
圖1 酶添加量對乳清分離蛋白脫酰胺度的影響(n=3)Fig.1 The effect of addition level of glutaminase on the degree of deamidation of WPI(n=3)
脫酰胺度隨反應時間的延長而增加(如圖2)。
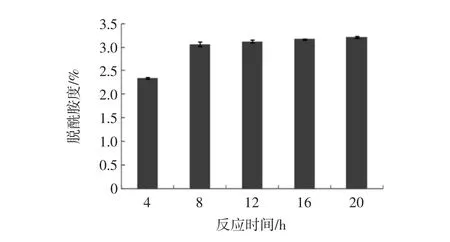
圖2 反應時間對乳清分離蛋白脫酰胺度的影響(n=3)Fig.2 The effect of reaction time of glutaminase on the degree of deamidation of WPI(n=3)
當反應達到8 h以上時,脫酰胺度趨于平緩狀態。說明即使繼續延長反應時間,也不會增加脫酰胺度。因此,酶添加量選取0.8 U/g乳清分離蛋白、反應時間在8 h以下為宜。
乳清分離蛋白的脫酰胺反應還與反應溫度及pH值有關(如圖3、圖4)。
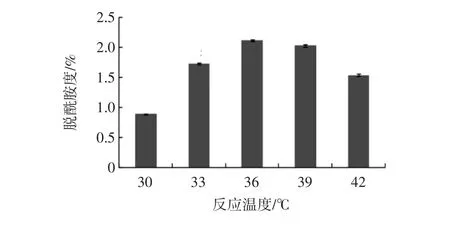
圖3 反應溫度對乳清分離蛋白脫酰胺度的影響(n=3)Fig.3 The effect of reaction temperature on the degree of deamidation of WPI(n=3)
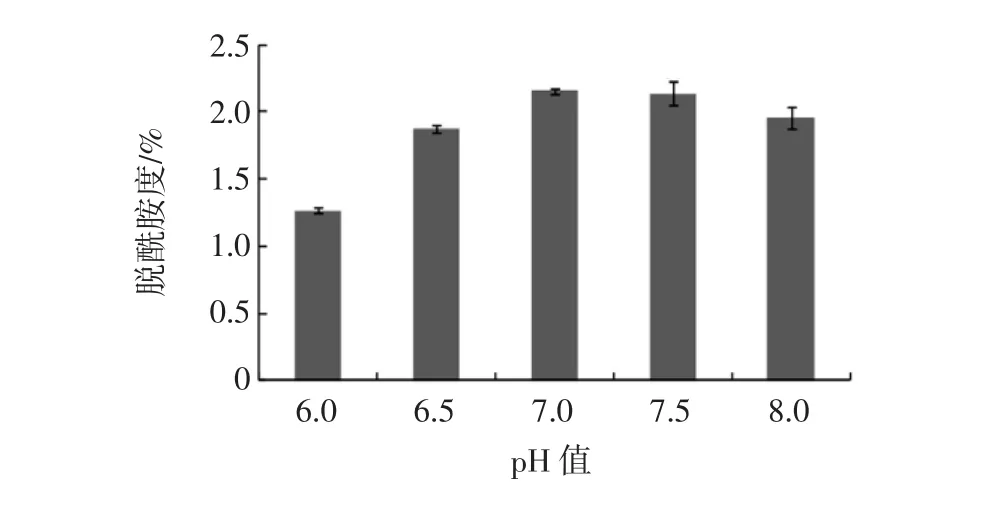
圖4 反應pH值對乳清分離蛋白脫酰胺度的影響(n=3)Fig.4 The effect of pH on the degree of deamidation of WPI(n=3)
隨著反應溫度的提高,乳清分離蛋白脫酰胺度呈先上升后下降的趨勢,當溫度為36℃時,脫酰胺度(2.1%)達到最高。另外,反應pH值對乳清分離蛋白脫酰胺度也有不同程度的影響。當pH值為7時,乳清分離蛋白脫酰胺度達到最高,這說明,谷氨酰胺酶在pH7條件下作用于乳清分離蛋白時,其酶活性達到最高。
因此,可以初步確定乳清分離蛋白限制性脫酰胺反應的適宜條件為:乳清分離蛋白溶液濃度5%、酶添加量0.8 U/g乳清分離蛋白、反應溫度36℃、反應pH為7。在此條件下,反應分別進行1、4、8 h時,乳清分離蛋白脫酰胺度分別為1.5%、2.3%、2.9%,在以后的研究中分別稱為脫酰胺乳清分離蛋白(deamidated whey protein isolated,DWPI)1、2、3(或 DWPI 1、DWPI 2、DWPI 3)。
2.2 脫酰胺對乳清分離蛋白界面性質的影響
2.2.1 乳化性質
食品蛋白質的功能特性與分子結構具有高度相關性,因此脫酰胺反應也必定影響到乳清分離蛋白的功能性質。乳清分離蛋白、脫酰胺乳清分離蛋白的乳化活性及乳化穩定性的相關評價結果如圖5、圖6所示。本研究選取脫酰胺反應1 h和8 h的乳清分離蛋白制品DWPI 1、DWPI 3作為分析對象。
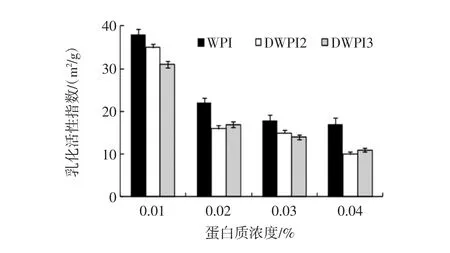
圖5 乳清分離蛋白與脫酰胺乳清分離蛋白的乳化活性指數(n=3)Fig.5 Emulsifying activity index of WPI and DWPI products(n=3)
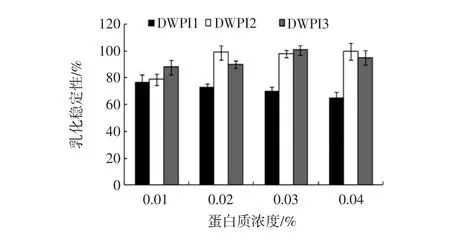
圖6 乳清分離蛋白與脫酰胺乳清分離蛋白的乳化穩定性(n=3)Fig.6 Emulsifying stability index of WPI and DWPI products(n=3)
由圖5可知,與乳清分離蛋白相比,4個濃度下的脫酰胺乳清分離蛋乳狀液的乳化活性指數均呈降低趨勢,而乳化穩定性都有不同程度的升高,尤其在高濃度下,脫酰胺乳清分離蛋白較乳清分離蛋白而言具有非常高的乳化穩定性。當蛋白質濃度為0.03%時,DWPI 1和DWPI 3的乳化穩定性接近100%,而WPI的乳化穩定性僅為70%。這一結果顯示,經谷氨酰胺酶脫酰胺的乳清分離蛋白制品提高了乳化穩定性,而削弱了乳化活性。乳清分離蛋白經脫酰胺后,會生成更多的谷氨酸殘基,從而乳清分離蛋白分子增加了許多帶負電荷的羧基。從而導致修飾后的蛋白質分子疏水性降低,蛋白質分子間的靜電斥力增大,與水結合的能力有所提高。從理論上講,蛋白質的疏水性降低會導致蛋白質修飾產物的乳化活性降低,而蛋白質間的靜電斥力和與水結合的能力增加,導致乳化穩定性提高。這也解釋了,脫酰胺乳清分離蛋白的乳化活性比乳清分離蛋白的低,而乳化穩定性有所提高的原因。
2.2.2 泡沫性質
經過對比乳清分離蛋白與脫酰胺乳清分離蛋白制品(DWPI 1、DWPI 3)的另外一個界面性質—泡沫性質發現,在同一濃度下,脫酰胺乳清分離蛋白的起泡性比乳清分離蛋白的起泡性有所提高,并且隨著脫酰胺度的增加,起泡性隨著增加,而泡沫穩定性隨脫酰胺度的增加有所降低(如圖7)。
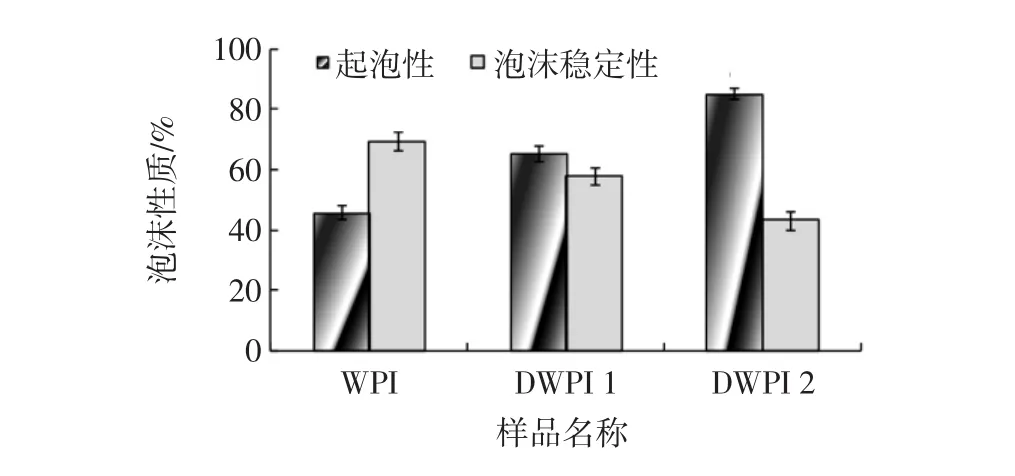
圖7 乳清分離蛋白與脫酰胺乳清分離蛋白的泡沫性質(n=3)Fig.7 Foam properties of WPI and DWPI products(n=3)
本研究中,DWPI 3的起泡性為85.2%,為WPI的1.86倍;而WPI的泡沫穩定性是DWPI 3的1.6倍。究其原因,起泡性的提高與脫酰胺度有關。
2.3 乳清分離蛋白及脫酰胺乳清分離蛋白對Fe2+/Zn2+的螯合能力
有研究表明,蛋白質水解物具有與金屬離子如鐵、鋅等螯合的能力,進而提高礦物質的溶解性和生物利用率[15]。本試驗測定了乳清分離蛋白及脫酰胺乳清分離蛋白產物DWPI 1、DWPI 2、DWPI 3與二價金屬離子的螯合能力,研究脫酰胺度對乳清分離蛋白與二價金屬離子螯合能力的影響,結果如表1所示。
從表1中能夠看出,與乳清分離蛋白相比,脫酰胺乳清分離蛋白螯合二價鐵的能力略有增加,當脫酰胺度達到2.9%時,DWPI 3與Fe2+螯合能力達到(2.98±0.19)%,比乳清分離蛋白的螯合能力提高了49.7%,即乳清分離蛋白殘基上谷氨酰胺轉化為谷氨酸的量越多,與二價鐵螯合能力越強。

表1 乳清分離蛋白與脫酰胺乳清分離蛋白產物的Fe2+、Zn2+螯合能力(n=3,p<0.05)Table 1 Iron,zinc chelating activity of WPI or DWPI products(n=3,p<0.05)
同樣,乳清分離蛋白及脫酰胺產物與Zn2+螯合能力的測定結果顯示,隨著脫酰胺度的增加,脫酰胺蛋白產物的Zn2+螯合能力呈現增大的趨勢,DWPI 3的Zn2+螯合能力較WPI的螯合能力提高了27.3%。Wang等[16]研究結果表明,蛋白質水解物與Zn2+螯合能力不同,是由其游離氨基的含量引起的,因此脫酰胺乳清分離蛋白表現出不同的Zn2+螯合能力也可能與其游離氨含量不同有關。
食品蛋白質螯合金屬離子能力越強,其相關生物活性就越強,如對Fe2+螯合能力越強,其蛋白質抗氧化能力越強;對Zn2+螯合能力越強,其蛋白質ACE抑制作用也相應提高[17]。因此,脫酰胺乳清分離蛋白與Fe2+/Zn2+的螯合能力有益于促進蛋白的其他生物活性。
3 結論
以脫酰胺度為評價指標,通過單因素分析考察酶添加量、反應溫度、反應pH值及反應時間對乳清分離蛋白限制性脫酰胺的影響并確定適宜的脫酰胺條件:乳清分離蛋白的濃度為5%、谷氨酰胺酶添加量0.8 U/g乳清分離蛋白、36℃、pH 7。在此適宜反應條件下分別反應1、4、8 h,制得3種脫酰胺乳清分離蛋白,其脫酰胺度分別為1.5%、2.3%、2.9%。限制性脫酰胺對乳清分離蛋白的一些功能性質有了不同程度的改變,其中脫酰胺反應提高了乳清分離蛋白的乳化穩定性、起泡性及對二價金屬離子Fe2+/Zn2+的螯合能力,并隨著脫酰胺度的增加而增加;而脫酰胺乳清分離蛋白的乳化活性及泡沫穩定性由于限制性脫酰胺作用而有所下降。研究結果可以為開發多功能食品提供很好的基料以及理論基礎。

