八氫菲選擇性催化裂化反應動力學
唐津蓮
(中國石化 石油化工科學研究院, 北京 100083)
在石油資源日益緊缺的情況下,為實現石油資源的高效利用,中國石化石油化工科學研究院針對重質FCC原料油特點并結合催化裂化過程反應化學提出了選擇性催化裂化的技術構思[1]。選擇性催化裂化(簡稱HSCC,Highly selective catalytic cracking)是將單程轉化率控制在一定范圍,通過催化裂化反應過程的時間約束與空間約束[2]使重質原料油中烷烴結構基團發生選擇性裂化反應并處于最佳狀態,盡可能地將原料油中雙環、三環以上芳烴和膠質的芳環結構保留在催化蠟油(簡稱FGO,FCC gas oil)中,從而使得重質原料油裂化的干氣和焦炭總選擇性最小。高效轉化原料油中的烷烴結構基團同時盡可能保留原料油中雙環、三環以上芳烴和膠質的芳環結構不受破壞,是HSCC工藝開發所面臨的重要問題之一。因此,HSCC技術的核心是實現多環芳烴的選擇性催化裂化。
唐津蓮等[3]研究表明,在質量空速為10 h-1、溫度450~550℃、劑/油質量比3~9范圍,隨著反應溫度升高或劑/油質量比增加,重質油環烷芳烴特征化合物八氫菲的轉化率提高,焦炭選擇性增加,尤其是劑/油質量比高于6時焦炭選擇性增加顯著,環烷環開環和烷基側鏈斷裂反應產物輕質油烴的選擇性顯著降低。
為了深入研究多環芳烴的選擇性催化裂化反應歷程,在小型固定流化床(FFB)實驗裝置上,采用具有適宜孔徑和酸度的HSCC催化劑,建立并考察了八氫菲的選擇性催化裂化反應動力學模型,進一步闡釋HSCC過程的反應化學。
1 實驗部分
1.1 儀器、原料與催化劑
采用煉廠氣分析儀(安捷倫公司產品)測定裂化氣與煙氣組成;采用質譜Agilent HP 6890/HP 5973和色譜柱HP-1 MS(30 m×250 μm×0.25 μm)測定液體產物中的烴類。將含Y分子篩的HSCC催化劑在790℃、100%水蒸氣下老化處理20 h,得到催化劑CAT-Y,其催化微反活性MAT=54[4]。
原料八氫菲(Octohydrophenanthrene,縮寫為OHF)由菲(實驗純,質量分數99%,美國ACROS公司產品)經加氫得到,其組成(質量分數)為八氫菲55.91%,全氫菲21.82%,四氫菲16.00%,9,10-二氫菲2.17%,菲3.96%,丁基十氫萘0.14%。
1.2 實驗方法與數據處理
在小型固定流化床(FFB)裝置上,以CAT-Y為催化劑,在保持質量空速10 h-1不變,反應溫度470~515℃、劑/油質量比3~9條件下,在消除內、外擴散影響的基礎上,考察八氫菲選擇性催化裂化的動力學特性。為確保數據真實可靠,每個實驗點進行3次平行實驗。
單位反應時間(1 s)內,每克進料所得氣體或液體產物中單體烴的收率計算如式(1)所示。
yx=y×wx×104/τ
(1)
1.3 內、外擴散影響的消除
實驗采用的催化劑CAT-Y為微球狀固體,平均粒徑(d)60~100 μm,比表面積95 m2/g,平均孔徑34 nm且80%集中在30~40 nm,屬于大孔徑小粒徑催化劑。通過催化劑細分粒度的方法來檢驗內擴散對反應速率的影響較難,故通過Mears準則來判斷現有粒度的催化劑的內擴散影響[5-6]。即當Thiele模數Φ?|n|-1成立時,對于n級反應內擴散對反應速率的影響可忽略。模數Φ的計算公式見式(2)。
Φ=(r)obsd2/(4DeCs)?|n|-1
(2)
文中涉及的催化裂化反應級數定為1。
八氫菲的裂化反應與蠟油催化裂化類似[7],Φ的數量級則為10-4~10-3,遠小于|n|-1=1,因此在本實驗范圍內可以不處理溫度梯度對氣體產物擴散的影響而忽略內、外擴散影響[8-9]。
1.4 八氫菲裂化反應動力學實驗設計
八氫菲裂化反應動力學采用正交實驗法設計,以反應溫度與劑/油質量比為因素, 每個因素取4個水平,選用正交表L32(44)[10]完成八氫菲裂化動力學的整體實驗設計。為維持相同的質量空速,劑/油質量比不同則進料時間不同。表1為八氫菲裂化的正交實驗因子和水平表及其不同劑/油質量比對應的進料時間。
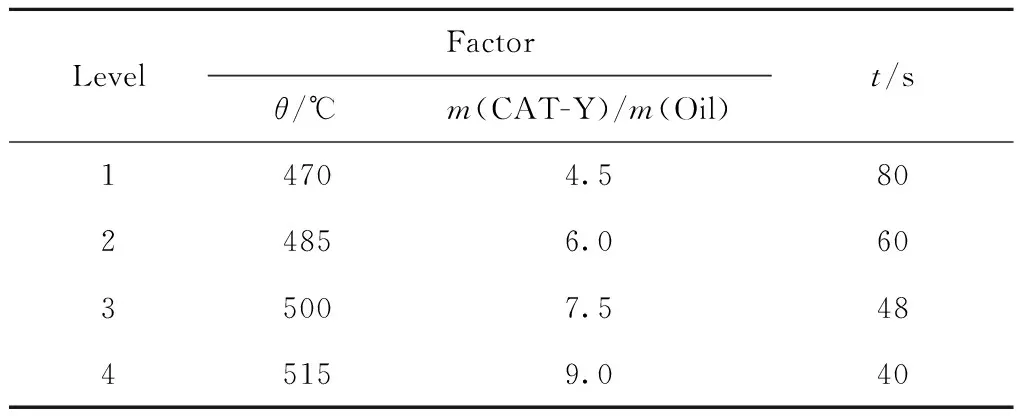
表1 八氫菲裂化的L32(44) 正交實驗因子和水平表及 其不同劑/油質量比對應的進料時間(t)Table 1 Factors and levels of L32(44) orthogonal design for octohydrophenanthrene catalytic cracking and feed time(t) under different m(CAT-Y)/m(Oil)
m(CAT-Y)=240 g; MHSV=10 h-1
2 結果與討論
2.1 八氫菲選擇性催化裂化反應途徑及其動力學模型
在FFB裝置上,在500℃、劑/油質量比6、質量空速10 h-1條件下,八氫菲在催化劑CAT-Y沸石表面或/和無定形基質的B酸中心上,通過正碳離子反應歷程主要發生環烷環開環反應以及脫氫縮合反應[3],其反應途徑如圖1所示。
由圖1可以看出,八氫菲在沸石催化劑上主要發生裂化開環反應生成丙烷、丙烯、丁烷、丁烯、甲基戊烷和環戊烷、環己烷等非芳烴,苯、烷基苯等單環芳烴以及裂化開環產物的氫轉移產物萘等雙環芳烴;另外,較少量的八氫菲脫氫縮合生成菲、芘等多環芳烴,多環芳烴深度氫轉移生成焦炭。據此,把不同溫度、不同劑/油比下八氫菲裂化反應物和裂化產物劃分為八氫菲、非芳烴、單環芳烴、多環芳烴和焦炭六集總,并建立八氫菲反應網絡如圖2 所示,以雙曲線型Langmuir-Hinshelwood(L-H)模型來描述八氫菲裂化的動力學行為。
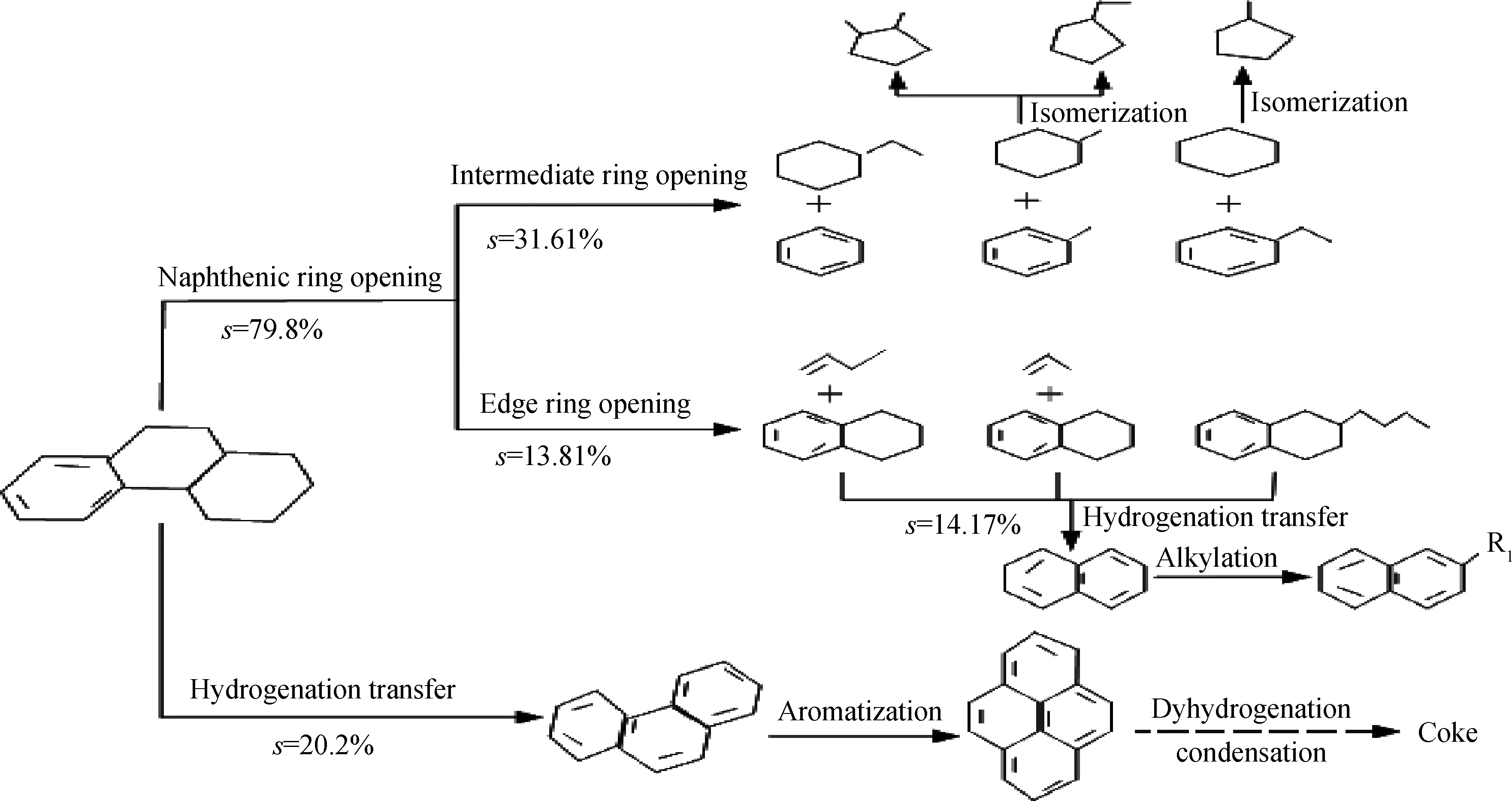
圖1 八氫菲選擇性催化裂化反應途徑Fig.1 Reaction pathway from selective catalytic cracking of OHF θ=500℃; m(CAT-Y)/m(Oil)=6; MHSV=10 h-1
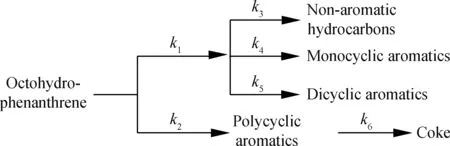
圖2 八氫菲選擇性催化裂化反應網絡Fig.2 Reaction network from selective catalytic cracking of OHF
根據圖2所示反應網絡建立八氫菲裂化六集總動力學模型及裂化反應本征反應動力學方程見式(3)。
(3)
假設催化劑CAT-Y為球形,則式(3)可改為式(4)。
擴散系數定義為ηss,計算式見式(5)。
(5)
由式(3)~(5)得到八氫菲本征反應動力學方程見式(6)。
(6)
對上述模型進行簡化,具體步驟如下:
a.八氫菲的吸附能力沒有可參考文獻,但有研究認為含多環芳烴重質油的吸附常數在計算裂化反應速率常數時可以忽略不計,因此八氫菲的吸附不予以考慮。
b.八氫菲分子直徑為1.0~1.1 nm,均小于催化劑孔徑(催化劑CAT-Y的中值孔徑為1.151 nm),反應溫度越高,氣體反應物擴散速率越快,越易于消除擴散對裂化反應的限制,且已進行擴散影響消除的分析 (見1.3節),因此可忽略裂化反應過程中的擴散控制,即:ηss=1。
c.實驗最低反應溫度470℃,最高515℃,由熱裂化產物選擇性分析可知,熱裂化反應比例極低,因此動力學計算過程可忽略熱裂化反應,熱裂化反應速率常數忽略不計。
基于以上內容簡化式(6),八氫菲的轉化速率方程,非芳烴、單環芳烴、雙環芳烴、焦炭的生成反應速率方程見式(7)~(12)。其中式(7)中k1=k3+k4+k5。
(7)
(8)
(9)
(10)
(11)
(12)
催化劑失活系數見式(13)。
(13)
反應動力學速率常數阿倫尼烏斯公式表達式見式(14)。
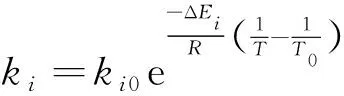
(14)
2.2 八氫菲選擇性催化裂化反應動力學模型參數估值
對式(7)~式(12)積分,并結合式(13),以最小二乘法求取各動力學參數,使求得的各產物收率的計算值與實驗值符合式(15)。
(15)
參數估值求得不同溫度下各動力學速率常數見表2。

表2 不同溫度下八氫菲選擇性催化裂化動力學常數Table 2 Estimated kinetic parameters for selective catalytic cracking of OHF at different temperatures
由表2可見,隨反應溫度升高,各反應速率常數均增大。這是因為隨反應溫度升高,原料分子碰撞幾率增大,從而使得其反應速率加快。八氫菲生成多環芳烴的速率常數(k2)明顯大于裂化開環反應速率常數(k1),這是因為環烷芳烴在酸性催化劑環境下較易發生脫氫縮合反應,生成多環芳烴。八氫菲環烷環開環反應中,非芳烴的生成速率常數(k3)大于單環芳烴的生成速率常數(k4),二者又均遠遠大于雙環芳烴的生成速率常數(k5),說明多環的環烷芳烴發生裂化開環反應,更容易生成C3~C6的低碳烷烴和環烷烴等非芳烴和單環芳烴,而單環芳烴脫氫生成雙環芳烴的幾率較低。八氫菲脫氫縮合反應中,多環芳烴的生成速率常數(k2)和多環芳烴轉化的生成焦炭速率常數(k6)隨著反應溫度升高而增大,但在500℃左右存在最大值。說明在500℃以下,反應溫度越高八氫菲越容易發生脫氫縮合反應;但是當反應溫度高于500℃時,脫氫縮合速率常數降低。這主要是動力學和熱力學因素對氫轉移反應交互影響的結果,500℃以下受動力學因素影響,脫氫縮合反應速率常數隨溫度升高而增大,但是氫轉移反應是放熱反應,高溫不利于氫轉移反應的發生,從而導致515℃脫氫縮合反應速率常數降低。此外,多環芳烴的生成速率常數(k2)高于多環芳烴轉化的生成焦炭速率常數(k6),而二者的差值隨著溫度升高而增大。由此可見,八氫菲縮合生成的多環芳烴在催化裂化過程中是可以保留下來的,并且可以利用反應溫度對氫轉移反應的影響,最大量保留生成的多環芳烴而抑制其生成焦炭。
采用表2數據及式(14),線性二元回歸法求得八氫菲裂化反應動力學方程各參數相應值見表3。由表3可見,八氫菲裂化環烷環開環反應活化能為70.63 J/mol,而其脫氫縮合反應活化能為48.71 J/mol。表3中各集總反應活化能較低,主要是由于求得的是總包反應活化能,其中包括吸附能力較強的八氫菲和多環芳烴的吸附熱,兩者吸附熱較高。因此,本實驗中各集總的反應活化能在23~72 J/mol之間,其數值在常規重油催化裂化反應活化能數值范圍內,所求得的各反應活化能數值是合理可信的。
因此,結合表3數值和公式(14)代入公式(7)~(13)分別得到八氫菲轉化速率方程,非芳烴、單環芳烴、雙環芳烴、多環芳烴和焦炭的反應速率方程見式(16)~(21)。
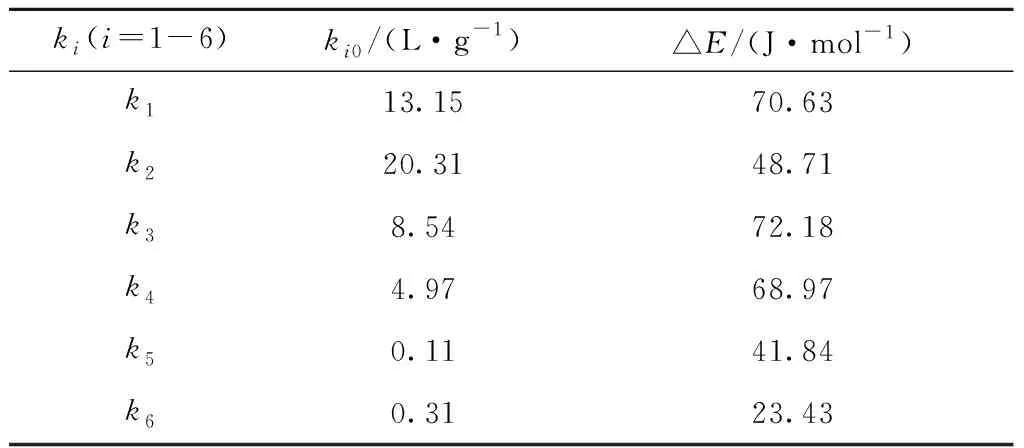
表3 八氫菲選擇性催化裂化反應動力學方程參數Table 3 Estimated kinetic parameters for selective catalytic cracking of OHF
(16)
(17)
(18)
(19)
(20)
(21)
2.3 八氫菲選擇性催化裂化反應動力學模型檢驗
由式(7)~式(12)積分求得各集總產物收率的計算值表達式,并根據得到的各反應常數,求得各集總產物收率的計算值與實驗值的平均誤差(Mean deviation)。八氫菲裂化動力學模型的殘差檢驗及復相關系數R檢驗結果均列于表4。
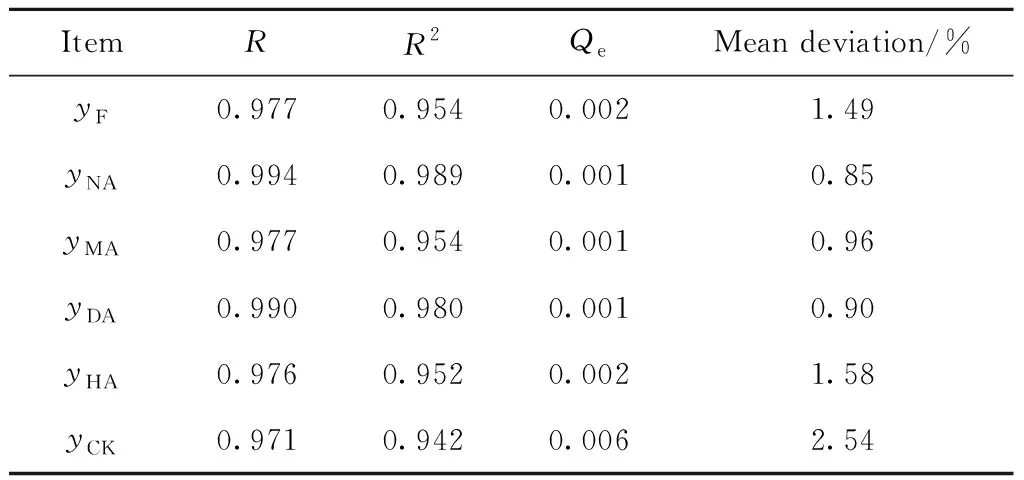
表4 八氫菲選擇性催化裂化動力學模型的統計檢驗Table 4 Statistical test data of estimated kinetic model for selective catalytic cracking of OHF
由表4可見,各參數的平均偏差均小于5%,符合動力學平均誤差不大于10%的要求,說明動力學模型方程線性回歸比較可靠;Qe值均小于0.01,復相關指數R和相關指數R2均大于0.95,說明通過復相關系數檢驗,可證實各個回歸模型方程的顯著性。因此,方差檢驗結果表明回歸模型方程整體來看是顯著和可信的,將其作為八氫菲裂化動力學行為的描述是可行的。
2.4 八氫菲選擇性催化裂化反應動力學模型意義
根據有效空間約束定義,唐津蓮等[4]定義了有效空間約束指數ESCI,即有效空間約束為FCC催化劑上芳烴側鏈斷裂和環烷環開環的選擇性催化裂化。根據此定義,八氫菲的有效空間約束指數計算公式見式(22)。
(22)
有效空間約束指數ESCI反映了環烷芳烴在裂化反應過程中發生環烷環開環反應與脫氫縮合反應的相對比例,該比值越大,環烷芳烴發生環烷環開環反應的比例越大,則發生脫氫縮合反應的相對比例越小。ESCI可用于篩選催化劑和確定單體烴HSCC的適宜工藝條件。
如果采用產物非芳烴、單環芳烴、雙環芳烴與多環芳烴和焦炭的動力學速率常數的比值來篩選催化劑,相比采用具體某一特定反應的環烷環開環反應產物與脫氫縮合反應產物的產率或選擇性比值,則更能反映出催化劑對原料選擇性催化裂化的性能。這是因為環烷環開環反應與脫氫縮合反應速率常數的比值只與反應溫度有關,不受原料組成、劑/油比、反應時間影響。因此,以八氫菲裂化環烷環開環反應動力學速率常數與其脫氫縮合反應動力學速率常數的比值作為原料中多環芳烴選擇性催化裂化的有效空間約束指數,定義為ψ1,即:
(23)
ψ1與ESCIOHF同樣反映了多環芳烴在裂化反應過程中環烷環開環反應與脫氫縮合反應的相對比例,但是ψ1比ESCIOHF更適宜用于多環芳烴HSCC催化劑的篩選。反應溫度越高,則ψ1越高;在同一反應溫度下,ψ1高的催化劑更有利于環烷環開環反應。
通過以上分析可見,八氫菲裂化L-H動力學模型具有一定的意義。所采用的裂化反應網絡是遵循八氫菲裂化開環生成非芳烴、單環芳烴和雙環芳烴,脫氫縮合反應生成三環以上多環芳烴,三環以上多環芳烴進一步脫氫縮合生成焦炭的反應步驟建立的。本動力學模型不僅有利于解釋催化裂化過程中環烷芳烴的反應途徑及其影響因素,而且對選擇性催化裂化的工藝條件選擇、反應途徑優化和工藝設計以及篩選HSCC催化劑有一定的參考價值。
3 結 論
(1)八氫菲在選擇性催化裂化(HSCC)催化劑表面裂化發生環烷環開環反應以及脫氫縮合反應,排除了內、外擴散控制影響,其生成速率取決于表面反應速率。
(2)在給出八氫菲催化裂化反應網絡的基礎上,建立了八氫菲裂化雙曲線型Langmuir-Hinshelwood(L-H)六集總動力學模型,結合實驗采用最小二乘法對其參數進行估值。
(3)八氫菲裂化環烷環開環反應活化能為70.63 J/mol,而其脫氫縮合反應活化能為48.71 J/mol。
(4)對所建立八氫菲裂化六集總動力學模型依次進行殘差檢驗和統計檢驗,檢驗結果表明,所得八氫菲裂化L-H型動力學模型殘差分布合理、參數回歸顯著,模型合理、可靠,能夠真實反映八氫菲裂化反應特性,可為富含環烷芳烴重質油的選擇性催化裂化工藝的工藝條件選擇、反應途徑優化和工藝設計以及篩選HSCC催化劑提供理論指導與設計依據。
符號說明:
CA——物質A的摩爾濃度,mol/L;
Ci,ex——反應物在催化劑表面摩爾濃度,mol/L;
Ci,in——反應物在催化劑孔道內摩爾濃度,mol/L;
Cs——反應物在催化劑表面的摩爾濃度,mol/L;
d——催化劑顆粒的直徑,cm;
De——反應物在催化劑顆粒中的有效擴散系數,cm2/min;
De,i——物種i分子在催化劑內的有效擴散系數;
ΔEi——反應活化能,i=1~6,J/mol;
ESCIOHF——八氫菲的有效空間約束指數;
f——偏差平方和
k1——八氫菲裂化環烷環開環反應生成非芳烴與單環芳烴的速率常數,s-1;
k2——八氫菲脫氫生成三環以上多環芳烴的反應速率常數,s-1;
k3——八氫菲裂化環烷環開環生成非芳烴的速率常數,s-1;
k4——八氫菲裂化環烷環開環生成單環芳烴的速率常數,s-1;
k5——八氫菲環烷環開環產物單環芳烴進一步氫轉移生成雙環芳烴的速率常數,s-1;
k6——八氫菲氫轉移產物多環芳烴進一步脫氫縮合生成焦炭的反應速率常數,s-1;
ki0——指前因子,i=1~6,L/g;
kai——某物質i的吸附速率常數,s-1;
ki——某物質i的初始動力學速率常數,s-1;
l——催化劑孔道內物種距催化劑表面的距離,cm;
mcr——催化劑藏量,g;
n′——樣本數;
n——反應級數;
Qe——Q檢驗值;
rA——反應物中某物質A的反應速率,mol/(L·min);
ri——物質i的產生、消耗速率,mol/(L·min);
rmean——反應速率,mol/(L·min);
(r)obs——表觀反應速率,mol/(L·min);
R——復相關指數;
Rcr——催化劑孔徑,cm;
R2——相關指數;
s——產物質量選擇性,%
t——反應時間,s;
T——反應溫度,K;
T0——反應初始溫度,K;
V——催化劑床層體積,L;
wx——反應氣體或液體產物中單體烴x的質量分數,%;
y——氣體或液體產物收率,%;
yCK——焦炭質量收率,%;
yDA——雙環芳烴質量收率,%;
yF——八氫菲進料的質量分數,%;
yHA——多環芳烴質量收率,%;
yi——某產物收率的實驗值,%;

yMA——單環芳烴質量收率,%;
yNA——非芳烴質量收率,%;
yx——每克進料所得氣體或液體產物中單體烴的收率,%;
α——多環芳烴與八氫菲原料平均相對分子質量的比值;
ε——催化劑空隙率;
Φ——改型Thiele模數;
ηss——擴散系數,cm2/s;
φint——催化劑失活函數;
λ——催化劑失活參數;
ρcr——催化劑密度,g/cm3;
τ——物料在反應器中停留時間,s;
ψ1——有效空間約束指數。

