超聲引導下不同部位神經阻滯用于胸腔鏡手術鎮痛的對比研究*
楊建兵,王浩杰,嚴峰
(浙江省余姚市人民醫院 麻醉科,浙江 余姚 315400)
超聲可視化技術在神經阻滯鎮痛的使用是醫學科學發展的趨勢,它使得傳統的鎮痛管理模式得到挑戰。現今,胸椎旁神經阻滯很流行,已經廣泛用于胸部手術的麻醉與鎮痛。2016年,FORERO等[1]報道了胸椎豎脊肌平面神經(erector spinae plane block,ESP)阻滯,將其用于胸部神經鎮痛中取得了很好的效果。本研究將擬采用隨機對照的方法,評價這種神經阻滯方式和胸椎旁神經阻滯(thoracic paravertebral nerve block,TPVB)在胸腔鏡肺葉切除術中輔助鎮痛的有效性和安全性,為選擇最佳的區域阻滯作為參考。
1 資料與方法
1.1 一般資料
隨機選擇我院擇期手術需要胸腔鏡肺葉切除手術的全麻患者,年齡18~60歲,性別不限,體重37~86 kg,美國麻醉醫師協會分級(American Society of Anesthesiologists,ASA)Ⅰ或Ⅱ級。經過醫院醫學倫理委員會同意,術前會診跟家屬交代神經阻滯的風險。排除標準:術前無嚴重高血壓、無嚴重心肺疾患,無病態肥胖[(體質指數(body mass index,BMI)>40 kg/m2],無對局麻藥物過敏,無肝腎功能不全或精神疾病,凝血檢查無異常,胸背穿刺部位皮膚無破損及感染,患者均為自愿接受術后鎮痛方案并簽署知情同意書。將患者隨機分成兩組:胸椎ESP阻滯聯合靜脈自控鎮痛泵(patient-controlled intravenous analgesia,PCIA)組(P組)和TPVB聯合PCIA組(C組)。兩組患者年齡、性別、體重、身高、ASA分級和手術時間等比較差異無統計學意義(P>0.05),具有可比性。見表1。

表1 兩組患者一般情況的比較Table 1 Comparison of clinical charatcteristics between the two groups
1.2 超聲引導下神經阻滯方法
1.2.1 麻醉前 麻醉前常規禁飲、禁食8 h。入室后開放外周靜脈,麻醉前右美托咪定靜脈泵注負荷劑量1μg/kg(10 min),常規監測血壓(blood pressure,BP)、心電圖(electrocardiogram,ECG)和脈搏血氧飽和度(pulse oxygen saturation,SpO2)等后開始神經阻滯操作。患者取側臥位(開胸側朝上)或坐位,T5胸椎棘突正中旁開約2.0~2.5 cm椎旁間隙為穿刺點,使用索諾聲TURBO型彩色多譜勒超聲診斷儀,探頭用超薄內鏡隔離消毒薄膜包裹,探頭與脊柱垂直在穿刺點附近掃描,在超聲下明確重要解剖標志的超聲圖像(棘突,橫突,胸膜和肋橫突韌帶),看到椎旁間隙圖像后(附圖),應用超聲平面內穿刺技術,在局麻藥充分浸潤皮膚和皮下組織后,使用20G局麻針,于超聲探頭一側進針,P組患者在T5胸椎橫突后回抽無血后注入0.375%羅哌卡因20 ml阻滯,C組患者在超聲實時引導下進針至T5椎旁間隙,回抽無血和氣后注入0.375%羅哌卡因20 ml阻滯。兩組患者在完成神經阻滯后即行全麻誘導,靜注咪達唑侖0.06 mg/kg、芬太尼3μg/kg、丙泊酚1.00 mg/kg、順式阿曲庫銨0.15 mg/kg,誘導后行氣管插管,接麻醉機行機控呼吸,調節潮氣量(tidal volume,VT)8~10 ml/kg,呼吸頻率(respiratory frequency,RR)10~12次/min,吸呼比(I∶E)1∶2,術中維持二氧化碳分壓(carbon dioxide partial pressure,PCO2)在 30 ~ 35 mmHg。
1.2.2 麻醉維持 靶控輸注丙泊酚4~8 mg/(kg·h)和順式阿曲庫銨1~2μg/(kg·h)。神經阻滯后20 min用冰塊法測定阻滯范圍,術者切皮前不追加任何鎮痛藥物。術中丙泊酚和瑞芬太尼進行麻醉維持。術中鎮痛和鎮靜藥物根據腦電雙頻指數(bispectral index,BIS)值調整,維持BIS值在40~60之間,芬太尼用量根據患者BP及心率(heart rate,HR)變化情況進行追加,維持波動范圍在術前基礎值±20%內。術中不給予非甾體抗炎藥物鎮痛。兩組患者均在術后給予PCIA。鎮痛液配方:舒芬太尼50μg+地佐辛10 mg稀釋至100 ml;鎮痛泵參數:背景劑量2 ml/h,負荷量2 ml,單次自控劑量0.5 ml,鎖定時間為15 min。在視覺模擬評分(visual analogue scale,VAS)>4分時給予嗎啡靜脈鎮痛。
1.3 觀察指標
記錄術后24 h內不同時點的靜息和咳嗽時VAS評分(0分:無痛;3分以下:有輕微的疼痛,能忍受;4~6分:患者疼痛并影響睡眠,尚能忍受;7~10分:患者有漸強烈的疼痛,疼痛難忍,影響食欲,影響睡眠)、鎮痛泵按壓次數、輸注總量。觀察記錄術后皮膚瘙癢、惡心嘔吐和呼吸抑制等不良反應的發生情況。
1.4 統計學方法
使用SPSS 18.0統計軟件進行數據分析。計量資料以均數±標準差(±s)表示,組內比較采用測量數據的方差分析,組間比較采用t檢驗或非參數秩和檢驗;計數資料以百分率(%)表示,組間比較采用χ2檢驗,等級資料比較采用Kruskal-WallisH檢驗。P<0.05為差異有統計學意義。
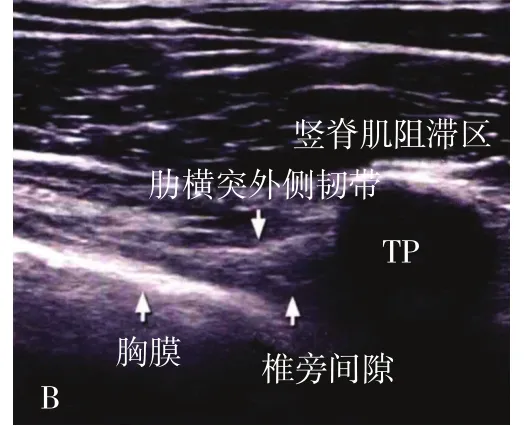
附圖 兩種神經阻滯的超聲下顯像Attached fig. Ultrasonic imaging of two different nerve blocks
2 結果
2.1 用冰塊法測定阻滯范圍
P組在胸部ESP阻滯20 min后,9例為T2~T6脊神經支配區域,11例患者平面為T2~T7脊神經支配區域。C組在胸椎旁神經阻滯20 min后,20例患者平面為T2~T7脊神經支配區域。
2.2 兩組患者術后不同時點的VAS評分
術后1~24 h內不同時點(1、6、12、18和24 h)兩組靜息和咳嗽VAS評分:1、6和12 h比較兩組無明顯差異(P>0.05),18和24 h P組的VAS評分高于C組,差異有統計學意義(P<0.05)。見表2~4。
2.3 兩組患者術后鎮痛泵按壓次數和輸注總量比較
有鎮痛泵的使用,可以通過多次按壓鎮痛泵來增加舒芬太尼的量達到鎮痛的目的。兩組鎮痛泵按壓次數和輸注總量比較結果無明顯差異(P>0.05)。見表5。
2.4 兩組術后不良反應比較
兩組患者術后惡心嘔吐、皮膚瘙癢發生率對比無明顯差異(P>0.05)。兩組患者術后均未出現過敏中毒、呼吸抑制、尿潴留和低血壓等不良反應。見表6。
表2 兩組患者術后不同時點靜息時VAS評分 (分,±s)Table 2 Comparison of VAS score at different points of resting after the operation between the two groups (score,±s)
組別 1 h 6 h 12 h 18 h 24 h P 組(n=20) 1.6±0.6 1.5±0.5 2.3±0.8 4.1±1.0 4.0±1.0 C 組(n =20) 1.7±0.5 1.7±0.2 2.2±0.9 2.4±1.0 2.5±1.0 t值 3.28 0.36 1.32 1.57 1.65 P值 0.257 0.332 0.321 0.006 0.005
表3 兩組患者術后不同時點咳嗽時VAS評分 (分,±s)Table 3 Comparison of VAS score at different points of cough after the operation between the two groups (score,±s)
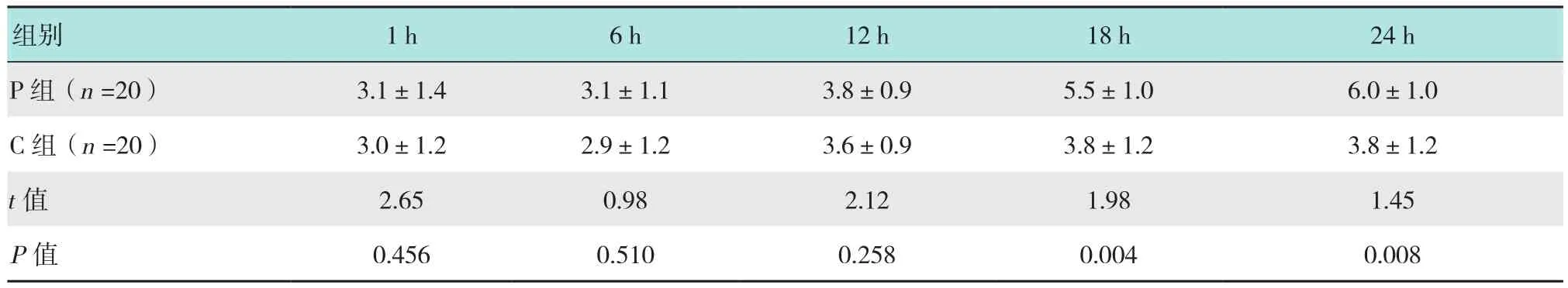
表3 兩組患者術后不同時點咳嗽時VAS評分 (分,±s)Table 3 Comparison of VAS score at different points of cough after the operation between the two groups (score,±s)
組別 1 h 6 h 12 h 18 h 24 h P 組(n=20) 3.1±1.4 3.1±1.1 3.8±0.9 5.5±1.0 6.0±1.0 C 組(n=20) 3.0±1.2 2.9±1.2 3.6±0.9 3.8±1.2 3.8±1.2 t值 2.65 0.98 2.12 1.98 1.45 P值 0.456 0.510 0.258 0.004 0.008
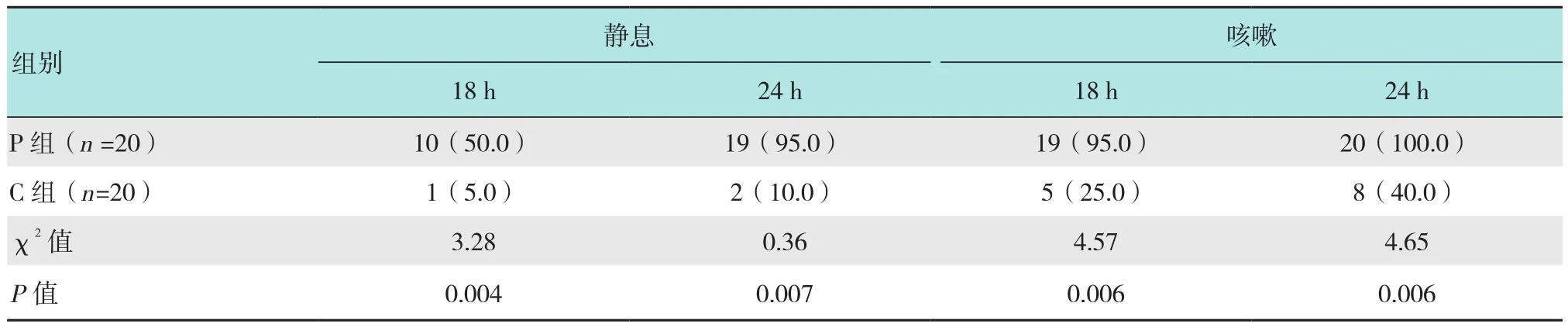
表4 兩組VAS>4分以上的例數的比較 例(%)Table 4 Comparison of the number of VAS>4 between the two groups n(%)
表5 兩組患者術后不同時間段鎮痛泵按壓次數和輸注總量比較 (±s)Table 5 Comparison of press times and consumption of analgesia pump at different points between the two groups (±s)

表5 兩組患者術后不同時間段鎮痛泵按壓次數和輸注總量比較 (±s)Table 5 Comparison of press times and consumption of analgesia pump at different points between the two groups (±s)
鎮痛泵按壓次數/次 鎮痛泵輸注總量/ml 0~12 h 0~24 h 0~12 h 0~24 h P 組(n=20) 1.2±0.8 3.0±1.5 25.1±1.9 52.2±3.4 C 組(n=20) 1.3±0.9 3.2±1.4 26.3±1.5 54.1±2.9 t值 3.65 4.55 3.28 2.65 P值 0.384 0.329 0.654 0.642組別
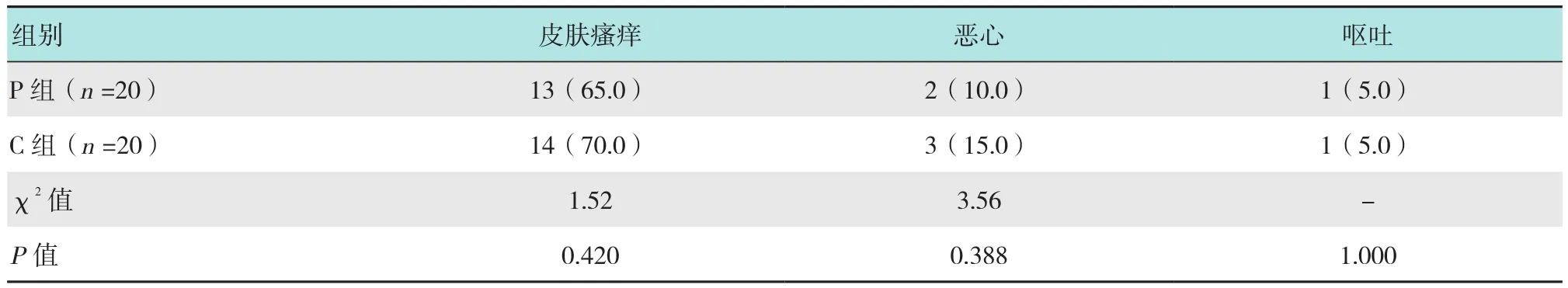
表6 兩組術后不良反應比較 例(%)Table 6 Comparison of adverse postoperative reactions between the two groups n(%)
3 討論
可視化技術在臨床麻醉中得到廣泛應用,它的應用使得傳統的麻醉技術得到變革性的改進。超聲技術在麻醉領域的發展,已經廣泛應用于氣道管理、臟器觀察和中心靜脈導管置入等領域,超聲下神經阻滯已經在各大醫院廣泛開展[2],超聲逐漸成為麻醉醫生的第三只眼睛[3]。超聲可視化技術的引進,能增加神經阻滯的安全性,盡管傳統的解剖學和神經刺激儀定位方式已經相當成熟,但通過超聲檢查方法觀察神經阻滯穿刺針的位置正確與否更加簡便和直觀,是麻醉技術邁出的一大步[4]。胸腔鏡術后創口的疼痛也是比較劇烈的,胸腔鏡手術術后早期易發生肺功能損傷,主要由限制性通氣障礙造成,而疼痛會加劇限制性通氣[5]。
傳統的硬膜外置管鎮痛被認為是胸科手術的一線輔助鎮痛方式。但是胸段硬膜外阻滯對心血管系統影響太大,并發癥太多[6],現在逐步被TPVB取代。TPVB是指將局麻藥注射到胸部脊神經從椎間孔穿出處,即椎旁間隙處,而產生注射部位同側鄰近多個節段的軀體和交感神經的阻滯,從而起到鎮痛的目的[7]。胸椎旁間隙解剖上位于肋骨頭和肋骨頸之間,是脊柱兩側的一個楔型解剖間隙。后面是肋橫突上韌帶,外側是肋間內膜后緣,前面是胸膜壁層,內側是椎體、椎間盤和椎間孔。近年來有研究表明,TPVB比硬膜外阻滯發生低血壓、惡心嘔吐、尿潴留和肺部并發癥的概率低,對鎮靜和低通氣的患者應用安全[8]。超聲引導的TPVB是一門新興的技術,當胸部解剖結構紊亂時效果非常好,如病態肥胖者、局部病理性改變者、脊柱畸形者和有過胸部手術史者,應用超聲引導的神經阻滯可以明顯提高阻滯的成功率,減少氣胸和誤入椎管內等并發癥的發生率。
隨著超聲引導下神經阻滯的研究深入,2017年FORERO等[9]發表了ESP阻滯的研究,在ESP阻滯研究中他們指出:局麻藥注射于T5ESP阻滯,可阻滯同側T2~T7胸脊神經背側支支配區域,跟本文的研究結果是一致的。解剖學上研究認為豎脊肌為脊柱后方的最長肌,分為中間最長肌、外側髂肋肌和內側棘肌三部分。胸神經根分為背側支和腹側支,椎間孔后大約1 cm處分出脊神經背側支,在此處被橫突韌帶和橫跨在兩橫突之間的肌肉所覆蓋,在橫突的內1/3處橫過其上緣進入豎脊肌并發出分支,支配胸腰部后方關節突關節、皮膚和肌肉等結構,胸椎棘突旁豎脊肌肌間隙中局部麻醉藥物可以上下擴散,相鄰節段的脊神經后支及其分支均會不同程度受到阻滯,來自手術切口區域的疼痛刺激也就相應被阻滯。在超聲引導下將局部麻醉藥物注射到豎脊肌肌間隙,即為ESP阻滯,ESP阻滯是最近提出的一種新的神經阻滯方式[10]。有學者將造影劑注射于T5橫突上,發現有一部分造影劑可以通過肋間內肌和肋間外肌,過肋橫突孔到達胸脊神經背側支和腹側支的起始發出部位來達到相應的擴散效果[11-15]。
本研究結果表明胸椎ESP阻滯在胸腔鏡肺葉切除術后VAS評分方面和減少術后阿片類藥物的用量方面在術后12 h內與TPVB是相似的,在18和24 h其VAS評分升高考慮是神經阻滯藥量過少,因為ESP阻滯是豎脊肌平面間隙阻滯,和腹橫肌平面阻滯、前鋸肌阻滯原理相似,通過肌肉筋膜間隙擴散鎮痛,如果和TPVB阻滯使用相同的量其難以達到同樣的鎮痛時間。
兩組患者有較多的皮膚瘙癢發生考慮是鎮痛泵配方中地佐辛的副作用,后經改良鎮痛泵配方(將地佐辛改成枸櫞酸舒芬太尼50μg)后該副作用均未發生。
綜上所述,超聲引導下胸椎ESP阻滯聯合PCIA在胸腔鏡下肺葉切除手術鎮痛方式是安全有效的,是一種新的可行的區域阻滯鎮痛方式,可以推廣使用。

