含CpG-ODN基序重組抑制素質粒的構建及其對小鼠顆粒細胞相關凋亡基因表達的影響
陽美霞,張虹亮,李藍祁,張羽芳,楊利國,王水蓮*
(1.湖南農業大學動物醫學院,長沙 410128;2.湖南省獸藥工程技術研究中心,長沙 410128;3.華中農業大學動物科技學院,武漢 430070)
哺乳動物的卵泡發育是由體內各種生長因子、垂體促性腺激素和類固醇激素共同調節的一個連續而復雜的生理過程[1-2]。在卵泡發育過程中,顆粒細胞分泌抑制素(inhibin, INH)、雌二醇(estradiol, E2)和胰島素樣生長因子(insulin-like growth factor, IGF)等細胞因子,影響卵母細胞成熟和卵泡發育[3-4]。INH是由α和β亞基組成的異二聚體糖蛋白,屬于轉化生長因子β(transforming growth factor beta,TGFβ)超家族成員之一,通過自分泌或旁分泌的方式調控顆粒細胞增殖、類固醇激素產生及卵母細胞成熟,參與卵泡發育[5-7]。INHβ能誘導體外培養豬顆粒細胞凋亡,甚至在豬的卵泡發育過程中上調卵泡閉鎖率[8]。合成的抑制素α(1~32)片段在牛顆粒細胞中能抑制細胞增殖,誘導細胞凋亡[9]。
CpG寡脫氧核苷酸(CpG-ODN)是含有非甲基化胞嘧啶-磷酸-鳥嘌呤基序的短單鏈合成DNA分子,是一種能誘導或增強各類免疫應答的免疫調節劑[10-12]。研究表明,CpG-ODN具有免疫刺激活性,能誘導Ⅰ型免疫應答,隨后激活機體的細胞和體液免疫[13]。激活人體細胞的最佳CpG-ODN基序是5′-GTCGTT-3′,而對小鼠細胞具有活化作用的最佳CpG-ODN基序是5′-GACGTT-3′[14]。Yeh等[15]研究發現,合成的CpG-ODN能有效激活人和小鼠TLR9介導的NF-κB和細胞因子,并產生相應的免疫應激。含CpG-ODN的疫苗可介導細胞增殖,干擾啟動子活性和免疫基因的表達,進而產生較強的免疫刺激,顯著增加動物體內IgM和抗病毒分子Mx2的含量[16]。
盡管CpG-ODN作為佐劑已表現出提高動物免疫力的能力,但CpG-ODN是否影響哺乳動物卵泡發育尚無報道。已有研究表明,INH可抑制豬顆粒細胞生長發育,主要表現為誘導細胞凋亡,影響類固醇激素生成,進而影響卵泡發育過程[8]。在Geng等[9]研究基礎上,本研究設計并合成了對小鼠細胞具有免疫刺激活性的CpG-ODN基序,構建含免疫基序CpG-ODN片段和抑制素α(1~32)片段的重組抑制素質粒pEGISI-CpG-ODN,并轉染原代培養的小鼠卵巢顆粒細胞,通過qRT-PCR法檢測細胞中死亡受體通路相關基因mRNA表達水平的變化,以探討CpG-ODN能否拮抗抑制素對顆粒細胞發育的抑制作用,為降低顆粒細胞凋亡和促進卵泡發育提供新思路。
1 材料與方法
1.1 材料
1.1.1 試驗動物 21~23日齡雌性ICR小鼠購于湖南斯萊克景達實驗動物有限公司。
1.1.2 菌種及生化試劑 抑制素質粒pEGISI(含綠色熒光蛋白(GFP)、乙肝表面抗原(HBsAg)S基因及抑制素(INH)基因)由曹少先等[17]構建,本實驗室保存;T4 DNA連接酶、限制性內切酶XhoⅠ、Hind Ⅲ、LiopfectamineTM2000、Opti-MEM培養基(Thermo scientific,美國);無內毒素質粒提取試劑盒、柱式RNA提取試劑盒(天恩澤,北京);PrimeScriptTMRT reagent Kit、SYBR?Premix Ex TaqTM(TaKaRa,日本);DME/F-12培養基(Hyclone,美國)。
1.2 方法
1.2.1 CpG-ODN片段的設計與合成 選擇對小鼠細胞具有激活作用的CpG基序:5′-GACGTT-3′,根據設計原則設計具有免疫作用的CpG-ODN片段,由華大基因技術有限公司合成(劃線部分為限制性內切酶XhoⅠ和Hind Ⅲ的酶切位點及其保護性堿基)。
正鏈:5′-CTCGAGCGGCACGTTGACGTTCACG-TTGACGTTCACGTTGACGTTCACGTTGACGTT CCCAAGCTTGGG-3′。
1.2.2 重組抑制素質粒pEGISI-CpG-ODN的構建及鑒定 將帶有酶切位點的CpG-ODN片段和pEGISI質粒分別用XhoⅠ和HindⅢ限制性內切酶進行雙酶切,然后用T4 DNA連接酶于4 ℃連接過夜,連接產物轉化到感受態細胞E.coliDH5α中,將冰浴好的混合物放入42 ℃水浴90 s,再冰浴2~3 min,混合物置于700 μL無抗性LB培養基中,37 ℃搖床培養45 min,然后取100 μL均勻地涂布于含有Kana抗生素的LB固體平板上,平板于37 ℃ 恒溫箱中倒置培養過夜。質粒進行單菌落篩選,上游引物:5′-CGCAATGGGCGGTAGGCGTG-3′,下游引物:5′-CCCAAGCTTGGGAACGTCAACGT-3′。用TaqDNA聚合酶進行擴增:94 ℃預變性4 min;94 ℃變性30 s,60 ℃退火30 s,72 ℃延伸10 s,共35個循環。
1.2.3 小鼠卵巢顆粒細胞的分離與培養 取21~23日齡雌性ICR小鼠5只,用乙醚麻醉小鼠后,迅速將其頸椎脫臼處死。小鼠腹部用75%的酒精棉球進行擦拭消毒。于無菌環境中迅速取出雙側卵巢,體式顯微鏡下去除多余的輸卵管、脂肪及其它組織。用預熱的PBS沖洗卵巢3遍,4號針頭刺破卵泡,釋放出顆粒細胞及卵母細胞。加入1 mL完全培養基(DME/F-12+15%FBS+1%青鏈霉素)進行吹打,用40 μm的過濾器過濾細胞懸液,以分離卵母細胞,得到的細胞懸液于1 000 r·min-1離心5 min,棄上清,獲得細胞沉淀。顆粒細胞以1×106·mL-1密度鋪板于細胞培養瓶中,于37 ℃、5% CO2細胞培養箱中培養。
1.2.4 質粒轉染 顆粒細胞以2×106·孔-1密度
鋪板于6孔板中,當細胞融合率達到80%左右進行轉染,轉染前24 h,更換為無雙抗培養基(DME/F-12+15%FBS)。試驗分為3組:pEGFP質粒轉染組為空載體組,抑制素重組質粒pEGISI轉染組為對照組,含CpG-ODN基序的重組抑制素質粒pEGISI-CpG-ODN轉染組為試驗組,每組設3個重復。用脂質體LipfectamineTM2000進行轉染。分別用47和44 μL Opti-MEM培養液稀釋DNA(3 μg)和LipofectamineTM2000(6 μL),室溫靜置5 min后,將兩者混合至體積為100 μL·孔-1,室溫靜置20 min,呈點滴狀添加到6孔板內,5 h后更換細胞培養液,轉染48 h收集細胞,進行qRT-PCR檢測。
1.2.5 細胞中總RNA的提取及反轉錄 根據柱式RNA提取試劑盒中說明書操作,每孔加入500 μL Trizol溶液提取細胞中的總RNA。通過OD260 nm/OD280nm的比值和瓊脂糖凝膠電泳來分析所提取RNA的質量及完整性。用PrimerScriptTMRT reagent Kit with gDNA Eraser反轉錄總RNA得到模板cDNA,將cDNA作為模板進行qRT-PCR檢測。
1.2.6 qRT-PCR檢測相關凋亡基因mRNA的表達 用熒光定量PCR儀(ABI Step One)檢測死亡因子受體(Fas)/死亡因子Fas配體(FasL)和死亡因子受體(DR4/5)/死亡因子DR4/5配體(TRAIL)通路中相關基因的表達。qRT-PCR反應體系:2×SYBR Premix Ex Taq 5 μL,上下游引物(10 μmol·L-1)各0.2 μL,50×ROX Reference Dye 0.2 μL,cDNA模板1 μL,ddH2O 3.4 μL,總體積10 μL。反應條件:95 ℃ 30 s;95 ℃ 5 s,60 ℃ 30 s,共40個循環。所有操作過程均在冰上完成。以β-actin作為內參基因,并用2-△△CT法分析試驗結果。qRT-PCR引物見表1。

表1 qRT-PCR引物序列
1.2.7 數據分析 數據以“平均值±標準差”表示。用SPSS 17.0的單因素方差分析法(One-way ANOVA)分析試驗數據,**P<0.01表示差異極顯著,*P<0.05表示差異顯著。
2 結 果
2.1 重組抑制素質粒 pEGISI-CpG-ODN的鑒定
2.1.1 擴增CpG-ODN 片段 重組抑制素質粒pEGISI-CpG-ODN經單菌落篩選,用普通PCR進行擴增,1.2%瓊脂糖凝膠電泳圖顯示,在100 bp左右出現目的片段,與擴增CpG-ODN片段的引物大小相符合(圖1)。以pEGISI-CpG-ODN 質粒為模板,進行PCR擴增,電泳結果顯示,在100 bp左右出現明顯條帶(圖1)。
2.1.2 測序結果 將pEGISI-CpG-ODN菌落條帶正確的單菌落進行擴菌,并用無內毒素質粒提取試劑盒進行質粒小提,質粒送華大基因公司進行測序。測序結果表明,含免疫片段的CpG-ODN核苷酸序列正確插入到pEGISI質粒中,證明重組抑制素質粒pEGISI-CpG-ODN構建成功(圖2)。
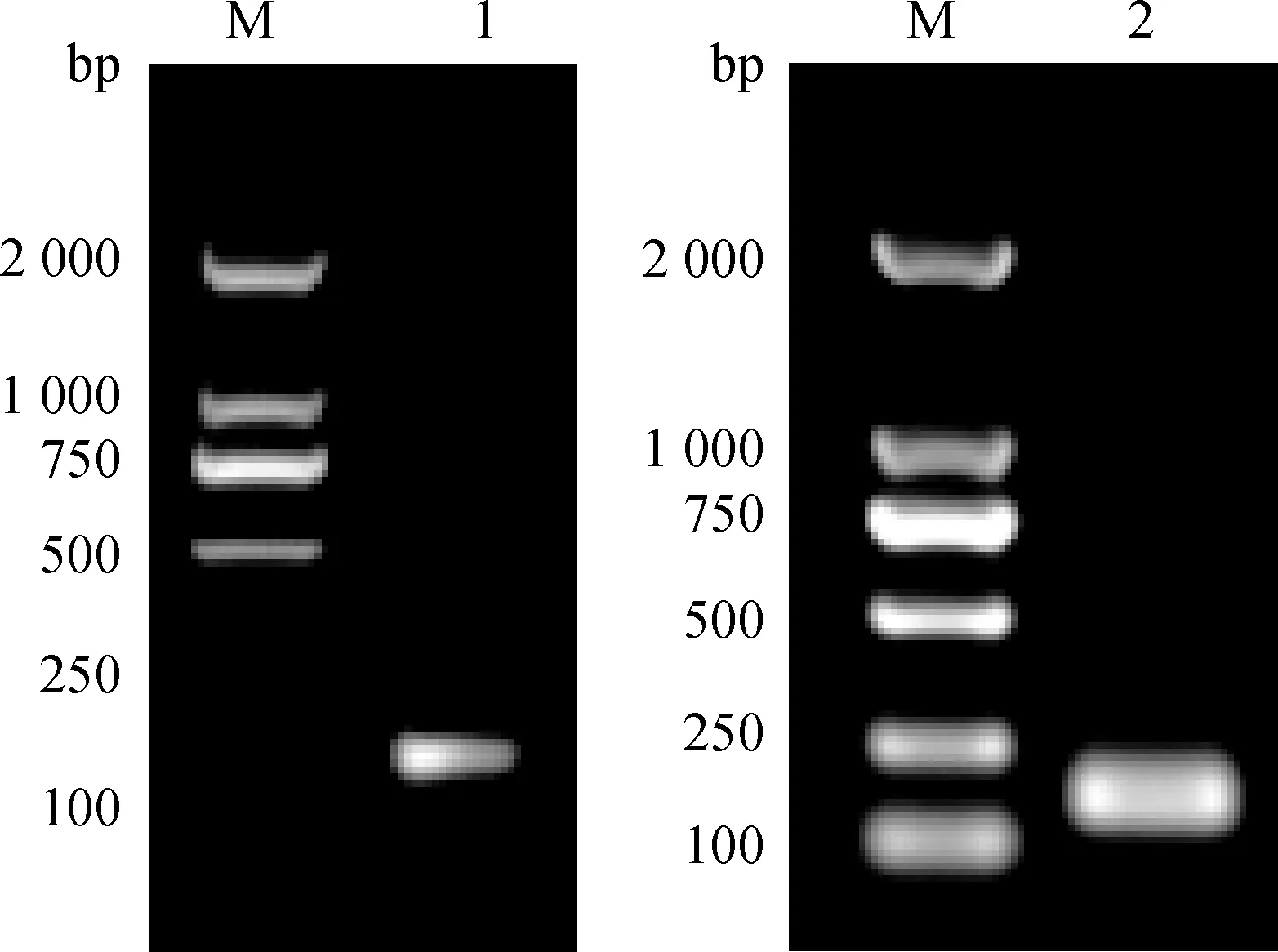
M. DL2000 DNA相對分子質量標準;1. pEGISI-CpG-ODN單菌落PCR擴增產物;2. CpG-ODN PCR擴增產物M.DL2000 DNA marker; 1. PCR amplification product of pEGISI-CpG-ODN single colony; 2. PCR amplification product of CpG-ODN圖1 PCR擴增結果Fig.1 The result of PCR amplification
2.2 質粒轉染效率的鑒定
3種質粒(pEGFP、pEGISI和pEGISI-CpG-ODN)轉染顆粒細胞48 h,熒光顯微鏡觀察各孔細胞中綠色熒光蛋白(EGFP)的熒光強度和轉染數目(圖3),各組轉染效率為60%左右。
圖2 pEGISI-CpG-ODN質粒測序結果Fig.2 The sequencing result of pEGISI-CpG-ODN plasmid

A. pEGFP;B. pEGISI;C. pEGISI-CpG-ODN圖3 熒光顯微鏡檢測質粒在顆粒細胞中的表達情況(10×10)Fig.3 The expression of plasmids in granulosa cells detected by fluorescence microscopy (10×10)
2.3 小鼠顆粒細胞RNA提取
3種質粒(pEGFP、pEGISI和pEGISI-CpG-ODN)轉染顆粒細胞48 h后收集細胞,根據RNA提取試劑盒說明書進行細胞中總RNA的提取,微量紫外可見分光光度計測定OD260 nm/OD280 nm比值均為1.8~2.0。1.2%瓊脂糖電泳鑒定RNA的完整性。28 S、18 S和5 S條帶清晰可見,表明所提總RNA質量良好,可用于后續研究(圖4)。
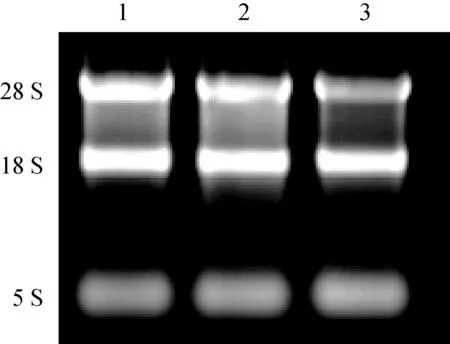
1.pEGFP;2. pEGISI;3. pEGISI-CpG-ODN圖4 小鼠顆粒細胞總RNA瓊脂糖凝膠電泳圖Fig.4 Results of the agarose gel electrophoresis of total RNA in mice GCs
2.4 質粒轉染小鼠顆粒細胞后CpG mRNA表達的變化
3種質粒(pEGFP、pEGISI和pEGISI-CpG-ODN)轉染顆粒細胞48 h后收集細胞,采用qRT-PCR法檢測CpG在各組細胞中的表達量。結果表明,與pEGFP組和pEGISI組相比,含CpG-ODN基序的pEGISI-CpG-ODN組中CpGmRNA的表達量極顯著升高(P<0.01)(圖5)。
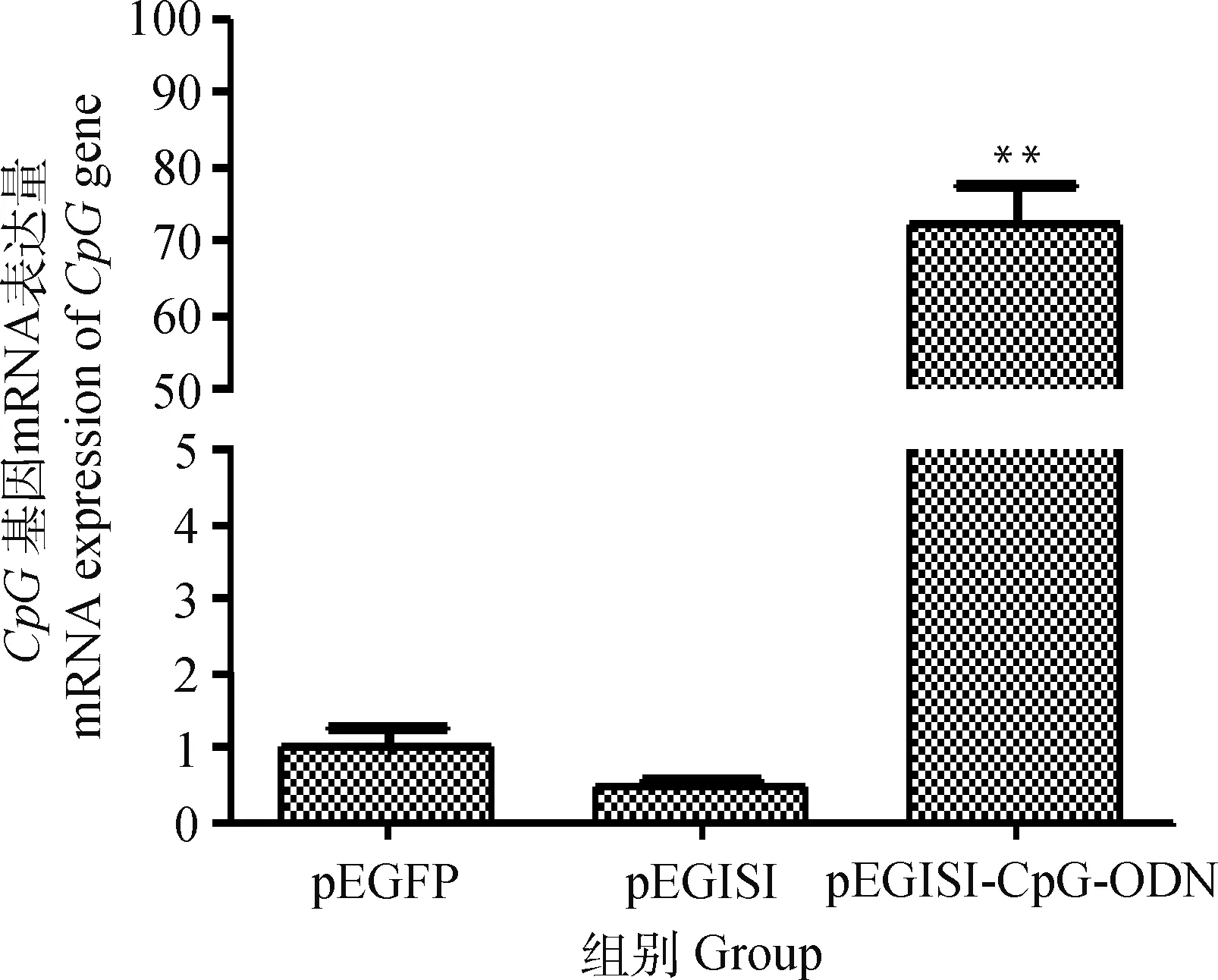
組間比較:*. P<0.05; **. P<0.01。下同Comparison among groups:*. P<0.05; **. P<0.01.The same as below圖5 質粒轉染顆粒細胞后CpG mRNA的表達Fig.5 The expression of CpG mRNA in the mouse granulosa cells after plasmid transfection
2.5 qRT-PCR檢測Fas/FasL死亡受體通路中基因的表達
3種質粒(pEGFP、pEGISI和pEGISI-CpG-ODN)轉染顆粒細胞48 h后收集細胞,用qRT-PCR法檢測Fas/FasL通路中關鍵基因在各組細胞中的含量。結果表明,與pEGFP組相比,pEGISI組中顆粒細胞促凋亡基因Fas的mRNA水平顯著上升(P<0.05),促凋亡基因FasL、Caspase8和Caspase3的mRNA水平極顯著上升(P<0.01);與pEGISI組相比,pEGISI-CpG-ODN組中顆粒細胞促凋亡基因Fas、FasL、Caspase8和Caspase3 mRNA的水平極顯著下降(P<0.01)(圖6A)。
2.6 qRT-PCR檢測DR4/5/TRAIL死亡受體通路中基因的表達
3種質粒(pEGFP、pEGISI和pEGISI-CpG-ODN)轉染小鼠顆粒細胞48 h后收集細胞,用qRT-PCR法檢測DR4/5/TRAIL通路中關鍵基因在各組細胞中的表達量。研究結果表明,與pEGFP組相比,pEGISI組中顆粒細胞促凋亡基因TRAIL的相對表達量顯著降低(P<0.05);與pEGISI組相比,pEGISI-CpG-ODN組中顆粒細胞促凋亡基因DR4/5、TRAIL的相對表達量極顯著降低(P<0.01)(圖6B)。
3 討 論
在雌性動物中,INHα亞基基因主要存在于卵泡顆粒細胞中,其功能是負反饋抑制垂體促卵泡激素(follicle stimulating hormone, FSH)的合成與分泌,拮抗激活素的活化作用,影響卵泡發育[18-19]。用含INHα(1~32)片段的重組質粒(pVAX-asd-IS)免疫小鼠,結果表明,重組抑制素蛋白具有免疫功能,并可在動物體內穩定復制40代[20]。Geng等[9]用過表達INHα(1~32)亞基的融合表達質粒(pEGISI)轉染牛顆粒細胞,在48和96 h處均能顯著抑制顆粒細胞增殖,細胞凋亡率極顯著上升,但48和96 h無顯著差異。另有研究表明,用抗INHα亞基抗體處理豬顆粒細胞,24 h后細胞增殖無明顯變化,但在處理后48 h能極顯著促進細胞增殖[21],表明用外源因子處理顆粒細胞48 h可能是影響細胞生長的最適時間點。
本研究結果表明,用含INHα(1~32)片段的抑制素質粒(pEGISI)轉染小鼠顆粒細胞48 h后,細胞中促凋亡基因FasL、Caspase8和Caspase3的表達
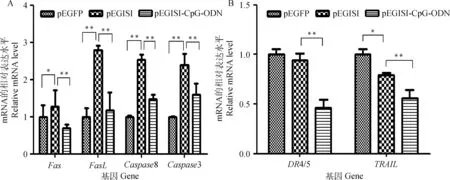
圖6 小鼠顆粒細胞轉染后凋亡基因mRNA的表達Fig.6 The mRNA expression levels of apoptotic genes in mouse granulosa cells after transfection plasmid
量極顯著高于pEGFP組(P<0.01),與上述報道一致。據報道,除Fas/FasL死亡受體通路外,腫瘤壞死因子中DR4/5死亡受體與其配體TRAIL結合能也誘導細胞凋亡[22],但其配體TRAIL不直接誘導細胞死亡,而是通過激活Caspase8的活性啟動下游凋亡基因的功能,進而誘發細胞凋亡[23]。
目前尚沒有關于INHα亞基是否通過影響DR4/5/TRAIL死亡受體通路中基因表達誘導細胞凋亡的報道。本研究表明,pEGISI質粒轉染顆粒細胞48 h后,DR4/5和TRAIL基因的表達量較pEGFP組出現降低趨勢,可能受顆粒細胞發育階段不同或種屬原因影響,但其具體機制還需深入研究。綜上,在顆粒細胞中過表達INHα亞基能增強內源性抑制素對顆粒細胞的抑制作用,引起細胞中死亡受體通路相關基因的表達量顯著升高(P<0.05),進而誘導細胞凋亡。CpG-ODN是近年來發現的一種新型免疫佐劑,可激活先天性免疫反應和適應性免疫反應[24],已在許多動物模型中表現出抗病毒、細菌、寄生蟲感染和增強抗腫瘤免疫應答等功效[25-28]。Yu等[29]用脂多糖(LPS)與CpG-ODN結合,發現結合CpG-ODN的LPS能顯著降低小鼠B細胞促凋亡基因CASP4、CASP9和Dapk1的表達情況,且上調抗凋亡基因IL-10的表達。另有研究報道,CpG-ODN與藥物結合后經腹腔注射治療腦損傷C57BL/6模型小鼠,能增加抗凋亡基因Bcl-2的水平,并減弱缺血腦組織中Bax和Caspase3的活性[30]。為進一步探討體外試驗中CpG-ODN與抑制素質粒DNA結合是否會對顆粒細胞凋亡產生調節作用,本研究以pEGISI質粒為表達載體,成功構建了含CpG-ODN的重組抑制素質粒pEGISI-CpG-ODN,且qRT-PCR結果表明,pEGISI-CpG-ODN組中CpGmRNA的含量顯著高于pEGFP組和pEGISI組(P<0.01)。同時,本研究通過檢測Fas/FasL和DR4/5/TRAIL兩條死亡受體通路中關鍵基因mRNA的表達水平,對重組抑制素質粒pEGISI-CpG-ODN的作用效果進行初步評估。結果顯示,pEGISI-CpG-ODN組與pEGISI組相比能極顯著下調顆粒細胞中Fas/FasL和DR4/5/TRAIL死亡受體通路中關鍵基因(Fas、FasL、DR4/5、TRAIL、Caspase8和Caspase3)mRNA的表達水平(P<0.01)。因此,本研究證實了CpG-ODN與pEGISI質粒融合能降低抑制素對小鼠卵巢顆粒細胞中促凋亡基因mRNA的表達水平,進而抑制細胞凋亡。
4 結 論
本研究成功構建了含CpG-ODN免疫基序的重組抑制素質粒pEGISI-CpG-ODN,并轉染至原代培養的小鼠卵巢顆粒細胞中,表明CpG-ODN能一定程度上減弱外/內源性抑制素對顆粒細胞凋亡的促進作用,下調細胞中促凋亡基因mRNA的表達,進而影響卵泡發育。

