鹽漬對鴨蛋的白蛋白影響
伍佰鑫 ,鄧 平 ,劉成國 (編譯)
(1.湖南省畜牧獸醫研究所,湖南 長沙 410131;2.湖南農業大學食品科技學院,湖南 長沙 410128)
鹽鴨蛋又稱腌蛋或咸蛋,用食鹽腌制,成熟期短,費用低廉;其蛋白軟嫩潔白,蛋黃松沙可口,中心油分積聚,外圍油分四溢,色澤桔紅或橙黃;是人們喜愛的傳統食品[1]。鹽鴨蛋中的蛋白含有4%~7%的氯化鈉(味道感覺太咸),可采用脫鹽工藝和電滲析法去除蛋白中的鹽[2]。也可預先分離新鮮鴨蛋中的白蛋白(用作其它食糜原材料),直接腌制蛋黃[3]。一般情況下,鴨蛋在鹽漬過程中,白蛋白的理化性質會發生改變,水分含量逐漸下降,而鹽、灰分、蛋白質和脂類含量增加;隨著腌制時間的延長,蒸煮全鴨蛋中的白蛋白硬度變得更低[4]。為了探索鴨蛋腌制期間(30d)白蛋白化學成分、胰蛋白酶抑制活性與凝膠特性的變化,泰國學者做了如下研究[5],可為國內蛋品加工行業創新提供“藥引子”。
1 研究方法
按 1個蛋/100ml的比例,室溫(28~30℃)配制鹵水或濃鹽水(25%,w/v)備用。從鴨場采集新鮮鴨蛋(產出后24h內),用自來水洗干凈,浸入鹵水或濃鹽水。每隔5d隨機取出一些鹽鴨蛋,手工敲碎、將白蛋白與蛋黃分離,對白蛋白進行分析。白蛋白中的水分、蛋白質和鹽分含量的測定,分別采用AOAC2000、雙縮尿(反應)法和 AOAC2011。運用8-苯胺-1-萘磺酸(德國)為探針,根據熒光強度對蛋白質濃度(線性回歸分析)的初始斜率,計算白蛋白的表面疏水性。
胰蛋白酶抑制活性的測定:取200μl白蛋白和 200μl豬胰蛋白酶(0.05mg/ml)37℃培養 15min;添加1000μl反應緩沖液 (50mM三羥甲基氨基甲烷鹽酸鹽,其中含有 20mM CaCl2,pH8.2); 添加200μl苯甲酰-DL-精氨酸-ρ-硝基苯胺(2mg/ml,美國);混合物 37℃培養 15min;添加 200μl的30%乙酸(v/v);用分光光度計(日本)測量410nm處的吸光度,對ρ-硝基苯胺的釋放進行監測;當酶引起吸光度增加0.01個單位/min,就定義為1個單位的胰蛋白酶活性;使胰蛋白酶活性降低1個單位,就定義為1個單位的胰蛋白酶抑制活性。
十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳:取2ml白蛋白與12ml 5%十二烷基硫酸鈉(德國)混合(制備蛋白質樣品);取15μg蛋白質樣品置于凝膠(12%電泳膠和4%積層凝膠)之上進行電泳(恒流 15mA/凝膠,美國);用染色液(德國,0.125%考馬斯藍Coomassie blue R-125滴入25%甲醇和10%乙酸之中)對凝膠進行染色;脫色采用40%甲醇和10%乙酸;最后估算蛋白條帶的分子量。
抑制活性染色:取白蛋白樣品與緩沖液(不含β-巰基乙醇)混合;混合樣不做熱處理,分別取15μg置于2個相同的凝膠之上,通過電泳將蛋白質分離,電泳裝置嵌在碎冰中以便減少產生的熱量;其中1個凝膠固定,用考馬斯藍R-250染色,作為對照組凝膠;另外1個凝膠用2.5%聚乙二醇辛基苯基醚沖洗15min,去除十二烷基硫酸鈉,再用蒸餾水沖洗,浸入50ml胰蛋白酶(0.2mg/ml)50mM三羥甲基氨基甲烷的緩沖液中 (其中含有20mM CaCl2,pH8.2);該凝膠 0~4℃培養 30min、置于室溫60min,讓胰蛋白酶擴散到凝膠中;用蒸餾水沖洗后浸入酪蛋白溶液(酪蛋白10mg/ml、50mM三羥甲基氨基甲烷的緩沖液,pH8.2),37℃培養90min;凝膠用蒸餾水漂洗、固定、用考馬斯藍R-250染色,形成抑制條帶,在清晰的背景上檢測暗帶;通過對照組比較標準的蛋白質遷移率,估算胰蛋白酶抑制劑的表觀分子量。
白蛋白凝膠制備與分析:先用蒸餾水作溶劑,制備白蛋白溶液(10%固形物),輕輕攪拌均勻;倒入套管 (直徑25mm),兩端都緊緊密封,加熱至90℃保持30min;立即冷卻至4℃并過一夜;分析之前將白蛋白凝膠切割成圓筒狀(直徑25mm、高度30mm)。 采用質構儀(Model TA-XT2i,英國)分析紋理輪廓:用壓縮圓柱形鋁探頭(直徑50mm)將凝膠壓縮至原始高度的40%;在3mm/s的十字頭速度下,記錄力距變形曲線,記錄速度也是3mm/s;用分析軟件(MicroStable,版本6,英國)評價硬度、膠粘性、彈性、粘聚性、彈力、咀嚼性和膠質。采用色度計(ColorFlex,美國)分析凝膠的亮度(L*)、紅度(a*)和黃度(b*);通過公式 100-[(100-L*)2+a*2+b*2]1/2計算出白色度。用掃描電子顯微鏡檢測腌制0、15d和30d的鹽鴨蛋蛋白凝膠的顯微結構:將白蛋白凝膠切成小塊(1×1×1mm3),用含有 2.5%戊二醛的0.2M磷酸鹽緩沖液(pH7.2,德國)固定12h;用蒸餾水漂洗1h;用6種濃度 (25%、50%、70%、80%、90%和100%)的乙醇脫水,每個濃度的脫水15min;對脫水樣品進行臨界點干燥;涂上一層100%金子(濺射噴涂機SPI-Module,美國);用掃描電鏡(JEOL JSM-5800LV,日本)觀察凝膠微觀結構。
所有試驗一式三份,一共三批樣品;數據采用單向方差分析(ANOVA),結果用平均值和標準差表示;采用多重比較分析樣本之間的差異,統計分析軟件是SPSS11.0(美國)。
2 研究結果
2.1 鹽漬時間對鴨蛋蛋白化學成分的影響 鹽漬期間,鴨蛋蛋白中的水分持續減少,從初期的87.93%減少到鹽漬30d的81.20%;同時,鹽分隨鹽漬時間延長而增加,從初期的0.31%增加到鹽漬 30d 的 6.19%。 蛋白的亮度(L*)減少、紅度(a*)、黃度(b*)和白色度增加,見表 1。
蛋白質表面疏水位點的數量和相對大小,通常決定蛋白質的溶解度,在pH、溫度和離子強度等生理條件下的聚集傾向。鴨蛋蛋白的表面疏水性隨鹽漬時間延長而逐漸增加,從初期的735.04增加到鹽漬20d的821.45,表明鹽漬誘導了蛋白質構象變化。在鹽漬的前15d期間,鴨蛋的胰蛋白酶抑制活性持續下降,只保持63%的活性;鹽漬30d的抑制活性最低 (5.68千單位/mg固體),因此,胰蛋白酶抑制劑的變性可能與其生物活性的喪失有關,從而推斷抗蛋白酶活性的降低與一些關鍵蛋白(如類卵母細胞和卵黃抑制劑)的退化有關。
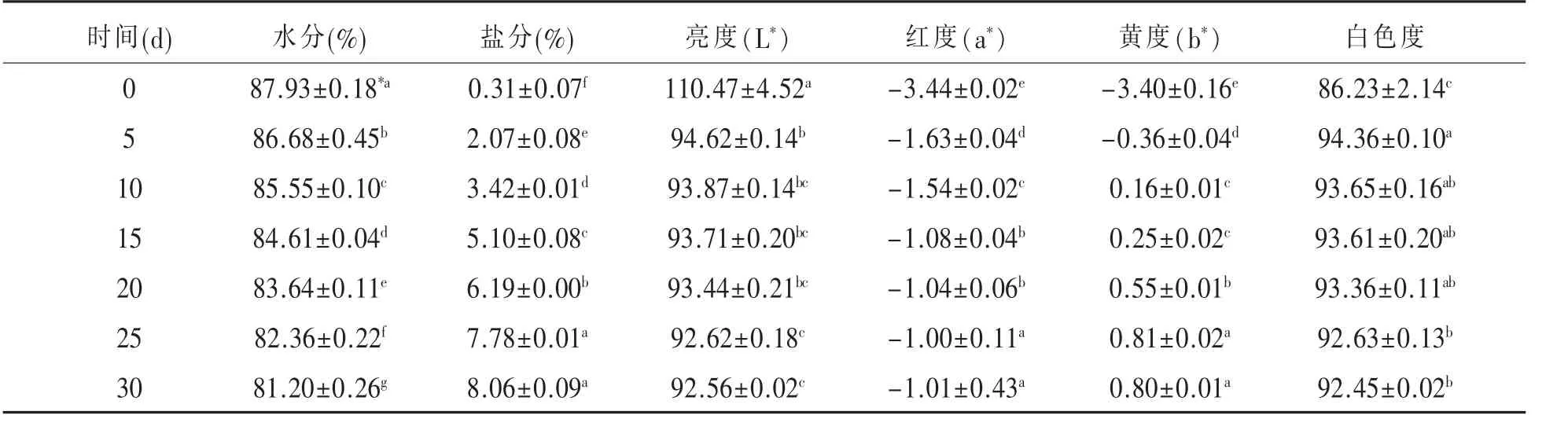
表1 鹽漬期間鴨蛋蛋白的水分/鹽分/色澤變化
電泳結果發現,鴨蛋蛋白最主要的蛋白質是卵清蛋白,分子量為44kda。在非還原條件下,發現有分子量分別為81、70和16kda的蛋白質,分子量為81kda的蛋白質更可能是卵傳鐵蛋白,分子量為16kda的蛋白質更可能是溶菌酶。對于抑制活性染色,只保留了分子量為44kda的蛋白帶,這種蛋白 (分子量類似)貌似卵清蛋白或其他蛋白質,對胰蛋白酶有抑制作用。抑制活性染色未檢出類卵母細胞和卵黃抑制劑,當十二烷基硫酸鈉用于電泳時,那些抑制劑可能失去了抑制活性,經胰蛋白酶消化后,那些蛋白條帶未被保留。鹽漬20d后,分子量為44kda的蛋白帶淡于新鮮鴨蛋和鹽漬10d鴨蛋的蛋白帶,這表明鹽漬期間,有抑制活性的蛋白質失去了一些活性,可能歸因于抑制蛋白的構象發生了改變,這一結果與鴨蛋白在鹽漬過程中降低了胰蛋白酶抑制活性是吻合的,也就是說,鹽漬時間對降低胰蛋白酶抑制活性有顯著影響。
2.2 鹽漬時間對白蛋白凝膠特性的影響 隨著鹽漬時間的增加,白蛋白凝膠的硬度降低 (P<0.05);新鮮鴨蛋的白蛋白凝膠硬度值(19.08N)最高,鹽漬30d鴨蛋的白蛋白凝膠硬度值(3.77N)最低,差異顯著(P<0.05);鹽漬5d鴨蛋的白蛋白凝膠硬度值(9.26N)就降低了50%,見表2。

表2 鹽漬期間鴨蛋的白蛋白凝膠質地變化
與鹽漬鴨蛋的白蛋白凝膠相比,新鮮鴨蛋的網絡更加密集、空隙更小;鹽漬鴨蛋的白蛋白凝膠有較大的空隙,鹽漬15d的白蛋白凝膠網絡變得較粗糙,均勻度較低;鹽漬30d與鹽漬15d的白蛋白凝膠質地沒有明顯差異,但由于鹽漬 (特別是30d)白蛋白中的蛋白質濃度更低、鹽分含量更高,蛋白質之間的相互聯系變得越來越少 (圖1),這與蛋白質網絡強度降低(表2)是吻合的。

圖1 鴨蛋的白蛋白凝膠掃描電鏡照片(放大 1萬倍/比例尺 5μm)
總而言之,鹽漬影響鴨蛋的白蛋白化學組成和凝膠特性,特別是蛋白酶抑制劑受鹽漬時間影響,鹽漬可將胰蛋白酶抑制活性減少到一定的程度。分子量為44kda的蛋白質在鴨蛋的白蛋白中充當胰蛋白酶抑制劑的角色。隨著鹽漬時間的延長,白蛋白的膠性變得更弱(吃起來感覺無韌性)、白色度增加。鹽漬白蛋白可應用于魚糜或其他肉制品,通過強化膠粘性、抑制蛋白質水解,改善其適口性等特性。

