可控性干預措施對磁共振介入下行氬氦刀冷凍的肺癌患者癌因性疲乏的療效觀察
聶穎,吳立華,張全剛
廊坊市人民醫院1門診部,2神經外科,河北 廊坊0650000
肺癌的發病率居中國惡性腫瘤的首位,中國早期肺癌的診斷率較低,多數患者在確診時已處于疾病中晚期,失去了手術切除的機會[1]。靶向介入治療主要借助現代醫療技術,對病灶精確定位,可以減少對正常組織的損傷,目前已廣泛應用于前列腺癌、肺癌、肝癌等治療,效果顯著[2-3],但由于腫瘤消耗及介入治療的不適,多數患者會出現疲乏等癥狀,此類表現稱為癌因性疲乏[4]。可控性干預主要是指通過醫護人員主觀努力可以實現的干預措施,目前已應用于多種疾病的治療,但肺癌介入治療的臨床報道仍然較少[5-6]。因此,本研究旨在探討肺癌介入治療中應用可控性干預的效果及其對患者癌因性疲乏的影響,現報道如下。
1 資料與方法
1.1 一般資料
回顧性分析2015年10月至2017年10月于廊坊市人民醫院就診的80例肺癌患者的臨床資料。將2015年10月至2016年10月40例接受常規護理干預的患者作為對照組,2016年11月至2017年10月40例接受可控性干預的患者作為觀察組。兩組患者均在磁共振成像(magnetic resonance imaging,MRI)介入下行氬氦刀冷凍治療。納入標準:①符合肺癌診斷標準[7],通過實驗室檢查、影像學檢查、術后病理學組織檢查等確診為肺癌;②TNM分期為Ⅱ~Ⅳ期。排除標準:①凝血功能異常;②有廣泛轉移的Ⅳ期肺癌;③有多組融合性縱隔淋巴結轉移。觀察組患者中,男23例,女17例;年齡為42~71歲,平均為(56.68±7.34)歲。對照組患者中,男25例,女15例;年齡為40~70歲,平均為(57.14±6.95)歲。兩組患者的性別、年齡、腫瘤類型、TNM分期等臨床特征比較,差異均無統計學意義(P﹥0.05),具有可比性,詳見表1。
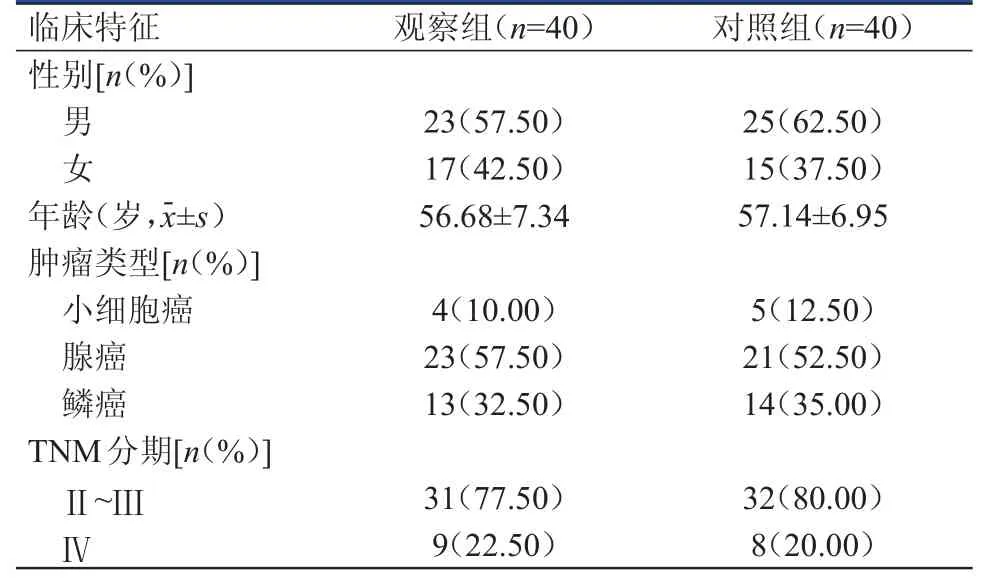
表1 兩組患者的臨床特征
1.2 干預方法
兩組患者均在MRI介入下行氬氦刀冷凍治療,取臥位,2%利多卡因局部浸潤麻醉。在磁共振成像系統、Passive Polaris醫學導航系統的引導下,于距腫瘤最近的胸壁位置,避開重要結構,經皮穿刺冷凍探針,進行掃描。根據動態MRI導航掃描圖像,確定腫瘤位置和治療靶點,并在導航系統的引導下實施氬氦刀冷凍治療,冷凍設備應用Cryo-HIT低溫冷凍系統。
對照組患者圍術期接受鎮痛、對癥治療、心理疏導、生命體征監測等常規干預,囑患者多休息。
觀察組患者圍術期接受可控性干預措施:①心理干預。護理人員經常與患者主動溝通,鼓勵、關心患者,給予相應的健康宣教,將治療和護理的目的、方法告知患者,講述恢復良好的病例,提高患者的治療信心,使其可以主動配合治療;積極分析、判斷患者出現癌因性疲乏的因素,進行身心整體評估并給予相應的指導。②營養干預。指導患者養成良好的飲食習慣,少食多餐,選擇高熱量、高維生素、高蛋白的食物,禁止食用含咖啡因、酒精的食物。③藥物干預。患者出現貧血時,可以給予選擇性5-羥色胺再攝取抑制劑、精神刺激類藥物、低劑量腎上腺素皮質激素等。④活動干預。根據患者術后恢復情況,指導其進行相應的日常鍛煉,包括散步、太極、體操、騎自行車等,鍛煉強度需要適當,不宜過于勞累。⑤并發癥干預。密切關注患者術后恢復情況,關注胸部體征和穿刺部位敷料是否出現滲血和皮下淤血等,術后常規應用止血藥物;指導患者多飲水,幫助尿酸沉淀物排除;采用無菌包扎,保持創面干燥清潔等。
1.3 觀察指標
于干預前、干預第15天,評價以下指標的變化:①癌因性疲乏評估參照美國癌癥中心疼痛研究小組所制定的簡易疲乏量表[8],該量表采用10分制數字描述,0分程度最輕,表示無疲乏;1~3分表示輕度疲乏;4~6分表示中度疲乏;7~10分表示重度疲乏。②生活質量評估采用腫瘤患者生活質量評定量表EORTC QLQ-C30[9],評價內容包括軀體功能、角色功能、認知功能、情緒功能、社會功能及總體健康狀況與生活質量,得分越高,提示生活質量越好。③記錄干預期間患者不良反應的發生情況。
1.4 統計學方法
采用SPSS 18.0軟件分析數據,計量資料以均數±標準差(±s)表示,組間比較采用獨立樣本t檢驗;計數資料以率(%)表示,采用χ2檢驗;等級資料采用秩和檢驗,P﹤0.05為差異有統計學意義。
2 結果
2.1 干預前后癌因性疲乏比較
干預前,兩組患者的癌因性疲乏情況比較,差異無統計學意義(Z=0.211,P﹥0.05);干預后,觀察組患者的癌因性疲乏情況明顯優于對照組,差異有統計學意義(Z=4.239,P﹤0.01)。(表2)
2.2 干預前后生活質量比較
干預前,兩組患者的軀體功能、角色功能、認知功能、情緒功能、社會功能、總體健康狀況與生活質量評分比較,差異均無統計學意義(P﹥0.05)。干預后,兩組患者的軀體功能、角色功能、認知功能、情緒功能、社會功能、總體健康狀況與生活質量評分均高于干預前,差異均有統計學意義(P﹤0.05);觀察組患者的上述各項評分均明顯高于對照組,差異均有統計學意義(P﹤0.01)。(表3)

表2 兩組患者干預前后癌因性疲乏情況[ n(%)]
表3 兩組患者干預前后生活質量評分比較(±s)
注:*本組與干預前比較,P<0.05
軀體功能干預前46.8±4.8 47.1±4.6 0.361 0.719組別觀察組(n=40)對照組(n=40)t值P值干預后71.3±5.6*60.4±5.1*9.042 0.000角色功能干預前42.8±3.4 42.6±3.6 0.331 0.741干預后64.9±4.6*55.7±3.9*9.636 0.000認知功能干預前48.6±5.3 48.2±5.5 0.363 0.718干預后72.5±6.5*61.8±6.3*7.490 0.000情緒功能干預前47.9±5.2 48.3±4.9 0.373 0.711干預后73.5±6.4*60.5±5.5*9.706 0.000社會功能干預前44.6±4.4 45.2±4.8 0.558 0.579干預后69.9±5.8*56.8±5.2*10.569 0.000總體健康狀況與生活質量干預前48.0±5.0 48.3±4.8 0.328 0.744干預后70.5±6.4*58.5±5.3*9.098 0.000
2.3 不良反應發生率比較
兩組患者的厭食、疼痛、呼吸困難、睡眠紊亂及肝功能異常的發生率比較,差異均無統計學意義(P﹥0.05)。(表4)
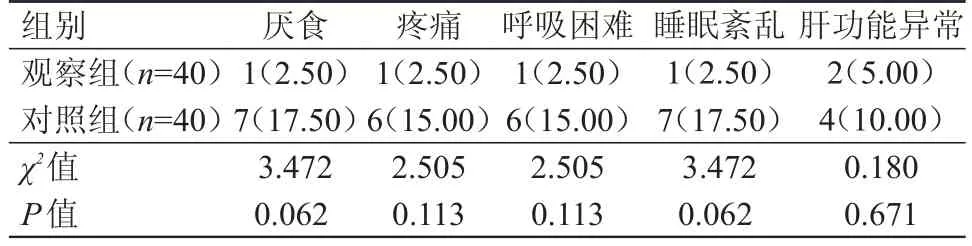
表4 兩組患者不良反應發生率比較[ n(%)]
3 討論
目前氬氦刀冷凍治療是比較成熟的腫瘤滅活術,可以迅速、徹底地殺滅腫瘤細胞,對正常組織的損傷較小[10-11]。而MRI導航是新興技術,具有較好的溫度敏感性,可以顯示體溫圖像,判斷有無殘留病灶。有報道顯示,MRI介入下行氬氦刀冷凍治療,具有創傷小、出血少、對正常臟器功能影響小和術后恢復快等優勢[12-13]。
癌因性疲乏是腫瘤患者治療過程中十分常見的并發癥。有研究顯示,在腫瘤患者的治療過程中,70%~100%的患者會出現疲乏,而有腫瘤轉移患者癌因性疲乏的發生率﹥75%,嚴重影響患者的生命質量[14]。出現此類現象的原因尚不明確,可能與心理、生理等因素相關。?zdelikara和Tan[15]的研究發現,貧血、營養不良、疼痛、睡眠質量欠佳、代謝紊亂等因素與癌因性疲乏有密切的關系。Hashemi等[16]認為,除患者自身對疾病的恐懼心理導致疲乏外,手術對機體的損傷也可導致代謝改變和應激反應的發生,在一定程度上可以導致癌因性疲乏。盡管腫瘤患者癌因性疲乏的發生率較高,但既往臨床上缺乏對癌因性疲乏的重視,醫師通常囑患者多休息,但是效果欠佳。近年來,較多學者開始重視對癌因性疲乏的干預,認為改善癌因性疲乏后可以使患者生活質量提高[17]。
本研究根據癌因性疲乏的影響因素,總結相應的針對性、可控性干預措施,通過心理干預,提高患者對治療的信心,而營養干預在促進患者術后機體恢復中有積極的意義。活動干預對緩解疲乏、增加機體運動能力的效果已得到較多研究證實。腫瘤患者術后活動較少,會降低患者的活動能力,必須采用更有效的活動干預,在一定程度上會增加疲乏程度,而給予簡單的日常鍛煉對減少疲乏有積極的意義[18-19]。
本研究顯示,接受可控性干預的患者癌因性疲乏的改善情況更好,中、重度疲乏患者明顯減少,說明針對癌因性疲乏的影響因素采用合理的可控性干預效果顯著。胡桂芳和杜麗梅[20]在白血病化療患者中采用可控性干預措施后,也得出與本研究結果相似的結論。同時,接受可控性干預的患者EORTC QLQ-C30量表中各項評分的升高更明顯,提示改善患者癌因性疲乏,有助于提高患者的生活質量。此外,在干預過程中,雖然接受可控性干預的患者厭食、疼痛、呼吸困難、睡眠紊亂的發生率均低于常規干預的患者,但差異均無統計學意義(P﹥0.05),考慮與樣本量較小有關。厭食、呼吸困難、睡眠紊亂作為常見的癌因性疲乏伴隨癥狀,在患者疲乏癥狀得到明顯改善后其發生率也隨之減少。疼痛的發生率減少,主要是由于可控性干預中有相應的并發癥護理,密切關注患者的病情變化并給予了積極處理。趙鵬和雷曉梅[21]也認為,術后疼痛是癌因性疲乏的重要因素,有效地緩解疼痛,有利于疲乏的改善。但此部分結論仍需擴大樣本量深入研究。
綜上所述,經MRI介入下氬氦刀治療的肺癌患者接受可控性干預,效果顯著,可以有效地緩解癌因性疲乏,改善生活質量,臨床應用價值高。

