高中化學通過電子式怎樣更好地學習化學鍵
(陜西省渭南市三賢中學 陜西渭南 714000)
引言
高中化學必修階段的化學鍵教學內容,屬于學生學習化學的重點內容,但也是普遍學生都表示難以理解的內容,有必要將教學內容作為著手點積極的尋找更有有效的教學策略。近年來,有部分學者提出可通過電子式進行化學鍵的學習,有助于提升學生的學習效率,從而強化高中化學教學質量,為此,文章選擇以此為方向進行綜合分析。
一、高中化學鍵教學問題分析
1.化學鍵與離子鍵以及共價鍵教學先后差異性問題
針對高中化學必修階段的化學鍵與離子鍵以及共價鍵教學順序差異進行分析,能夠在促進學生理解化學鍵科學本質的視角了解化學鍵的實質。在高中化學教學過程中,需要關注到的是學生思維中對微粒間作用的已有認知,經由宏觀現象促使學生能夠更為直觀的發現微粒間所存在的相互作用,間接的引導學生意識到化學鍵屬于較強的相互作用,在依據相互作用方式的差異性,輔助學生構建離子鍵與共價鍵。在認知心理學視角進行分析,有學者提出,學生的已有知識與即將學習的全新知識之間存在著多重關系,包括上位、下位、并列組合的三種關系,將此理論作為基礎,現階段高中化學鍵教學內容應該歸屬于下位觀念。基于此,在實際教學活動中,需要將情境教學作為基礎手段,將化學鍵作為優先教學順序,構建下位概念離子鍵與共價鍵,促使學生能夠處于下位學習環境中,有助于學生構建化學鍵知識整體結構。
2.電子式教學功能與要求問題
大量教學實踐顯示出,應用電子式表示離子鍵與共價鍵的形成過程,能夠更為直觀的輔助學生去理解與區分離子鍵與共價鍵的實質,同時也能夠促使學生在微觀層面上區分離子化合物與共價化合物。從這一點來看,電子式對化學鍵的教學具有著重要作用,但值得注意的是,如何發揮出電子式的教學作用,如何處理電子式表達離子鍵與共價鍵形成過程更為適合等問題,只有將這些問題進行解決,才能夠合理的應用分子式進行化學鍵的教學。在實際教學活動中,教師教育學生學習如何利用電子式。眾多教學實踐結果中能夠發現,部分教師試圖在正式教學活動開展之前用一定的時間講述電子式的表示與書寫,后在實際教學活動中引導學生在學習過程中將化學鍵作為工具去使用,在實踐結果上來看,學生對于電子式的理解以及應用水平有明顯提升。
二、經由電子式學習化學鍵
1.尋找配對
在較早的時間就已經有科學家提出,物質形成過程中電子在一個原子轉移到另一個原子呼死你經由兩個原子共享電子,促使每一個原子的最外層電子數能夠達到八隅體的穩定結構,此理論從出現起一直到現代仍然適用,且作為現代人們進行電子式書寫的主要參考存在[3]。
例如,有科學家將硝酸鈉與氧化鈉在573K下反應式獲取到離子化合物Na3NO4,在測定后發現,Na3NO4中各個原子的最外層電子均達到了6電子的穩定結構,的電子式為?
關于此問題的分析如下:

圖1 電子式(1)
2.等價取代
單原子與簡單物質分子的電子式書寫較為簡單,針對復雜的物質電子式,則需要選擇比較常見的或是相似的物質作為基礎,用眾多各簡單的電子式去表達整個復雜電子式。
例如,書寫H202、O2F2、O3F2的電子式?
此問題分析過程為:首先需要書寫H20與羚基的電子式,后將H20的電子式進行變形,用一價的的電子式替代中的一個H原子,也就是獲取到雙氧水的電子式對于O2F2分子,基于氟的非金屬性超出氧原子,為此F原子在分子中需要處于終端,氟與氟之間的共用電子對應偏向氟原子,促使氧顯+1價,也就是形成正二價過氧鏈,O2F2的分子式為,將此作為標準,對O3F2分子,可將其視為正二價臭氧鏈的兩端接上兩個F原子,為此,其電子式應該是。
3.合理遷移
創造需要建立在模仿的基礎上,而模仿基于已經存在的知識上,已經存在的知識加工與遷移是全新知識得以出現的基礎條件。
例如,已知(OCN)2的電子式為,如圖3所示,
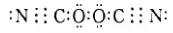
圖3 (OCN)2的電子式
則可以知道SCN-的電子式為()
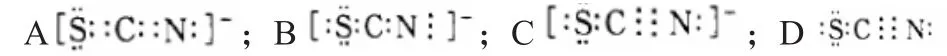
對于此問題的分析過程為:經由已知信息的分析,能夠將氧氰(OCN)2分子的電子式分別為兩個氧氰離子,基于氧與硫為同一主族的相鄰元素,性質較為相近,為此,可利用S原子代替O原子,最終明確正確選擇應該是C。
結語
化學鍵屬于化學的核心知識,對于學生的整個化學學習具有著較大影響,其教學內容涉及到理論、化學鍵類型、共價鍵分類等眾多內容。從本文對分子式與化學鍵的分析結果來看,通過電子式學習化學鍵具有可行性,且能夠輔助學生更為直觀的認識化學鍵,有助于提升學生的學習效率。在實際教學活動中,教師需要關注電子式學習表層下的價值,避免片面要求學生進行電子式背誦的教學形式出現,需要在理解電子式表達模式的基礎上,了解到如何利用電子式去學習化學鍵。

