五味子多糖的酶解輔助提取及其對小鼠腸道菌群的影響
王琳,高辰哲,崔石陽,劉冬,劉丹儀,韓建春,2,*
(1.東北農業大學食品學院,黑龍江哈爾濱150030;2.黑龍江省綠色食品科學研究院,黑龍江哈爾濱150030)
五味子一般指木蘭科植物五味子的成熟果實,具有抗疲勞[1]、鎮痛[2]、抗氧化[3]與調節腸道菌群[4]等生物功效,為中醫常用滋陰強腎藥,廣泛應用于肝炎、神經衰弱等病癥的治療[5]。五味子中含有多糖、木質素、揮發油等生物活性成分[6],其中多糖已經有研究證實具有多種功效[7]。近年來的研究發現,多糖具有抗腫瘤、抗病毒、增強免疫力、抗血脂、抗輻射、免疫調節等功效,對多糖的提取和活性研究成為了新的熱點[8]。傳統多糖的提取方法以水提醇沉為主,但存在提取率較低的缺陷。復合酶法提取多糖因其破壞細胞壁效果好,提取條件溫和,正逐漸受到廣大研究者的重視,將復合酶法應用于五味子多糖的提取目前研究較少。
腸道內的菌群具有輔助營養吸收、生物拮抗、免疫調節等作用,可以為宿主的腸道形成一道天然屏障[9]。有研究表明,多糖可以促進腸道中有益菌的生長,產生短鏈脂肪酸,抑制有害菌的生長[10]。五味子多糖已經被發現具有抗腫瘤[11]、降脂[12]、抗氧化[13]等功能,而五味子多糖能否對腸道菌群產生影響目前尚無明確報道。
本研究采用復合酶輔助提取五味子多糖,優化五味子多糖的提取條件,并通過建立小鼠腸道菌群紊亂模型,對比不同劑量五味子多糖的攝入對小鼠腸道菌群的影響,初步揭示五味子多糖對腸道菌群的調節作用,為其在腸道紊亂防治方面的應用提供思路。
1 材料與方法
1.1 材料與試劑
五味子:黑龍江省北安市農貿市場。
石油醚、苯酚、濃硫酸、氯仿:盛達生化科技有限公司;鹽酸林可霉素注射液:河南福森藥業有限公司;BBL瓊脂培養基、伊紅美藍瓊脂、Pfizer腸球菌選擇性瓊脂、MRS瓊脂培養基:青島海博生物技術有限公司。
木瓜蛋白酶(活力50 000 U/g):北京奧博星生物技術有限責任公司;果膠酶(20 000 U/g)、纖維素酶(活力5 000 U/g):上海藍季科技發展有限公司;3種酶按質量比1∶1∶1混合成復合蛋白酶。
1.2 儀器與設備
DHP-9162電熱恒溫培養箱、LDZX-50 KB立式壓力蒸汽滅菌器、LRH-250型生化培養箱:上海一恒科技有限公司;FD-1型冷凍干燥機:上海田楓實業有限公司;JD500-2型電子天平:沈陽天平儀器有限公司;TGL-16 C型高速離心機:江蘇牡丹離心機制造有限公司;SW-CJ-1 F超凈工作臺:蘇州江東精密儀器有限公司;索氏抽提器:上海比朗儀器制造有限公司;UV-2401型紫外可見分光光度計:日本島津公司;GFSJ-8高速粉碎機:安丘市經欣粉體加工設備有限公司;HYQX-II厭氧培養箱:寧波賽福實驗儀器有限公司。
1.3 五味子多糖的提取
選取干燥的成熟五味子果實,使用高速粉碎機粉碎,40目篩網過篩得五味子干粉。使用石油醚索式抽提12 h后取出,將溶劑揮發干凈,得到預處理的脫脂樣品。各組樣品取5 g脫脂樣品,加入蒸餾水調節濃度達0.05 g/mL,在攪拌條件下,各組使用檸檬酸-氫氧化鈉-鹽酸緩沖溶液調節不同的pH值,注意調節過程緩慢攪拌,保證最終pH值的穩定準確。各組分別添加相應體積的復合酶液,在一定溫度下600 r/min勻速攪拌指定時間。加入溶液體積3%的雙氧水4℃靜置脫色處理一夜,使用截留分子量為3 600 u的透析袋4℃透析48 h,透析液冷凍干燥得到五味子多糖凍干粉。以提取溫度、提取時間、提取pH值、復合酶添加量為主要因素變量,經過單因素初篩后進行正交試驗。
1.4 多糖含量與得率的測定
使用徐世忱等[14]的苯酚-硫酸法并做部分改動。取2 mL樣液(若檢測時吸光值超過0.9則將樣品按一定比例稀釋至2 mL)依次加入1 mL含6%苯酚的乙醇溶液、5 mL濃硫酸,常溫靜置10 min,以葡萄糖為標準物,在490 nm波長處測定標準物質量濃度與吸光度的對應關系,制備標準曲線,計算總糖含量。
采用3,5-二硝基水楊酸比色法[15],取2 mL樣液(若吸光值超過0.9,則按一定比例稀釋至2 mL)至25 mL具塞試管中,加入2 mL含有3,5-二硝基水楊酸的顯色劑,在沸水浴中加熱2 min后迅速冷卻,加水至刻度混勻,測定在波長540 nm下的吸光度,制備標準曲線,計算還原糖含量。
多糖含量/mg=總糖含量(mg)-還原糖含量(mg)多糖提取率/%=樣品中多糖含量(mg)/樣品質量(mg)×100
1.5 試驗動物處理
采用同一批次、健康的昆明小鼠(KM mice,品系編碼202)120只,購自北京維通利華實驗動物技術有限公司,5周齡~8周齡,雄性,體重18 g~22 g。適應性飼養一周后,將小鼠隨機分為5組:空白對照組、紊亂自然恢復組、多糖低劑量干預組、多糖中劑量干預組及多糖高劑量干預組。實驗開始,紊亂自然恢復組和各多糖干預組使用300 mg/mL鹽酸林可霉素灌胃,每天灌胃2次,每次0.3 mL,持續3 d,建立腸道菌群紊亂模型,空白組使用相同體積的生理鹽水灌胃[16]。小鼠在實驗期間均自由采食、取水,按照表1方案,每天定時對各組小鼠灌胃持續14 d,不同劑量的多糖使用生理鹽水預先溶解,當天現用現配。

表1 小鼠處理方案Table 1 Treatment of mice
1.6 樣品的采集與處理
1.6.1 樣品采集
灌胃14 d后,頸部脫臼處死小鼠,無菌條件下,收集回盲部末端6 cm以內的盲腸內容物,置于干燥滅菌試管中,無菌取1 g樣品加入9 mL生理鹽水,震蕩至盲腸內容物完全分散。
1.6.2 盲腸內容物菌液稀釋
每份樣品分別取裝有9 mL生理鹽水的帶塞試管8支,滅菌后放置到室溫待用。取震蕩完全分散的盲腸內容物1 mL加入到生理鹽水中,依次10倍稀釋至第8 支,稀釋度為 10-8[17]。
1.6.3 接種
如表2所示,在不同的選擇性培養基上涂布相應稀釋度的樣品100 μL,每個稀釋度重復3個平行,按照表3所示培養條件分別進行培養。

表2 細菌接種稀釋度Table 2 Bacterial dilution

表3 腸道主要菌群培養條件Table 3 Culture conditions of main intestinal flora
1.7 菌群培養與計數
使用平板活菌計數法進行計數,選擇單板單菌落數在30個~300個之間的稀釋倍數計數,計算菌落總數,結果以對數形式表示[18]。
1.8 統計學方法
用Statistix 8.0軟件進行數據分析,3次重復獨立實驗的結果表達為平均值±標準偏差(means±SD),方差分析(ANOVA)使用Tukey模式,各干預組與對照組、紊亂自然恢復組的比較采用單因素方差分析法,P<0.05表示有顯著性差異,P<0.01為差異極顯著,采用Sigmaplot軟件進行作圖。
2 試驗結果與分析
2.1 酶解輔助提取單因素試驗
設定提取溫度(30、35、40、45、50、55 ℃),提取時間(20、40、60、80、100、120 min),提取 pH 值(4、4.5、5、5.5、6、6.5),復合酶添加量(0.5%、1%、1.5%、2%、2.5%、3%)(相對于底物),4個變量中的3個保持不變,分別研究單因素指標不同對多糖得率造成的影響,結果如圖1所示。
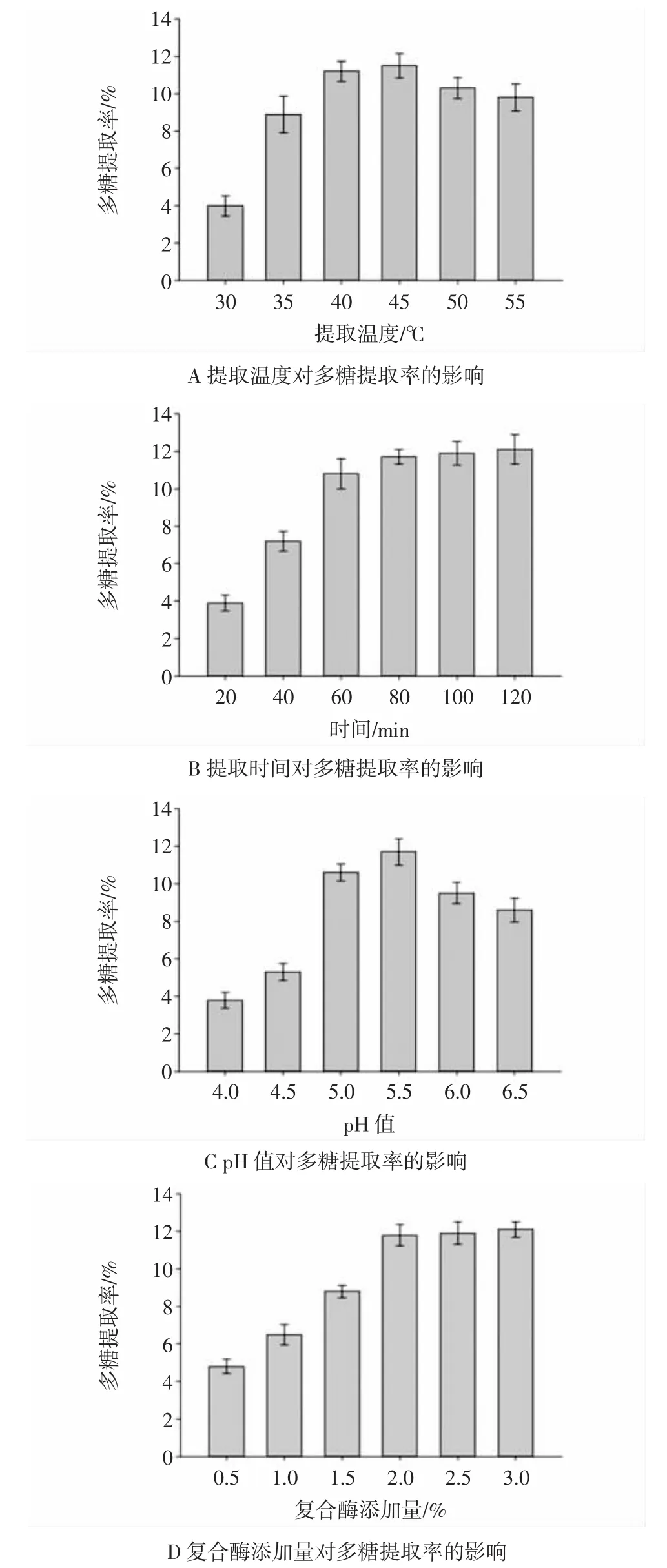
圖1 不同因素對五味子多糖得率的影響Fig.1 Effect of different factors on the yield of polysaccharides
由圖1A可知,溫度對于多糖得率有一定影響,適當升高溫度可以增加多糖得率,這是由于溫度升高提高多糖類物質的布朗運動水平,使其加速擴散到周圍溶劑中,同時適當的溫度也可以增加酶的活性,加快了細胞壁的破壞從而促進多糖溶出。當溫度過高時,雖然能提高多糖的溶解效率,但酶的活力受到抑制,對多糖得率也造成了一定損失,為了保證較高的多糖得率,選擇40、45、50℃作為后續正交試驗多糖提取溫度變量。
由圖1B可知隨著提取時間的延長,多糖的得率得到提高,當時間超過80 min時,多糖的得率不再顯著變化。這主要是因為五味子多糖隨著時間的延長逐步溶解入水中,同時,由于復合酶的作用,使五味子細胞壁受到破壞,更多的多糖類物質逐漸溶出。而隨著時間的延長,溶劑中多糖濃度越來越高,濃度差變小減慢了多糖進入溶劑的速度,多糖溶解入水中的速度逐漸減緩,而酶解的底物也逐漸消耗殆盡,對于多糖溶出的促進作用越發不明顯[19]。再延長提取時間對于提取率沒有顯著的促進作用,會造成時間和能源的浪費。綜合時間和提取率,選擇60、80、100 min作為后續正交試驗的提取時間變量。
由圖1C可知,pH值對于多糖的得率有顯著影響,當pH值為5.5時,多糖得率達到最佳。表明此pH值條件下的復合酶活力較高,多糖溶出率也較高。隨著pH值提高或降低,酶活隨之下降,從而影響了多糖得率,這可能與多糖親水基團及疏水基團的暴露有關系。因此,選擇5.0、5.5、6.0作為后續正交試驗的提取pH值變量。
由圖1D可知,當復合酶用量達到提取液質量的2.0%時,多糖得率最高達到11.8%。隨著復合酶用量的增加,相同時間內更多的五味子細胞壁被酶解破壞,造成了多糖的溶出。而當復合酶添加量達到一定程度時,更多的酶制劑對改善多糖得率的效果微乎其微,這可能是由于復合酶含量相對于底物過高,底物過早被消耗而造成了酶制劑的浪費[20]。為了讓酶解有效率且不過分浪費酶制劑,選擇了1.5%、2.0%、2.5%添加量作為后續正交試驗的復合酶變量。
2.2 正交試驗結果及分析
五味子多糖提取工藝優化正交試驗水平表見表4,正交試驗設計及結果見表5。
由表5可知,影響酶解輔助提取五味子多糖的主次因素為:提取復合酶添加量>pH值>酶解時間>酶解溫度。K值得最適條件為A2B2C1D1,以最佳提取條件進行驗證試驗,在最佳條件下,五味子多糖提取率為11.5%,沒有A2B2C3D1條件下獲得的五味子多糖得率高,因此試驗選用A2B2C3D1條件,即提取溫度45℃、提取時間80 min、提取pH 6.0、復合酶添加量1.5%。
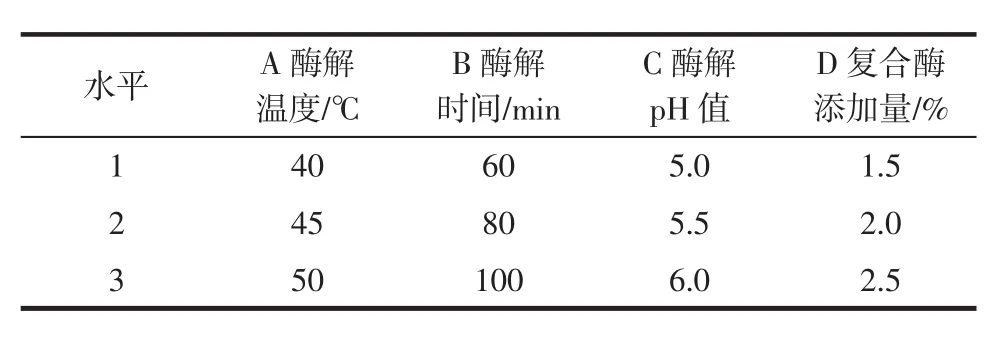
表4 五味子多糖提取工藝優化正交試驗水平表Table 4 Factors and coded levels used in the orthogonal array design for optimization of polysaccharide from Schisandra chinensis extraction
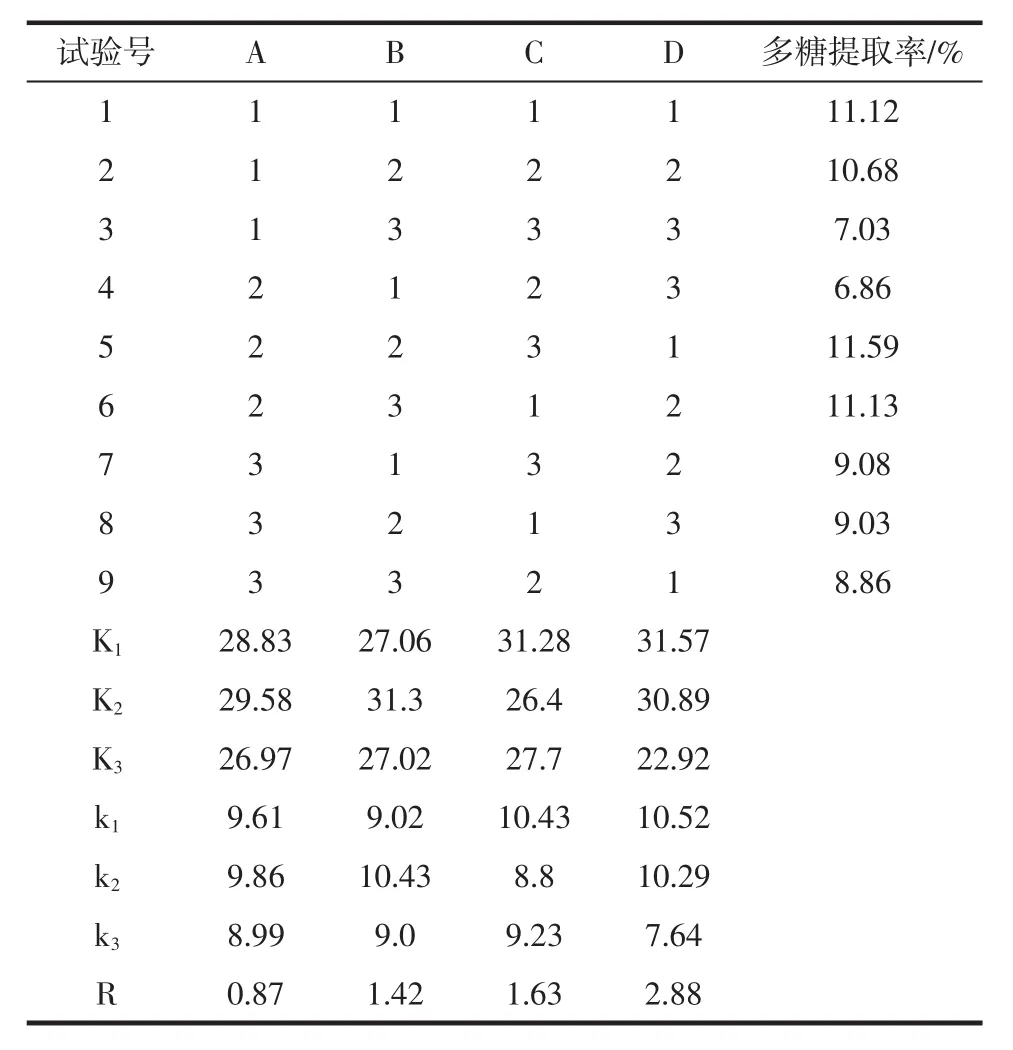
表5 五味子多糖提取工藝優化正交試驗設計及結果Table 5 Orthogonal array design scheme and corresponding results for optimization of polysaccharide from Schisandra chinensis extraction
2.3 五味子多糖的攝入對小鼠腸道菌群的影響
2.3.1 攝入五味子多糖對雙歧桿菌的作用
經過超濾、凍干等步驟的操作,最終能夠得到的五味子粉末多糖純度經檢測可達到92.32%。
分別使用不同劑量的五味子多糖灌胃造模小鼠0、7、14天后,連同空白對照組和紊亂自然恢復組,研究不同劑量五味子多糖的攝入對于小鼠腸道內雙歧桿菌含量的影響,如圖2所示。
由圖2可知,五味子多糖有助于提升小鼠腸道內雙歧桿菌的含量,持續攝入五味子多糖,小鼠腸道內雙歧桿菌逐漸增多,而且隨著多糖攝入量的提高,小鼠腸道內雙歧桿菌的含量有所提高。雙歧桿菌具有抑制致病菌、免疫調節、抗腫瘤以及調節腸道內環境的作用,本研究結果顯示五味子多糖能夠促進益生菌之一——雙歧桿菌的生長,且促進作用與多糖攝入劑量呈正相關。
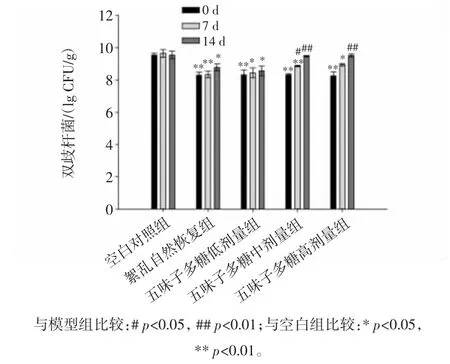
圖2 各組小鼠腸道內雙歧桿菌數量Fig.2 The quantity of Bifidodacterium on intestinal flora of mice in each group
2.3.2 攝入五味子多糖對乳桿菌的作用
分別使用不同劑量的五味子多糖灌胃造模小鼠0、7、14天后,連同空白對照組和紊亂自然恢復組,研究不同劑量五味子多糖的攝入對于小鼠腸道內乳桿菌含量的影響,如圖3所示。

圖3 各組小鼠腸道內乳桿菌數量Fig.3 The quantity of Lactobacilus on intestinal flora of mice in each group
由圖3可知,第7天,對比紊亂自然恢復組,中劑量組小鼠腸道內乳桿菌的數量有極顯著增加,第14天,高劑量組小鼠腸道內乳桿菌的數量顯著增加,持續攝入五味子多糖可以提高小鼠腸道內乳桿菌的含量,高劑量的五味子多糖長時間飼喂能夠顯著提高小鼠腸道中的乳桿菌含量,且促進作用與多糖攝入劑量呈正相關。
2.3.3 攝入五味子多糖對腸球菌的作用
分別使用不同劑量的五味子多糖灌胃造模小鼠0、7、14天后,連同空白對照組和紊亂自然恢復組,研究不同劑量五味子多糖的攝入對于小鼠腸道內腸球菌含量的影響,如圖4所示。
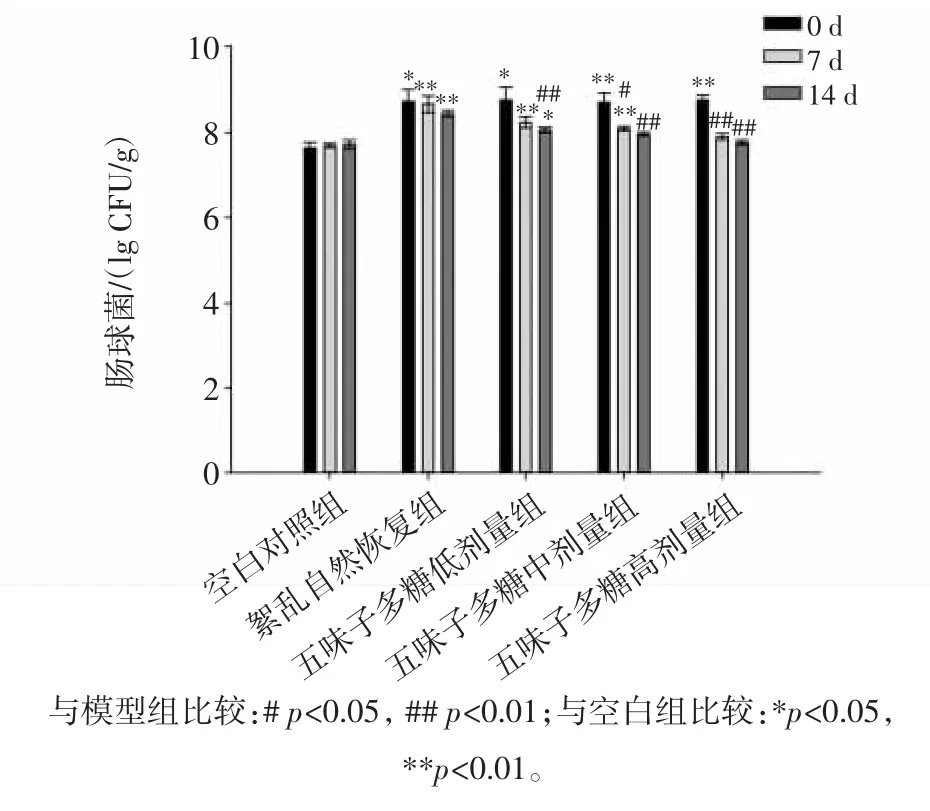
圖4 各組小鼠腸道內腸球菌數量Fig.4 The quantity of Enterococcus on intestinal flora of mice in each group
由圖4可知,灌胃鹽酸林可霉素后,紊亂自然恢復組小鼠腸道內腸球菌數量極顯著升高,從第7天開始,五味子多糖中劑量組小鼠腸道內腸球菌數量顯著降低,第14天時,低、中、高劑量組小鼠腸道內腸球菌數量均極顯著降低,持續攝入五味子多糖可以顯著降低小鼠腸道內腸球菌的含量,且存在劑量效應關系。
2.3.4 攝入五味子多糖對大腸桿菌的作用
分別使用不同劑量的五味子多糖灌胃造模小鼠0、7、14天后,連同空白對照組和紊亂自然恢復組,研究不同劑量五味子多糖的攝入對于小鼠腸道內大腸桿菌含量的影響,如圖5所示。
由圖5可知,灌胃鹽酸林可霉素后,小鼠腸道內大腸桿菌數量顯著升高,喂食五味子多糖后小鼠腸道內大腸桿菌數量呈下降趨勢,在第14天時,中、高劑量五味子多糖組小鼠腸道內大腸桿菌數量分別顯著、極顯著降低,持續攝入五味子多糖可以顯著降低小鼠腸道內腸球菌的含量,且存在劑量效應關系。
2.4 五味子多糖對小鼠體重的影響
實驗期間各組小鼠體重變化見圖6。
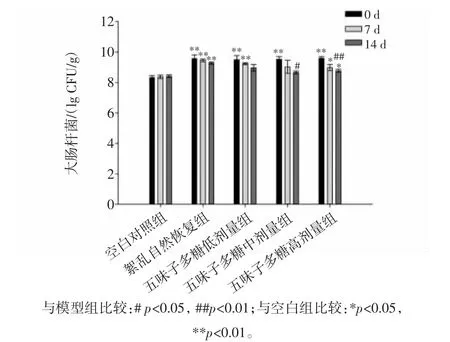
圖5 各組小鼠腸道內大腸桿菌數量Fig.5 The quantity of Escherichia on intestinal flora of mice in each group
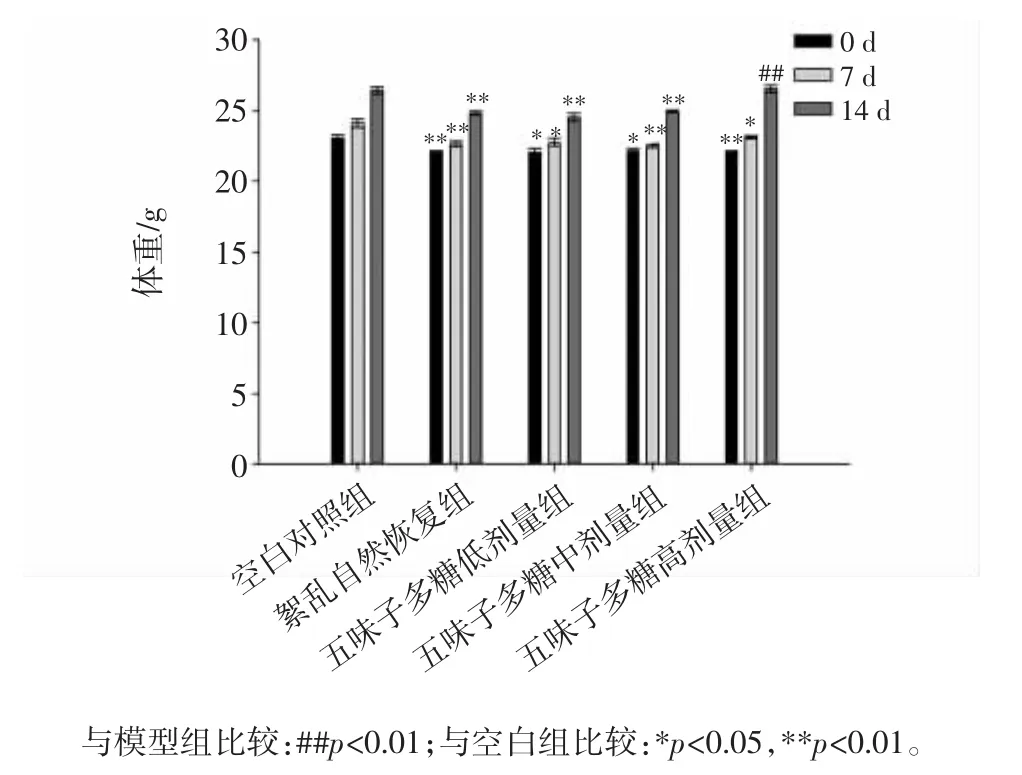
圖6 實驗期間各組小鼠體重變化Fig.6 The body weight of mice in each group during the experiment
由圖6可見,小鼠喂食期間體重的變化可見,同空白組比較,紊亂自然恢復組小鼠體重極顯著降低,不同劑量五味子多糖對小鼠體重的影響有差異,其中高劑量組小鼠體重變化與空白組相似,可見,不同劑量五味子多糖在發揮調節腸道菌群作用的同時對小鼠機體的生長有一定的影響
3 結論與討論
健康的人體內存在大量微生物,長期與機體保持平衡。腸道內菌群形成微生態系統,以保護機體免受各種疾病的損傷。當人體腸道的菌群紊亂時,益生菌會大量減少,有害菌會大量增殖,破壞腸道環境。腸道內雙歧桿菌、乳桿菌等有益菌共同保護機體免受外界環節的干擾,適當提高腸道內有益菌的數量可以更好的為機體設立防御系統。
通過單因素和正交試驗可知,酶解輔助提取五味子多糖的最佳條件為提取溫度45℃、提取時間80 min、提取pH 6.0、復合酶添加量1.5%,復合酶添加量對酶法提取五味子多糖影響最大,多糖提取率達到11.59%,五味子粉末多糖純度經檢測可達到92.32%。
與空白對照組比較,紊亂自然恢復組內雙歧桿菌、乳桿菌數量均顯著減低,腸球菌、大腸桿菌數量極顯著增加,表明成功建立了腸道菌群失調小鼠模型,破壞了小鼠腸道內菌群形成的微生態系統。在此條件下攝入五味子多糖,腸道內雙歧桿菌、乳桿菌等有益菌數量顯著增高,腸球菌、大腸桿菌等條件性致病菌的數量顯著降低,且均存在劑量效應關系,同時對小鼠機體的生長有一定的影響。表明五味子多糖確實能夠在一定程度上調節因鹽酸林可霉素導致的腸道紊亂,且高劑量的多糖對以上指標的改善效果最好。這可能是由于腸道內有益菌利用多糖進行代謝后產生了乳酸、乙酸等短鏈脂肪酸,降低了腸道內的pH值,從而抑制腸球菌、大腸桿菌的生長。

